Что такое антиоксиданты и механизм их действия
Все живые организмы, и человек в том числе, в процессе метаболизма используют кислород. Метаболизм – это и есть различные реакции, происходящие в организме. Синоним метаболизма – обмен веществ. В процессе метаболических процессов или обмена веществ, человек получает энергию из питательных веществ, т.е. из еды. Главный окислитель — кислород. В процессе окисления в организме человека с участием кислорода происходят химические реакции, в процессе которых усваиваются белки, жиры, углеводы. То есть производится энергия, которая нам нужна для жизни.
Иногда в процессе окисления остается не связанный ни с какими другими молекулами свободный атом кислорода. Вот такие свободные атомы кислорода называются свободными радикалами. Не вдаваясь в научные термины всех соединений, которые образуются в организме, отметим только, что этот свободный атом кислорода сам по своей природе очень агрессивный. Он все время стремится вступить в реакцию с другими молекулами.
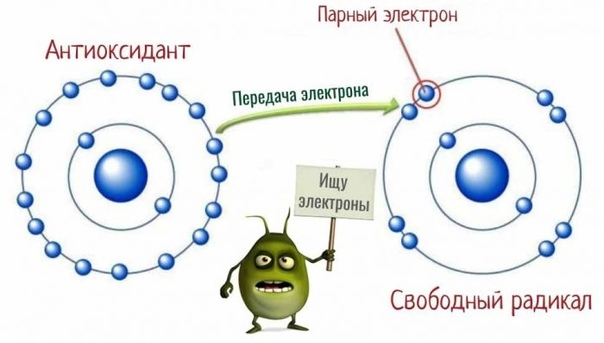 Это в свою очередь может привести к серьезным заболеваниям. Именно действием свободных радикалов ученые и врачи считают такие заболевания, как:
Это в свою очередь может привести к серьезным заболеваниям. Именно действием свободных радикалов ученые и врачи считают такие заболевания, как:Онкологические;
Болезни сердца;
Снижение функций головного мозга;
Снижение иммунитета.
Это только маленькая часть болезней, к которым может привести разрушительная сила свободных радикалов. Вообще ученые считают их причиной около 50 различных болезней. Болезнь Паркинсона и Альцгеймера, артрит, дегенеративные изменения сетчатки глаз – вот малая доля из этого списка. Как уже было написано выше, свободные радикалы содержат свободный электрон, который стремится проникнуть и захватить себе пару от любой клетки организма. Но, оторвав себе «пару», он порождает цепную реакцию. Как считают многие ученые, именно так может происходить не контролируемый процесс деления клетки. За несколько секунд могут появиться тысячи свободных радикалов. Чтобы избежать и остановить такую цепную реакцию, на помощь приходят антиоксиданты.
 Продукты антиоксиданты Самыми лучшими источниками антиоксидантов являются фрукты и овощи, продукты растительного происхождения. Есть очень много продуктов, которые содержат антиоксидантные соединения, витамины антиоксиданты, такие, как витамин С, А, Е, селен, бета-каротин. Условно продукты можно разделить на несколько групп.
Продукты антиоксиданты Самыми лучшими источниками антиоксидантов являются фрукты и овощи, продукты растительного происхождения. Есть очень много продуктов, которые содержат антиоксидантные соединения, витамины антиоксиданты, такие, как витамин С, А, Е, селен, бета-каротин. Условно продукты можно разделить на несколько групп.Продукты, содержащие витамин С. Этот витамин в большом количестве содержится в цитрусовых, помидорах, красном, желтом и зеленом перце, в темно зеленых овощах.
Бета-каротин. Им богаты морковь, красный и желтый перец, брокколи, сладкий картофель, манго и очень много других фруктов и овощей.
Витамин Е. этот витамин в большом количестве можно найти в орехах, растительных маслах, коричневом рисе, бобовых, цельном зерне, темно зеленых листовых салатах.
Селен. Этот редкий минерал содержится в некоторых видах рыбы, морепродуктах, бразильском орехе, мясе птицы, цельном зерне, молочных продуктах, чесноке, луке, в проростках пшеницы.
Главное, что важно знать – нужно, как можно больше разнообразить свое питание, чтобы получить максимум пользы от продуктов. А также периодически посещать врача с целью профилактического осмотра, чтобы убедиться, что с вашим организмом все в порядке, а если это не так, успеть вовремя принять необходимые меры!
А также периодически посещать врача с целью профилактического осмотра, чтобы убедиться, что с вашим организмом все в порядке, а если это не так, успеть вовремя принять необходимые меры!
Враги старения и болезней. Что такое антиоксиданты и в чем их искать | ЗДОРОВЬЕ
Об антиоксидантах сегодня слышал почти каждый. Об их пользе для здоровья и сохранения молодости сказано немало. И хотя это утверждение, как и многие другие вопросы в медицине, пока предмет споров, многие врачи склонны считать, что антиоксиданты оказывают положительное воздействие на организм, причем тот или иной элемент — на конкретные функции или органы. Что же представляют собой антиоксиданты, какова их роль для человека и главное, в чем их искать, «АиФ-Волгоград» рассказала врач-методист Волгоградского областного центра медицинской профилактики Нина Ларченко.
На страже здоровья«Антиоксиданты — те вещества, которые призваны уравновесить окислительный процесс, подавить появление и рост свободных радикалов, — рассказывает Нина Ларченко. — Свободные радикалы — это «неполные» химические молекулы с неспаренным электроном. Такие молекулы ведут себя агрессивно, стремясь отобрать недостающий электрон у других соединений. Они атакуют клетки нашего организма, внедряясь не только в клеточные мембраны органов, но и в ДНК. Это может привести к серьезным заболеваниям. Причём у каждого человека свободные радикалы повреждают наиболее уязвимый орган».
— Свободные радикалы — это «неполные» химические молекулы с неспаренным электроном. Такие молекулы ведут себя агрессивно, стремясь отобрать недостающий электрон у других соединений. Они атакуют клетки нашего организма, внедряясь не только в клеточные мембраны органов, но и в ДНК. Это может привести к серьезным заболеваниям. Причём у каждого человека свободные радикалы повреждают наиболее уязвимый орган».
По словам врача, антиоксиданты имеют широкий спектр действий: обладают противовоспалительными, сосудорасширяющими, противоаллергенными, иммуностимулирующими, противоопухолевыми и другими защитными и восстанавливающими свойствами. Делятся они на природные и синтетические.Первые мы получаем с продуктами, вторые — в виде разнообразных добавок.
«В последнее время многие медики пришли к выводу, что из множества антиоксидантов, содержащихся в продуктах питания и с помощью которых можно усилить защиту организма от старения и болезней, особенно важны витамины Р, А, С, Е и микроэлементы, в том числе селен, — говорит Нина Ларченко.
Природные антиоксиданты делятся на витамины и минералы. И те, и другие можно получить из пищи. Врач Нина Ларченко приводитс лишь некоторые основные свойства витаминов и микроэлементов.
Витамины-антиоксиданты
Витамин Р – бифланоиды
Чем полезны. Снижают холестерин в крови, а так же предупреждают образование тромбов. Способствуют укреплению иммунитета и лечению болезней сердечнососудистой системы, заболеваний глаз, дерматитов.
Витамин А и провитамин А являются жирорастовримым, содержащие его продукты следует принимать с животным или растительным жиром — маслами, сливками и т.д.Где искать. Виноград, свекла, черника, баклажаны, краснокочанная капуста.
Витамин А разделяют на ретиноиды — готовый витамин А и каратиноиды. Последний -провитамин, то есть превращается в витамин А уже в организме. Каратиноиды содержатся в растительной пище.
Витамин А — ретиноиды. Влияют на устойчивость к инфекционным заболеваниям, укрепляют иммунитет, участвуют в процессе роста, в развитии костей, а также синтезе эритроцитов и производстве мужских половых клеток. Витамин А применяют при кожных заболеваниях, в онкологии, в косметологии и др.
Где находится. Преимущественно в продуктах животного происхождения: коровье молоко, креветки, яйца, лосось, палтус, сыр, йогурт, сардины, тунец, треска и курица.
Провитамин А — каратиноиды. Обладают мощной антиоксидантной и противовоспалительной активностью. Используются для профилактики заболеваний глаз, кожных заболеваний, лечения хронических заболеваний желудочно-кишечного тракта и печени. Кроме того, каратиноиды повышают иммунитет, поддерживают в нормальном состоянии волосы, кожу, слизистые оболочки.
Где находятся. Морковь, тыква, абрикосы, капуста.
Витамин Е – токоферол. Является мощным антиоксидантом.Замедляет процессы старения, укрепляет стенки кровеносных сосудов, борется с ожирением, тромбами, благотворно влияет на работу сердца. Выводит из организма токсины и химические вещества. Витамин Е используют при кожных заболеваниях, при заболеваниях нервной системы. Кроме того, витамин Е влияет на плод во время беременности.
Где находится. Растительные масла (много – в хлопковом и горчичном), шпинат, капуста брокколи, орехи, семечки, фасоль, зеленые кислые яблоки, зерновые продукты (только неочищенные), молодые ростки злаков.
Витамин С – аскорбиновая кислота. Является мощным антиоксидантом. Влияет на стабилизацию психики, оказывает укрепляющее действие на костную ткань, кожу, сухожилия, зубы, особенно на микроскопические капилляры. Повышает эластичность и прочность кровеносных сосудов, ускоряет заживление ран.
Для чего нужен. Обеспечивает надежную иммунную защиту, в связи с чем его часто назначают для профилактики простудных заболеваний. Применяется при нарушении мозгового кровообращения, гипертонии.Витамин С противостоит аллергическим реакциям, а также таким заболеваниям как гепатит, диабет, оказывает помощь в лечении простуд.Применяется при различных отравлениях, полезен при синдроме хронической усталости.
Применяется при нарушении мозгового кровообращения, гипертонии.Витамин С противостоит аллергическим реакциям, а также таким заболеваниям как гепатит, диабет, оказывает помощь в лечении простуд.Применяется при различных отравлениях, полезен при синдроме хронической усталости.
Очень аккуратно необходимо применять витамин С при почечно-каменной болезни. Ежедневный прием высоких доз витамина С повышает риск образования камней в почках.
Где находится. Шиповник (предпочтительно сушеный), барбарис, земляника, чёрная смородина, облепиха, дыня, рябина, малина, ежевика, перец, капуста кольраби, брюссельская, цветная и белокочанная капуста, боярышник, киви, цитрусовые, щавель, яблоки отечественные.
Минералы – антиоксиданты
Минералы-антиоксиданты дополняют и усиливают роль витаминов в организме человека.
Цинк
Применяют для укрепления иммунитета, для заживления ран. Используют вместе с селеном для профилактики гипертонии.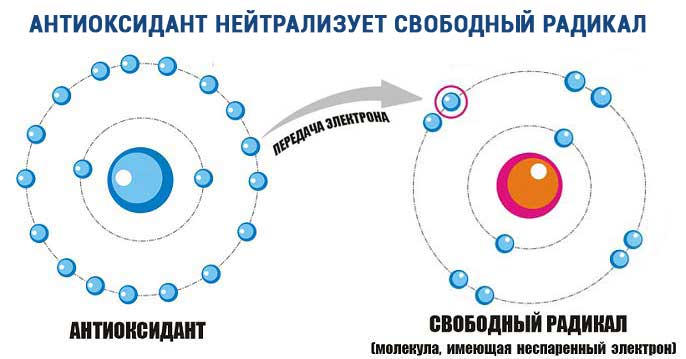
Где находится. Яблоки, апельсины, лимон, инжир, грейпфрут, зеленые овощи, мед, черная смородина, малина, финики. Кроме этого, цинк содержат большинство овощей, мясо большинства морских рыб, постная говядина, молоко, свекла столовая и сахарная, сельдерей, спаржа и др. Большое количество цинка содержат пшеничные отруби и проросшие пшеничные зерна, тыквенные семечки и семена подсолнечника.
Селен
Иммуностимулятор. Применяется для профилактики гипертонической болезни. Необходим для восстановления сердечной мышцы после инфаркта, для профилактики и лечения артрозов и остеохондроза, для профилактики и лечения заболеваний щитовидной железы. Принимают при аллергических дерматитах. Селен «работает» в содружестве с витамином Е.
Где находится. Дрожжи, яйца (желток), печень (индейки, курицы, утки, говяжья, свининая), креветки, рыба, устрицы. Из растений селен содержат овсяная и гречневая крупы, грибы, кукуруза, чеснок, пророщенные зерна пшеницы.
Марганец
Усиливает действие инсулина, принимает участие в синтезе гормона щитовидной железы, в регулировании уровня сахара в крови, способствует свертываемости крови. Улучшает работу иммунной системы, благотворно влияет на нервную систему. Препятствует отложению жира в печени, повышает выносливость мышц.
Где находится. Куриное мясо, печень говяжья, сыр, яичный желток, картофель, свекла, морковь, лук, фасоль, горох, салат, сельдерей, бананы, чай (листовой), имбирь, гвоздика.
Медь
Медь входит в состав ферментов организма. Обладает антибактериальным, обезболивающим и кровоостанавливающим свойствами, успокаивает нервную систему, восстанавливает сон. Она снимает многие воспалительные процессы. Медь необходима при анемиях, полезна медь при заболеваниях печени и почек, при атеросклерозе.
Где находится. Морепродукты (креветки, устрицы), говяжья (телячья) печень, мясо, рыба, орехи, семечки, какао, чернослив, вишня, баклажаны, свекла, картофель, алоэ вера, чеснок, горох, морская капуста, петрушка и др. Хром применяют для лечения остеопороза, используют для профилактики глаукомы, сердечнососудистых заболеваний.
Хром применяют для лечения остеопороза, используют для профилактики глаукомы, сердечнососудистых заболеваний.
Хром
Ускоряет процессы обмена углеводов , выполняет антисклеротическое, ранозаживляющее и язвозаживляющее действие, улучшает половые функции. Особенно полезен хром в пожилом возрасте, а также беременным и кормящим женщинам. Хром применяют для облегчения хронических головных болей, для лечения угревой сыпи.
Где находится. Пивные дрожжи, печень, пшеничные отруби, проросшие зерна пшеницы, кисломолочные продукты, пшеничные зародыши, семена подсолнечника, хлеб с отрубями.
Антиоксиданты: что действительно следует знать
Большинство современных образованных людей, по крайней мере, что-то слышало о том, что богатые антиоксидантами пищевые продукты и добавки полезны для здоровья. Однако многие, возможно, не совсем понимают, – что вообще такое антиоксиданты и как это работает в организме.
В журнале «Biomolecules» была опубликована статья, в которой, кроме прочего, говорилось о самом словечке «антиоксидант»: это один из наиболее туманных и сбивающих с толку научных терминов, который в специальной литературе до настоящего времени не находит четкого определения.
В данном материале попробуем немного глубже, чем обычно это делается, разобраться в сути понятия «антиоксиданты», в механизме их действия и влияния на здоровье.
Что такое антиоксиданты?Антиоксиданты – это соединения, способные нейтрализовать свободные радикалы и тем самым снизить или предотвратить повреждение клеток. В свою очередь, свободные радикалы представляют собой молекулы, несущие на внешней орбите один или несколько неспаренных электронов, – что делает их нестабильными и очень реактивными. Уточним, что под реактивностью в данном случае понимается способность свободных радикалов вступать в различные биохимические реакции с другими молекулами.
В организме свободные радикалы образуются в ходе нормальных эндогенных (внутренних) метаболических процессов, включая процессы энергообеспечения. Кроме того, организм вырабатывает свободные радикалы в ответ на внешние, средовые воздействия, а также на факторы, связанные с образом жизни: в качестве примера можно привести пребывание под открытым солнцем, курение, потребление спиртосодержащих напитков, психоэмоциональные перегрузки и т. д.
д.
Антиоксиданты ингибируют (подавляют) процессы окисления, т.е. химические реакции соединения с т.н. активным кислородом. Молекула кислорода с неспаренным электроном – это очень активный свободный радикал. В результате реакций с ним повреждаются клетки, организм «закисливается» и появляются новые нестабильные, высоко реактивные и потому опасные молекулы с неспаренными электронами.
Антиоксиданты взаимодействуют с такими молекулами безопасным для тканей образом, нейтрализуя их до того, как будут повреждены молекулы протеинов (белков), липидов (жиров) или ДНК (дезоксирибонуклеиновая кислота, носитель генетической информации).
Оксидативный стресс (от англ. «stress» – удар, сотрясение, перегрузка, давление и т.п.) возникает при наличии чрезмерного количества свободных радикалов. Такой дисбаланс, в свою очередь, может быть обусловлен либо повышенной продукцией свободных радикалов в организме, либо недостаточностью механизмов антиоксидантной защиты.
Подчеркнем: свободные радикалы не хороши и не плохи. В естественных, нормальных для данного организма концентрациях они необходимы для эффективного и здорового протекания физиологических энергообменных процессов. Опасен лишь избыток свободных радикалов: в этом случае повышается риск развития всевозможных хронических заболеваний, в том числе столь серьезных, как, например, сердечнососудистая или опухолевая патология. Кроме того, в последнее время все большее внимание привлекает теория, согласно которой процессы старения представляют собой не что иное, как прогрессирующий оксидативный стресс.
В естественных, нормальных для данного организма концентрациях они необходимы для эффективного и здорового протекания физиологических энергообменных процессов. Опасен лишь избыток свободных радикалов: в этом случае повышается риск развития всевозможных хронических заболеваний, в том числе столь серьезных, как, например, сердечнососудистая или опухолевая патология. Кроме того, в последнее время все большее внимание привлекает теория, согласно которой процессы старения представляют собой не что иное, как прогрессирующий оксидативный стресс.
Клетки нашего организма обладают определенными биохимическими механизмами, которые позволяют держать под контролем выработку свободных радикалов. Например, в клетках содержатся особые антиоксидантные энзимы (ферменты, т.е. расщепляющие вещества), снижающие концентрацию молекул с непарными электронами. К первичным антиоксидантным энзимам относятся, в частности, супероксиддисмутаза (SOD), каталаза (CAT), глутатионпероксидаза (GPx) и глутатион редуктаза (GRx). Эти вещества представляют собой, так сказать, первый эшелон антиоксидантной обороны. Они регулируют уровень свободных радикалов, вступая с ними (а также с другими молекулами, которые потенциально могут стать свободными радикалами) в безопасные нейтрализующие реакции.
Эти вещества представляют собой, так сказать, первый эшелон антиоксидантной обороны. Они регулируют уровень свободных радикалов, вступая с ними (а также с другими молекулами, которые потенциально могут стать свободными радикалами) в безопасные нейтрализующие реакции.
Аналогичные вещества-регуляторы, – метаболические антиоксиданты, – образуются также в сложных биохимических каскадах обмена веществ. К метаболическим антиоксидантам относят липоевую кислоту, глутатион, коэнзим Q10, мелатонин, мочевую кислоту, Л-аргинин, металл-хелатирующие белки, билирубин, трансферрин.
Вместе с тем, ряд необходимых антиоксидантов сам организм не производит, и получить их мы можем только извне, с пищей или пищевыми добавками. К таким антиоксидантам относятся, в частности, каротиноиды, некоторые витамины с антиоксидантным эффектом (напр., витамины С и Е), селен, марганец, цинк, флавоноиды, жирные кислоты омега-3 и омега-6. Пищевые и дополнительные антиоксиданты неизменно находятся в центре внимания диетологической науки, поскольку укрепить антиоксидантную защиту организма способен лишь рацион, богатый перечисленными соединениями,
Естественные пищевые (нутриентные) антиоксиданты в сравнении с пищевыми добавкамиРазобраться в тонкостях циркуляции и взаимодействий антиоксидантов-нутриентов весьма непросто, здесь легко запутаться. С одной стороны, множество веществ и соединений антиоксидантного действия естественным образом присутствует в обычных и привычных нам продуктах питания. С другой, – бесчисленные пищевые добавки рекламируются производителями как незаменимые средства повышения антиоксидантной защиты.
С одной стороны, множество веществ и соединений антиоксидантного действия естественным образом присутствует в обычных и привычных нам продуктах питания. С другой, – бесчисленные пищевые добавки рекламируются производителями как незаменимые средства повышения антиоксидантной защиты.
Фрукты, овощи, специи, орехи содержат тысячи различных соединений, обладающих антиоксидантным эффектом. Например, в винограде, яблоках, грушах, вишнях, ягодах содержится группа растительных веществ, называемых полифенольными антиоксидантами, – на сегодняшний день известно более восьми тысяч природных полифенолов-антиоксидантов. Другой класс антиоксидантов, – каротиноиды, – в высоких концентрациях содержится, как правило, в ярко окрашенных фруктах и овощах.
Вместе с тем, эти натуральные антиоксиданты, поступающие в организм с пищей, очень отличаются от биоактивных веществ, которые входят в состав пищевых добавок. Скажем, витамин Е (сложный эфирный ацетат альфа-токоферола) существует во многих формах, как природных, так и синтетических, причем эти формы обладают в организме разным эффектом. Возможно, настолько разным, что становится понятно, почему исследования потенциальной пользы витамина Е для здоровья зачастую приносят противоречивые результаты.
Возможно, настолько разным, что становится понятно, почему исследования потенциальной пользы витамина Е для здоровья зачастую приносят противоречивые результаты.
Пищевые добавки обычно содержат высокие дозы изолированных антиоксидантных соединений, которые могут влиять на организм иначе, чем самая богатая антиоксидантами пища. Такая диета чрезвычайна питательна и важна для здоровья, в то время как концентрированные антиоксидантные добавки показаны не всем и, более того, могут оказаться вредоносными для некоторых людей.
Могут ли антиоксиданты нанести вред здоровью?Должно быть совершенно ясно, что рацион, богатый овощами, фруктами и другими естественными контейнерами антиоксидантов, полезен для общего состояния здоровья.
Профилактический эффект антиоксидантных пищевых добавок, т.е. способность последних предотвращать те или иные заболевания, гораздо менее очевиден.
Многие исследования показали, что в определенных аспектах такие концентрированные добавки также могут быть полезны для здоровья. Подобные выводы публиковались, например, в отношении омега-3 жирных кислот, куркумина, селена, ресвератрола, витамина С, – с описанием различных положительных эффектов, наблюдаемых при тех или иных условиях в различных по составу выборках. Однако отсюда вовсе не следует, что прием дополнительных антиоксидантов безопасен или необходим каждому человеку. Напротив, проводились и такие исследования, результаты которых свидетельствуют о способности некоторых синтетических антиоксидантов конфликтовать с естественными сигнальными путями организма, что в конечном счете оказывает негативное влияние на состояние здоровья.
Подобные выводы публиковались, например, в отношении омега-3 жирных кислот, куркумина, селена, ресвератрола, витамина С, – с описанием различных положительных эффектов, наблюдаемых при тех или иных условиях в различных по составу выборках. Однако отсюда вовсе не следует, что прием дополнительных антиоксидантов безопасен или необходим каждому человеку. Напротив, проводились и такие исследования, результаты которых свидетельствуют о способности некоторых синтетических антиоксидантов конфликтовать с естественными сигнальными путями организма, что в конечном счете оказывает негативное влияние на состояние здоровья.
И даже более того: достоверные научные данные говорят о том, что некоторым категориям населения высокодозовые антиоксидантные добавки попросту противопоказаны. Скажем, у здоровых мужчин добавки с высоким содержанием витамина Е повышают риск рака предстательной железы. Подобно этому, бета-каротиновые добавки связаны с повышенным риском рака легких у заядлых курильщиков.
Добавим, что до сих пор ни одно исследование не выявило каких-либо решающих преимуществ антиоксидантных добавок в плане профилактики заболеваний, но зато есть убедительные доказательства того, что концентрированные дозы витамина Е, витамина А и его предшественника бета-каротина могут повышать вероятность преждевременной смерти.
Вышеизложенное говорит о том, что бесконтрольный и бездумный прием пищевых добавок, содержащих определенные классы антиоксидантов, может разбалансировать естественные, собственные механизмы антиоксидантной защиты организма, что приведет к серьезным последствиям для здоровья.
И напротив, в постоянно расширяемой базе научных знаний до сих пор не появлялось указаний на то, что богатое антиоксидантами питание, включающее овощи, фрукты, специи, рыбу, орехи, чай и прочие природные источники, каким-то образом может быть связано с негативными эффектами или последствиями в плане здоровья. Именно поэтому ведущие эксперты в области диетологии (подчеркнем: особенно независимые эксперты) настоятельно рекомендуют сосредоточиться на нормализации и оптимизации собственного рациона, чтобы обеспечить достаточное поступление природных антиоксидантов с пищей. Крайне не рекомендуется принимать какие бы то ни было концентрированные антиоксидантные добавки, – за исключением тех случаев, когда это в явной форме предписано врачом.
По материалам сайта Medical News Today
Антиоксиданты — плацебо, спасение или угроза
Слово «антиоксиданты», которое переводится с латыни на русский как «антиокислители», стало очень популярным в последние годы. Его можно услышать в рекламе, увидеть на упаковках витаминных комплексов, косметических средств и на продуктах питания.
Их продвигают как «дарителей» молодости, красоты и здоровья. Для многих наличие этого слова на коробочке — стимул приобрести продукт или товар. «МК» в Питере» узнал, как эти таинственные антиоксиданты помогают нашему организму, в каком виде бесполезны, а в каких случаях могут навредить.
Как они работают и какие бывают?
Сразу отметим, антиокислители уже присутствуют в организме человека. Функция у них более чем важная. Это вещества, которые нейтрализуют пагубное воздействие на клетки воспалений и свободных радикалов. При наличии воспаления в организме клетки начинают с ним борьбу, в ходе которой появляются свободные радикалы (активные формы кислорода). Они могут повредить как мембрану клетки, так и, в некоторых случаях, ее ДНК. Антиоксиданты, подобно куполу, «закрывают» клетку, защищая ее от видоизменений. То есть предотвращают вредоносные последствия борьбы организма с вирусами и бактериями.
При наличии воспаления в организме клетки начинают с ним борьбу, в ходе которой появляются свободные радикалы (активные формы кислорода). Они могут повредить как мембрану клетки, так и, в некоторых случаях, ее ДНК. Антиоксиданты, подобно куполу, «закрывают» клетку, защищая ее от видоизменений. То есть предотвращают вредоносные последствия борьбы организма с вирусами и бактериями.
Более того, антиокислители обладают свойством связывать свободные радикалы и выводить их из организма. Именно благодаря этому замедляются разрушительные окислительные процессы. Если сократить цепочку разъяснений, то вывод прост: антиоксиданты оказывают помощь нашему иммунитету и отодвигают старение.
К линейке антиоксидантов относятся: бета-каротин, ликопин, лютеин, антоцианы, селен, флавин и флавоноиды, танины, витамины А, Е и С.
Антиокислители бывают природными и синтетическими. Первые можно получить из продуктов питания растительного происхождения. Вторые входят в состав некоторых видов БАДов, состав лекарств, пищевых добавок («Е» от 300 до 399 номера), в виде консервантов (продлевают срок хранения продуктов).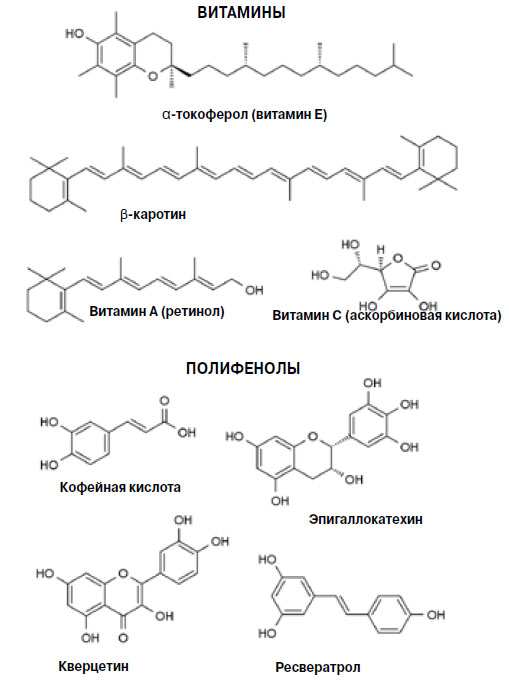
Когда антиоксиданты бессильны?
Исследованиями воздействия антиоксидантов на организм ученые занимаются уже более 35 лет. В частности, с 1985 по 2008 год этому вопросу уделяли повышенное внимание специалисты Кокрейн. Кокрейн — это глобальная международная некоммерческая организация, сеть исследователей, специалистов, пациентов и волонтеров, ухаживающих за больными, которая изучает эффективность медицинских технологий путем критической оценки, анализа и синтеза результатов научных исследований по строгой систематизированной технологии. Специалисты этой организации систематизировали и проанализировали итоги исследований, в которых принимали участие 200 тысяч человек. Они пришли к выводу, что антиоксиданты в таблетках не оказывают на организм никакого полезного влияния. Однако у 38% подопытных был отмечен эффект плацебо.
Также антиоксиданты бессильны при наличии у человека вредных привычек (они разрушаются под воздействием никотина и алкоголя), вдыхании загазованного выхлопами воздуха, излишнем пребывании на пляже или в солярии, дефиците свежего воздуха и частом употреблении лекарств. Помочь организму можно, отказавшись от вредных привычек, чаще бывая на свежем воздухе и ограничивая время нахождения на солнце.
Помочь организму можно, отказавшись от вредных привычек, чаще бывая на свежем воздухе и ограничивая время нахождения на солнце.
Могут ли они навредить?
Увы, да. Переизбыток антиокислителей в организме приводит к превращению антиоксидантов в прооксиданты, что провоцирует возникновение проблем со здоровьем. Исследование, проведенное в Финляндии еще с 1985 по 1993 годы (в нем приняло участие 29 тысяч мужчин-курильщиков), доказало, что употребление повышенных доз бета-каротина (витамина А) курильщиками на 18 % увеличивает риск развития рака легких. При приеме повышенных доз витамина Е увеличивается риск возникновения рака предстательной железы и инсульта.
Вред могут нанести и косметические средства с высоким содержанием антиоксидантов, которые, как мы уже говорили, при своем избытке трансформируются в прооксиданты. Однако если их содержание в косметических средствах невелико, то такие препараты действительно будут содействовать регенерации кожи и защищать от УФ-лучей.
Что насытит организм этим веществом?
Самый мощный источник природных антиоксидантов — фрукты и овощи. Также в больших количествах они содержатся в ягодах, травах, крупах и орехах.
Исследователи Министерства сельского хозяйства США, протестировав более 100 продуктов питания на уровень концентрации в них природных антиоксидантов, пришли к интересному выводу. Определить самые полезные фрукты, овощи и ягоды можно по цвету. О высоком наличии антиокислителя в растительной продукции сообщит их синий, черный, красный или оранжевый цвет. Чуть меньше вещества содержится в продуктах желтого и зеленого цветов.
Лидеры по содержанию антиоксидантов — красная фасоль, клюква, черника и ежевика. За ними следуют богатые природными антиокислителями чернослив, малина, клубника, орех пекан, черешня, слива, картофель, черная фасоль и яблоки сортов Red Delicious и Гала.
Богаты антиоксидантами также свекла, кабачки, баклажаны, но при интенсивной термической обработке витамины, содержащиеся в этих продуктах, разрушаются.
Нерафинированные масла холодного первого отжима богаты витамином Е (природный антиоксидант).
Вывод логичен: чтобы организм успешно боролся с воспалениями и свободными радикалами, антиоксиданты необходимо получать из свежих овощей, фруктов и ягод. А чтобы антиокислители работали, нужно отказаться от вредных привычек и больше бывать на свежем воздухе.
Антиоксиданты для защиты организма от действия свободных радикалов
Окислительные процессы в организме
Окислительным стрессом (оксидативным стрессом) называется процесс повреждения клетки в результате окисления.
В процессе жизнедеятельности любого организма в клетках и межклеточном пространстве происходит один из самых универсальных процессов – образование свободных радикалов. Они составляют особый класс химических веществ, различных по своему атомарному составу, но характеризующихся наличием в молекуле непарного электрона. Свободные радикалы – это вещества, являющиеся непременными спутниками кислорода и обладающие высокой химической активностью.
Их действие специалисты рассматривают как звено в метаболизме клетки, необходимое при иммунных реакциях, окислительном фосфорилировании (получении энергии в виде АТФ при клеточном дыхании), биосинтезе простагландинов и нуклеиновых кислот. У человека же оксидативный стресс является основной причиной либо важной составляющей многих серьезных заболеваний, таких как атеросклероз, гипертензия, диабет. Но самое серьезное влияние оксидативного стресса на организм – его непосредственное участие в процессе старения организма.
Однако в некоторых случаях оксидативный стресс совершенно необходим человеку как защитный механизм, так как иммунная система организма «использует» оксидативный стресс для борьбы с патогенами (факторами внешней среды, способными вызвать повреждение каких-либо систем организма или развитие заболеваний).
Как образуются свободные радикалы
Свободные радикалы представляют собой активные неустойчивые частицы, образующиеся в ходе процессов естественного метаболизма клеток. Их образованию способствуют многие процессы, сопровождающие жизнедеятельность организма: стрессы, экзогенные и эндогенные интоксикации, влияние техногенных загрязнений окружающей среды и излучения. Легкость образования свободных радикалов связана с уникальными свойствами молекул кислорода. В химических соединениях атомы кислорода двухвалентны (иллюстрацией этого является молекула воды). Однако в молекуле кислорода оба атома соединены только одинарной связью, а остающийся на каждом атоме кислорода один электрон свободен. И когда их валентности направлены в разные стороны, образуется очень опасный для биологических субстанций нестабильный токсичный кислород.
Их образованию способствуют многие процессы, сопровождающие жизнедеятельность организма: стрессы, экзогенные и эндогенные интоксикации, влияние техногенных загрязнений окружающей среды и излучения. Легкость образования свободных радикалов связана с уникальными свойствами молекул кислорода. В химических соединениях атомы кислорода двухвалентны (иллюстрацией этого является молекула воды). Однако в молекуле кислорода оба атома соединены только одинарной связью, а остающийся на каждом атоме кислорода один электрон свободен. И когда их валентности направлены в разные стороны, образуется очень опасный для биологических субстанций нестабильный токсичный кислород.
Опасность оксидативного стресса
По данным некоторых авторов, деятельность свободных радикалов способствует появлению и развитию более 100 различных заболеваний. Патологическое действие свободных радикалов связано, прежде всего, с их влиянием на клеточные мембраны.
Это приводит к тому, что начинается разрушительная цепная реакция, которая губительно действует на живые клетки. В результате организм начинает преждевременно СТАРЕТЬ, начинаются патологические изменения, которые могут стать причиной рака, сердечно-сосудистых заболеваний, диабета, ослабления зрения, памяти. Ученые предполагают, что начальной стадией многих заболеваний – от простого кашля до онкозаболевания – является именно большое количество свободных радикалов в организме.
В результате организм начинает преждевременно СТАРЕТЬ, начинаются патологические изменения, которые могут стать причиной рака, сердечно-сосудистых заболеваний, диабета, ослабления зрения, памяти. Ученые предполагают, что начальной стадией многих заболеваний – от простого кашля до онкозаболевания – является именно большое количество свободных радикалов в организме.
Мишени свободных радикалов – клетки, их составляющие или даже целые органы. Так, чаще всего воздействию свободных радикалов подвергается ДНК-кислота, обеспечивающая хранение и передачу генетической программы. Подсчитано, что ДНК подвергается их нападению до 10 000 раз в день. С повреждением структур ДНК свободными радикалами связывают в настоящее время такие болезни, как рак, артрозы, инфаркт, ослабление иммунной системы.
Изменения молекул мембран клеток, вызванные атакой свободных радикалов, оказывают разрушительное воздействие на сердечно-сосудистую систему: компоненты крови становятся «липкими», стенки сосудов пропитываются липидами и холестерином, в результате возникают тромбоз, атеросклероз и другие заболевания.
Особо чувствителен к гиперпродукции свободных радикалов и окислительному стрессу головной мозг, так как в нем содержится множество ненасыщенных жирных кислот, таких как, например, лецитин. При их окислении в мозгу повышается уровень липофусцина. Это один из пигментов изнашивания, избыток которого ускоряет процесс старения.
В отличие от других органов легкие непосредственно подвергаются действию кислорода – инициатора окисления, а также оксидантов, содержащихся в загрязненном воздухе (озона, диоксидов азота, серы и т.д.). Ткань легких содержит в избытке ненасыщенные жирные кислоты, которые оказываются жертвами свободных радикалов. На легкие также прямо воздействуют оксиданты, образующиеся при курении.
Также экспериментально доказано, что свободные радикалы могут являться факторами, провоцирующими развитие сахарного диабета и вызывающими его осложнения. Обычно здоровый организм сам справляется со свободными радикалами, однако неблагоприятные внешние факторы приводят к ситуации, когда ему необходима поддержка.
Как защитить организм
Наряду со свободнорадикальным окислением в процессе функционирования биологических объектов из групп радикалов вырабатываются вещества, обладающие антиоксидантным действием, которые называют стабильными радикалами. Они не способны нанести урон клеточным мембранам.
Такие химические соединения называются антиоксидантами, так как механизм их действия основан на торможении свободнорадикальных процессов в тканях организма. В отличие от нестабильных свободных радикалов, оказывающих повреждающее действие на клетки, антиоксиданты тормозят развитие деструктивных процессов.
В настоящее время биологические и химически синтезированные аниоксиданты подразделяются на жирорастворимые (самый известный – токоферол) и водорастворимые (наиболее распространенный – глутатион).
Полезная пища для защиты организма от свободных радикалов
В борьбе со свободными радикалами принимают участие не только антиоксидантные вещества, вырабатываемые организмом, но и антиоксиданты, поступающие с пищей. К антиоксидантам относятся также минеральные вещества (соединения селена, магния, меди), некоторые аминокислоты и растительные полифенолы (флавоноиды). А самыми сильными антиоксидантными свойствами обладают флавоноиды и антоцианы – вещества, содержащиеся в растениях, и определяющие их окраску. Поэтому в продуктах растительного происхождения антиоксидантов больше всего, особенно в кисло-сладких и кислых фруктах и овощах красного, оранжевого, синего и черного цвета. В желтых, ярко-зеленых и темно-зеленых растениях антиоксидантов тоже много, и есть даже список наиболее богатых ими растительных продуктов, хотя мнения ученых по этому поводу могут быть различными.
К антиоксидантам относятся также минеральные вещества (соединения селена, магния, меди), некоторые аминокислоты и растительные полифенолы (флавоноиды). А самыми сильными антиоксидантными свойствами обладают флавоноиды и антоцианы – вещества, содержащиеся в растениях, и определяющие их окраску. Поэтому в продуктах растительного происхождения антиоксидантов больше всего, особенно в кисло-сладких и кислых фруктах и овощах красного, оранжевого, синего и черного цвета. В желтых, ярко-зеленых и темно-зеленых растениях антиоксидантов тоже много, и есть даже список наиболее богатых ими растительных продуктов, хотя мнения ученых по этому поводу могут быть различными.
В один из таких списков попали фасоль – пестрая, черная и красная. Особенно ценятся мелкая фасоль, дикая и садовая, смородина, черная и красная, малина, клюква, клубника, слива и чернослив, черешня, сухофрукты и орехи, некоторые сорта яблок, артишок. Из орехов лучшими антиоксидантами считаются миндаль, грецкие орехи, фундук, фисташки и пекан.
Интересный факт: обычно считается, что при тепловой обработке продукты теряют свои полезные свойства, тем не менее, в вареном артишоке антиоксидантов становится на порядок больше, чем в сыром. Содержание антиоксидантов в продуктах может сильно отличаться, и ученые пока не могут сказать, чем это обусловлено, да и исследования проводились далеко не во всех областях. Например, мелкую фасоль считают самой полезной, но многие виды фасоли остаются пока неизученными. Лесные ягоды тоже исследованы не все, но одно можно сказать наверняка: чем ярче и насыщеннее цвет продукта, тем богаче он антиоксидантами. Ярко-желтая кукуруза содержит лютеин, оранжевые овощи и фрукты – каротин, ярко-красные помидоры – ликопин, темно-синие и черные ягоды богаты антоцианами.
Антиоксиданты в соках
В свежевыжатых соках ягод и фруктов антиоксидантов очень много: в гранатовом, виноградном, соке цитрусовых; антиоксиданты содержатся также в белом слое под их кожурой. Почти столько же антиоксидантов в яблочном соке и соке черноплодной рябины, вишни, и многих ягод и плодов, выращиваемых по всей России.
К продуктам, богатым антиоксидантами, относится и чай: зеленый, красный, черный и другие его виды. Содержание антиоксидантов, однако, зависит от технологии приготовления чая и от того, как он выращивался.
Как антиоксиданты помогают организму защититься от преждевременного старения
Поддержание здоровья стало основным и самым популярным трендом 2020 года. В условиях пандемии мы изучили принцип работы иммунной системы, узнали в мельчайших подробностях, как правильно носить медицинские маски и какие продукты являются лидерами по содержанию полезных для организма витаминов. Безусловно, все мы стали бережнее относиться к своему здоровью и заботиться о близких, поэтому постоянно находимся в поиске дополнительного источника помощи нашему организму в борьбе с влиянием негативных внешних факторов.
О пользе антиоксидантов для человека в последнее время говорят очень много, стремительно ухудшающаяся экологическая обстановка и как следствие, ухудшение качества жизни в целом, беспокоит ученых, медиков и обычных граждан. Как защитить клетки от разрушения, вызываемого воздействием свободных радикалов? Для начала разберемся, как эти опасные молекулы попадают в наши ткани, и перечислим основные источники:
– Ультрафиолет и радиация;
– Курение и употребление алкоголя;
– Неблагоприятная экологическая обстановка;
– Продукты питания, содержащие опасные канцерогены;
– Выхлопные газы и промышленные выбросы.
Попадая в человеческий организм, свободные радикалы забирают недостающие соединения у здоровых клеток, вызывая тем самым окислительный стресс, нарушая баланс и подрывая здоровье. Вот лишь основные возможные негативные последствия: нарушения в работе иммунной, костной и нервной систем, преждевременное старение, онкология, проблемы со зрением и сосудами, вмешательство в нормальную структуру ДНК.
Наука пока не научилась препятствовать проникновению свободных радикалов в ткани человека, однако, мудрая природа позаботилась о нашем благополучии и создала незаменимые полезные антиоксиданты. Какие они, эти чудесные помощники и как попадают в наш организм? Антиоксиданты оказывают прямо противоположное воздействию свободных радикалов влияние, находят поврежденные или разрушенные клетки и передают им свои электроны. Таким образом, клетки человеческого организма восстанавливаются, очищаются и омолаживаются. При этом, структурная устойчивость самих антиоксидантов не страдает.
Правда ли, что антиоксиданты замедляют старение? Американские ученые провели эксперимент над мышами, в рамках которого, в организме животных усиливали выработку антиоксидантных ферментов, вследствие чего продолжительность жизни подопытных увеличилась на 20%. Для человека эти данные говорили бы об увеличении жизни в среднем до 100 лет. Все дело в том, что останавливая вредоносный процесс воздействия свободных радикалов на организм, антиоксиданты восстанавливают нормальное течение химических процессов в клетках, не позволяя начаться преждевременному старению тканей.
Наш организм обладает резервными запасами антиоксидантов, однако, при усилении негативных факторов, такие запасы могут истощаться. Стоит напомнить, что вредные привычки, стрессы и неправильное питание существенно снижают запасы полезных ферментов в организме и препятствуют их накоплению. Например, одна выкуренная сигарета разрушает суточную норму витамина С, что является достаточной мотивацией для отказа от пагубной привычки.
Запасы антиоксидантов в организме человека необходимо регулярно пополнять. Перечень полезных ферментов достаточно большой и для достижения оптимального баланса необходимо их разнообразие. Выделяют антиоксиданты с наиболее сильным спектром воздействия:
- Убихинон Q10. Ученые настаивают на том, что старение человека напрямую связано с уменьшением фермента Q10. Наш организм умеет самостоятельно его вырабатывать, однако с возрастом эта способность существенно замедляется. Современная медицина предлагает большой выбор препаратов, с помощью которых можно пополнить запасы убихинона. Кроме того, он содержится в следующих продуктах: радужная форель, сельдь, говядина, куриные яйца, арахис, фисташки, кунжут, цветная капуста и брокколи.
- Глутатион. Это трипептид, способный выводить из организма тяжелые металлы и токсины. Его наш организм синтезирует самостоятельно, однако стоит позаботиться о достаточном его количестве и добавить в рацион: молочные продукты и мясо птицы, свежие фрукты и овощи, а также полезные пряности, такие как куркума, тмин и корица.
- Астаксантин. Уникальной возможностью данного фермента является его способность вбирать в себя ультрафиолет. Вещество очень полезно для кожи, так как защищает ее от преждевременного старения. Кроме того, астаксантин повышает иммунитет и снижает кровяное давление. Запасы этого полезного антиоксиданта можно пополнить, употребив в пищу следующие продукты: лосось, форель, креветки, ракообразные. Например, в одной порции лосося содержится суточная норма астаксантина. Производители БАДов предлагают фермент, полученный из водорослей.
- Ресвератол. Учеными доказана способность антиоксиданта защищать организм от раковых клеток и снижать давление. Кроме того, ресвератол защищает мозг и нервную систему. Этот полезный фермент присутствует в красных ягодах, орехах и бобах. Особенно много ресвератола в красном винограде и красном вине.
- Альфа-липоевая кислота. Выводит из организма тяжелые металлы, помогает купировать и подавлять воспалительные процессы, играет важную роль в кислородном метаболизме. Больше всего этот антиоксидант содержится в продуктах животного происхождения, молоке, рисе, капусте и зелени.
Антиоксидантами являются также витамины А, Е, С и минералы цинк, селен, медь, марганец и хром, но их употребление должно нормироваться установленными дозировками. При регулярном и сбалансированном употреблении продуктов, богатых полезными антиоксидантами, улучшается общее самочувствие и внешний вид, замедляются процессы старения, снижается риск развития различных заболеваний, что, несомненно, является необходимым человеку ресурсом, в борьбе за сохранение здоровья и долголетия.
В случае применения биологически активных добавок мы рекомендуем вам получить консультацию терапевта.
Антиоксиданты: польза и вред, что это такое и зачем нужны | Vogue Ukraine
Антиоксиданты полезны – это знают все. Но чем именно хороши антиоксиданты в уходе за кожей, разбирается не каждый. Генетик, ученый, разработчик средств марки HydroPeptide Нил Китчен рассказывает, как работают антиоксиданты, какие из них – самые эффективные, и что нужно знать, чтобы добиться от продуктов с антиоксидантами максимальной эффективности.
Антиоксиданты – популярный ингредиент в средствах для ухода за кожей. Это один из лучших ингредиентов в уходе с точки зрения клинических результатов. Они дают заметный мгновенный эффект, ощутимую пользу в долгосрочной перспективе и ощущение роскоши в уходе за кожей.
Что такое антиоксиданты и зачем они нужны?
Чтобы понять, что такое антиоксиданты и чем они хороши в уходе за кожей, нужно ознакомиться с понятием «свободные радикалы». Свободные радикалы, или активные формы кислорода, – это атомы, в структуре которых отсутствуют некоторые электроны. Поэтому остальные электроны становятся нестабильными и пытаются забрать электроны у здоровых молекул. Это наносит вред клеткам – в том числе, клеткам кожи. Чтобы их защитить, и нужны антиоксиданты. Эти молекулы позволяют отдавать электроны свободным радикалам и снова делать их цельными. А значит, они не вредят здоровым клеткам.
Откуда появляются свободные радикалы? У них есть много источников: ультрафиолетовое излучение, загрязнение атмосферы, стресс и плохое питание. Особенно важно защищать кожу с помощью витаминов и антиоксидантов летом: солнце, источник ультрафиолета, становится агрессивным. На нашу кожу влияет два типа ультрафиолетовых лучей — UVB (вызывает ожоги) и UBА (провоцирует фотостарение и рак кожи). UVA-лучи провоцируют образование активных форм кислорода и вызывают оксидативный стресс. Это, в свою очередь, запускает выработку провоспалительных цитокинов, усиленное выделение матричных металлопротеиназ и уменьшает выработку коллагена. Результат – потеря структурных протеинов и заметное ухудшение состояния кожи.
Существует много типов свободных радикалов, которые угрожают здоровью кожи. А значит, антиоксидантная защита тоже должна быть разнообразной. Антиоксиданты должны быть подобраны так, чтобы противостоять каждой из активных форм кислорода. Когда мы создаем формулу на основе антиоксидантов для HydroPeptide, используем различные ингредиенты для защиты от солнца и других источников повреждения свободными радикалами.
Как используют антиоксиданты в косметике
Формулы на основе антиоксидантов могут создаваться с помощью различных подходов. Первый источник – экстракты растений. Одно из преимуществ использования таких экстрактов – антиоксиданты надежно защищены внутри растения, а значит – они являются более мощными. В команде HydroPeptide изучали, как растение защищает и стабилизирует собственные антиоксиданты, чтобы повторить этот механизм и добиться лучшего эффекта на коже. Так, они заметили, что в составе масла зерен винограда является витамин Е и другие ключевые антиоксиданты. Витамин Е стабилизирует их, делая более мощными и полезными для кожи. «Это помогло нам изолировать более сильные антиоксиданты, чтобы использовать их в средствах для ухода», – объясняет доктор Китчен.
Для создания эффективных формул HydroPeptide используют комбинацию ботанических экстрактов и антиоксидантов-витаминов. Для средств для ухода за кожей это очень важно, потому что такой прием имеет двойное действие: антиоксиданты одновременно успешно доставляются в кожу и защищают средство в тюбике, не позволяя ему потерять активность. «Мы применяем армию антиоксидантов, чтобы добиться синергетического эффекта на кожу. Скажем, не используем только витамин С, а объединяем его с другими антиоксидантами и пептидами, чтобы обеспечить формулу мощностью и ризноплановистю в плане эффекта», – говорит Нил.
Какие антиоксиданты считаются лучшими и используются в уходе за кожей чаще всего?
Витамин С – пожалуй, самый известный антиоксидант. В формулах средств для ухода его используют в нескольких самых популярных формах. Например, THD (Тетрагексидил аскорбат) – стабильная форма витамина С, которая встречается в продуктах на основе масел. MAP (магния аскорбил фосфат) и SAP (Sodium Ascorbyl Phosphate) – еще две популярные стабильные формы витамина С. А вот L-аскорбиновая кислота – активная форма, которая не может похвастаться стабильностью. Поэтому HydroPeptide, например, использует ее в сопровождении ингредиентов, способных ее стабилизировать. В маске с витамином С HydroPeptide используется запатентованная технология на основе высушенной L-аскорбиновой кислоты: в такой форме она лучше сохраняет эффективность.
Ниацинамид, или витамин В3. Он способен улучшать состояние кожи на нескольких уровнях. Ниацинамид подавляет воспаление кожи, уменьшает видимость пор и хорошо показывает себя в борьбе с последствиями ультрафиолетового излучения. И, конечно, как антиоксидант он отлично борется с окислительным стрессом.
Витамин А, или ретинол – еще один известный витаминный антиоксидант. Его полезные свойства многочисленны и разнообразны, а также хорошо изучены: витамин А используют в средствах для ухода уже более 50 лет. Клинически доказано, что он стимулирует выработку коллагена и борется с разрушительными процессами в коже. В некоторых случаях витамин А может вызвать раздражение кожи. Поэтому определенные формы витамина А – третиноин и изотретиноин – можно применять только по назначению врача. Для большинства пациентов лучшая форма ретинола – ретинальдегид. В HydroPeptide используют ретинол отсроченной активации в инкапсулированной форме. Это обеспечивает витамину А более глубокое проникновение в кожу и сводит к минимуму вероятность раздражения.
Витамин Е – важный антиоксидант, о котором мы часто незаслуженно забываем. Он не настолько мощный, как витамины А и С, но его роль важна и существенна: он стабилизирует другие антиоксиданты и позволяет сохранить их активность в момент нанесения. В большинстве формул HydroPeptide используется токоферол, производная витамина Е .
Ресвератрол. Содержится в винограде и арахисе. В HydroPeptide его используют и производят в больших масштабах. Мы используем процесс ферментации дрожжей, чтобы создать уникальный тип ресвератрола. Его можно найти в составе средства LumaPro-C, где в сочетании с витамином С ресвератрол усиливает антиоксидантный эффект.
Липоевая кислота. Лучшие ее источники – в еде: помидоры, брокколи, свекла и шпинат. Иногда эту кислоту называют противовоспалительным антиоксидантом. Одна из ее грандиозных преимуществ – она стимулирует организм вырабатывать больше собственных антиоксидантов. Это очень важный момент: наше тело само способно производить антиоксиданты. Поэтому ингредиенты вроде липоевой кислоты столь важны.
Ellagi C. Он помогает витаминам А и С активно взаимодействовать с клетками кожи. Этот антиоксидант улучшает и упрощает процесс входа витаминов в фибробласт – и, таким образом, усиливает выработку коллагена. HydroPeptide используют Ellagi C в нескольких формулах – например, в составе крема Nimni с ретинолом отсроченного действия.
Бустер Firma-Bright, запущенный HydroPeptide в прошлом году, – сочетание различных антиоксидантов, каждый из которых усиливает действие друг друга. К ним добавили мощные пептиды. В результате этот бустер считают в компании лучшей формулой на основе витамина С на рынке.
Свободные радикалы, антиоксиданты и функциональные продукты питания: влияние на здоровье человека
Pharmacogn Rev. Июль-декабрь 2010 г .; 4 (8): 118–126.
В. Лобо
Кафедра ботаники, колледж Бирла, Калян — 421 304, Махарастра, Индия .
А. Патил
Кафедра ботаники, колледж Бирла, Калян — 421 304, Махарастра, Индия .
А. Фатак
Кафедра ботаники, Колледж Бирла, Калян — 421 304, Махарастра, Индия .
Н. Чандра
Отделение ботаники, Колледж Бирла, Калян — 421 304, Махарастра, Индия .
Отделение ботаники, Колледж Бирла, Калян — 421 304, Махарастра, Индия .
Адрес для корреспонденции: Г-жа Виджая Чаван Лобо, кафедра ботаники, колледж Бирла, Калян — 421 301, Индия. E-mail: moc.liamffider@obolayajivПоступило 4 марта 2010 г .; Пересмотрено 8 марта 2010 г.
Это статья в открытом доступе, распространяемая в соответствии с условиями Creative Commons Attribution-Noncommercial-Share Alike 3.0 Unported, что разрешает неограниченное использование, распространение и воспроизведение на любом носителе при условии правильного цитирования оригинальной работы.
Эта статья цитируется в других статьях в PMC.Abstract
В последние годы большое внимание уделяется химии свободных радикалов. Свободные радикалы, активные формы кислорода и активные формы азота, генерируются нашим телом различными эндогенными системами, воздействием различных физико-химических условий или патологических состояний.Баланс между свободными радикалами и антиоксидантами необходим для правильного физиологического функционирования. Если свободные радикалы подавляют способность организма регулировать их, возникает состояние, известное как окислительный стресс. Таким образом, свободные радикалы неблагоприятно изменяют липиды, белки и ДНК и вызывают ряд заболеваний человека. Следовательно, применение внешнего источника антиоксидантов может помочь справиться с окислительным стрессом. Недавно сообщалось, что синтетические антиоксиданты, такие как бутилированный гидрокситолуол и бутилированный гидроксианизол, опасны для здоровья человека.Таким образом, в последние годы активизировался поиск эффективных, нетоксичных природных соединений, обладающих антиоксидантной активностью. В настоящем обзоре представлен краткий обзор клеточных повреждений, опосредованных окислительным стрессом, и роли диетических антиоксидантов как функциональных продуктов питания в лечении заболеваний человека.
Ключевые слова: Старение, антиоксидант, свободные радикалы, окислительный стресс
ВВЕДЕНИЕ
Недавний рост знаний о свободных радикалах и активных формах кислорода (АФК) в биологии произвел революцию в медицине, которая обещает новую эру здоровья и ведение болезней.[1] Парадоксально, что кислород, незаменимый для жизни элемент [2], в определенных ситуациях оказывает пагубное воздействие на человеческий организм. [3] Большинство потенциально вредных воздействий кислорода связано с образованием и активностью ряда химических соединений, известных как АФК, которые имеют тенденцию отдавать кислород другим веществам. Свободные радикалы и антиоксиданты стали широко используемыми терминами в современных дискуссиях о механизмах заболевания. [4]
СВОБОДНЫЕ РАДИКАЛЫ
Свободный радикал можно определить как любую молекулу, способную к независимому существованию, которая содержит неспаренный электрон на атомной орбитали.Наличие неспаренного электрона приводит к определенным общим свойствам, которые присущи большинству радикалов. Многие радикалы нестабильны и обладают высокой реакционной способностью. Они могут либо отдавать электрон, либо принимать электрон от других молекул, поэтому ведут себя как окислители или восстановители. [5] Наиболее важными кислородсодержащими свободными радикалами при многих болезненных состояниях являются гидроксильный радикал, супероксид-анион-радикал, перекись водорода, синглет кислорода, гипохлорит, радикал оксида азота и радикал пероксинитрита.Это высокоактивные виды, способные в ядре и мембранах клеток повредить биологически значимые молекулы, такие как ДНК, белки, углеводы и липиды. [6] Свободные радикалы атакуют важные макромолекулы, что приводит к повреждению клеток и нарушению гомеостаза. Мишени свободных радикалов включают в себя все виды молекул в организме. Среди них основными мишенями являются липиды, нуклеиновые кислоты и белки.
Производство свободных радикалов в организме человека
Свободные радикалы и другие АФК образуются либо в результате нормальных основных метаболических процессов в организме человека, либо из внешних источников, таких как воздействие рентгеновских лучей, озона, курения сигарет, загрязнителей воздуха и промышленные химикаты.[3] Образование свободных радикалов происходит в клетках непрерывно в результате как ферментативных, так и неферментативных реакций. Ферментативные реакции, которые служат источником свободных радикалов, включают те, которые участвуют в дыхательной цепи, в фагоцитозе, в синтезе простагландинов и в системе цитохрома P-450. [7] Свободные радикалы также могут образовываться в неферментативных реакциях кислорода с органическими соединениями, а также в реакциях ионизации.
Некоторыми внутренними источниками свободных радикалов являются [8]
Митохондрии
Ксантиноксидаза
Пероксисомы
Воспаление
4
1
Арацихозид
Путь фагоциктозаИшемия / реперфузионное повреждение
Некоторые внешние источники свободных радикалов:
Сигаретный дым
Загрязнители окружающей среды
Радиация
Промышленные растворители
Озон
0
Свободные радикалы в биологии
Ожидается, что реакции свободных радикалов вызовут прогрессирующие неблагоприятные изменения, которые с возрастом накапливаются во всем организме [].Такие «нормальные» изменения с возрастом относительно характерны для всех. Однако на эту общую закономерность накладываются закономерности, на которые влияет генетика и различия в окружающей среде, которые модулируют повреждение свободными радикалами. Они проявляются в виде болезней в определенном возрасте, которые определяются генетическими факторами и факторами окружающей среды. Рак и атеросклероз, две основные причины смерти, являются основными заболеваниями «свободных радикалов». Возникновение и распространение рака связано с хромосомными дефектами и активацией онкогенов. Возможно, что эндогенные свободнорадикальные реакции, например инициированные ионизирующим излучением, могут привести к образованию опухоли.Высоко значимая корреляция между потреблением жиров и масел и уровнем смертности от лейкемии и злокачественных новообразований груди, яичников и прямой кишки среди людей старше 55 лет может быть отражением более сильного перекисного окисления липидов [9]. Исследования атеросклероза показывают вероятность того, что заболевание может быть вызвано реакциями свободных радикалов с участием липидов пищевого происхождения в стенке артерий и сыворотки крови с выделением пероксидов и других веществ. Эти соединения вызывают повреждение эндотелиальных клеток и вызывают изменения в стенках артерий.[10]
Таблица 1
КОНЦЕПЦИЯ ОКИСЛИТЕЛЬНОГО СТРЕССА
Этот термин используется для описания состояния окислительного повреждения, возникающего, когда критический баланс между образованием свободных радикалов и антиоксидантной защитой неблагоприятен. [14] Окислительный стресс, возникающий в результате дисбаланса между производством свободных радикалов и антиоксидантной защитой, связан с повреждением широкого спектра молекулярных видов, включая липиды, белки и нуклеиновые кислоты. [15] Кратковременный окислительный стресс может возникать в тканях, поврежденных травмой, инфекцией, тепловым повреждением, гипертоксией, токсинами и чрезмерными упражнениями.Эти поврежденные ткани производят повышенные ферменты, генерирующие радикалы (например, ксантиноксидаза, липогеназа, циклооксигеназа), активацию фагоцитов, высвобождение свободного железа, ионов меди или нарушение цепей переноса электронов окислительного фосфорилирования, производя избыток АФК. Возникновение, развитие и прогрессирование рака, а также побочные эффекты лучевой и химиотерапии были связаны с дисбалансом между АФК и системой антиоксидантной защиты. АФК участвуют в индукции и осложнениях сахарного диабета, возрастных заболеваний глаз и нейродегенеративных заболеваний, таких как болезнь Паркинсона.[16]
Окислительный стресс и болезни человека
Роль окислительного стресса была постулирована во многих состояниях, включая антерсклероз, воспалительные состояния, некоторые виды рака и процесс старения. В настоящее время считается, что оксидативный стресс вносит значительный вклад во все воспалительные заболевания (артрит, васкулит, гломерулонефрит, красная волчанка, синдром респираторных заболеваний взрослых), ишемические заболевания (болезни сердца, инсульт, ишемия кишечника), гемохроматоз, синдром приобретенного иммунодефицита, эмфизема и т. трансплантация органов, язва желудка, гипертония и преэклампсия, неврологические расстройства (болезнь Альцгеймера, болезнь Паркинсона, мышечная дистрофия), алкоголизм, заболевания, связанные с курением, и многие другие.[17] Избыток окислительного стресса может привести к окислению липидов и белков, что связано с изменениями их структуры и функций.
Сердечно-сосудистые заболевания
Сердечно-сосудистые заболевания продолжают оставаться главной причиной смерти, на них приходится около половины всех смертей. Следовательно, окислительные процессы могут влиять на сердечно-сосудистые заболевания; он может принести огромную пользу для здоровья и продолжительности жизни. Полиненасыщенные жирные кислоты являются основной частью липопротеинов низкой плотности (ЛПНП) в крови, и окисление этих липидных компонентов в ЛПНП играет жизненно важную роль при атеросклерозе.[18] Три наиболее важных типа клеток в стенке сосуда — эндотелиальные клетки; гладкомышечные клетки и макрофаги могут выделять свободные радикалы, которые влияют на перекисное окисление липидов. [19] При постоянном высоком уровне окисленных липидов повреждение кровеносных сосудов в процессе реакции продолжается и может привести к образованию пенистых клеток и появлению налетов симптомов атеросклероза. Окисленный ЛПНП является антерогеном и, как полагают, играет важную роль в образовании бляшек от антисклероза. Кроме того, окисленные ЛПНП цитотоксичны и могут напрямую повреждать эндотелиальные клетки.Антиоксиданты, такие как B-каротин или витамин E, играют жизненно важную роль в профилактике различных сердечно-сосудистых заболеваний.
Канцерогенез
Активные формы кислорода и азота, такие как супероксид-анион, перекись водорода, гидроксильный радикал и оксид азота, и их биологические метаболиты также играют важную роль в канцерогенезе. АФК вызывают повреждение ДНК, поскольку реакция свободных радикалов с ДНК включает модификацию основания разрыва цепи и перекрестные связи белков ДНК. Многие исследователи предположили участие свободных радикалов в канцерогенезе, мутации и трансформации; ясно, что их присутствие в биосистеме может привести к мутации, трансформации и, в конечном итоге, к раку.Индукция мутагенеза, наиболее известного из биологических эффектов радиации, происходит в основном за счет повреждения ДНК HO. Радикальные и другие виды образуются радиолизом, а также прямым радиационным воздействием на ДНК, реакционным воздействием на ДНК. Реакция HO. Радикалы в основном представляют собой присоединение к двойной связи пиримидиновых оснований и отрыв водорода от сахарного фрагмента, что приводит к цепной реакции ДНК. Эти эффекты вызывают мутагенез клеток и канцерогенез, перекиси липидов также ответственны за активацию канцерогенов.
Антиоксиданты могут снижать канцерогенез, вызванный окислительным стрессом, путем прямого удаления АФК и / или ингибирования пролиферации клеток, вторичной по отношению к фосфорилированию белка. B-каротин может защищать от рака благодаря своей антиоксидантной функции, поскольку продукты окисления могут вызывать генетические повреждения. Таким образом, фотозащитные свойства B-каротина могут защищать от канцерогенеза, вызванного ультрафиолетовым светом. Иммуноусиление B-каротина может способствовать защите от рака.B-каротин также может оказывать антиканцерогенное действие, изменяя метаболизм канцерогенов в печени. [20] Витамин С может помочь предотвратить рак. [21] Возможные механизмы, с помощью которых витамин С может влиять на канцерогенез, включают антиоксидантные эффекты, блокирование образования нитрозанимов, усиление иммунного ответа и ускорение детоксикации ферментов печени. Витамин Е, важный антиоксидант, играет роль в иммунокомпетентности за счет повышения гуморальной защиты антител, устойчивости к бактериальным инфекциям, клеточного иммунитета, выработки фактора некроза опухоли Т-лимфоцитами, ингибирования образования мутагена, восстановления мембран в ДНК и блокирования. формирование микроклеточной линии.[22] Таким образом, витамин E может быть полезен для профилактики рака и подавления канцерогенеза за счет стимуляции иммунной системы. Введение смеси трех вышеуказанных антиоксидантов выявило наибольшее снижение риска развития рака сердца.
Свободные радикалы и старение
Человеческое тело находится в постоянной борьбе за то, чтобы не стареть. Исследования показывают, что повреждение клеток свободными радикалами приводит к патологическим изменениям, связанным со старением. [23] Растущее число заболеваний или нарушений, а также сам процесс старения демонстрируют прямую или косвенную связь с этими реактивными и потенциально деструктивными молекулами.[24] Главный механизм старения связан с ДНК или накоплением клеточных и функциональных повреждений. [25] Уменьшение количества свободных радикалов или снижение скорости их образования может замедлить старение. Некоторые пищевые антиоксиданты замедляют процесс старения и предотвращают болезни. На основании этих исследований выяснилось, что повышенный окислительный стресс обычно возникает в процессе старения, а антиоксидантный статус может значительно влиять на эффекты окислительного повреждения, связанные с пожилым возрастом.Исследования показывают, что свободные радикалы оказывают значительное влияние на старение, что повреждение свободными радикалами можно контролировать с помощью адекватной антиоксидантной защиты и что оптимальное потребление антиоксидантных питательных веществ может способствовать повышению качества жизни. Недавние исследования показывают, что антиоксидант может даже положительно влиять на продолжительность жизни.
Окислительное повреждение белка и ДНК
Окислительное повреждение белка
Белки могут подвергаться окислительной модификации тремя способами: окислительной модификацией конкретной аминокислоты, свободнорадикальным расщеплением пептида и образованием перекрестных связей белка из-за реакции с липидом продукты перекисного окисления.Белки, содержащие аминокислоты, такие как метионин, цистеин, аргинин и гистидин, по-видимому, наиболее уязвимы для окисления. [26] Модификация белков, опосредованная свободными радикалами, увеличивает восприимчивость к ферментному протеолизу. Окислительное повреждение белковых продуктов может повлиять на активность ферментов, рецепторов и мембранный транспорт. Белковые продукты, поврежденные окислением, могут содержать очень реактивные группы, которые могут способствовать повреждению мембраны и многих клеточных функций. Пероксильный радикал обычно считается разновидностью свободных радикалов для окисления белков.АФК могут повреждать белки и производить карбонилы и другие модификации аминокислот, включая образование сульфоксида метионина и карбонилов белка, и другие модификации аминокислот, включая образование сульфоксида метионина и пероксида белка. Окисление белков влияет на изменение механизма передачи сигнала, активности ферментов, термостабильности и восприимчивости к протеолизу, что приводит к старению.
Перекисное окисление липидов
Окислительный стресс и окислительная модификация биомолекул вовлечены в ряд физиологических и патофизиологических процессов, таких как старение, артеросклеоз, воспаление и канцерогенез, а также токсичность лекарств.Перекисное окисление липидов — это свободнорадикальный процесс, в котором участвует источник вторичных свободных радикалов, который, кроме того, может действовать как вторичный посредник или может напрямую реагировать с другой биомолекулой, усиливая биохимические поражения. Перекисное окисление липидов происходит на полинасыщенных жирных кислотах, расположенных на клеточных мембранах, и далее протекает по цепной радикальной реакции. Считается, что гидроксильный радикал инициирует АФК и удаляет атом водорода, таким образом образуя липидный радикал и затем превращаясь в диеновый конъюгат. Далее при добавлении кислорода он образует пероксильный радикал; этот высокореактивный радикал атакует другую жирную кислоту, образуя гидропероксид липида (LOOH) и новый радикал.Таким образом распространяется перекисное окисление липидов. В результате перекисного окисления липидов образуется ряд соединений, например алканы, маланоальдегид и изопротаны. Эти соединения используются в качестве маркеров в анализе перекисного окисления липидов и были проверены при многих заболеваниях, таких как нейрогенеративные заболевания, ишемическое реперфузионное повреждение и диабет. [27]
Окислительное повреждение ДНК
Многие эксперименты четко демонстрируют, что ДНК и РНК подвержены окислительному повреждению. Сообщалось, что ДНК считается основной мишенью, особенно при старении и раке.[28] Было обнаружено, что окислительные нуклеотиды, такие как гликоль, dTG и 8-гидрокси-2-дезоксигуанозин, повышаются во время окислительного повреждения ДНК под действием УФ-излучения или повреждения свободными радикалами. Сообщалось, что митохондриальная ДНК более восприимчива к окислительному повреждению, которое играет роль во многих заболеваниях, включая рак. Было высказано предположение, что 8-гидрокси-2-дезоксигуанозин можно использовать в качестве биологического маркера окислительного стресса. [29]
АНТИОКСИДАНТЫ
Антиоксидант — это молекула, достаточно стабильная, чтобы отдать электрон буйствующему свободному радикалу и нейтрализовать его, тем самым уменьшая его способность к повреждению.Эти антиоксиданты задерживают или ингибируют повреждение клеток, главным образом благодаря их способности улавливать свободные радикалы. [30] Эти низкомолекулярные антиоксиданты могут безопасно взаимодействовать со свободными радикалами и прекращать цепную реакцию до того, как будут повреждены жизненно важные молекулы. Некоторые из таких антиоксидантов, включая глутатион, убихинол и мочевую кислоту, вырабатываются в ходе нормального метаболизма в организме. [31] В рационе присутствуют и другие более легкие антиоксиданты. Хотя в организме есть несколько ферментных систем, которые удаляют свободные радикалы, основными микронутриентами (витаминами) и антиоксидантами являются витамин E (α-токоферол), витамин C (аскорбиновая кислота) и B-каротин.[32] Организм не может производить эти питательные микроэлементы, поэтому они должны поступать с пищей.
История
Термин «антиоксидант» первоначально использовался для обозначения химического вещества, предотвращающего потребление кислорода. В конце 19 — начале 20 века обширные исследования были посвящены использованию антиоксидантов в важных промышленных процессах, таких как предотвращение коррозии металлов, вулканизация резины и полимеризация топлива при загрязнении двигателей внутреннего сгорания.[33]
Ранние исследования роли антиоксидантов в биологии были сосредоточены на их использовании для предотвращения окисления ненасыщенных жиров, которое является причиной прогорклости. [34] Антиоксидантную активность можно было измерить, просто поместив жир в закрытый контейнер с кислородом и измерив скорость потребления кислорода. Однако именно идентификация витаминов А, С и Е как антиоксидантов произвела революцию в этой области и привела к осознанию важности антиоксидантов в биохимии живых организмов.[35,36] Возможные механизмы действия антиоксидантов были впервые исследованы, когда было признано, что вещество с антиоксидантной активностью, вероятно, само по себе легко окисляется. [37] Исследования того, как витамин E предотвращает процесс перекисного окисления липидов, привели к идентификации антиоксидантов как восстановителей, предотвращающих окислительные реакции, часто за счет удаления АФК до того, как они могут повредить клетки. [38]
Антиоксидантная защитная система
Антиоксиданты действуют как поглотители радикалов, доноры водорода, доноры электронов, разлагатели перекиси, гасители синглетного кислорода, ингибиторы ферментов, синергисты и хелатирующие металлы агенты.Как ферментные, так и неферментативные антиоксиданты существуют во внутриклеточной и внеклеточной среде для детоксикации АФК [39].
Механизм действия антиоксидантов
Было предложено два основных механизма действия антиоксидантов. [40] Первый — это механизм разрыва цепи, с помощью которого первичный антиоксидант отдает электрон свободному радикалу, присутствующему в системах. Второй механизм включает удаление инициаторов активных форм азота / активных форм азота (вторичных антиоксидантов) путем гашения катализатора, инициирующего цепь.Антиоксиданты могут оказывать свое влияние на биологические системы с помощью различных механизмов, включая донорство электронов, хелатирование ионов металлов, соантиоксиданты или регуляцию экспрессии генов. [41]
Уровни антиоксидантного действия
Антиоксиданты, действующие в защитных системах, действуют на разных уровнях, таких как профилактика, удаление радикалов, восстановление и de novo, а также четвертая линия защиты, то есть адаптация.
Первая линия защиты — профилактические антиоксиданты, подавляющие образование свободных радикалов.Хотя точный механизм и место образования радикалов in vivo еще недостаточно изучены, индуцированное металлами разложение гидропероксидов и пероксида водорода должно быть одним из важных источников. Чтобы подавить такие реакции, некоторые антиоксиданты заранее восстанавливают гидропероксиды и перекись водорода до спиртов и воды, соответственно, без образования свободных радикалов и некоторых белков, секвестрирующих ионы металлов.
Известно, что глутатионпероксидаза, глутатион-s-трансфераза, фосфолипидгидропероксид, глутатионпероксидаза (PHGPX) и пероксидаза разлагают гидропероксиды липидов до соответствующих спиртов.PHGPX уникален тем, что может восстанавливать гидропероксиды фосфолипидов, интегрированные в биомембраны. Глутатионпероксидаза и каталаза восстанавливают перекись водорода до воды.
Вторая линия защиты — это антиоксиданты, которые улавливают активные радикалы, подавляя инициирование цепи и / или прерывая реакции роста цепи. Известны различные эндогенные антиоксиданты, улавливающие радикалы: некоторые из них являются гидрофильными, а другие — липофильными. Витамин C, мочевая кислота, билирубин, альбумин и тиолы являются гидрофильными антиоксидантами, улавливающими радикалы, в то время как витамин E и убихинол являются липофильными антиоксидантами, улавливающими радикалы.Витамин Е считается наиболее мощным липофильным антиоксидантом, улавливающим радикалы.
Третья линия защиты — это ремонт и de novo антиоксидантов. Протеолитические ферменты, протеиназы, протеазы и пептидазы, присутствующие в цитозоле и митохондриях клеток млекопитающих, распознают, разлагают и удаляют окислительно модифицированные белки и предотвращают накопление окисленных белков.
Системы репарации ДНК также играют важную роль в общей системе защиты от окислительного повреждения.Известны различные виды ферментов, таких как гликозилазы и нуклеазы, которые восстанавливают поврежденную ДНК.
Существует еще одна важная функция, называемая адаптацией, когда сигнал для производства и реакции свободных радикалов индуцирует образование и транспортировку соответствующего антиоксиданта в нужное место. [42]
ENZYMATIC
Типы антиоксидантов
Клетки защищены от окислительного стресса взаимодействующей сетью антиоксидантных ферментов. [43] Здесь супероксид, высвобождаемый в результате таких процессов, как окислительное фосфорилирование, сначала превращается в перекись водорода, а затем восстанавливается с образованием воды.Этот путь детоксикации является результатом действия множества ферментов: супероксиддисмутазы катализируют первую стадию, а затем каталазы и различные пероксидазы удаляют перекись водорода. [44]
Супероксиддисмутаза
Супероксиддисмутазы (SOD) — это класс близкородственных ферментов, которые катализируют распад супероксид-аниона на кислород и перекись водорода. [45,46] Ферменты SOD присутствуют почти во всех аэробных клетках и во внеклеточных жидкостях. . [47] Существует три основных семейства супероксиддисмутазы, в зависимости от кофактора металла: Cu / Zn (который связывает медь и цинк), типы Fe и Mn (которые связывают железо или марганец) и, наконец, тип Ni, который связывает никель.[48] У высших растений изоферменты СОД локализованы в различных клеточных компартментах. Mn-SOD присутствует в митохондриях и пероксисомах. Fe-SOD был обнаружен в основном в хлоропластах, но также был обнаружен в пероксисомах, а CuZn-SOD был локализован в цитозоле, хлоропластах, пероксисомах и апопластах. [48–50]
У людей (как и у всех других млекопитающих и других млекопитающих). большинство хордовых) присутствуют три формы супероксиддисмутазы. SOD1 находится в цитоплазме, SOD2 — в митохондриях, а SOD3 — внеклеточный.Первый — димер (состоит из двух звеньев), остальные — тетрамеры (четыре субъединицы). SOD1 и SOD3 содержат медь и цинк, в то время как SOD2 имеет марганец в его реактивном центре. [51]
Каталаза
Каталаза — это обычный фермент, обнаруженный почти во всех живых организмах, которые подвергаются воздействию кислорода, где он действует, чтобы катализировать разложение перекиси водорода до воды и кислорода. [52] Перекись водорода является вредным побочным продуктом многих нормальных метаболических процессов: чтобы предотвратить повреждение, ее необходимо быстро преобразовать в другие, менее опасные вещества.С этой целью клетки часто используют каталазу, чтобы быстро катализировать разложение перекиси водорода на менее реактивные газообразные молекулы кислорода и воды. [53] Все известные животные используют каталазу во всех органах, особенно в печени. [54]
Системы глутатиона
Система глутатиона включает глутатион, глутатионредуктазу, пероксидазы глутатиона и S-трансферазы глутатиона. Эта система обнаружена у животных, растений и микроорганизмов.[55] Глутатионпероксидаза — это фермент, содержащий четыре кофактора селена, которые катализируют распад перекиси водорода и органических гидропероксидов. У животных существует по крайней мере четыре различных изофермента глутатионпероксидазы. [56] Глутатионпероксидаза 1 является наиболее распространенным и очень эффективным поглотителем перекиси водорода, в то время как глутатионпероксидаза 4 наиболее активна с гидропероксидами липидов. S-трансферазы глутатиона проявляют высокую активность в отношении перекисей липидов. Эти ферменты находятся на особенно высоком уровне в печени и также участвуют в детоксикационном метаболизме.[57]
НЕФЕНЗИМАТИЧЕСКАЯ
Аскорбиновая кислота
Аскорбиновая кислота или «витамин С» представляет собой моносахаридный антиоксидант, обнаруженный как у животных, так и у растений. Поскольку он не может быть синтезирован в организме человека и должен быть получен с пищей, это витамин. [58] Большинство других животных способны вырабатывать это соединение в своем организме и не нуждаются в нем в своем рационе. В клетках он поддерживается в восстановленной форме за счет реакции с глутатионом, которая может катализироваться протеиндисульфидизомеразой и глутаредоксинами.[59] Аскорбиновая кислота является восстанавливающим агентом и может снижать и тем самым нейтрализовать АФК, такие как перекись водорода. [60] Помимо своего прямого антиоксидантного действия, аскорбиновая кислота также является субстратом для антиоксидантного фермента аскорбатпероксидазы, функции, которая особенно важна для устойчивости растений к стрессу [61].
Глутатион
Глутатион — цистеинсодержащий пептид, встречающийся в большинстве форм аэробной жизни. [62] Он не требуется в диете и вместо этого синтезируется в клетках из составляющих его аминокислот.Глутатион обладает антиоксидантными свойствами, поскольку тиоловая группа в его цистеиновой части является восстанавливающим агентом и может обратимо окисляться и восстанавливаться. В клетках глутатион поддерживается в восстановленной форме ферментом глутатионредуктазой и, в свою очередь, восстанавливает другие метаболиты и ферментные системы, а также вступает в непосредственную реакцию с оксидантами. [63] Из-за своей высокой концентрации и центральной роли в поддержании окислительно-восстановительного состояния клетки глутатион является одним из важнейших клеточных антиоксидантов [33]. У некоторых организмов глутатион заменяется другими тиолами, например, микотиолом в актиномицетах или трипанотионом в кинетопластидах.[64]
Мелатонин
Мелатонин, также известный как N-ацетил-5-метокситриптамин, [65] является естественным гормоном, обнаруженным у животных и некоторых других живых организмов, включая водоросли. [66] Мелатонин — мощный антиоксидант, который может легко проникать через клеточные мембраны и гематоэнцефалический барьер. [67] В отличие от других антиоксидантов, мелатонин не подвергается окислительно-восстановительному циклу, то есть способности молекулы подвергаться многократному восстановлению и окислению. После окисления мелатонин не может быть восстановлен до прежнего состояния, потому что он образует несколько стабильных конечных продуктов при взаимодействии со свободными радикалами.Поэтому его называют терминальным (или суицидным) антиоксидантом. [68]
Токоферолы и токотриенолы (витамин E)
Витамин E — это собирательное название набора из восьми родственных токоферолов и токотриенолов, которые представляют собой жирорастворимые витамины с антиоксидантными свойствами. [69] Из них альфа-токоферол наиболее изучен, так как он имеет наивысшую биодоступность, причем организм преимущественно абсорбирует и метаболизирует эту форму [70]. Было заявлено, что форма α-токоферола является наиболее важным жирорастворимым антиоксидантом и что она защищает мембраны от окисления, реагируя с липидными радикалами, образующимися в цепной реакции перекисного окисления липидов.[71] Это удаляет промежуточные продукты свободных радикалов и предотвращает продолжение реакции распространения. В результате этой реакции образуются окисленные α-токофероксильные радикалы, которые могут быть возвращены обратно в активную восстановленную форму путем восстановления другими антиоксидантами, такими как аскорбат, ретинол или убихинол. [72]
Мочевая кислота
Мочевая кислота составляет примерно половину антиоксидантной способности плазмы. Фактически, мочевая кислота могла заменить аскорбат в эволюции человека. [73] Однако, как и аскорбат, мочевая кислота также может опосредовать производство активных форм кислорода.
РАСТЕНИЯ КАК ИСТОЧНИК АНТИОКСИДАНТОВ
Синтетические и натуральные пищевые антиоксиданты обычно используются в пищевых продуктах и медицине, особенно в тех, которые содержат масла и жиры, для защиты пищевых продуктов от окисления. Яркими примерами являются ряд синтетических фенольных антиоксидантов, среди которых бутилированный гидрокситолуол (ВНТ) и бутилированный гидроксианизол (ВНА). Эти соединения широко используются в качестве антиоксидантов в пищевой, косметической и терапевтической промышленности. Однако некоторые физические свойства BHT и BHA, такие как их высокая летучесть и нестабильность при повышенных температурах, строгое законодательство по использованию синтетических пищевых добавок, канцерогенная природа некоторых синтетических антиоксидантов и предпочтения потребителей сместили внимание производителей с синтетических на натуральные. антиоксиданты.[74] Ввиду увеличения факторов риска для человека различных смертельных заболеваний, во всем мире наблюдается тенденция к использованию натуральных веществ, присутствующих в лекарственных растениях и пищевых добавках, в качестве терапевтических антиоксидантов. Сообщается, что существует обратная зависимость между потреблением с пищей богатой антиоксидантами пищи и лекарственных растений и заболеваемостью людей. Использование природных антиоксидантов в пищевой, косметической и терапевтической промышленности было бы многообещающей альтернативой синтетическим антиоксидантам в отношении низкой стоимости, высокой совместимости с диетическим потреблением и отсутствия вредного воздействия на организм человека.Многие антиоксидантные соединения, встречающиеся в природе в растительных источниках, были идентифицированы как поглотители свободных радикалов или активного кислорода. [75] Были предприняты попытки изучить антиоксидантный потенциал самых разных овощей, таких как картофель, шпинат, помидоры и бобовые. [76] Есть несколько отчетов, показывающих антиоксидантный потенциал фруктов. [77] Сильная антиоксидантная активность обнаружена в ягодах, вишне, цитрусовых, черносливе и оливках. В недавнем прошлом зеленый и черный чаи широко изучались на предмет антиоксидантных свойств, поскольку они содержат до 30% от сухого веса в виде фенольных соединений.[78]
Помимо пищевых источников, индийские лекарственные растения также содержат антиоксиданты, в том числе (с общепринятыми / аюрведическими названиями в скобках) Acacia catechu (kair), Aegle marmelos (бенгальская айва, Бельгия), Allium cepa (лук), A. sativum (чеснок, Лахасуна), Aleo vera (индейское алоэ, Ghritkumari), Amomum subulatum (большой кардамон, Bari elachi), Andrographis paniculata, Recemosus (Шатавари), Azadirachta indica (Ним, Нимба), Bacopa monniera (Брахми), Butea monosperma (Палас, Дак), Camellia sinensis Cinnum (зеленый чай) (зеленый чай) , Cinnamomum tamala (Теджпат), Curcma longa (Куркума, Харидра), Emblica officinalis (Инхийский крыжовник, Амлаки), Glycyrrhiza glapra (Яштимуду), Hemudhu an Sarasparilla, Anantamul), Indigofera tinctoria, Mangifera indica (манго, амра), Momordica charantia (горькая тыква), Murraya koenigii (лист карри), Nigella sativa , Nigella sativa (черный тмин) (Святой базилик, Тусил), Onosma echioides (Ratanjyot), Picrorrhiza kurroa (Katuka), Жук-волынщик, Plumbago zeylancia (Chitrak), Sesamum indicum, Sidaul cordifolia, Sesamum indicum, Sidaul cordifolia, , Syzigium cumini (Jamun), Terminalia ariuna (Арджун), Terminalia bellarica (Beheda), Tinospora cordifolia (лунное семя с сердечными листьями, Guduchi), Trigonella foenum-graecium (Fenomifereek ) (Fenomifereek ) Зимняя вишня, Ашванганда) и Zingiber officinalis (имбирь).[79]
АНТИОКСИДАНТНЫЙ ПОТЕНЦИАЛ ИНДИЙСКИХ ФУНКЦИОНАЛЬНЫХ ПРОДУКТОВ
Концепции функциональных пищевых продуктов и нутрицевтиков
За последнее десятилетие профилактическая медицина значительно продвинулась вперед, особенно в развитых странах. Исследования показали, что питание играет решающую роль в предотвращении хронических заболеваний, поскольку большинство из них может быть связано с диетой. Функциональное питание входит в концепцию рассмотрения пищи не только необходимой для жизни, но и как источника психического и физического благополучия, способствуя предотвращению и уменьшению факторов риска для некоторых заболеваний или усилению определенных физиологических функций.[80] Пища может считаться функциональной, если доказано, что она благотворно влияет на одну или несколько целевых функций в организме, помимо адекватного пищевого воздействия, таким образом, который имеет отношение либо к состоянию самочувствия и здоровья, либо к снижению риск заболевания. Благоприятные эффекты могут заключаться в поддержании или улучшении самочувствия или здоровья и / или в снижении риска патологического процесса или заболевания [81]. Цельные продукты представляют собой простейший пример функционального питания.Брокколи, морковь и помидоры считаются функциональными продуктами питания из-за высокого содержания в них физиологически активных компонентов (сульфорафена, B-каротина и ликопина соответственно). Зеленые овощи и специи, такие как горчица и куркума, широко используемые в индийской кухне, также могут подпадать под эту категорию. [82] «Нутрицевтики» — это термин, придуманный в 1979 году Стивеном ДеФелисом [83]. Он определяется «как продукт питания или его части, которые обеспечивают медицинские преимущества или пользу для здоровья, включая профилактику и лечение заболеваний.«Нутрицевтики могут варьироваться от изолированных питательных веществ, пищевых добавок и диет до генетически модифицированных« дизайнерских »продуктов питания, растительных продуктов и продуктов переработки, таких как хлопья, супы и напитки. Нутрицевтики — это любые нетоксичные пищевые экстракты, которые обладают научно доказанной пользой для здоровья как для лечения, так и для профилактики заболеваний. [84] Растущий интерес к нутрицевтикам отражает тот факт, что потребители слышат об эпидемиологических исследованиях, указывающих на то, что конкретная диета или компонент диеты связаны с более низким риском развития определенного заболевания.Основными активными нутрицевтическими ингредиентами растений являются флавоноиды. Как это типично для фенольных соединений, они могут действовать как мощные антиоксиданты и хелаторы металлов. Также давно признано, что они обладают противовоспалительным, противоаллергическим, гепатопротекторным, антитромботическим, противовирусным и антиканцерогенным действием [85].
Индийские диетические и лекарственные растения как функциональные продукты
Ингредиенты, которые делают пищу функциональной, — это пищевые волокна, витамины, минералы, антиоксиданты, олигосахариды, незаменимые жирные кислоты (омега-3), культуры молочнокислых бактерий и лигнины.Многие из них присутствуют в лекарственных растениях. Индийские системы медицины считают, что сложные заболевания можно лечить с помощью сложной комбинации ботанических средств, в отличие от западных, с помощью отдельных лекарств. Таким образом, цельные продукты используются в Индии как функциональные продукты, а не как добавки. Некоторые лекарственные растения и диетические компоненты, обладающие функциональными свойствами, представляют собой специи, такие как лук, чеснок, горчица, красный перец чили, куркума, гвоздика, корица, шафран, лист карри, пажитник и имбирь. Некоторые травы, такие как Bixa orellana, и овощи, такие как амла, пшеница, соевые бобы и Gracinia cambogia, обладают противоопухолевым действием.Другие лекарственные растения с функциональными свойствами включают A.marmelos, A. cepa, Aloe vera, A. paniculata, Azadirachta india и Brassica juncea. [86]
ЗАКЛЮЧЕНИЕ
Повреждение свободными радикалами вносит вклад в этиологию многих хронических проблем со здоровьем, таких как сердечно-сосудистые и воспалительные заболевания, катаракта и рак. Антиоксиданты предотвращают повреждение тканей, вызванное свободными радикалами, предотвращая образование радикалов, удаляя их или способствуя их разложению. Недавно сообщалось, что синтетические антиоксиданты опасны для здоровья человека.Таким образом, в последние годы активизировался поиск эффективных нетоксичных природных соединений с антиоксидантной активностью. В дополнение к системам эндогенной антиоксидантной защиты, потребление диетических антиоксидантов и антиоксидантов растительного происхождения, по-видимому, является подходящей альтернативой. Пищевые и другие компоненты растений являются основным источником антиоксидантов. Традиционная индийская диета, специи и лекарственные растения являются богатыми источниками природных антиоксидантов; более высокое потребление продуктов с функциональными характеристиками, включая высокий уровень антиоксидантов и антиоксидантов в функциональных продуктах питания, является одной из стратегий, которая приобретает все большее значение.
Новые подходы, использующие совместные исследования и современные технологии в сочетании с устоявшимися традиционными принципами здоровья, в ближайшем будущем принесут дивиденды в улучшении здоровья, особенно среди людей, которые не имеют доступа к использованию более дорогих западных систем медицины.
Сноски
Источник поддержки: Нет
Конфликт интересов: Не заявлено
ССЫЛКИ
1. Aruoma OI. Методологические соображения для характеристики потенциального антиоксидантного действия биоактивных компонентов в растительной пище.Mutat Res. 2003; 532: 9–20. [PubMed] [Google Scholar] 2. Мохаммед А.А., Ибрагим А.А. Патологические роли активных форм кислорода и их защитный механизм. Сауди Фарм Дж. 2004; 12: 1–18. [Google Scholar] 3. Багчи К., Пури С. Свободные радикалы и антиоксиданты в здоровье и болезнях. East Mediterranean Health Jr. 1998; 4: 350–60. [Google Scholar] 4. Aruoma OI. Аспекты свободных радикалов и антиоксидантов, связанные с питанием и здоровьем. Food Chem Toxicol. 1994; 32: 671–83. [PubMed] [Google Scholar] 5. Чизмен К.Х., Слейтер Т.Ф.Введение в химию свободных радикалов. Br Med Bull. 1993; 49: 481–93. [PubMed] [Google Scholar] 7. Лю Т., Стерн А., Робертс Л.Дж. Изопростаны: новые простангландиноподобные продукты перекисного окисления арахидоновой кислоты, катализируемого свободными радикалами. J Biomed Sci. 1999; 6: 226–35. [PubMed] [Google Scholar] 8. Эбади М. Антиоксиданты и свободные радикалы в здоровье и болезнях: Введение в активные формы кислорода, окислительное повреждение, гибель нейрональных клеток и терапию нейродегенеративных заболеваний. Аризона: видная пресса; 2001 г.[Google Scholar] 9. Lea AJ. Факторы питания, связанные с уровнем смертности от некоторых новообразований у человека. Ланцет. 1966; 2: 332–3. [PubMed] [Google Scholar] 10. Харман Д. Роль свободных радикалов в старении и болезнях. Ann N Y Acad Sci. 1992; 673: 126–41. [PubMed] [Google Scholar] 11. Сис Х. Окислительный стресс: Вступительное слово. В: Sies H, редактор. Окислительный стресс. Сан-Диего: Academic Press; 1985. С. 1–7. [Google Scholar] 12. Докампо Р. Антиоксидантные механизмы. В: Марр Дж., Мюллер М., редакторы. Биохимия и молекулярная биология паразитов.Лондон: Academic Press; 1995. С. 147–60. [Google Scholar] 13. Райс-Эванс К.А., Гопинатан В. Кислородная токсичность, свободные радикалы и антиоксиданты при заболеваниях человека: биохимические последствия атеросклероза и проблемы недоношенных новорожденных. Очерки Биохимии. 1995; 29: 39–63. [PubMed] [Google Scholar] 14. Rock CL, Джейкоб Р.А., Боуэн ЧП. Обновление биологических характеристик антиоксидантных микроэлементов — витамина С, витамина Е и каротиноидов. J Am Diet Assoc. 1996; 96: 693–702. [PubMed] [Google Scholar] 15.Mc Cord JM. Эволюция свободных радикалов и окислительного стресса. Am J Med. 2000; 108: 652–9. [PubMed] [Google Scholar] 16. Рао А.Л., Бхарани М., Паллави В. Роль антиоксидантов и свободных радикалов в здоровье и болезнях. Adv Pharmacol Toxicol. 2006; 7: 29–38. [Google Scholar] 17. Стефанис Л., Берк Р. Э., Грин Л. А.. Апоптоз при нейродегенеративных расстройствах. Curr Opin Neurol. 1997. 10: 299–305. [PubMed] [Google Scholar] 18. Эстербауэр Х., Пуби Х., Дибер-Ротендер М. Влияние антиоксидантов на окислительную модификацию ЛПНП.Ann Med. 1991; 23: 573–81. [PubMed] [Google Scholar] 19. Neuzil J, Thomas SR, Stocker R. Требование к стимулированию или ингибированию α-токоферола радикально индуцированного инициирования перекисного окисления липопротеинов плазмы. Free Radic Biol Med. 1997; 22: 57–71. [PubMed] [Google Scholar] 20. Поппель Г.В., Гольддбом РА. Эпидемиологические данные о β — каротине и профилактике рака. Am J Clin Nutr. 1995; 62: 1393–5. [PubMed] [Google Scholar] 21. Glatthaar BE, Horing DH, Moser U. Роль аскорбиновой кислоты в канцерогенезе.Adv Exp Med Biol. 1986; 206: 357–77. [PubMed] [Google Scholar] 22. Сокол РЖ. Дефицит витамина Е и неврологические заболевания. Анну Рев Нутр. 1988. 8: 351–73. [PubMed] [Google Scholar] 23. Ашок Б.Т., Али Р. Парадокс старения: свободнорадикальная теория старения. Exp Gerontol. 1999; 34: 293–303. [PubMed] [Google Scholar] 24. Састре Дж, Пеллардо Ф.В., Вина Дж. Глутатион, окислительный стресс и старение. Возраст. 1996; 19: 129–39. [Google Scholar] 25. Кантути-Кастельветри I, Шукитт-Хейл Б., Джозеф Дж. А. Нейроповеденческие аспекты антиоксидантов при старении.Int J Dev Neurosci. 2000; 18: 367–81. [PubMed] [Google Scholar] 26. Фримен Б.А., Крапо Д.Д. Биология болезни: свободные радикалы и повреждение тканей. Lab Invest. 1982; 47: 412–26. [PubMed] [Google Scholar] 27. Ловелл М.А., Эманн В.Д., Buffer BM, Markesberry WR. Повышение реакционноспособности тиобарбитуровой кислоты и активности антиоксидантных ферментов в головном мозге при болезни Альземерса. Неврология. 1995; 45: 1594–601. [PubMed] [Google Scholar] 28. Ву Р.А., Мелур К.Г., Ли П.В. ДНК-зависимая протеинкиназа действует выше р53 в ответ на повреждение ДНК.Природа. 1998. 394: 700–4. [PubMed] [Google Scholar] 29. Hattori Y, Nishigori C, Tanaka T., Ushida K, Nikaido O, Osawa T. 8 Гидрокси-2-дезоксигуанозин увеличивается в эпидермальных клетках бесшерстных мышей после хронического воздействия ультрафиолета B. J Invest Dermatol. 1997; 89: 10405–9. [PubMed] [Google Scholar] 30. Холливелл Б. Как охарактеризовать антиоксидант — обновленная информация. Biochem Soc Symp. 1995; 61: 73–101. [PubMed] [Google Scholar] 31. Ши Х.Л., Ногучи Н., Ники Н. Сравнительное исследование динамики антиоксидантного действия α-токоферилгидрохинона, убихинола и α-токоферола против перекисного окисления липидов.Free Radic Biol Med. 1999; 27: 334–46. [PubMed] [Google Scholar] 32. Левин М., Рэмси С.К., Дарувара Р. Критерии и рекомендации по потреблению витамина С. ДЖАМА. 1991; 281: 1415–23. [PubMed] [Google Scholar] 34. Герман Дж. Пищевая промышленность и окисление липидов. Adv Exp Med Biol. 1999; 459: 23–50. [PubMed] [Google Scholar] 35. Джейкоб Р. Три эпохи открытия витамина С. Subcell Biochem. 1996; 25: 1–16. [PubMed] [Google Scholar] 36. Найт Дж. Свободные радикалы: их история и текущее состояние при старении и болезнях. Ann Clin Lab Sci.1998. 28: 331–46. [PubMed] [Google Scholar] 37. Моро, Dufraisse Comptes Rendus des Séances et Mémoires de la Société de Biologie. 1922; 86: 321. [Google Scholar] 38. Вольф Г. Открытие антиоксидантной функции витамина Е: вклад Генри А. Маттилла. J Nutr. 2005. 135: 363–6. [PubMed] [Google Scholar] 39. Frie B, Stocker R, Ames BN. Антиоксидантная защита и перекисное окисление липидов в плазме крови человека. Proc Natl Acad Sci. 1988; 37: 569–71. [Google Scholar] 40. Райс-Эванс CA, Diplock AT. Текущее состояние антиоксидантной терапии.Free Radic Biol Med. 1993; 15: 77–96. [PubMed] [Google Scholar] 41. Кринский Н.И. Механизм действия биологических антиоксидантов. Proc Soc Exp Biol Med. 1992; 200: 248–54. [PubMed] [Google Scholar] 42. Ники Э. Антиоксидантная защита в эукариотических клетках. В: Poli G, Albano E, Dianzani MU, редакторы. Свободные радикалы: от фундаментальной науки до медицины. Базель, Швейцария: Birkhauser Verlag; 1993. С. 365–73. [Google Scholar] 43. Сис Х. Окислительный стресс: окислители и антиоксиданты. Exp Physiol. 1997; 82: 291–5. [PubMed] [Google Scholar] 44.Магненат Дж. Л., Гарганоам М., Цао Дж. Природа механизмов антиоксидантной защиты: урок трансгенных исследований. Перспектива здоровья окружающей среды. 1998. 106: 1219–28. [Бесплатная статья PMC] [PubMed] [Google Scholar] 45. Зелко И., Мариани Т., Фольц Р. Мультигенное семейство супероксиддисмутазы: сравнение структур, эволюции и экспрессии генов CuZn-SOD (SOD1), Mn-SOD (SOD2) и EC-SOD (SOD3). Free Radic Biol Med. 2002; 33: 337–49. [PubMed] [Google Scholar] 46. Баннист Дж., Баннистер В., Ротилио Г. Аспекты структуры, функции и применения супероксиддисмутазы.CRC Crit Rev Biochem. 1987; 22: 111–80. [PubMed] [Google Scholar] 47. Джонсон Ф., Джуливи С. Супероксиддисмутазы и их влияние на здоровье человека. Мол Аспекты Мед. 2005; 26: 340–52. [PubMed] [Google Scholar] 48. Wuerges J, Lee JW, Yim YI, Yim HS, Kang SO, Djinovic Carugo K. Кристаллическая структура никельсодержащей супероксиддисмутазы выявляет другой тип активного центра. Proc Natl Acad Sci. 2004. 101: 8569–74. [Бесплатная статья PMC] [PubMed] [Google Scholar] 49. Corpas FJ, Barroso JB, дель Рио, Лос-Анджелес. Пероксисомы как источник активных форм кислорода и сигнальных молекул оксида азота в растительных клетках.Trends Plant Sci. 2001; 6: 145–50. [PubMed] [Google Scholar] 50. Corpas FJ, Fernández-Ocaña A, Carreras A, Valderrama R, Luque F, Esteban FJ, et al. Экспрессия различных форм супероксиддисмутазы зависит от типа клеток в листьях оливы (Olea europaea L.). Physiol растительной клетки. 2006; 47: 984–94. [PubMed] [Google Scholar] 51. Цао Х, Антонюк С.В., Ситараман С.В., Уитсон Л.Дж., Тейлор А.Б., Холлоуэй С.П. и др. Структуры варианта SOD1 G85R при семейном боковом амиотрофическом склерозе. J Biol Chem.2008. 283: 16169–77. [Бесплатная статья PMC] [PubMed] [Google Scholar] 52. Chelikani P, Fita I, Loewen PC. Разнообразие структур и свойств каталаз. Cell Mol Life Sci. 2004. 61: 192–208. [PubMed] [Google Scholar] 53. Гаэтани Г., Феррарис А., Рольфо М., Мангерини Р., Арена С., Киркман Х. Преобладающая роль каталазы в утилизации перекиси водорода в человеческих эритроцитах. Кровь. 1996; 87: 1595–9. [PubMed] [Google Scholar] 55. Мейстер А., Андерсон М. Глутатион. Анну Рев Биохим. 1983; 52: 711–60. [PubMed] [Google Scholar] 56.Бригелиус-Флоэ Р. Тканеспецифические функции индивидуальных пероксидаз глутатиона. Free Radic Biol Med. 1999; 27: 951–65. [PubMed] [Google Scholar] 57. Hayes J, Flanagan J, Jowsey I. Трансферазы глутатиона. Annu Rev Pharmacol Toxicol. 2005. 45: 51–88. [PubMed] [Google Scholar] 58. Смирнов Н. Биосинтез L-аскорбиновой кислоты. Vitam Horm. 2001; 61: 241–66. [PubMed] [Google Scholar] 59. Мейстер А. Антиоксидантная система глутатион-аскорбиновая кислота у животных. J Biol Chem. 1994; 269: 9397–400. [PubMed] [Google Scholar] 60.Padayatty S, Katz A, Wang Y, Eck P, Kwon O, Lee J и др. Витамин С как антиоксидант: оценка его роли в профилактике заболеваний. J Am Coll Nutr. 2003. 22: 18–35. [PubMed] [Google Scholar] 61. Шигеока С., Исикава Т., Тамой М., Миягава Ю., Такеда Т., Ябута Ю. и др. Регуляция и функция изоферментов аскорбатпероксидазы. J Exp Bot. 2002; 53: 1305–19. [PubMed] [Google Scholar] 62. Мейстер А., Андерсон А. Глутатион. Анну Рев Биохим. 1983; 52: 711–60. [PubMed] [Google Scholar] 63. Мейстер А. Метаболизм глутатиона и его селективная модификация.J Biol Chem. 1988; 263: 17205–8. [PubMed] [Google Scholar] 64. Fairlamb AH, Cerami A. Метаболизм и функции трипанотиона в кинетопластиде. Annu Rev Microbiol. 1992; 46: 695–729. [PubMed] [Google Scholar] 65. Нассар Э., Маллиган С., Тейлор Л., Керксик С., Галбрит М., Гринвуд М. и др. Влияние однократной дозы N-ацетил-5-метокситриптамина (мелатонина) и упражнений с отягощениями на ось гормона роста / IGF-1 у молодых мужчин и женщин. J Int Soc Sports Nutr. 2007; 4: 14. [Бесплатная статья PMC] [PubMed] [Google Scholar] 66.Каниато Р., Филиппини Р., Пиован А., Пуричелли Л., Борсарини А., Каппеллетти Е. Мелатонин в растениях. Adv Exp Med Biol. 2003. 527: 593–7. [PubMed] [Google Scholar] 67. Рейтер Р. Дж., Карнейро Р. К., О, CS. Мелатонин в отношении механизмов антиоксидантной защиты клеток. Horm Metab Res. 1997; 29: 363–72. [PubMed] [Google Scholar] 68. Tan DX, Manchester LC, Reiter RJ, Qi WB, Karbownik M, Calvo JR. Значение мелатонина в системе антиоксидантной защиты: реакции и продукты. Прием сигналов Биол. 2000; 9: 137–59.[PubMed] [Google Scholar] 69. Эррера Э, Барбас С. Витамин Е: действие, метаболизм и перспективы. J Physiol Biochem. 2001; 57: 43–56. [PubMed] [Google Scholar] 70. Бригелиус-Флоэ Р., Трабер М. Витамин Е: функция и метаболизм. FASEB J. 1999; 13: 1145–55. [PubMed] [Google Scholar] 72. Ван X, Куинн П. Витамин Е и его функция в мембранах. Prog Lipid Res. 1999. 38: 309–36. [PubMed] [Google Scholar] 73. Jaeschke H, Gores GJ, Cederbaum AI, Hinson JA, Pessayre D, Lemasters JJ. Механизмы гепатотоксичности.Toxicol Sci. 2002; 65: 166–76. [PubMed] [Google Scholar] 74. Папас AM. Диета и антиоксидантный статус. Food Chem Toxicol. 1999; 37: 999–1007. [PubMed] [Google Scholar] 75. Браун Дж. Э., Райс-Эван CA. Богатый лютеолином экстракт артишока защищает липопротеины низкой плотности от окисления in vitro. Free Radic Res. 1998. 29: 247–255. [PubMed] [Google Scholar] 76. Фурута С., Нишиба Ю., Суда И. Флуорометрический анализ для скрининга антиоксидантной активности овощей. J Food Sci. 1997; 62: 526–8. [Google Scholar] 77. Ван Х, Цао Джи, Приор Р.Л.Общая антиоксидантная способность плодов. J. Agric Food Chem. 1996; 44: 701–5. [Google Scholar] 78. Lin JK, Lin CH, Ling YC, Lin-Shian SY, Juan IM. Обзор катехинов, галловой кислоты и метилксантинов в зеленом, улун, пуэре и черном чае. J. Agric Food Chem. 1998. 46: 3635–42. [Google Scholar] 79. Девасагаям Т.П., Тилак Дж.С., Болур К.К., Сане К.С., Гаскадби С.С., Леле Р.Д. Свободные радикалы и антиоксиданты в здоровье человека: текущее состояние и перспективы на будущее. J Assoc Physitors Индия. 2004. 52: 794–803. [PubMed] [Google Scholar] 80.Лопес-Варела С., Гонсалес-Гросс М., Маркос А. Функциональные продукты питания и иммунная система: обзор. Eur J Clin Nutr. 2002; 56: S29–33. [PubMed] [Google Scholar] 81. Роберфроид МБ. Что полезно для здоровья? Понятие о функциональном питании. Food Chem Toxicol. 1999; 37: 1034–41. [PubMed] [Google Scholar] 82. Кришнасвами К. Индийское функциональное питание: роль в профилактике рака. Nutr Rev.1996; 54: 127–31. [PubMed] [Google Scholar] 83. DeFelice SL. Нутрицевтики: возможности на развивающихся рынках. Scrip Mag.1992; 9: 14–5. [Google Scholar] 84. Диллард CJ, немецкий JB. Фитохимические вещества: нутрицевтики и здоровье человека. J Sci Food Agric. 2000; 80: 1744–56. [Google Scholar] 85. Tapas AR, Sakarkar DM, Kakde RB. Обзорная статья флавоноиды как нутрицевтики: обзор. Trop J Pharm Res. 2008; 7: 1089–99. [Google Scholar]Антиоксидантные эффекты для здоровья
Антиоксиданты, как и прооксиданты, вызывающие окислительное повреждение, играют важную роль в здоровье и болезнях людей. Некоторые из основных полезных ролей включают в себя профилактику и лечение заболеваний.
Профилактика заболеваний антиоксидантами
В организме есть несколько антиоксидантных систем, которые помогают справиться с окислительным стрессом, возникающим в результате регулярных метаболических процессов. Антиоксиданты в диете также могут нейтрализовать повреждающее клетки действие свободных радикалов. Эти антиоксидантные добавки действуют в дополнение к эндогенным системам, и их недостаток может вызвать несколько пагубных последствий окислительного стресса.
Есть свидетельства того, что некоторые виды овощей и фруктов защищают от ряда видов рака и других заболеваний.Крупные исследования показали, что люди, которые регулярно принимали антиоксиданты из фруктов и овощей, по-видимому, реже страдали этими заболеваниями. Кроме того, те, кто принимал меньшее количество антиоксидантов или подвергался чрезмерному воздействию прооксидантов, таких как курение сигарет и т. Д., Имели более высокий риск этих расстройств.
Например, окисление липопротеинов низкой плотности (ЛПНП) в крови способствует сердечным заболеваниям. Те, кто принимал добавки с витамином Е, имели более низкий риск развития сердечных заболеваний.
Однако точное количество антиоксидантных добавок и их точную профилактическую роль определить не удалось. Это означало, что некоторые люди действительно болели раком и другими расстройствами, связанными с окислительным стрессом, несмотря на адекватное потребление фруктов и овощей и антиоксидантов.
Для профилактики сердечных заболеваний, например, было проведено семь крупных клинических испытаний, чтобы проверить эффекты антиоксидантной добавки с витамином Е в дозах от 50 до в день. Ни одно из этих испытаний не выявило статистически значимого влияния витамина Е на общее количество смертей или смертей от сердечных заболеваний.
При этом есть несколько незаменимых витаминов, минералов и антиоксидантов, включая ресвератрол (из виноградных косточек или корней спорыша), бета-каротин (провитамин А), витамин С, витамин Е и селен или травы, содержащие антиоксиданты, такие как зеленый чай. и цзяогулан.
Лечение болезней антиоксидантами
Некоторые жизненно важные органы, такие как сердце, легкие и мозг, уязвимы для окислительного повреждения. В частности, мозг уязвим из-за высокого содержания кислорода, высокой скорости метаболизма и повышенного уровня полиненасыщенных липидов — мишени перекисного окисления липидов.
Доступно несколько антиоксидантных добавок для лечения нервных повреждений при окислительном стрессе. Повреждение головного мозга может привести к повреждению его частей после инсульта, болезни Альцгеймера, болезни Паркинсона и других нейродегенеративных расстройств. Например, после инсульта мозг подвергается реперфузионному повреждению, вызванному окислительным стрессом.
Миметики супероксиддисмутазы, тиопентал натрия и пропофол используются для лечения реперфузионного повреждения и черепно-мозговой травмы, в то время как экспериментальный препарат NXY-059 и эбселен применяются для лечения инсульта.Эти соединения, по-видимому, предотвращают окислительный стресс в нейронах. Они помогают предотвратить гибель нервных клеток.
Антиоксиданты также исследуются в качестве возможных методов лечения нейродегенеративных заболеваний, таких как болезнь Альцгеймера, болезнь Паркинсона и боковой амиотрофический склероз.
Вредное действие антиоксидантных добавок
Некоторые антиоксиданты при чрезмерном употреблении с пищей могут принести больше вреда, чем пользы. Например, когда человек принимает чрезмерное количество сильных восстановителей в качестве антиоксидантов, у него может развиться дефицит нескольких минералов, таких как железо и цинк.Всасывание этих минералов из желудочно-кишечного тракта предотвращается.
Примечательными примерами являются щавелевая кислота, дубильные вещества и фитиновая кислота, которых много в растительных диетах. Кроме того, у людей, принимающих слишком много фитиновой кислоты из фасоли, бобовых, кукурузы и цельнозернового хлеба, может наблюдаться дефицит кальция и железа. Точно так же щавелевая кислота присутствует в какао, шоколаде, шпинате, репе и ревене, а дубильные вещества присутствуют в капусте, чае и бобах. Их избыток в рационе может препятствовать всасыванию минералов.
Эвгенол, антиоксидант, содержащийся в гвоздичном масле, также обладает токсическим действием в больших количествах.
Токсичность, связанная с высокими дозами водорастворимых антиоксидантов, таких как аскорбиновая кислота, не вызывает беспокойства, поскольку они могут быстро выводиться с мочой. Очень высокие дозы некоторых жирорастворимых антиоксидантов могут оказывать долгосрочное вредное воздействие.
Список литературы
- https://www.kraftbrands.com/sites/KraftNutrition/PDF/knu-Article-For-Professionals-08-Spring.pdf
- https://www.crnusa.org/benpdfs/CRN008benefits_eyesetc.pdf
- https://www.akspublication.com/Paper05_Jul-Dec2006_.pdf
- https://acudoc.com/Antioxidants.PDF
- https://ocw.jhsph.edu/courses/humannutrition/PDFs/Lecture8.pdf
- https://www.womenfirst.net/pdf/ADA/ADA_Antioxidants.pdf
- https://class.fst.ohio-state.edu/fst821/Lect/AA.pdf
- https://www.medlabs.com/Downloads/Antiox_acti_.pdf
Дополнительная литература
Обзор, применение, побочные эффекты, меры предосторожности, взаимодействия, дозировка и обзоры
Аллен, С., Бриттон, Дж. Р., и Леонарди-Би, Дж. А. Связь между витаминами-антиоксидантами и показателями результатов астмы: систематический обзор и метаанализ. Торакс 2009; 64 (7): 610-619. Просмотреть аннотацию.
Бардиа, А., Тлейдж, И. М., Серхан, Дж. Р., Суд, А. К., Лимбург, П. Дж., Эрвин, П. Дж., И Монтори, В. М. Эффективность добавок антиоксидантов в снижении заболеваемости и смертности от первичного рака: систематический обзор и метаанализ.Mayo Clin.Proc. 2008; 83 (1): 23-34. Просмотреть аннотацию.
Jiang, L., Yang, KH, Tian, JH, Guan, QL, Yao, N., Cao, N., Mi, DH, Wu, J., Ma, B., and Yang, SH Эффективность антиоксиданта добавки витаминов и селена в профилактике рака простаты: метаанализ рандомизированных контролируемых исследований. Nutr.Cancer 2010; 62 (6): 719-727. Просмотреть аннотацию.
Мэтью М.С., Эрвин А.М., Тао Дж. И Дэвис Р.М. Прием антиоксидантных витаминов для предотвращения и замедления прогрессирования возрастной катаракты.Cochrane.Database.Syst.Rev. 2012; 6: CD004567. Просмотреть аннотацию.
Myung, SK, Ju, W., Cho, B., Oh, SW, Park, SM, Koo, BK, и Park, BJ Эффективность витаминных и антиоксидантных добавок в профилактике сердечно-сосудистых заболеваний: систематический обзор и метаанализ рандомизированных контролируемых исследований. BMJ 2013; 346: f10. Просмотреть аннотацию.
Мён, С. К., Джу, В., Ким, С. С. и Ким, Х. Потребление витаминов или антиоксидантов (или уровень сыворотки) и риск цервикального новообразования: метаанализ.BJOG. 2011; 118 (11): 1285-1291. Просмотреть аннотацию.
Исследовательская группа по изучению возрастных глазных болезней. Рандомизированное плацебо-контролируемое клиническое испытание приема высоких доз витаминов C и E, бета-каротина и цинка при возрастной дегенерации желтого пятна и потере зрения. Отчет AREDS № 8. Arch Ophthalmol 2001; 119: 1417-36. Просмотреть аннотацию.
Исследовательская группа по изучению возрастных глазных болезней. Рандомизированное, плацебо-контролируемое клиническое испытание приема высоких доз витаминов C и E и бета-каротина при возрастной катаракте и потере зрения: отчет AREDS No.9. Arch Ophthalmol 2001; 119: 1439-52. Просмотреть аннотацию.
Исследовательская группа по изучению возрастных глазных болезней. Потенциальное влияние результатов исследования возрастных заболеваний глаз на общественное здоровье: отчет AREDS No. 11. Arch Ophthalmol 2003; 121: 1621-4. Просмотреть аннотацию.
Али-Хасан-Аль-Саег С., Мирхоссейни С.Дж., Тахернеджад М. и др. Влияние добавок антиоксидантов на сердечно-почечную защиту в кардиохирургии: обновленный и всесторонний метаанализ и систематический обзор. Cardiovasc Ther.2016 Октябрь; 34 (5): 360-70. Просмотреть аннотацию.
Али-Хассан-Сайег С., Мирхоссейни С.Дж., Резаисадрабади М. и др. Добавки антиоксидантов для профилактики фибрилляции предсердий после кардиохирургических вмешательств: обновленный комплексный систематический обзор и метаанализ 23 рандомизированных контролируемых исследований. Interact Cardiovasc Thorac Surg 2014; 18 (5): 646-54. Просмотреть аннотацию.
Антиоксиданты: глубже. Информационный центр Национального центра дополнительного и комплексного здравоохранения (NCCIH). Ноябрь 2013.Доступно по адресу: https://www.nccih.nih.gov/health/antioxidants-in-depth. По состоянию на 30 июня 2020 г.
Bjelakovic G, Nikolova D, Gluud LL, et al. Смертность в рандомизированных исследованиях антиоксидантных добавок для первичной и вторичной профилактики: систематический обзор и метаанализ. JAMA 2007; 297: 842-57. Просмотреть аннотацию.
Bolignano D, Cernaro V, Gembillo G, Baggetta R, Buemi M, D’Arrigo G. Антиоксидантные средства для задержки прогрессирования диабетической болезни почек: систематический обзор и метаанализ.PLoS One. 2017; 12 (6): e0178699. Просмотреть аннотацию.
Чанг Й.Дж., Мён С.К., Чунг С.Т. и др. Влияние витаминной терапии или добавок с предполагаемыми антиоксидантными свойствами на профилактику рака кожи: метаанализ рандомизированных контролируемых исследований. Дерматология. 2011; 223 (1): 36-44. Просмотреть аннотацию.
Chew EY, Clemons TE, Agrón E, Sperduto RD, Sangiovanni JP, Kurinij N, Davis MD; Исследовательская группа по изучению возрастных глазных болезней. Долгосрочное влияние витаминов C и E, ß-каротина и цинка на возрастную дегенерацию желтого пятна: отчет AREDS №35. Офтальмология. 2013 август; 120 (8): 1604-11.e4. Просмотреть аннотацию.
Ciofu O, Lykkesfeldt J. Антиоксидантные добавки для лечения заболеваний легких при муковисцидозе. Кокрановская база данных Syst Rev.2014; (8): CD007020. Просмотреть аннотацию.
Ciofu O, Smith S, Lykkesfeldt J. Антиоксидантные добавки для лечения заболеваний легких при муковисцидозе. Кокрановская база данных Syst Rev.2019; 10 (10): CD007020. Просмотреть аннотацию.
Crowe FL, Roddam AW, Key TJ, et al. Потребление фруктов и овощей и смертность от ишемической болезни сердца: результаты Европейского проспективного исследования рака и питания (EPIC) — Heart Study.Европейский журнал сердца. 2011; 32 (10): 1235-1243. Просмотреть аннотацию.
Эванс Дж. Р., Лоуренсон Дж. Дж. Антиоксидантные витаминные и минеральные добавки для предотвращения возрастной дегенерации желтого пятна. Кокрановская база данных Syst Rev.2017; 7 (7): CD000253. Просмотреть аннотацию.
Эванс Дж. Р., Лоуренсон Дж. Дж. Антиоксидантные витаминные и минеральные добавки для замедления прогрессирования возрастной дегенерации желтого пятна. Кокрановская база данных Syst Rev.2017; 7: CD000254. Просмотреть аннотацию.
Газиано Дж. М., Глинн Р. Дж., Кристен В. Г. и др.Витамины E и C в профилактике тотального рака простаты у мужчин: рандомизированное контролируемое исследование, проведенное врачами. JAMA 2009; 301: 52-62. Просмотреть аннотацию.
Geng J, Qian J, Si W, Cheng H, Ji F, Shen Z. Клинические преимущества периоперационной антиоксидантной витаминной терапии у пациентов, перенесших кардиохирургию: метаанализ. Взаимодействовать Cardiovasc Thorac Surg. 2017; 25 (6): 966-974. Просмотреть аннотацию.
Gooshe M, Abdolghaffari AH, Nikfar S, Mahdaviani P, Abdollahi M. Антиоксидантная терапия при остром, хроническом и постэндоскопическом ретроградном панкреатите холангиопанкреатографии: обновленный систематический обзор и метаанализ.Мир Дж. Гастроэнтерол. 2015; 21 (30): 9189-208. Просмотреть аннотацию.
Гу WJ, Вэй CY, Инь RX. Добавки антиоксидантов для профилактики постэндоскопического ретроградного панкреатита холангиопанкреатографии: метаанализ рандомизированных контролируемых исследований. Нутр Дж. 2013; 12: 23. Просмотреть аннотацию.
Джайеди А., Рашиди-Пур А., Парохан М., Заргар М.С., Шаб-Бидар С. Диетические антиоксиданты, концентрации циркулирующих антиоксидантов, общая антиоксидантная способность и риск смерти от всех причин: систематический обзор и метаанализ доза-реакция проспективных наблюдательных исследований.Adv Nutr. 2018; 9 (6): 701-716. Просмотреть аннотацию.
Дженкинс Д.А., Киттс Д., Джованнуччи Е.Л. и др. Селен, антиоксиданты, сердечно-сосудистые заболевания и смертность от всех причин: систематический обзор и метаанализ рандомизированных контролируемых исследований. Am J Clin Nutr. 2020 10 декабря; 112 (6): 1642-1652. Просмотреть аннотацию.
Kandhare AD, Mukherjee A, Bodhankar SL. Антиоксидант для лечения диабетической нефропатии: систематический обзор и метаанализ. Chem Biol Interact. 2017 25 декабря; 278: 212-221. Просмотреть аннотацию.
Кляйн Э.А., Томпсон И.М. мл., Танген С.М. и др. Витамин E и риск рака простаты: испытание по профилактике рака селеном и витамином E (SELECT). JAMA 2011; 306: 1549-56. Просмотреть аннотацию.
Куши Л.Х., Фолсом А.Р., Принас Р.Дж. и др. Диетические витамины-антиоксиданты и смерть от ишемической болезни сердца у женщин в постменопаузе. N Engl J Med 1996; 334: 1156-62. Просмотреть аннотацию.
Липпманн С.М., Кляйн Э.А., Гудман П.Дж. и др. Влияние селена и витамина E на риск рака простаты и других видов рака: исследование профилактики рака селеном и витамином E (SELECT).JAMA 2009; 301: 39-51. Просмотреть аннотацию.
Лирусси Ф., Аззалини Л., Орандо С., Орландо Р., Анджелико Ф. Антиоксидантные добавки при неалкогольной жировой болезни печени и / или стеатогепатите. Кокрановская база данных Syst Rev.2007; 2007 (1): CD004996. Просмотреть аннотацию.
Magalhães PV, Dean O, Andreazza AC, Berk M, Kapczinski F. Антиоксидантное лечение шизофрении. Кокрановская база данных Syst Rev.2016; 2: CD008919. Просмотреть аннотацию.
Мён СК, Ким И, Джу В., Чхве Х.Дж., Пэ В.К. Влияние антиоксидантных добавок на профилактику рака: метаанализ рандомизированных контролируемых исследований.Энн Онкол. 2010; 21 (1): 166-79. Просмотреть аннотацию.
Оррелл Р.В., Лейн Р.Дж., Росс М. Антиоксидантное лечение бокового амиотрофического склероза / болезни двигательных нейронов. Кокрановская база данных Syst Rev.2007; (1): CD002829. Просмотреть аннотацию.
Park SJ, Myung SK, Lee Y, Lee YJ. Эффекты витаминов и антиоксидантных добавок в профилактике рака мочевого пузыря: метаанализ рандомизированных контролируемых исследований. J Korean Med Sci. 2017; 32 (4): 628-635. Просмотреть аннотацию.
Рустаги Т., Нджей Б. Антиоксидантная терапия для уменьшения боли у пациентов с хроническим панкреатитом: систематический обзор и метаанализ.Поджелудочная железа. 2015; 44 (5): 812-8. Просмотреть аннотацию.
Tenório MB, Ferreira RC, Moura FA, Bueno NB, Goulart MOF, Oliveira ACM. Пероральная антиоксидантная терапия для профилактики и лечения преэклампсии: метаанализ рандомизированных контролируемых исследований. Нутр Метаб Кардиоваск Дис. 2018 сентябрь; 28 (9): 865-876. Просмотреть аннотацию.
Ван Дж., Ван Т., Динг В. и др. Эффективность антиоксидантной терапии при оценке качества спермы после варикоцелэктомии: систематический обзор и метаанализ. Андрология. 2019; 51 (10): e13396.Просмотреть аннотацию.
Ye Y, Li J, Yuan Z. Влияние добавок антиоксидантных витаминов на сердечно-сосудистые исходы: метаанализ рандомизированных контролируемых исследований. PLoS One. 2013; 8 (2): e56803. Просмотреть аннотацию.
Zhou D, Wang W, Cheng X, Wei J, Zheng S. Антиоксидантная терапия для пациентов с хроническим панкреатитом: систематический обзор и метаанализ. Clin Nutr. 2015; 34 (4): 627-34. Просмотреть аннотацию.
Антиоксиданты и профилактика рака — Национальный институт рака
Diplock AT, Charleux JL, Crozier-Willi G и др.Функциональная наука о питании и защита от активных форм кислорода. Британский журнал питания 1998; 80 (Приложение 1): S77-S112.
[Аннотация PubMed]Валко М., Лейбфриц Д., Монкол Дж. И др. Свободные радикалы и антиоксиданты при нормальных физиологических функциях и болезнях человека. Международный журнал биохимии и клеточной биологии 2007; 39 (1): 44-84.
[Аннотация PubMed]Буайед Дж., Бон Т.Экзогенные антиоксиданты — палки о двух концах в клеточном восстановительном состоянии: положительное воздействие на здоровье при физиологических дозах по сравнению с пагубным воздействием при высоких дозах. Окислительная медицина и долголетие клеток 2010; 3 (4): 228-237.
[Аннотация PubMed]Davis CD, Tsuji PA, Milner JA. Селенопротеины и профилактика рака. Ежегодный обзор питания 2012 г .; 32: 73-95.
[Аннотация PubMed]Patterson RE, White E, Kristal AR и др.Витаминные добавки и риск рака: эпидемиологические данные. Причины рака и борьба с ними 1997; 8 (5): 786-802.
[Аннотация PubMed]Blot WJ, Li JY, Taylor PR, et al. Испытания диетических вмешательств в Линьсяне, Китай: добавление определенных комбинаций витаминов / минералов, заболеваемость раком и смертность от конкретных болезней среди населения в целом. Журнал Национального института рака 1993; 85: 1483–91.
[Аннотация PubMed]Цяо Ю.Л., Доуси С.М., Камангар Ф. и др.Общая смертность и смертность от рака после приема витаминов и минералов: продолжение исследования Linxian General Population Nutrition Intervention Trial. Журнал Национального института рака 2009; 101 (7): 507-518.
[Аннотация PubMed]Группа изучения профилактики рака с альфа-токоферолом и бета-каротином. Влияние витамина Е и бета-каротина на заболеваемость раком легких и другими видами рака у курящих мужчин. Медицинский журнал Новой Англии 1994; 330: 1029–35.
[Аннотация PubMed]Rautalahti MT, Virtamo JR, Taylor PR и др. Влияние добавок с альфа-токоферолом и бета-каротином на частоту и смертность от рака поджелудочной железы в рандомизированном контролируемом исследовании. Cancer 1999; 86 (1): 37-42.
[Аннотация PubMed]Виртамо Дж., Эдвардс Б.К., Виртанен М. и др. Влияние дополнительных альфа-токоферола и бета-каротина на рак мочевыводящих путей: заболеваемость и смертность в контролируемом исследовании (Финляндия). Причины рака и борьба с ними 2000; 11 (10): 933-939.
[Аннотация PubMed]Албейнс Д., Малила Н., Тейлор П.Р. и др. Влияние дополнительных альфа-токоферола и бета-каротина на колоректальный рак. Причины рака и борьба с ними 2000; 11 (3): 197-205.
[Аннотация PubMed]Райт М.Э., Виртамо Дж., Хартман А.М. и др. Влияние добавок альфа-токоферола и бета-каротина на рак верхних отделов пищеварительного тракта в большом рандомизированном контролируемом исследовании. Рак 2007; 109 (5): 891-898.
[Аннотация PubMed]Omenn GS, Goodman GE, Thornquist MD, et al. Влияние комбинации бета-каротина и витамина А на рак легких и сердечно-сосудистые заболевания. Медицинский журнал Новой Англии 1996; 334 (18): 1150-1155.
[Аннотация PubMed]Goodman GE, Thornquist MD, Balmes J, et al. Исследование эффективности бета-каротина и ретинола: частота случаев рака легких и смертность от сердечно-сосудистых заболеваний в течение 6-летнего периода наблюдения после прекращения приема добавок бета-каротина и ретинола. Журнал Национального института рака 2004; 96 (23): 1743-1750.
[Аннотация PubMed]Neuhouser ML, Barnett MJ, Kristal AR, et al. Использование пищевых добавок и риск рака простаты в испытании эффективности каротина и ретинола. Эпидемиология рака, биомаркеры и профилактика 2009; 18 (8): 2202-2206.
[Аннотация PubMed]Hennekens CH, Buring JE, Manson JE, Stampfer M, Rosner B, Cook NR, et al.Отсутствие эффекта от длительного приема бета-каротина на частоту злокачественных новообразований и сердечно-сосудистых заболеваний. Медицинский журнал Новой Англии 1996; 334: 1145–9.
[Аннотация PubMed]Ли И.М., Кук Н.Р., Мэнсон Дж. Добавки бета-каротина и заболеваемость раком и сердечно-сосудистыми заболеваниями: исследование здоровья женщин. Журнал Национального института рака 1999; 91: 2102–6.
[Аннотация PubMed]Ли И.М., Кук Н.Р., Газиано Дж. М. и др.Витамин Е в первичной профилактике сердечно-сосудистых заболеваний и рака: Исследование здоровья женщин: рандомизированное контролируемое исследование. JAMA 2005; 294 (1): 56-65.
[Аннотация PubMed]Hercberg S, Galan P, Preziosi P, et al. Исследование SU.VI.MAX: рандомизированное плацебо-контролируемое исследование воздействия на здоровье антиоксидантных витаминов и минералов. Архив внутренней медицины 2004; 164 (21): 2335-2342.
[Аннотация PubMed]Hercberg S, Kesse-Guyot E, Druesne-Pecollo N, et al.Заболеваемость раком, ишемическими сердечно-сосудистыми заболеваниями и смертность в течение 5-летнего наблюдения после прекращения приема антиоксидантных витаминов и минералов: последующее наблюдение после вмешательства в исследовании SU.VI.MAX. Международный журнал рака 2010; 127 (8): 1875-1881.
[Аннотация PubMed]Hercberg S, Ezzedine K, Guinot C и др. Прием антиоксидантов увеличивает риск рака кожи у женщин, но не у мужчин. Журнал питания 2007; 137 (9): 2098-2105.
[Аннотация PubMed]Ezzedine K, Latreille J, Kesse-Guyot E, et al. Заболеваемость раком кожи в течение 5-летнего наблюдения после прекращения приема антиоксидантных витаминов и минеральных добавок. Европейский журнал рака 2010; 46 (18): 3316-3322.
[Аннотация PubMed]Лонн Э., Бош Дж., Юсуф С. и др. Влияние длительного приема витамина E на сердечно-сосудистые события и рак: рандомизированное контролируемое исследование. JAMA 2005; 293 (11): 1338-1347.
[Аннотация PubMed]Липпман С.М., Кляйн Э.А., Гудман П.Дж. и др. Влияние селена и витамина E на риск рака простаты и других видов рака: испытание по профилактике рака селеном и витамином E (SELECT). JAMA 2009; 301 (1): 39-51.
[Аннотация PubMed]Кляйн Э.А., Томпсон И.М., Танген С.М. и др. Витамин E и риск рака простаты: испытание по профилактике рака селеном и витамином E (SELECT). JAMA 2011; 306 (14): 1549-1556.
[Аннотация PubMed]Газиано Дж. М., Глинн Р. Дж., Кристен В. Г. и др. Витамины E и C в профилактике рака простаты и тотального рака у мужчин: рандомизированное контролируемое исследование, проведенное в исследовании «Здоровье врачей II». JAMA 2009; 301 (1): 52-62.
[Аннотация PubMed]Fortmann SP, Burda BU, Senger CA и др. Витаминные и минеральные добавки в первичной профилактике сердечно-сосудистых заболеваний и рака: обновленный систематический обзор данных для U.S. Целевая группа по профилактическим услугам. Анналы внутренней медицины 2013; 159 (12): 824-834.
[Аннотация PubMed]Lawenda BD, Kelly KM, Ladas EJ и др. Следует ли избегать дополнительного приема антиоксидантов во время химиотерапии и лучевой терапии? Журнал Национального института рака 2008; 100 (11): 773-783.
[Аннотация PubMed]Сайин В.И., Ибрагим М.Х., Ларссон Э. и др.Антиоксиданты ускоряют прогрессирование рака легких у мышей. Трансляционная медицина 2014; 6 (221): 221ra15.
[Аннотация PubMed]Ле Гал К., Ибрагим М.Х., Виль С. и др. Антиоксиданты могут увеличивать метастазирование меланомы у мышей. Трансляционная медицина 2015; 7 (308): 308re8.
[Аннотация PubMed]Пискунова Е., Агатоклеус М., Мерфи М.М. и др. Окислительный стресс подавляет отдаленные метастазы клетками меланомы человека. Природа 2015; 527 (7577): 186-191.
[Аннотация PubMed]Живой вопрос: может быть, у вас слишком много антиоксидантов?
Вопрос: Можно ли есть слишком много продуктов, богатых антиоксидантами?
Антиоксидант — одно из тех слов, как «органический» или «натуральный», которое стало синонимом хорошего здоровья.
Производители пищевых продуктов, кажется, знают об этом. Многие продукты с гордостью носят свой антиоксидантный статус, вы увидите, что они указаны на всем, от темного шоколада и красного вина до ягод годжи и зеленого чая.
Эта статья содержит контент, который больше не доступен.
Это не просто еда: антиоксидантные добавки выстилают полки супермаркетов, аптек и магазинов здорового питания, обещая сдержать приливы старения и хронических заболеваний.
Тем не менее, исследования показывают, что антиоксиданты не всегда оправдывают ажиотаж, когда речь идет о пользе для здоровья. Еще большее беспокойство вызывают доказательства того, что прием антиоксидантных добавок иногда может принести больше вреда, чем пользы.
Свободные радикалы
Чтобы понять антиоксиданты, сначала мы должны понять окислители, более известные как свободные радикалы.
Свободные радикалы — это естественные побочные продукты, которые создают наши клетки, когда они превращают пищу в энергию. Они являются нормальной частью функционирования нашего организма, а естественные окислители легко переносятся.
«Свободные радикалы — это, по сути, маленькие неприятные химические вещества, которые крадут электроны у других молекул в вашем теле и вызывают повреждения в организме», — сказала д-р Эмма Беккет, специалист по молекулярному питанию из Университета Ньюкасла.
Какой у вас животрепещущий вопрос?
Можете ли вы разбудить лунатика? Почему мы скрипим зубами и как нам остановиться?
Если у вас есть животрепещущий вопрос о здоровье, вы всегда хотели знать ответ, чтобы связаться с ним через health @ your.abc.net.au. Затем мы передадим ваш вопрос экспертам.
Мы также сталкиваемся со свободными радикалами во многих аспектах нашей повседневной жизни. Солнечный свет вызывает образование свободных радикалов в нашей коже и глазах; они также присутствуют в пище, которую мы едим, и в воздухе, которым мы дышим. Сигаретный дым, загрязнение окружающей среды, алкоголь и стресс также могут способствовать развитию свободных радикалов.
Что делает свободные радикалы неприятными, так это то, что они вступают в реакцию с любой молекулой, с которой они сталкиваются. Эта реакция называется окислением, и во многом подобно окислению, которое вызывает ржавчину железа или коричневое цветное яблоко, оно вызывает повреждение.
Ущерб, наносимый свободными радикалами, считается одним из ключевых факторов постепенного ухудшения состояния вашего тела, которое происходит с возрастом. Это может повлиять на защитные мембраны, которые окружают каждую из наших клеток, а также на белки и молекулы ДНК внутри каждой клетки.
Доктор Беккет сказал, что повреждение ДНК свободными радикалами может вызывать мутации клеток и способствовать развитию рака. Свободные радикалы также могут окислять липопротеины низкой плотности (ЛПНП или «плохой холестерин»), повышая вероятность их накопления на стенках артерий, затвердевания кровеносных сосудов и возникновения сердечно-сосудистых заболеваний.
Антиоксиданты на помощь
Учитывая постоянный поток свободных радикалов, с которыми сталкивается ваше тело, неудивительно, что вы снабжены некоторыми защитными молекулами. Это возвращает нас к антиоксидантам.
«Антиоксиданты — это умные маленькие молекулы, которые приходят и останавливают цепную реакцию свободных радикалов», — сказал доктор Беккет.
«Обычно, если свободный радикал крадет электрон у другой молекулы, эта молекула становится свободным радикалом.Это похоже на цепную реакцию.
«Антиоксиданты — единственные вещи, которые могут отдать электрон этой реакции, не превращаясь сами в свободные радикалы. Так что они останавливают эту отрицательную цепную реакцию».
Известно, что сотни веществ действуют как антиоксиданты в присутствии свободных радикалов. Каждый из них имеет свои уникальные биологические и химические свойства, поэтому не существует единого антиоксиданта, который действовал бы как серебряная пуля против всех свободных радикалов, плавающих вокруг вашего тела.
«Антиоксиданты содержатся в пище, но ваше тело также вырабатывает некоторые из них естественным образом — это могут быть ферменты или другие молекулы», — сказал доктор Беккет.
- Витамин A можно синтезировать из продуктов с бета-каротином: брюссельской капусты, ростков люцерны и желтых, оранжевых и красных фруктов и овощей.
- Витамин C присутствует в цитрусовых, черной смородине, брокколи и сырой капусте.
- Витамин E содержится в цельнозерновых, орехах, зеленых листовых овощах и сладком картофеле.
- Флавоноиды присутствуют в красном вине, луке, баклажанах, салате, петрушке, грушах, ягодах, вишне, бобовых, соевых бобах, тофу и мисо.
- Специи могут уменьшить окислительный стресс: имбирь, куркума, экстракт виноградных косточек и розмарин.
- Изюм, черника, клюква, инжир, чернослив, гранаты, красный перец, капуста, шпинат и темный шоколад — отличные универсальные антиоксиданты .
Life Matters: Можете ли вы съесть слишком много яблок?
Журналист ABC Health Оливия Уиллис вместе с Амандой Смит в журнале Life Matters обсуждает все, что касается антиоксидантов.
ПодробнееБольше не всегда лучше
Когда исследователи впервые начали связывать свободные радикалы с хроническими заболеваниями и старением, казалось логичным, что увеличение потребления антиоксидантов, особенно с помощью добавок, будет противоядием. Но, как это часто бывает, научные доказательства этого не подтверждают.
«Больше — это не всегда больше в питании. И слишком много может быть плохо, особенно в мега-высоких дозах добавок», — сказал доктор Беккет.
Фактически, исследования показали, что в некоторых случаях прием антиоксидантных добавок может причинить вред и даже увеличить риск рака. Доктор Беккет сказал, что это связано с тем, что при высоких концентрациях вещества, которые обычно действуют как антиоксиданты, могут иметь противоположный эффект и действовать как прооксиданты.
«Я бы настоятельно рекомендовал соблюдать осторожность при использовании добавок», — сказал д-р Беккет.
Итог
То, что диета, полная фруктов и овощей, полезна, все еще остается в силе, но остается неясным, насколько это связано с антиоксидантами, которые вы едите или пьете.
Доктор Беккет сказал, что преимущества богатой антиоксидантами пищи, вероятно, связаны с полной питательной ценностью натуральных и цельных продуктов, и что антиоксиданты сами по себе не являются «проходом без свободных радикалов».
«Тот факт, что что-то продается как продукт с высоким содержанием антиоксидантов, не означает, что это лучше для вас, чем ваши обычные фрукты и овощи.
» [Идея суперпродуктов] заставляет людей думать, что здоровое питание — это дорого, и это не так. Этого не должно быть.Вы можете получить все необходимое из разнообразных стандартных фруктов и овощей «, — сказал доктор Беккет.
Яблоко в день — хорошее начало, но лучшее, что вы можете сделать, — это придерживаться здоровой и сбалансированной диеты, включающей пять до восьми порций фруктов и овощей каждый день.
Здоровье в вашем почтовом ящике
Получайте последние новости о здоровье и информацию со всего ABC.
Антиоксиданты для здоровья и болезней
Антиоксидант можно определить как: «любое вещество, которое , когда он присутствует в низких концентрациях по сравнению с концентрацией окисляемого субстрата, значительно задерживает или ингибирует окисление этого субстрата ». 1 Физиологическая роль антиоксидантов, как следует из этого определения, заключается в предотвращении повреждения клеточных компонентов, возникающего в результате химических реакций с участием свободных радикалов. В последние годы появилось множество доказательств, подтверждающих ключевую роль свободных радикалов во многих фундаментальных клеточных реакциях и предполагающих, что окислительный стресс может играть важную роль в патофизиологии распространенных заболеваний, включая атеросклероз, хроническую почечную недостаточность и сахарный диабет.Цель этого обзора — рассмотреть механизмы образования свободных радикалов в организме, последствия повреждения тканей, вызванного свободными радикалами, а также функцию систем антиоксидантной защиты при здоровье и болезнях.
Свободные радикалы и их химические реакции
Свободный радикал можно определить как любую молекулу, способную к независимому существованию, которая содержит неспаренный электрон на атомной орбитали. 2 Наличие неспаренного электрона приводит к определенным общим свойствам, которые присущи большинству радикалов.Радикалы слабо притягиваются к магнитному полю и считаются парамагнитными. Многие радикалы обладают высокой реакционной способностью и могут либо отдавать электрон, либо извлекать электрон из других молекул, поэтому ведут себя как окислители или восстановители. В результате такой высокой реакционной способности большинство радикалов имеют очень короткий период полураспада (10 -6 секунд или меньше) в биологических системах, хотя некоторые виды могут выжить намного дольше. 2 Наиболее важными свободными радикалами при многих болезненных состояниях являются производные кислорода, особенно супероксид и гидроксильный радикал.Радикальное образование в организме происходит по нескольким механизмам с участием как эндогенных факторов, так и факторов окружающей среды (рис. 1).
Рисунок 1Основные источники свободных радикалов в организме и последствия повреждения свободными радикалами.
Супероксид (O 2 -. ) образуется путем добавления одного электрона к кислороду, и существует несколько механизмов, с помощью которых супероксид может образовываться in vivo. 3 Некоторые молекулы, включая адреналин, флавинуклеотиды, тиоловые соединения и глюкозу, могут окисляться в присутствии кислорода с образованием супероксида, и эти реакции значительно ускоряются в присутствии переходных металлов, таких как железо или медь. Цепь переноса электронов во внутренней митохондриальной мембране выполняет восстановление кислорода до воды. Во время этого процесса образуются свободнорадикальные промежуточные соединения, которые обычно прочно связаны с компонентами транспортной цепи.Однако происходит постоянная утечка нескольких электронов в матрицу митохондрий, что приводит к образованию супероксида. 4 Активность некоторых других ферментов, таких как оксидаза цитохрома p450 в печени и ферментов, участвующих в синтезе гормонов надпочечников, также приводит к утечке нескольких электронов в окружающую цитоплазму и, следовательно, к образованию супероксида. Также может быть непрерывное производство супероксида эндотелием сосудов для нейтрализации оксида азота, 5 , 6 производство супероксида другими клетками для регулирования роста и дифференцировки клеток, 7 и производство супероксида фагоцитарными клетками во время респираторный взрыв. 8
Любая биологическая система, генерирующая супероксид, также будет производить перекись водорода в результате спонтанной реакции дисмутации. Кроме того, несколько ферментативных реакций, в том числе катализируемых гликолатоксидазой и оксидазой D-аминокислот, могут напрямую продуцировать перекись водорода. 9 Перекись водорода сама по себе не является свободным радикалом, но обычно включается в общую рубрику активных форм кислорода (АФК). Это слабый окислитель, который может напрямую повредить белки и ферменты, содержащие реактивные тиоловые группы.Однако его наиболее важным свойством является способность свободно пересекать клеточные мембраны, чего супероксид обычно не может. 10 Следовательно, перекись водорода, образующаяся в одном месте, может диффундировать на значительное расстояние, прежде чем разложиться с образованием высокореактивного гидроксильного радикала, который, вероятно, опосредует большинство токсических эффектов, приписываемых перекиси водорода. Следовательно, перекись водорода действует как канал для передачи вызванных свободными радикалами повреждений через клеточные компартменты и между клетками.В присутствии перекиси водорода миелопероксидаза будет генерировать хлорноватистую кислоту и синглетный кислород, реакция, которая играет важную роль в уничтожении бактерий фагоцитами. 11
Гидроксильный радикал (OH , ) или близкородственные ему виды, вероятно, являются последним медиатором большинства повреждений тканей, вызванных свободными радикалами. 12 Все химически активные формы кислорода, описанные выше, проявляют большую часть своих патологических эффектов, вызывая образование гидроксильных радикалов.Причина этого в том, что гидроксильный радикал реагирует с чрезвычайно высокими константами скорости почти со всеми типами молекул, обнаруженными в живых клетках, включая сахара, аминокислоты, липиды и нуклеотиды. Хотя образование гидроксильных радикалов может происходить несколькими путями, наиболее важным механизмом in vivo, вероятно, является катализируемое переходными металлами разложение супероксида и пероксида водорода. 13
Все элементы в первой строке d-блока периодической таблицы классифицируются как переходные металлы.Как правило, они содержат один или несколько неспаренных электронов и поэтому сами являются радикалами в элементарном состоянии. Однако их ключевым свойством с точки зрения свободнорадикальной биологии является их переменная валентность, которая позволяет им вступать в реакции с переносом одного электрона. Наиболее важными переходными металлами при заболеваниях человека являются железо и медь. Эти элементы играют ключевую роль в производстве гидроксильных радикалов in vivo. 13 Перекись водорода может реагировать с железом II (или медью I) с образованием гидроксильного радикала, реакция, впервые описанная Фентоном в 1894:
.Эта реакция может происходить in vivo, но ситуация осложняется тем фактом, что обычно также присутствует супероксид (основной источник перекиси водорода in vivo).Супероксид и пероксид водорода могут взаимодействовать вместе напрямую с образованием гидроксильного радикала, но константа скорости этой реакции в водном растворе практически равна нулю. Однако, если присутствуют ионы переходных металлов, устанавливается последовательность реакций, которые могут протекать с большой скоростью: чистый результат:
Общий результат проиллюстрированной выше последовательности реакций известен как реакция Габера-Вейсса. Хотя большая часть железа и меди в организме изолирована в формах, которые недоступны для катализа этой последовательности реакций, они по-прежнему важны как механизм образования гидроксильного радикала in vivo.Однако фактические реакции могут быть несколько более сложными, чем описанные выше, и возможно также образование других реакционноспособных промежуточных продуктов, таких как феррильный и перферрильный радикалы. 12
У среднего взрослого человека содержится примерно 4,5 г железа, большая часть которого содержится в молекуле гемоглобина и других гемсодержащих белках. Пищевое железо абсорбируется преимущественно из проксимальной части тонкой кишки в двухвалентной форме и передается в кровоток, в котором оно переносится трансферрином. 14 В большинстве случаев железо остается прочно связанным с одним из нескольких белков, включая трансферрин, лактоферрин, белки гема, ферритин или гемосидерин. В дополнение, однако, кажется вероятным, что небольшой пул железа будет поддерживаться в виде комплексов с множеством небольших молекул, таких как нуклеотиды и цитрат, в цитоплазме и субклеточных органеллах. 14 Этот пул, вероятно, способен катализировать реакцию Фентона, управляемую железом, in vivo. Конечно, эти комплексы могут способствовать образованию гидроксильных радикалов in vitro. 15 Редокс-реактивное железо можно измерить с помощью анализа железа с блеомицином, 16 , хотя остается неясным, в какой степени железо, обнаруженное с помощью этого анализа, коррелирует с каким-либо дискретным анатомическим или физиологическим пулом. В нормальных условиях в плазме здоровых субъектов не обнаруживается реактивное с блеомицином железо, что означает, что трансферрин или железо, связанное с ферритином, недоступно для управления производством гидроксильных радикалов. 17 Однако трансферрин высвобождает свое железо при кислом pH, особенно в присутствии хелатирующих агентов с малой молекулярной массой, таких как АДФ, АТФ и цитрат. 15 Такие состояния обнаруживаются в областях активного воспаления и во время реперфузионного повреждения ишемией, 18 , и поэтому вполне вероятно, что гидроксильные радикалы вносят вклад в повреждение тканей в этих условиях. Железо высвобождается из ферритина восстановителями, включая аскорбат и сам супероксид, 19 , 20 , а перекись водорода может выделять железо из ряда белков гема. 21 Следовательно, хотя железосвязывающие белки эффективно хелатируют железо и предотвращают любые заметные окислительно-восстановительные эффекты в нормальных физиологических условиях, эта защита может разрушаться при болезненных состояниях.Роль меди аналогична описанной выше для железа. 22 , 23
Хотя образование свободных радикалов происходит в результате эндогенных реакций, описанных выше, и играет важную роль в нормальном функционировании клеток, важно помнить, что экзогенные факторы окружающей среды также могут способствовать образованию радикалов. Ультрафиолетовый свет приводит к образованию синглетного кислорода и других активных форм кислорода в коже. 24 Загрязняющие атмосферу вещества, такие как озон и диоксид азота, приводят к образованию радикалов и истощению антиоксидантов в жидкости бронхоальвеолярной выстилки, что может усугубить респираторное заболевание. 25 — 27 Сигаретный дым содержит миллимолярные количества свободных радикалов наряду с другими токсинами. 28
Различные ксенобиотики также вызывают повреждение тканей в результате образования свободных радикалов, включая паракват, 29 парацетамол, 30 блеомицин, 31 и антрациклины. 32
Антиоксидантные защитные системы
Поскольку радикалы обладают способностью реагировать неизбирательным образом, приводя к повреждению практически любого клеточного компонента, присутствует широкий спектр антиоксидантной защиты, как эндогенной, так и экзогенной, для защиты клеточных компонентов от повреждений, вызванных свободными радикалами. Их можно разделить на три основные группы: антиоксидантные ферменты, антиоксиданты, разрушающие цепь, и белки, связывающие переходные металлы 2 (рис. 2).
Рисунок 2Антиоксидантная защита от атаки свободных радикалов. Антиоксидантные ферменты катализируют распад свободных радикалов, обычно во внутриклеточной среде. Белки, связывающие переходные металлы, предотвращают взаимодействие переходных металлов, таких как железо и медь, с перекисью водорода и супероксидом с образованием высокореакционных гидроксильных радикалов. Антиоксиданты, разрушающие цепь, являются мощными донорами электронов и реагируют преимущественно со свободными радикалами до того, как будут повреждены важные молекулы-мишени.При этом антиоксидант окисляется, и его необходимо регенерировать или заменить. По определению, антиоксидантный радикал относительно инертен и не способен атаковать другие молекулы.
АНТИОКСИДАНТНЫЕ ФЕРМЕНТЫ
Каталаза
Каталаза была первым антиоксидантным ферментом, который был охарактеризован и катализирует двухстадийное превращение перекиси водорода в воду и кислород:
Каталаза состоит из четырех белковых субъединиц, каждая из которых содержит группу гема и молекулу НАДФН. 33 Константа скорости описанных выше реакций чрезвычайно высока (∼10 7 М / сек), что означает, что практически невозможно насытить фермент in vivo. Каталаза в основном находится внутри клеток в пероксисомах, которые также содержат большинство ферментов, способных генерировать перекись водорода. Количество каталазы в цитоплазме и других субклеточных компартментах остается неясным, поскольку пероксисомы легко разрушаются во время манипуляции с клетками. Наибольшая активность проявляется в печени и эритроцитах, но некоторое количество каталазы обнаружено во всех тканях.
Глутатионпероксидазы и глутатионредуктаза
Глутатионпероксидазы катализируют окисление глутатиона за счет гидропероксида, которым может быть перекись водорода или другие соединения, такие как гидропероксид липидов 34 :
Другие пероксиды, включая гидропероксиды липидов, также могут действовать как субстраты для этих ферментов, которые, следовательно, могут играть роль в восстановлении повреждений, вызванных перекисным окислением липидов.Глутатионпероксидазам необходим селен в активном центре, и дефицит может возникать при наличии серьезного дефицита селена. 35 Некоторые ферменты глутатионпероксидазы кодируются отдельными генами. 36 Считается, что плазменная форма глутатионпероксидазы синтезируется в основном в почках. 37 Внутри клеток самые высокие концентрации обнаруживаются в печени, хотя глутатионпероксидаза широко распространена почти во всех тканях. Преобладающее субклеточное распределение находится в цитозоле и митохондриях, что позволяет предположить, что глутатионпероксидаза является основным поглотителем перекиси водорода в этих субклеточных компартментах.Активность фермента зависит от постоянной доступности восстановленного глутатиона. 38 Соотношение восстановленного и окисленного глутатиона обычно поддерживается очень высоким в результате активности фермента глутатионредуктазы:
НАДФН, необходимый этому ферменту для пополнения запасов восстановленного глутатиона, обеспечивается пентозофосфатным путем. Любой конкурирующий путь, в котором используется НАДФН (например, путь альдозоредуктазы), может привести к дефициту восстановленного глутатиона и, следовательно, нарушить действие глутатионпероксидазы.Глутатионредуктаза представляет собой фермент, зависимый от флавинуклеотидов, и имеет такое же распределение в тканях, что и глутатионпероксидаза. 39
Супероксиддисмутаза
Супероксиддисмутазы катализируют дисмутацию супероксида в пероксид водорода:
Затем перекись водорода должна быть удалена каталазой или глутатионпероксидазой, как описано выше. В тканях млекопитающих существует три формы супероксиддисмутазы, каждая из которых имеет определенное субклеточное расположение и различное тканевое распределение.
Супероксиддисмутаза цинка и меди (CuZnSOD): CuZnSOD обнаружен в цитоплазме и органеллах практически всех клеток млекопитающих. 40 Он имеет молекулярную массу приблизительно 32 000 кДа и имеет две белковые субъединицы, каждая из которых содержит каталитически активный атом меди и цинка.
Супероксиддисмутаза марганца (MnSOD): MnSOD обнаружен в митохондриях почти всех клеток и имеет молекулярную массу 40 000 кДа. 41 Он состоит из четырех белковых субъединиц, каждая из которых, вероятно, содержит один атом марганца. Аминокислотная последовательность MnSOD полностью отличается от CuZnSOD и не ингибируется цианидом, что позволяет отличать активность MnSOD от активности CuZnSOD в смесях двух ферментов.
Внеклеточная супероксиддисмутаза (EC-SOD): EC-SOD была описана Marklund в 1982 г. 42 и представляет собой секреторную SOD, содержащую медь и цинк, отличную от CuZnSOD, описанного выше.EC-SOD синтезируется только несколькими типами клеток, включая фибробласты и эндотелиальные клетки, и экспрессируется на поверхности клетки, где он связан с гепарансульфатами. EC-SOD является основной SOD, обнаруживаемой во внеклеточных жидкостях, и высвобождается в кровоток с поверхности эндотелия сосудов после инъекции гепарина. 43 EC-SOD может играть роль в регуляции сосудистого тонуса, потому что эндотелиальный релаксирующий фактор (оксид азота или близкородственное соединение) нейтрализуется в плазме супероксидом. 44
АНТИОКСИДАНТЫ, РАЗРЫВАЮЩИЕ ЦЕПЬ
Каждый раз, когда свободный радикал взаимодействует с другой молекулой, могут образовываться вторичные радикалы, которые затем могут реагировать с другими мишенями с образованием еще более радикальных частиц. Классическим примером такой цепной реакции является перекисное окисление липидов, и реакция будет продолжаться до тех пор, пока два радикала не объединятся с образованием стабильного продукта или радикалы не будут нейтрализованы антиоксидантом, разрывающим цепь. 45 Антиоксиданты, разрывающие цепь, представляют собой небольшие молекулы, которые могут получать электрон от радикала или отдавать электрон радикалу с образованием стабильных побочных продуктов. 46 Как правило, заряд, связанный с присутствием неспаренного электрона, диссоциирует на поглотитель, и полученный продукт с трудом принимает электрон от другой молекулы или передает электрон другой молекуле, предотвращая дальнейшее распространение цепной реакции. Такие антиоксиданты можно удобно разделить на антиоксиданты в водной фазе и липидной фазе.
Антиоксиданты, разрушающие липидную фазу
Эти антиоксиданты удаляют радикалы в мембранах и липопротеиновых частицах и имеют решающее значение для предотвращения перекисного окисления липидов. Наиболее важным антиоксидантом липидной фазы, вероятно, является витамин Е. 47 Витамин Е встречается в природе в восьми различных формах, которые сильно различаются по степени биологической активности. Токоферолы (α, β, γ и δ) имеют хроманольное кольцо и фитильный хвост и различаются числом и положением метильных групп в кольце.Токотриенолы (α, β, γ и δ) структурно похожи, но имеют ненасыщенные хвосты. Оба класса соединений липидорастворимы и обладают ярко выраженными антиоксидантными свойствами. 48 Они реагируют с пероксильными радикалами быстрее, чем полиненасыщенные жирные кислоты, и, следовательно, нарушают цепную реакцию перекисного окисления липидов. Помимо своей антиоксидантной роли, витамин E может также играть структурную роль в стабилизации мембран. 49 Фрэнк. Дефицит витамина Е редко встречается у людей, хотя он может вызывать гемолиз 50 и может способствовать периферической невропатии, которая возникает при абеталипопротеинемии. 51
Абсорбция, транспорт и регуляция плазменных концентраций витамина E у людей были рассмотрены Kayden and Traber, 52 , хотя в целом метаболизм витамина E описан недостаточно хорошо. В клеточных мембранах и липопротеинах основная антиоксидантная функция витамина Е заключается в улавливании пероксильных радикалов и прерывании цепной реакции перекисного окисления липидов. 53 Витамин Е не препятствует начальному образованию углеродных центрированных радикалов в среде, богатой липидами, но сводит к минимуму образование вторичных радикалов.α-Токоферол является самым мощным антиоксидантом из токоферолов, а также наиболее распространен в организме человека. Он быстро реагирует с пероксильным радикалом с образованием относительно стабильного токофероксильного радикала, причем избыточный заряд, связанный с дополнительным электроном, рассеивается по хроманольному кольцу. Этот стабилизированный резонансом радикал может впоследствии отреагировать одним из нескольких способов. α-Токоферол может быть регенерирован реакцией на водной границе раздела с аскорбатом 54 или другим антиоксидантом, разрывающим цепь в водной фазе, таким как восстановленный глутатион или урат. 55 Альтернативно, два α-токофероксильных радикала могут объединяться с образованием стабильного димера, или радикал может быть полностью окислен с образованием токоферолхинона.
Каротиноиды представляют собой группу жирорастворимых антиоксидантов, основанную на изопреноидном углеродном скелете. 56 Самым важным из них является β-каротин, хотя по крайней мере 20 других могут присутствовать в мембранах и липопротеинах. Они являются особенно эффективными поглотителями синглетного кислорода, 57 , но также могут улавливать пероксильные радикалы при низком давлении кислорода с эффективностью, по крайней мере, такой же, как у α-токоферола.Поскольку эти условия преобладают во многих биологических тканях, каротиноиды могут играть роль в предотвращении перекисного окисления липидов in vivo. 58 Другая важная роль некоторых каротиноидов — это предшественники витамина А (ретинол). Витамин А также обладает антиоксидантными свойствами, 59 , которые, однако, не зависят от концентрации кислорода.
Флавоноиды — это большая группа полифенольных антиоксидантов, содержащихся во многих фруктах, овощах и напитках, таких как чай и вино. 60 — 62 Было идентифицировано более 4000 флавоноидов, которые разделены на несколько групп в соответствии с их химической структурой, включая флавонолы (кверцетин и кемферол), флавонолы (катехины), флавоны (апигенин) и изофлавоны ( геништейн). Эпидемиологические исследования предполагают обратную связь между потреблением флавоноидов и заболеваемостью хроническими заболеваниями, такими как ишемическая болезнь сердца (ИБС). 63 — 65 Однако в настоящее время мало что известно об абсорбции и метаболизме флавоноидов, и эпидемиологические ассоциации могут быть следствием влияния других факторов.Имеющиеся данные свидетельствуют о низкой биодоступности многих флавоноидов, 66 — 68 и очень низких значениях в плазме крови, хотя есть некоторые свидетельства того, что увеличение потребления флавоноидов может улучшить биохимические показатели окислительного повреждения. 68 , 69 Помимо флавоноидов, другие диетические фенольные соединения также могут вносить небольшой вклад в общую антиоксидантную способность. 70
Убихинол-10, восстановленная форма кофермента Q10, также является эффективным липидорастворимым антиоксидантом, разрушающим цепь. 71 Хотя он присутствует в более низких концентрациях, чем альфа-токоферол, он может улавливать липидные пероксильные радикалы с большей эффективностью, чем альфа-токоферол или каротиноиды, а также может регенерировать связанный с мембраной альфа-токоферол из токоферильного радикала. 72 Действительно, всякий раз, когда плазма или изолированный холестерин липопротеинов низкой плотности (ЛПНП) подвергаются воздействию радикалов, образующихся в липидной фазе, убихинол-10 является первым антиоксидантом, который должен потребляться, что позволяет предположить, что он может иметь особое значение для предотвращения распространения инфекции. перекисное окисление липидов. 73 Однако работа по дальнейшему уточнению его роли была затруднена из-за легкости, с которой убинхинол-10 окисляется во время работы с пробами или анализа.
Антиоксиданты, разрушающие цепь в водной фазе
Эти антиоксиданты будут непосредственно улавливать радикалы, присутствующие в водной среде. Качественно важнейшим антиоксидантом этого типа является витамин С (аскорбат). 74 У человека аскорбат действует как важный кофактор для нескольких ферментов, катализирующих реакции гидроксилирования.В большинстве случаев он обеспечивает электроны для ферментов, которым для достижения полной ферментативной активности требуются ионы простетических металлов в восстановленной форме. Его наиболее известная роль — кофактор пролил- и лизилоксидаз в синтезе коллагена. Однако, в дополнение к этим четко определенным действиям, несколько других биохимических путей зависят от присутствия аскорбата. 75 В дополнение к его роли кофактора фермента, другая основная функция аскорбата — это антиоксидант, разрушающий ключевую цепь в водной фазе. 76 Было показано, что аскорбат поглощает супероксид, перекись водорода, гидроксильный радикал, хлорноватистую кислоту, водные пероксильные радикалы и синглетный кислород. Во время своего антиоксидантного действия аскорбат подвергается двухэлектронному восстановлению, сначала до полудегидроаскорбильного радикала, а затем до дегидроаскорбат. Полудегидроаскорбильный радикал относительно стабилен из-за дисперсии заряда, связанного с присутствием одного электрона по трем атомам кислорода, и его можно легко обнаружить с помощью электронного спинового резонанса в жидкостях организма в присутствии повышенного образования свободных радикалов. 77 Дегидроаскорбат относительно нестабилен и легко гидролизуется до дикетогулоновой кислоты, которая впоследствии расщепляется до щавелевой кислоты. Описаны два механизма, с помощью которых дегидроаскорбат может восстанавливаться до аскорбата; один опосредуется селеноферментной тиоредоксинредуктазой 78 , а другой является неферментной реакцией, в которой используется восстановленный глутатион. 79 Дегидроаскорбат в плазме, вероятно, быстро поглощается эритроцитами до рециркуляции, поэтому в плазме присутствует очень мало дегидроаскорбат, если он вообще присутствует. 80
Помимо аскорбата, в плазме в высоких концентрациях присутствуют другие антиоксиданты. Мочевая кислота эффективно улавливает радикалы, превращаясь в процессе в аллантоин. 81 Ураты могут быть особенно важны для защиты от некоторых окислителей, таких как озон. 82 Действительно, было высказано предположение, что увеличение продолжительности жизни, которое произошло в ходе эволюции человека, можно частично объяснить защитным действием мочевой кислоты в плазме крови человека. 83 Часть антиоксидантного действия урата может быть связана с образованием стабильных нереактивных комплексов с железом, но он также является прямым акцептором свободных радикалов. Связанный с альбумином билирубин также является эффективным поглотителем радикалов, 84 , и было высказано предположение, что он может играть особенно важную роль в защите новорожденных от окислительного повреждения, 85 , потому что дефицит других антиоксидантов, разрывающих цепь, часто встречается у новорожденных.
Другими основными антиоксидантами, разрушающими цепь, в плазме крови являются тиоловые группы, связанные с белками.Сульфгидрильные группы, присутствующие в белках плазмы, могут действовать как антиоксиданты, разрушающие цепь, отдавая электрон для нейтрализации свободных радикалов, что приводит к образованию тиильного радикала белка. Альбумин является преобладающим белком плазмы и вносит основной вклад в сульфгидрильные группы плазмы, хотя он также обладает рядом других антиоксидантных свойств. 86 Альбумин содержит 17 дисульфидных мостиков и имеет единственный оставшийся цистеиновый остаток, и именно этот остаток отвечает за способность альбумина реагировать с пероксильными радикалами и нейтрализовать их. 87 Это свойство важно с учетом роли, которую альбумин играет в транспортировке свободных жирных кислот в крови. Кроме того, альбумин обладает способностью связывать ионы меди и ингибировать медьзависимое перекисное окисление липидов и образование гидроксильных радикалов. Он также является мощным поглотителем хлорноватистой кислоты фагоцитарного продукта и обеспечивает основную защиту плазмы от этого окислителя. 88
Поскольку сам альбумин повреждается, когда он действует как антиоксидант, его рассматривают как жертвенную молекулу, которая предотвращает повреждение более жизненно важных видов. 86 Высокая концентрация альбумина в плазме и относительно короткий период полураспада означают, что любое нанесенное повреждение вряд ли будет иметь биологическое значение. Однако работа in vitro показала, что тиильные радикалы белка могут сами действовать как потенциальный источник реактивных окислителей. Тиильный радикал может отщеплять электрон от полиненасыщенной жирной кислоты, чтобы инициировать процесс перекисного окисления липидов, 89 , реакцию, которая может быть ингибирована аскорбатом и ретинолом. Было показано, что антиоксидантные эффекты альбумина и других белков уменьшаются при высоких концентрациях, и было высказано предположение, что это связано с тем, что тиильные радикалы могут окислительно повредить другие молекулы.Важность этих открытий для антиоксидантной роли альбумина in vivo остается неясной.
Восстановленный глутатион (GSH) является основным источником тиоловых групп во внутриклеточном компартменте, но не имеет большого значения во внеклеточном пространстве. 90 GSH может действовать непосредственно как антиоксидант, улавливая множество радикалов, а также действовать как важный фактор для глутатионпероксидазы (обсуждалось выше). Тиоредоксин также может действовать как ключевой внутриклеточный антиоксидант, особенно при окислительно-восстановительной активации факторов транскрипции. 91
ВЗАИМОДЕЙСТВИЯ АНТИОКСИДАНТОВ, РАЗРЫВАЮЩИХ ЦЕПЬ
Хотя действие антиоксидантов, разрывающих цепь, было рассмотрено отдельно выше, важно помнить, что in vivo комплексные взаимодействия между антиоксидантами могут иметь место. Например, вероятно, что аскорбат будет рециркулировать токоферильный радикал на границе раздела вода-липид, таким образом регенерируя токоферол. 54 Это может иметь решающее значение для поддержания концентрации токоферола в липопротеинах и мембранах.Подобным образом глутатион может регенерировать аскорбат из дегидроаскорбат. Следовательно, между антиоксидантами, вероятно, будет существовать сложное взаимодействие, что затрудняет прогнозирование того, как антиоксиданты будут действовать in vivo. Поэтому становится бессмысленным спрашивать, какой антиоксидант наиболее важен: ответ будет зависеть от обстоятельств, существующих в конкретном микросреде в конкретное время, и от природы происходящего окислительного повреждения.
Вторым важным свойством антиоксидантов, разрывающих цепь, является их способность действовать как прооксиданты.В определенных обстоятельствах присутствие антиоксиданта может парадоксальным образом привести к усилению окислительного повреждения. Например, сообщалось, что прием витамина С может иногда приводить к усилению окислительного повреждения, особенно если также вводится железо. 92 Точно так же in vitro было ясно показано, что токоферол может способствовать окислению ЛПНП в отсутствие антиоксиданта водной фазы, такого как аскорбат. 93 Важны ли эти реакции in vivo, пока неясно.Однако возможность того, что антиоксиданты могут оказывать прооксидантное действие in vivo, необходимо учитывать при разработке и интерпретации результатов клинических испытаний добавок антиоксидантов.
БЕЛКИ, СВЯЗЫВАЮЩИЕ ПЕРЕХОДНЫЕ МЕТАЛЛЫ
Как обсуждалось выше, белки, связывающие переходные металлы (ферритин, трансферрин, лактоферрин и церулоплазмин), действуют как решающий компонент системы антиоксидантной защиты, связывая железо и медь, так что они не могут управлять образованием гидроксильного радикала.Основной белок, связывающий медь, церулоплазмин, также может действовать как антиоксидантный фермент, который может катализировать окисление двухвалентного железа. 94
Fe 2+ представляет собой форму железа, которая запускает реакцию Фентона, и поэтому быстрое окисление Fe 2+ до менее реакционной формы Fe 3+ является антиоксидантным эффектом.
Последствия окислительного повреждения
Окислительный стресс, возникающий в результате дисбаланса между производством свободных радикалов и антиоксидантной защитой, связан с повреждением широкого спектра молекулярных видов, включая липиды, белки и нуклеиновые кислоты.Липопротеиновые частицы или мембраны обычно подвергаются процессу перекисного окисления липидов, что приводит к образованию множества продуктов, включая короткоцепочечные альдегиды, такие как малоновый диальдегид или 4-гидроксиноненаль, алканы и алкены, конъюгированные диены и различные гидроксиды и гидропероксиды. 45 Многие из этих продуктов можно определить как маркеры перекисного окисления липидов. Подробное обсуждение этого сложного вопроса выходит за рамки данного обзора, но измерение изопростанов с помощью газовой хроматографии, масс-спектроскопии, вероятно, является наиболее специфическим маркером повреждения липидов свободными радикалами. 95 Окислительное повреждение белков и нуклеиновых кислот аналогичным образом приводит к появлению множества специфических продуктов повреждения в результате модификаций аминокислот или нуклеотидов. 45 Такое окислительное повреждение также может приводить к клеточной дисфункции, и именно это может вносить вклад в патофизиологию широкого спектра заболеваний.
Окислительный стресс и болезни
Роль окислительного стресса была постулирована во многих состояниях, включая атеросклероз, воспалительные состояния, 96 определенных видов рака, 97 и процесс старения. 98 Во многих случаях это следует за наблюдением повышенного количества продуктов повреждения свободными радикалами, особенно маркеров перекисного окисления липидов, в жидкостях организма. Однако важно помнить, что перекисное окисление липидов — неизбежное сопровождение гибели клеток по любой причине. В большинстве случаев перекисное окисление является вторичным явлением, и поэтому это напрямую не указывает на важную роль окислительного стресса в данном заболевании. Если основная роль окислительного стресса в определенных условиях должна поддерживаться, должен существовать правдоподобный механизм, с помощью которого может происходить увеличение выработки свободных радикалов или снижение антиоксидантной защиты.Кроме того, признаки окислительного стресса должны быть обнаружены до начала повреждения тканей, а повышение антиоксидантного статуса на ранней стадии должно либо предотвратить, либо значительно уменьшить повреждение тканей.
Атеросклероз можно рассматривать как пример процесса, для которого есть существенные доказательства роли окислительного стресса. Гиперхолестеринемия повсеместно считается основным фактором риска атеросклероза. Однако при любой данной концентрации холестерина в плазме по-прежнему существует большая вариабельность возникновения сердечно-сосудистых событий.Одним из главных достижений в исследованиях атерогенеза стало осознание того, что окислительная модификация ЛПНП может быть критически важным шагом в развитии атеросклеротической бляшки. 99 , 100 Образование пенистых клеток из макрофагов, происходящих из моноцитов, в ранних атеросклеротических поражениях не вызывается нативным ЛПНП, а только после модификации ЛПНП различными химическими реакциями, такими как окисление. Окисление ЛПНП — это процесс, инициируемый и распространяемый свободными радикалами или одним из нескольких ферментов, 101 , и считается, что он происходит в основном в стенке артерии в микросреде, где антиоксиданты могут истощаться.Все клетки стенки сосуда — эндотелиальные клетки, клетки гладких мышц, макрофаги и лимфоциты — могут изменять ЛПНП in vitro. 102 — 104 Вероятно задействованы несколько механизмов, включая опосредованное ионами переходного металла образование гидроксильных радикалов, производство активных форм кислорода такими ферментами, как миелопероксидаза и липоксигеназа, и прямая модификация реактивными формами азота. Поскольку окисление ЛПНП является в первую очередь процессом, опосредованным свободными радикалами, который ингибируется антиоксидантами, истощение запасов антиоксидантов может быть фактором риска сердечно-сосудистых заболеваний (ССЗ).
Доказательства окисления ЛПНП in vivo в настоящее время хорошо установлены. В иммуноцитохимических исследованиях антитела против окисленных ЛПНП окрашивают атеросклеротические поражения, но не нормальную артериальную ткань. 105 Было показано, что ЛПНП, экстрагированные из поражений животных и человека, окисляются и быстро поглощаются рецепторами скавенджеров макрофагов. 106 У молодых людей, переживших инфаркт миокарда (ИМ), была продемонстрирована связь между повышенной восприимчивостью ЛПНП к окислению и степенью коронарного атеросклероза, 107 , тогда как было показано присутствие цероида, продукта перекисного окисления липидов. в запущенных атеросклеротических бляшках. 108
Окисленный ЛПНП обладает рядом свойств, способствующих атерогенезу, помимо быстрого поглощения макрофагами через рецептор скавенджера. Окисленные формы ЛПНП являются хемотаксисом для циркулирующих макрофагов и гладкомышечных клеток и способствуют адгезии моноцитов к эндотелию и проникновению в субэндотелиальное пространство. 109 Окисленные ЛПНП также цитотоксичны по отношению к артериальным эндотелиальным клеткам 110 и ингибируют высвобождение оксида азота и, как следствие, зависимую от эндотелия вазодилатацию. 111 Следовательно, существует потенциальная роль окисленных ЛПНП в изменении вазомоторных реакций, что, возможно, способствует вазоспазму в пораженных сосудах. Кроме того, окисленные ЛПНП иммуногенны; аутоантитела против различных эпитопов окисленных ЛПНП были обнаружены в сыворотке крови человека. 112 , 113 и иммуноглобулин (IgG), специфичный для эпитопов окисленных ЛПНП, могут быть обнаружены в очагах поражения. 114 Окисленные ЛПНП могут побуждать клетки стенки артерии продуцировать хемотаксические факторы, молекулы адгезии, цитокины и факторы роста, которые играют роль в развитии бляшки. 115 , 116
Помимо атерогенных последствий окисления ЛПНП, все более широко признается, что активные формы кислорода и азота напрямую взаимодействуют с сигнальными механизмами в стенке артерии, регулируя функцию сосудов. 117 Активность ферментов, генерирующих оксидант, в стенке артерии регулируется как активацией рецептора, так и путями, не опосредованными рецептором. Воздействие антиоксидантов на эти процессы является сложным, но обеспечивает альтернативные механизмы, с помощью которых добавление антиоксидантов может улучшить патологию сосудов, например, за счет улучшения функции эндотелия.
Доказательства того, что антиоксидантные микронутриенты потенциально снижают риск ИБС, получены из четырех основных источников. Во-первых, исследования приема антиоксидантных добавок на животных моделях атеросклероза в целом показали снижение заболеваемости. 118 , 119 Во-вторых, многие исследования показали, что прием антиоксидантных добавок у здоровых субъектов или пациентов с ИБС может снизить уровни продуктов повреждения свободными радикалами и защитить ЛПНП от окисления. 120 , 121 Витамин Е оказался наиболее эффективным антиоксидантом; и β-каротин, и витамин C увеличили время задержки окисления только в нескольких исследованиях, хотя остается возможность, что они могут иметь положительный эффект у людей с плохим исходным статусом.В-третьих, крупномасштабные эпидемиологические исследования обычно показывают, что низкое потребление антиоксидантов связано с повышенным риском сердечно-сосудистых заболеваний после корректировки других факторов риска. 122 — 125 Эпидемиологические доказательства наиболее убедительны в случае витамина Е. В частности, в двух крупных продольных исследованиях в США изучалась связь между приемом антиоксидантов и риском ИБС. В группе из 39 910 медицинских работников-мужчин мужчины, которые принимали добавки витамина Е в дозах не менее 100 МЕ / день в течение более двух лет, имели относительный риск ИБС на 37% ниже, чем те, кто не принимал добавки витамина Е, после корректировки. относительно возраста, факторов риска коронарных заболеваний и потребления витамина С и β-каротина. 126 В исследовании здоровья медсестер с участием 87 245 медсестер выяснилось, что у женщин, которые принимали добавки витамина Е более двух лет, относительный риск серьезной коронарной болезни был на 41% ниже. 127 Этот эффект сохранялся после корректировки с учетом возраста, курения, ожирения, физических упражнений, артериального давления, холестерина и использования заместительной терапии эстрогенами в постменопаузе, аспирина, витамина С и β-каротина. Высокое потребление витамина Е из пищевых источников не было связано со значительным снижением риска, хотя даже самые высокие уровни потребления витамина Е с пищей были намного ниже, чем его потребление среди пользователей добавок.
Доказательства связи водорастворимого витамина С с сердечно-сосудистыми заболеваниями менее убедительны, чем для витамина Е. В последующем исследовании врачей высокое потребление витамина С не было связано с более низким риском ИБС у мужчин, в то время как у женщин из По данным обследования состояния здоровья медсестер, первоначальный эффект был ослаблен после корректировки на использование поливитаминов. Только одно проспективное исследование с участием 11 348 взрослых продемонстрировало обратную зависимость между потреблением витамина С и общей смертностью от сердечно-сосудистых заболеваний. 128 Этот эффект в значительной степени является результатом использования витамина С в добавках и мог быть вызван другими витаминами-антиоксидантами в поливитаминных препаратах.Проспективное популяционное исследование 1605 здоровых мужчин в возрасте 42, 48, 54 или 60 лет в Финляндии недавно показало, что мужчины с дефицитом витамина С имели относительный риск ИМ 2,5 по сравнению с мужчинами с более высокими концентрациями витамина С в плазме после корректировки. для других факторов риска. 129 Есть также некоторые признаки того, что повышенное потребление β-каротина с пищей связано со снижением риска ИБС, хотя опять же доказательства менее убедительны, чем для витамина Е. В ходе обследования состояния здоровья будущих медсестер потребление витаминов А и β-каротин в пище и добавках слабо предсказывает заболеваемость ИБС; Газиано и Хеннекенс подсчитали снижение риска на 22% для женщин с самым высоким квинтилем β-каротина по сравнению с женщинами с самым низким. 130
Таким образом, существует правдоподобный случай, подтвержденный экспериментальными исследованиями, экспериментами на животных и эпидемиологией, связывающими окислительный стресс и атеросклероз. Ключевой тест такой гипотезы заключается в том, можно ли показать, что повышенное потребление антиоксидантов предотвращает клинические проявления атеросклероза у людей. В настоящее время эта проблема рассматривается в нескольких опубликованных рандомизированных исследованиях, а другие в настоящее время продолжаются. Первые результаты не обнадеживают.
Исследование α-токоферола и β-каротина по профилактике рака (ATBC), проведенное среди 29 133 мужчин, заядлых курильщиков в Финляндии, не выявило снижения заболеваемости или смертности от ИБС в течение пяти-восьми лет лечения витамином E (50 мг в день) или β-каротин (20 мг в день). 131 У тех, кому назначен витамин Е, не было значительного снижения смертности от ишемической болезни сердца (ИБС), но на 50% больше случаев смерти от церебрального кровоизлияния, тогда как у тех, кому назначен бета-каротин, смертность от ИБС увеличилась на 11%. В дальнейшем анализе рассматривалась подгруппа исходных субъектов, перенесших ранее перенесенный ИМ. 132 Конечной точкой этого подисследования было первое серьезное коронарное событие после рандомизации. Доля серьезных коронарных событий не уменьшалась ни при приеме добавок альфа-токоферола, ни бета-каротина.Фактически, β-каротин приводил к увеличению риска ИБС со смертельным исходом (повышение риска на 75%). Было отмечено положительное влияние витамина Е на нелетальный ИМ со снижением риска на 38%. В отличие от этого, в китайском исследовании профилактики рака, проведенном среди 29 584 плохо питающихся жителей Линьсяня, Китай, рандомизированных на 5,25 лет для комбинированного режима приема 15 мг / день β-каротина, 30 мг / день витамина E и 50 мкг / день. day selenium привел к значительному снижению общей смертности на 9%, значительному снижению смертности от рака желудка на 21% и незначительному снижению смертности от цереброваскулярных заболеваний на 10%. 133 Однако разумность обобщения этих результатов на хорошо питаемое население остается сомнительной.
Исследование эффективности β-каротина и ретинола (CARET), предназначенное для проверки эффектов комбинированной добавки, содержащей 30 мг β-каротина и 25000 МЕ ретинола в день среди 18 314 курильщиков сигарет и лиц с профессиональным воздействием асбеста, было завершено досрочно, когда исследователи признали повышенный риск смерти от рака легких у тех, кто получал β-каротин, и, опять же, не было обнаружено положительного влияния на сердечно-сосудистые заболевания. 134 Что касается смертности от сердечно-сосудистых заболеваний, то в группе лечения наблюдалось незначительное увеличение на 26% (p = 0,06).
В медицинском исследовании приняли участие более 22 000 американских врачей-мужчин, получавших 50 мг β-каротина или плацебо через день в среднем в течение 12 лет. Судя по всему, исследование было проведено тщательно, и его результаты серьезно ставят под сомнение какое-либо положительное влияние таких добавок на сердечно-сосудистые заболевания в хорошо питающихся группах населения. Не наблюдалось значительного влияния на индивидуальные исходы или комбинированную конечную точку нефатального ИМ, нефатального инсульта и сердечно-сосудистой смерти, для которых относительный риск составлял 1.0 (95% доверительный интервал от 0,91 до 1,09). 135 Не было также доказательств вреда (или пользы) среди 11% участников, которые курили в настоящее время на исходном уровне, хотя нельзя было исключать небольшие эффекты.
Гринберг и др. изучали влияние добавок β-каротина (50 мг / день) у 1720 мужчин и женщин в течение среднего периода 4,3 года со средним периодом наблюдения 8,2 года. 136 Субъекты, чьи плазменные значения β-каротина находились в наивысшем квартиле в начале исследования, имели самый низкий риск смерти от всех причин по сравнению с лицами, находящимися в самом низком квартиле.Однако добавки не повлияли ни на все причины, ни на смертность от сердечно-сосудистых заболеваний. Таким образом, добавление β-каротина, по-видимому, не дает общих преимуществ для тех людей с хорошим питанием, которые относятся к низкому или среднему риску развития ИБС. Однако ситуация может быть иной для тех, у кого в анамнезе уже было такое заболевание.
Hodis и др. показали снижение прогрессирования ИБС (измеренное ангиографически) у мужчин, получавших 100 МЕ витамина Е ежедневно, хотя не было обнаружено никаких преимуществ для витамина С. 137 Singh и др. обнаружили, что комбинация витаминов A, C, E и β-каротина, вводимая в течение нескольких часов после острого инфаркта миокарда и продолжающаяся в течение 28 дней, приводила к значительно меньшему количеству сердечных приступов и снижению частоты стенокардии. в дополненной группе. 138 Кембриджское исследование сердечных антиоксидантов (CHAOS), испытание добавок витамина E на 2002 пациентах с ангиографическими признаками ишемической болезни сердца, было проведено со средней продолжительностью лечения 1.4 года. 139 Было обнаружено, что это краткосрочное добавление альфа-токоферола (268 или 537 мг / день) снижает заболеваемость ИБС у пациентов, поскольку у пациентов значительно (77%) снижается риск последующего нефатального ИМ. Однако не было обнаружено никаких преимуществ с точки зрения смертности от сердечно-сосудистых заболеваний, с незначительным превышением среди участников, получавших витамин Е.
В исследовании GISSI-P рандомизировано 11 324 мужчин, переживших инфаркт миокарда, которые получали 300 мг витамина E, 1 г n-3 полиненасыщенных жирных кислот (ПНЖК), оба или ни одного в рандомизированном плацебо-контролируемом исследовании. 140 Результаты показали положительный эффект n-3 ПНЖК, но не положительный эффект витамина E (p = 0,07). Однако дальнейший анализ вторичных конечных точек показал некоторые положительные эффекты витамина Е. Кроме того, действие витамина Е могло быть улучшено средиземноморской диетой испытуемых. Ни одна из этих квалификаций не верна для исследования HOPE, 141 , в котором было задействовано более 9000 субъектов, которые, вероятно, придерживались типичной североевропейской диеты, которые имели высокий риск сердечно-сосудистых событий, потому что у них были сердечно-сосудистые заболевания или диабет в дополнение к еще одному фактору риска. .Субъекты были случайным образом распределены по факторному плану два на два для получения либо 400 МЕ витамина Е ежедневно из природных источников, либо соответствующего плацебо и либо ингибитора ангиотензинпревращающего фермента (рамиприл), либо соответствующего плацебо в течение в среднем 4,5 года. Добавки витамина Е не влияли на первичные или вторичные сердечно-сосудистые конечные точки.
Таким образом, в отношении витамина Е в западных популяциях единственные доступные данные испытаний первичной профилактики получены из исследования ATBC, которое не показало никакого эффекта.При вторичной профилактике накапливающиеся данные испытаний витамина Е менее последовательны, хотя и не особенно обнадеживают. Исследование CHAOS было положительным, хотя и страдает ограничениями дизайна. Исследование GISSI-P дало пограничный результат, тогда как исследование HOPE было однозначно отрицательным.
Как мы должны интерпретировать несоответствие между данными когортных исследований и результатами клинических испытаний? В общем, может случиться так, что продолжительность клинических испытаний слишком коротка, чтобы показать пользу, и что для предотвращения атеросклероза требуется прием антиоксидантов в течение многих лет.Необходимо продумать дизайн исследования с учетом дозы, продолжительности лечения и периода последующего наблюдения, начальных значений антиоксидантов и рациона, а также степени и распределения существующего атеросклероза. На животных моделях почти всегда проверяли влияние антиоксидантов на ранние атеросклеротические поражения. Еще предстоит выяснить, оказывают ли антиоксиданты ингибирующее действие на более поздних стадиях. Кроме того, сложная смесь антиоксидантных микронутриентов, содержащихся в диете с высоким содержанием фруктов и овощей, может быть более эффективной, чем большие дозы небольшого количества витаминов-антиоксидантов.Возможно, некоторые из этих соединений работают вместе, но не действуют по отдельности, или что другие диетические компоненты (например, микроэлементы) могут быть эффекторами антиоксидантного действия. Доказательства испытаний, доступные до сих пор, относятся только к α-токоферолу и β-каротину. Хотя эти антиоксиданты эффективны для защиты от перекисного окисления липидов, они мало влияют на функцию эндотелия артерий. Аскорбат, напротив, кажется более эффективным в улучшении функции эндотелия, хотя существует меньше эпидемиологических подтверждений защитного действия аскорбата.
С другой стороны, значимые результаты, связывающие потребление антиоксидантов с риском ИБС, наблюдаемые в когортных исследованиях, могут быть результатом смешения с другим образом жизни. Слэттери и др. изучали диетические антиоксиданты и липиды плазмы в исследовании развития риска коронарных артерий у молодых людей (CARDIA) и обнаружили, что более высокое потребление антиоксидантов было связано с другими факторами образа жизни, такими как физическая активность и отказ от курения. 142 Концентрации антиоксидантов в плазме связаны с социальным классом, они выше в более обеспеченных группах.Хотя эти переменные можно индивидуально контролировать в анализах, возможно, потребуется изучить сложную модель поведения на протяжении всей жизни, прежде чем делать выводы относительно антиоксидантов и ИБС. Например, недавно было показано, что пассивное курение оказывает атерогенное влияние на ЛПНП, 143 , однако курение является сложной переменной образа жизни, которую трудно контролировать в когортном анализе.
Выводы
Имеются неопровержимые доказательства того, что окислительный стресс возникает в клетках как следствие нормальных физиологических процессов и взаимодействий с окружающей средой, и что сложная сеть систем антиоксидантной защиты играет ключевую роль в защите от окислительного повреждения.Эти процессы, по-видимому, нарушаются во многих условиях, и может быть построена правдоподобная гипотеза, предполагающая, что окислительный стресс является причиной повреждения тканей. Однако, как показано на примере ИБС, попытки терапевтического вмешательства с использованием антиоксидантных добавок до сих пор в значительной степени не увенчались успехом. Более полное понимание биохимических событий, происходящих на клеточном уровне и влияющих на окислительное повреждение, необходимо для руководства будущими терапевтическими достижениями.
Каталожные номера
- ↵
Halliwell B, Gutteridge JC.Определение и измерение антиоксидантов в биологических системах. Free Radic Biol Med 1995; 18: 125–6.
- ↵
Halliwell B; Gutteridge JM. Свободные радикалы в биологии и медицине , 2-е изд. Оксфорд: Clarendon Press, 1989.
- ↵
Halliwell B, Gutteridge JC. Биологически релевантное образование гидроксильных радикалов, зависимое от ионов металлов, — обновленная информация. FEBS Lett 1992; 307: 108–12.
- ↵
Беккер Л. Б., Ванден Хук Т. Л., Шао Ч., и др. .Генерация супероксида в кардиомиоцитах при ишемии перед реперфузией. Am J Physiol 1999; 277: h3240–6.
- ↵
Barbacanne MA, Margeat E, Arnal JF, и др. . Высвобождение супероксида сливающимися эндотелиальными клетками, исследование электронно-спинового резонанса (ЭПР). Дж. Хим. Физ. Физ. Хим. Биол., 1999; 96: 85–92.
- ↵
Tsao PS, Heidary S, Wang A, et al . Протеинкиназа C-эпсилон опосредует индуцированное глюкозой продукцию супероксида и экспрессию MCP-1 в эндотелиальных клетках.FASEB J 1998; 12: 512.
- ↵
Мастерс CJ. Клеточная передача сигналов: роль пероксисомы. Cell Signal 1996; 8: 197–208.
- ↵
Curnutte JT, Babior BM. Хроническая гранулематозная болезнь. Adv Hum Genet 1987; 16: 229–45.
- ↵
Chance B, Sies H, Boveris A. Метаболизм гидропероксида в органах млекопитающих. Physiol Rev 1979; 59: 527–605.
- ↵
Halliwell B, Gutteridge JMC.Роль свободных радикалов и каталитических ионов металлов в заболеваниях человека: обзор. Методы Enzymol 1990; 186: 1–85.
- ↵
Тацузава Х., Маруяма Т., Хори К., и др. . Синглетный кислород как основной окислитель в опосредованном миелопероксидазой уничтожении бактерий в фагосомах нейтрофилов. Biochim Biophys Res Commun 1999; 262: 647–50.
- ↵
Ллойд Р.В., Ханна П.М., Мейсон Р.П. Происхождение гидроксильного радикала кислорода в реакции Фентона.Free Radic Biol Med 1997; 22: 885–8.
- ↵
Stohs SJ, Bagchi D. Окислительные механизмы токсичности ионов металлов. Free Radic Biol Med 1995; 18: 321–36.
- ↵
Goldenberg HA. Регуляция метаболизма железа у млекопитающих: текущее состояние и потребность в дополнительных знаниях. Crit Rev Clin Lab Sci 1997; 34: 529–72.
- ↵
Аруома О.И., Холливелл Б.Супероксид-зависимое и аскорбат-зависимое образование гидроксильных радикалов из пероксида водорода в присутствии железа. Biochem J, 1987; 241: 273–8.
- ↵
Гаттеридж Дж. М., Роули Д. А., Холливелл Б. Супероксид-зависимое образование гидроксильных радикалов в присутствии солей железа. Biochem J 1981; 199: 263–5.
- ↵
Gutteridge JC, Quinlan GJ, Evans TW. Транзиторная перегрузка железом блеомицином, обнаруживаемое в плазме крови пациентов с респираторным дистресс-синдромом у взрослых.Thorax 1994; 49: 707–10.
- ↵
Pepper JR, Mumby S, Gutteridge JC. Последовательное окислительное повреждение и изменения связывания железа и окисляющих железо антиоксидантов плазмы во время операции искусственного кровообращения. Free Radic Res 1994; 21: 377–85.
- ↵
Gutteridge JMC, Quinlan GJ. Образование малонового диальдегида из гидропероксидов липидов в тесте с тиобарбитуровой кислотой: роль липидных радикалов, солей железа и хелаторов металлов.J Appl Biochem 1983; 5: 293–9.
- ↵
О’Коннелл М., Холливелл Б., Мурхаус С, и др. . Образование гидроксильных радикалов в присутствии ферритина и гемосидерина. Является ли образование гемосидерина биологическим защитным механизмом? Biochem J 1986; 234: 727–31.
- ↵
Бенатти Ю., Морелли А., Гуида Л., и др. . Производство активированных форм кислорода за счет взаимодействия метгемоглобина с аскорбатом.Biochem Biophys Res Commun. 1983; 111: 980–7.
- ↵
Свейн Дж., Гаттеридж Дж. М.. Прооксидантное железо и медь с ферроксидазной и ксантиноксидазной активностями в атеросклеротическом материале человека. FEBS Lett 1995; 368: 513–15.
- ↵
Коидзуми М., Фуджи Дж., Сузуки К., и др. . Заметное увеличение уровней свободной меди в плазме и печени крыс LEC: животная модель болезни Вильсона и рака печени.Free Radic Res 1998; 28: 441–50.
- ↵
McCaughan JS. Фотодинамическая терапия — обзор. Наркотики старения 1999; 15: 49–68.
- ↵
Cross CE, Ван дер Вильт А., О’Нил С., и др. . Окислители, антиоксиданты и жидкости, выстилающие дыхательные пути. Environ Health Perspect 1994; 102: 185–91.
Kelly FJ, Mudway I, Krishna MT, и др. .Свободные радикалы в основе загрязнения воздуха сосредоточены на озоне. Респир Мед 1995; 89: 647–56.
- ↵
Келли Ф.Дж., Тетли ТД. Двуокись азота истощает мочевую кислоту и аскорбиновую кислоту, но не глутатион из жидкости слизистой оболочки легких. Biochem J 1997; 325: 95–9.
- ↵
Pourcelot S, Faure H, Firoozi F, и др. . Моча 8-оксо-7,8-дигидро-2′-дезоксигуанозина и 5- (гидроксиметил) урацила у курильщиков.Free Radic Res 1999; 30: 173–80.
- ↵
Вильгельм Дж., Фридрихова М., Визек М. Перекись водорода в дыхании крыс: эффекты гипоксии и параквата. Physiol Res 1999; 48: 445–9.
- ↵
Kapiotis S, Sengoelge G, Hermann M, et al . Парацетамол катализирует инициируемое миелопероксидазой окисление липидов в ЛПНП. Артериосклер Thromb Vasc Biol 1997; 17: 2855–60.
- ↵
Weijl NI, Cleton FJ, Osanto S.Свободные радикалы и антиоксиданты при токсичности, вызванной химиотерапией. Cancer Treat Rev 1997; 23: 209–40.
- ↵
Гевиртц Д.А. Критическая оценка предложенных механизмов действия противоопухолевых эффектов антрациклиновых антибиотиков адриамицина и даунорубицина. Biochem Pharmacol 1999; 57: 727–41.
- ↵
Киркман Х.Н., Галиано С., Гаэтани Г.Ф. Функция NADPH, связанного с каталазой. J Biol Chem 1987; 262: 660–5.
- ↵
Takahashi K, Cohen HJ. Селен-зависимый белок и активность глутатионпероксидазы: иммунологические исследования клеточных ферментов и ферментов плазмы. Кровь 1986; 68: 640–6.
- ↵
Накане Т., Асаяма К., Кодера К., и др. . Влияние дефицита селена на клеточные и внеклеточные глутатионпероксидазы: иммунохимическое обнаружение и анализ мРНК в почках и сыворотке крыс.Free Radic Biol Med 1998; 25: 504–11.
- ↵
Бригелиус-Флоэ Р. Тканеспецифические функции отдельных глутатионпероксидаз. Free Radic Biol Med 1999; 27: 951–65.
- ↵
Roxborough HE, Mercer C, McMaster D, et al . Активность глутатионпероксидазы в плазме снижается у пациентов, находящихся на гемодиализе. Нефрон 1999; 81: 278–83.
- ↵
Холбен Д.Х., Смит AM.Разнообразная роль селена в селенопротеинах: обзор. J Am Diet Assoc 1999; 99: 836–43.
- ↵
Гибсон Д.Г., Гаврилко Дж., Маккей ПБ. GSH-зависимое ингибирование перекисного окисления липидов: свойства мощной цитозольной системы, которая защищает клеточные мембраны. Липиды 1985; 20: 704–10.
- ↵
Liou W, Chang L-Y, Geuze HJ, et al. . Распределение супероксиддисмутазы CuZn в печени крыс.Free Rad Biol Med 1993; 14: 201–7.
- ↵
Вайзигер Р.А., Фридович И. Митохондриальная супероксиддисмутаза: сайт синтеза и внутримитохондриальная локализация. J Biol Chem 1973; 248: 4793–6.
- ↵
Марклунд С. Человеческая медьсодержащая супероксиддисмутаза с высокой молекулярной массой. Proc Natl Acad Sci U S. A 1982; 79: 7634–8.
- ↵
Карлссон К., Сандстром Дж., Эдлунд А., и др. .Фармакокинетика внеклеточной супероксиддисмутазы в сосудистой системе. Free Radic Biol Med 1993; 14: 185–90.
- ↵
McIntyre M, Bohr DF, Dominiczak AF. Гипертония функции эндотелия — роль супероксид-аниона. Гипертония 1999; 34: 539–45.
- ↵
Де Цварт Л.Л., Меерман Дж. Н., Командор Дж. М., и др. . Биомаркеры воздействия свободных радикалов у экспериментальных животных и людей.Free Radic Biol Med 1999; 26: 202–26.
- ↵
Холливелл Б. Как охарактеризовать антиоксидант: обновленная информация. Biochem Soc Symp 1995; 61: 73–101.
- ↵
Esterbauer H, Dieber-Rotheneder M, Striegl G, et al . Роль витамина Е в предотвращении окисления липопротеидов низкой плотности. Am J Clin Nutr 1991; 53: 314s – 21s.
- ↵
Horwitt MH.Данные, подтверждающие добавление витамина E к людям. J Nutr 1991; 121: 424–9.
- ↵
Урано С., Иномори Ю., Сугавара Т., и др. . Витамин-E — ингибирование ретинол-индуцированного гемолиза и мембраностабилизирующего поведения. J Biol Chem 1992; 267: 18365–70.
- ↵
Суонн, Иллинойс, Кендра-младший. Анемия, дефицит витамина Е и нарушение нормального развития у младенца. Clin Lab Haematol 1998; 20: 61–3.
- ↵
Сокол РЖ. Дефицит витамина Е и неврологические заболевания. Анну Рев Нутр 1988; 8: 351–73.
- ↵
Кайден Х.Дж., Трабер МГ. Абсорбция, транспорт липопротеинов и регуляция плазменных концентраций витамина Е у человека. J. Lipid Res 1993; 34: 343–58.
- ↵
Burton GW, Ingold KU. Витамин E: применение принципов физической органической химии к исследованию его структуры и функций.Acc Chem Res 1986; 19: 194–201.
- ↵
May JM, Qu ZC, Mendiratta S. Защита и рециркуляция альфа-токоферола в человеческих эритроцитах с помощью внутриклеточной аскорбиновой кислоты. Arch Biochem Biophys 1998; 349: 281–9.
- ↵
Каган В.Е., Тюрина Ю.Ю. Рециклинг и окислительно-восстановительный цикл фенольных антиоксидантов. На пути к продлению здоровой жизни. Энн Н. Ю. Акад. Наук 1998; 854: 425–34.
- ↵
Купер Д.А., Элдридж А.Л., Петерс Дж.С.Диетические каротиноиды и некоторые виды рака, болезни сердца и возрастная дегенерация желтого пятна: обзор недавних исследований. Nutr Rev 1999; 57: 201–14.
- ↵
Fukuzawa K, Inokami Y, Tokumura A, et al . Константы скорости тушения синглетного кислорода и активности по ингибированию перекисного окисления липидов каротиноидов и альфа-токоферола в липосомах. Липиды 1998; 33: 751–6.
- ↵
Chaudiere J, Ferrari-Iliou R.Внутриклеточные антиоксиданты: от химических механизмов к биохимическим. Food Chem Toxicol 1999; 37: 949–62.
- ↵
Ключи SA, Циммерман ВФ. Антиоксидантная активность ретинола, глутатиона и таурина в мембранах фоторецепторных клеток крупного рогатого скота. Exp Eye Res 1999; 68: 693–702.
- ↵
Rice-Evans CA, Miller NJ, Paganga G. Взаимосвязь между структурой и антиоксидантной активностью флавоноидов и фенольных кислот.Free Radic Biol Med 1996; 20: 933–56.
Hertog MGL, Hollman PCH, Katan MB. Содержание потенциально антиканцерогенных флавоноидов в 28 овощах и 9 фруктах, обычно потребляемых в Нидерландах. J Agric Food Chem 1992; 40: 2379–83.
- ↵
Hertog MGL, Hollman PCH, Putte B. Содержание потенциально антиканцерогенных флавоноидов в чайных настоях, винах и фруктовых соках. J. Agric Food Chem 1993; 41: 1242–6.
- ↵
Hertog MGL, Feskens EJM, Hollman PCH, и др. . Диетические антиоксидантные флавоноиды и риск ишемической болезни сердца: исследование пожилых людей Zutphen. Ланцет 1993; 342: 1007–11.
Hertog MGL, Kromhout D, Aravanis C, и др. . Потребление флавоноидов и долгосрочный риск ишемической болезни сердца и рака в исследовании 7 стран. Arch Intern Med 1995; 155: 381–6.
- ↵
Rimm EB, Katan MB, Ascerio A, и др. .Связь между приемом флавоноидов и риском ишемической болезни сердца у мужчин-медиков. Энн Интерн Мед 1996; 125: 384–9.
- ↵
Hollman PCH, Vries JHM, Leeuwen SD, и др. . Поглощение пищевых гликозидов кверцетина и квецетина у здоровых добровольцев после илеостомии. Am J Clin Nutr 1995; 62: 1276–82.
McAnlis GT, McEneny J, Pearce J, et al. . Всасывание и антиоксидантные эффекты кверцетина из лука у человека.Eur J Clin Nutr 1999; 53: 92–6.
- ↵
Серафини М., Гизелли А., Ферро-Луцци А. Антиоксидантный эффект зеленого и черного чая у человека in vivo. Eur J Clin Nutr 1996; 50: 28–32.
- ↵
Штейн Дж. Х., Кивил Дж. Г., Вибе Д. А., и др. . Фиолетовый виноградный сок улучшает функцию эндотелия и снижает восприимчивость холестерина ЛПНП к окислению у пациентов с ишемической болезнью сердца. Тираж 1999 г. 100: 1050–5.
- ↵
Day AP, Кемп Х.Дж., Болтон С., и др. . Влияние употребления концентрированного сока красного винограда на антиоксидантную способность сыворотки крови и окисление липопротеинов низкой плотности. Энн Нутр Метаб 1997; 41: 353–7.
- ↵
Shi HL, Noguchi N, Niki E. Сравнительное исследование динамики антиоксидантного действия альфа-токоферилгидрохинона, убихинола и альфа-токоферола против перекисного окисления липидов.Free Radic Biol Med 1999; 27: 334–46.
- ↵
Lass A, Sohal RS. Связанный с электронным транспортом убихинон-зависимый рециклинг альфа-токоферола ингибирует автоокисление митохондриальных мембран. Arch Biochem Biophys 1998; 352: 229–36.
- ↵
Thomas SR, Neuzil J, Stocker R. Дополнительные добавки с коферментом Q предотвращают прооксидантный эффект альфа-токоферола и повышают устойчивость ЛПНП к инициированию окисления, зависимого от переходных металлов.Артериосклер Thromb Vasc Biol 1996; 16: 687–96.
- ↵
Левин М., Рамси С.К., Дарувала Р., и др. . Критерии и рекомендации по приему витамина С. JAMA 1999; 281: 1415–23.
- ↵
Левин М. Новые концепции в биологии и биохимии аскорбиновой кислоты. N Engl J Med 1986; 314: 892–902.
- ↵
Jialal I, Vega GL, Grundy SM.Физиологические уровни аскорбата подавляют окислительную модификацию липопротеинов низкой плотности. Атеросклероз 1990; 82: 185–91.
- ↵
Пьетри С., Сегин Дж. Р., Дарбиньи П., и др. . Свободный радикал аскорбила — неинвазивный маркер окислительного стресса в хирургии открытого сердца человека. Free Radic Biol Med 1994; 16: 523–8.
- ↵
May JM, Cobb CE, Mendiratta S, et al . Восстановление свободных радикалов аскорбила до аскорбата с помощью тиоредоксинредуктазы.J Biol Chem 1998; 273: 23039–45.
- ↵
May JM, Qu ZC, Whitesell RR, et al . Рециркуляция аскорбата в эритроцитах человека: роль GSH в снижении дегидроаскорбат. Free Radic Biol Med 1996; 20: 543–51.
- ↵
Koshiishi I, Mamura Y, Liu J, et al. . Оценка кислотной депротеинизации для измерения аскорбата и дегидроаскорбат в образцах плазмы.Clin Chem 1998; 44: 863-8.
- ↵
Grootveld M, Halliwell B. Измерение аллантоина и мочевой кислоты в жидкостях человеческого тела. Потенциальный показатель свободнорадикальных реакций in vivo? Biochem J. 1987; 243: 803-8.
- ↵
Cross CE, Reznick AZ, Packer L, и др. . Окислительное повреждение белков плазмы человека озоном. Free Radic Res Commun 1992; 15: 347–52.
- ↵
Эймс Б.Н., Кэткарт Р., Швиерс Э., и др. .Мочевая кислота обеспечивает антиоксидантную защиту человека от старения и рака, вызванного окислителями и радикалами. Proc Natl Acad Sci U S. A, 1981; 78: 6858–62.
- ↵
Frei B, Stocker R, Ames BN. Антиоксидантная защита и перекисное окисление липидов в плазме крови человека. Proc Natl Acad Sci U S A 1988; 85: 9748–52
- ↵
Гопинатан В., Миллер Н.Дж., Милнер А.Д., и др. . Антиоксидантная активность билирубина и аскорбата в плазме новорожденных.FEBS Lett 1994; 349: 97–200.
- ↵
Halliwell B. Альбумин — важный внеклеточный антиоксидант? Biochem Pharmacol 1988; 37: 569–71.
- ↵
Stocker R, Frei B. Эндогенная антиоксидантная защита в плазме крови человека. В: Rice-Evans C, ed. Окислительный стресс: оксиданты и антиоксиданты . Лондон: Academic Press, 1991: 213–43.
- ↵
Ху М.Л., Луи С., Кросс CE, и др. .Антиоксидантная защита от хлорноватистой кислоты в плазме крови человека. J Lab Clin Med 1993; 121: 257–62.
- ↵
Ридл А., Шамси З., Андертон М. Различные свойства белков в мембранах могут приводить к антиоксидантному или прооксидантному действию: противоположные эффекты на перекисное окисление липидов алкогольдегидрогеназы и альбумина в липосомальных системах. Редокс Реп 1996; 2: 35-40.
- ↵
Sastre J, Pallardo FV, Vina J.Глутатион, окислительный стресс и старение. Возраст 1996; 19: 129–39.
- ↵
Арриго AP. Экспрессия генов и окислительно-восстановительное состояние тиолов. Free Radic Biol Med 1999; 27: 936–44.
- ↵
Suh J, Zhu BZ, Frei B. Анти- и прооксидантные эффекты аскорбата на железо-опосредованное окислительное повреждение бычьего сывороточного альбумина. Free Radic Biol Med 1999; 27: 305s1.
- ↵
Neuzil J, Thomas SR, Stocker R.Требование, стимулирование или ингибирование альфа-токоферолом радикально-индуцированного инициирования перекисного окисления липопротеинов плазмы. Free Radic Biol Med 1997; 22: 57–71.
- ↵
Атанасиу Р.Л., Стеа Д., Матееску М.А., и др. . Прямое свидетельство антиоксидантных свойств церулоплазмина. Mol Cell Biochem 1998; 189: 127–35.
- ↵
Лю Т., Стерн А., Робертс Л.Дж., и др. . Изопростаны: новые простагландиноподобные продукты перекисного окисления арахидоновой кислоты, катализируемого свободными радикалами.J Biomed Sci 1999; 6: 226–35.
- ↵
Розенфельд МЭ. Воспаление, липиды и свободные радикалы: уроки атерогенного процесса. Семин Репрод Эндокринол 1998; 16: 249–61.
- ↵
Hecht SS. Канцерогены табачного дыма и рак легких. J Natl Cancer Inst 1999; 91: 1194–210.
- ↵
Ашок Б.Т., Али Р. Парадокс старения: свободнорадикальная теория старения.Exp Gerontol 1999; 34: 293–303.
- ↵
Witztum JL, Steinberg D. Роль окисленных ЛПНП в атерогенезе. Дж. Клин Инвест, 1991; 88: 1785–92.
- ↵
Witztum JL, Horkko S. Роль окисленных ЛПНП в атерогенезе: иммунологический ответ и антифосфолипидные антитела. Энн Н. Ю. Акад. Наук 1997; 811: 88–99.
- ↵
Heinecke JW. Механизмы окислительного повреждения липопротеидов низкой плотности при атеросклерозе человека.Curr Opin Lipidol 1997; 8: 268–74.
- ↵
Morel DW, DiCorleto PE, Chisholm GM. Эндотелиальные и гладкомышечные клетки изменяют липопротеины низкой плотности in vitro путем свободнорадикального окисления. Артериосклероз 1984; 4: 357–64.
Хенриксен Т., Махони Е.М., Стейнберг Д. Усиленная деградация макрофагами липопротеинов низкой плотности, ранее инкубированных с культивированными эндотелиальными клетками: распознавание рецептором ацетилированных липопротеинов низкой плотности.Proc Natl Acad Sci U S. A 1981; 78: 6499–503.
- ↵
Фольчик В.А., Нивар-Аристы Р.А., Краевский Л.П., и др. Липоксигеназа способствует окислению липидов в атеросклеротических бляшках человека. J Clin Invest 1995; 96: 504–10.
- ↵
Итабе Х., Ямамото Х., Иманака Т., и др. . Чувствительное обнаружение окислительно модифицированного липопротеина низкой плотности с использованием моноклональных антител.J. Lipid Res 1996; 37: 45–53.
- ↵
Yla-Herttuala S, Palinski W, Rosenfeld ME, и др. . Доказательства присутствия окислительно модифицированного липопротеина низкой плотности в атеросклеротических поражениях кролика и человека. Дж. Клин Инвест 1989; 84: 1086–95.
- ↵
Регнстром Дж., Нильссон Дж., Торнвалл П., и др. . Восприимчивость к окислению липопротеинов низкой плотности и атеросклерозу коронарных артерий у человека.Lancet 1992; 339: 1183–6.
- ↵
Болл Р.Й., Карпентер К.Л., Митчинсон М.Дж. Какое значение имеет цероид при атеросклерозе человека? Arch Pathol Lab Med 1987; 111: 1134–40.
- ↵
Navab M, Imes S, Hama S, и др. . Трансмиграция моноцитов, индуцированная модификациями ЛПНП в сокультурах клеток стенки аорты человека, происходит из-за индукции синтеза хемотаксического белка I моноцитов и отменяется ЛПВП.Дж. Клин Инвест, 1991; 88: 2039–46.
- ↵
Hessler JR, Робертсон А.Л., Чисолм GM. Цитотоксичность ЛПНП и ее ингибирование ЛПВП в гладких мышцах сосудов человека и культуре эндотелиальных клеток. Атеросклероз 1979; 32: 213.
- ↵
Kugiyama K, Kerns SA, Morrisett JD, et al. . Нарушение эндотелиально-зависимой артериальной релаксации лизолецитином в модифицированных липопротеинах низкой плотности.Nature 1990; 344: 160–2.
- ↵
Salonen JT, Yla-Herttuala S, Yamamoto R, et al . Аутоантитела против окисленных ЛПНП и прогрессирования атеросклероза сонных артерий. Lancet 1992; 339: 883–7.
- ↵
Bergmark C, Wu R, de Faire U, и др. . У пациентов с ранним началом заболевания периферических сосудов повышен уровень аутоантител к окисленным ЛПНП. Артериосклер Thromb Vasc Biol 1995; 15: 441–5.
- ↵
Либби П., Ханссон Г.К. Участие иммунной системы в атерогенезе человека: современные знания и вопросы, на которые нет ответов. Lab Invest 1991; 64: 5–15.
- ↵
Кита Т., Куме Н., Исии К., и др. . Окисленный ЛПНП и экспрессия молекул адгезии моноцитов. Клиническая практика диабета, 1999; 45: 123–6.
- ↵
Huang YH, Schafer-Elinder L, Wu R, et al .Лизофосфатидилхолин (LPC) индуцирует провоспалительные цитокины посредством механизма, зависимого от рецептора фактора активации тромбоцитов (PAF). Clin Exp Immunol 1999; 116: 326–31.
- ↵
Wolin MS. Взаимодействие оксидантов с сигнальными системами сосудов. Артериосклер Thromb Vasc Biol 2000; 20: 1430–42.
- ↵
Bjorkhem I, Henrikssonfreyschuss A, Breuer O, et al . Антиоксидант бутилированный гидрокситолуол защищает от атеросклероза.Артериосклер Тромб 1991; 11: 15–22.
- ↵
Verlangieri AJ, Буш MJ. Влияние добавок d-альфа-токоферола на экспериментально индуцированный атеросклероз приматов. J Am Coll Nutr 1992; 11: 131–8.
- ↵
Stocker R, Bowry VW, Frei B. Убихинол-10 защищает липопротеины низкой плотности человека более эффективно от перекисного окисления липидов, чем альфа-токоферол. Proc Natl Acad Sci U S A, 1991; 88: 1646–50.
- ↵
Esterbauer H, Puhl H, Dieber-Rotheneder M, и др. . Влияние антиоксидантов на окислительную модификацию ЛПНП. Энн Мед 1991; 23: 573–81.
- ↵
Reaven PD, Khouw A, Beltz WF, и др. . Влияние диетических комбинаций антиоксидантов на человека. Защита ЛПНП витамином Е, но не бета-каротином. Артериосклер Тромб 1993; 13: 590–600.
Гей К.Г., Пуска П., Иордания П., и др. .Обратная корреляция между витамином Е и смертностью от ишемической болезни сердца в кросс-культурной эпидемиологии. Am J Clin Nutr 1991; 53: S326–34.
Riemersma RA, Wood DA, MacIntyre CCA, и др. . Риск стенокардии и концентрации в плазме витаминов A, C и E и каротина. Ланцет 1991; 337: 1–5.
- ↵
Salonen JT, Salonen R, Seppanen K, et al .Связь сывороточного селена и антиоксидантов с липопротеинами плазмы, агрегация тромбоцитов и распространенная ишемическая болезнь сердца у мужчин восточной Финляндии. Атеросклероз 1988; 70: 155–60.
- ↵
Rimm EB, Stampfer MJ, Ascherio A, и др. . Потребление витамина Е и риск ишемической болезни сердца у мужчин. N Engl J Med 1993; 328: 1450–6.
- ↵
Stampfer MJ, Hennekens CH, Manson JE, et al .Потребление витамина Е и риск ишемической болезни сердца у женщин. N Engl J Med 1993; 328: 1444–9.
- ↵
Enstrom JE, Kanim LE, Klein MA. Потребление витамина С и смертность среди выборки населения США. Эпидемиология 1992; 3: 194–202.
- ↵
Нюссонен К., Парвиайнен М.Т., Салонен Р., и др. . Дефицит витамина С и риск инфаркта миокарда: проспективное популяционное исследование мужчин из восточной Финляндии.BMJ 1997; 314: 634–8.
- ↵
Gaziano JM, Hennekens CH. Роль бета-каротина в профилактике сердечно-сосудистых заболеваний. Энн Н. Ю. Акад. Наук 1993; 691: 148–55.
- ↵
Альфа-токоферол, Исследовательская группа по профилактике рака бета-каротина. Влияние витамина Е и бета-каротина на заболеваемость раком легких и другими видами рака у курящих мужчин. N Engl J Med 1994; 330: 1029–35.
- ↵
Rapola JM, Virtamo J, Ripatti S, и др. .Рандомизированное испытание добавок альфа-токоферола и бета-каротина по частоте серьезных коронарных событий у мужчин с перенесенным инфарктом миокарда. Ланцет 1997; 349: 1715–20.
- ↵
Blot WJ, Li JY, Taylor PR, и др. . Испытания диетических вмешательств в Линьсяне, Китай: добавление определенных комбинаций витаминов / минералов, заболеваемость раком и смертность от конкретных болезней среди населения в целом. J Natl Cancer Inst 1993; 85: 1483–92.
- ↵
Omenn GS, Goodman GE, Thornquist MD, и др. . Влияние комбинации бета-каротина и витамина А на рак легких и сердечно-сосудистые заболевания. N Engl J Med 1996; 334: 1150–5.
- ↵
Hennekens CH, Buring JE, Manson JE, et al . Отсутствие эффекта от длительного приема бета-каротина на частоту злокачественных новообразований и сердечно-сосудистых заболеваний.N Engl J Med 1996; 334: 1145–9.
- ↵
Гринберг Э. Р., Барон Дж. А., Карагас М. Р., и др. . Смертность связана с низкой концентрацией бета-каротина в плазме и действием пероральных добавок. JAMA 1996; 275: 699–703.
- ↵
Hodis HN, Mack WJ, LaBrec L, и др. . Серийные коронарные ангиографические доказательства того, что прием витаминов-антиоксидантов снижает прогрессирование атеросклероза коронарных артерий.JAMA 1995; 273: 1849–54.
- ↵
Сингх РБ, Ниаз М.А., Растоги СС, и др. . Полезность витаминов-антиоксидантов при подозрении на острый инфаркт миокарда. Am J Cardiol 1996; 77: 232–6.
- ↵
Стивенс Н.Г., Парсонс А., Скофилд П.М., и др. . Рандомизированное контролируемое исследование витамина Е у пациентов с ишемической болезнью сердца: Кембриджское исследование сердечных антиоксидантов (CHAOS). Lancet 1996; 347: 781–6.
- ↵
Valagussa F, Franzosi MG, Geraci E, et al . Пищевые добавки с n-3 полиненасыщенными жирными кислотами и витамином E после инфаркта миокарда: результаты исследования GISSI-Prevenzione. Ланцет 1999; 354: 447–55.
- ↵
Юсуф С., Фил Д., Дагенаис Г., и др. . Добавки витамина Е и сердечно-сосудистые события у пациентов из группы высокого риска. N Engl J Med 2000; 342: 154–60.
- ↵
Слэттери М.Л., Джейкобс Д.Р., Дайер А, и др. . Диетические антиоксиданты и липиды плазмы: исследование CARDIA. J Am Coll Nutr 1995; 14: 635–42.
- ↵
Валконен М., Кууси Т. Пассивное курение вызывает атерогенные изменения липопротеинов низкой плотности. Тираж 1998; 97: 2012–16.
Гипотезы об антиоксидантах — полная чушь
Полифенолы в чернике и зеленом чае, бета-каротин в моркови и витамин С в красном перце и лимонах.
Это некоторые из классических антиоксидантов, которые, как часто думают, помогают бороться со свободными радикалами и окислением в организме и тем самым предотвращают такие заболевания, как рак и болезни сердца.
Но то, что мы едим много этих антиоксидантов, не означает, что они выполняют свою работу, — говорит профессор Ларс Порскьер Кристенсен из Университета Южной Дании, изучающий полезные для здоровья эффекты биологически активных веществ.
«Традиционные гипотезы об антиоксидантах — полная чушь», — говорит Кристенсен.
«Они говорят, что вещества, обладающие антиоксидантным действием в лаборатории, так называемые« прямые антиоксиданты », будут иметь такой же эффект в организме, если вы потребляете продукты, содержащие эти вещества, и что они будут иметь благотворно влияет на наше здоровье, уничтожая вредные свободные радикалы », — говорит он.
«Это предположение никогда не было доказано в действительности», — говорит он.
Кишечник плохо усваивает антиоксиданты
Есть несколько причин, по которым эта гипотеза неверна, говорит Кристенсен.
«Концентрация полифенолов и других антиоксидантов в крови часто настолько низка, что они не действуют», — говорит он.
«Многие [антиоксиданты] с трудом проходят через жировые мембраны, потому что они относительно полярны. Прежде чем они смогут пройти через клеточную мембрану, их нужно расщепить и сделать менее полярными, чем бактерии желудка ».
«Кроме того, в печени образуются антиоксиданты, большая часть которых быстро выводится с мочой.В остальном мы мало знаем о том, куда попадают вещества и сколько всасывается в клетки, где происходят центральные окислительно-восстановительные процессы », — говорит Кристенсен.
Профессор Ларс Ове Драгстед с факультета питания, физических упражнений и спорта Копенгагенского университета, Дания, согласен с этим.
«Это большое предположение, что прямые антиоксиданты, такие как полифенолы, действуют как антиоксиданты в организме человека и, следовательно, делают нас более здоровыми», — говорит Драгстед.
«Антиоксиданты и антиоксиданты — сложные понятия, потому что антиоксиданты включены в так называемый окислительно-восстановительный баланс организма.Это полностью зависит от окружающей среды, в которой они находятся, и они могут действовать как антиоксидант в одной ситуации и как прооксидант в другой », — говорит он.
Хорошим примером этого является витамин С, который может действовать как антиоксидант и как прооксидант.
Подробнее: Антиоксиданты удвоили распространение рака у мышей и клеток человека
Есть еще причины есть фрукты и овощи
Так следует ли нам забыть о фруктах и овощах?
Абсолютно нет, говорят ученые, поскольку они содержат другие биологически активные вещества, которые обладают антиоксидантным действием на организм.
«Фрукты и овощи содержат биологически активные вещества, которые во многих случаях не действуют как антиоксиданты, если вы анализируете их вне организма. Но похоже, что они действительно действуют как антиоксидант внутри организма, поскольку они активируют собственный антиоксидантный ответ организма и борются с окислительным стрессом », — говорит Кристенсен.
«Эти биологически активные вещества, на мой взгляд, являются настоящим секретом употребления фруктов и особенно овощей», — говорит он.
«Это естественные токсины растений, которые действуют как непрямые антиоксиданты, увеличивая собственные защитные белки организма, такие как ферменты детоксикации и антиоксидантные ферменты», — говорит он.
Подробнее: Антиоксиданты могут снизить эффект тренировки на выносливость
Работают ли какие-либо прямые антиоксиданты?
Антиоксиданты, такие как полифенолы, могут иметь косвенную пользу, если они стимулируют собственную антиоксидантную реакцию организма, — говорит Драгстед.
«Несмотря на то, что полифенолы демонстрируют сильный антиоксидантный эффект в лабораторных условиях, мы абсолютно уверены, что они не действуют как прямой антиоксидант в организме. В целом они, вероятно, работают как непрямой антиоксидант, который может стимулировать собственную антиоксидантную реакцию организма, но нам нужны дополнительные исследования, чтобы знать наверняка », — говорит он.
Но Драгстед уверен, что некоторые из наиболее известных антиоксидантов, включая витамин C, E и бета-каротин, не оказывают желаемого эффекта на человеческий организм.
«Исследования витаминов C и E в основном отрицательны. Большинство исследований показывают, что они не влияют на окислительно-восстановительный баланс. Они, конечно, важны для борьбы с недостатками, но брать больше, чем нужно, не помогает », — говорит он. И добавляет, что у большинства здоровых людей их достаточно, и им не нужно потреблять больше.
Бета-каротины обладают антиоксидантным действием только в определенных системах, например в растениях, и их чрезмерное употребление (намного больше, чем содержится во фруктах и овощах) может увеличить риск рака у курильщиков.
Селен может оказывать непрямое антиоксидантное действие на организм, но результаты неоднозначны.
«Селен — это еще один тип непрямого антиоксиданта, и существует множество исследований, посвященных его влиянию на организм. Некоторые исследования показали положительный эффект, а другие — нет.Но эффект зависит от формы, в которой он был принят, что может объяснить, почему некоторые исследования не показывают пользы для здоровья », — говорит Драгстед.
Ешьте фрукты и овощи, но избегайте антиоксидантных добавок
Ученые советуют продолжать есть фрукты и овощи, но избегать высоких уровней антиоксидантов, содержащихся в пищевых добавках.
В таких высоких дозах они могут иметь противоположный эффект и действовать как прооксидант, который вреден для нашего организма.
«Если, например, вы потребляете большое количество полифенолов, это имеет противоположный эффект, потому что кислород тела окисляет полифенолы, образуя новые радикалы, которые антиоксиданты должны удалять из организма», — говорит Кристенсен.
Он подчеркивает, что здоровое потребление пищи не является проблемой, и что такие высокие дозы потребляются только с помощью пищевых добавок.
————-
Прочтите датскую версию этой статьи на Videnskab.dk
Переведено: Catherine Jex
Внешние ссылки
Сопутствующие материалы
Антиоксиданты могут снизить эффект тренировок на выносливость
Если вы принимаете высокие ежедневные дозы антиоксидантов, витаминов C и E, вы рискуете получить меньше от тренировки.
Антиоксиданты удвоили распространение рака среди мышей и клеток человека
Научное мнение об антиоксидантах меняется, поскольку «противораковое» чудо приносит больше вреда, чем пользы.
Добавки кальция могут увеличить риск сердечного приступа и инсульта
Прием кальция и витамина D может помочь предотвратить переломы костей у пожилых женщин.Однако это преимущество может быть сведено на нет повышенным риском сердечного приступа и инсульта.
Пищевая добавка Q10 продлевает жизнь
Согласно датским исследованиям, пищевая добавка Q10 дает почти половине всех пациентов с сердечными заболеваниями лучшую жизнь и помогает им жить на годы дольше.