Какова роль воды в организме человека?
Вода в организме человека играет важную роль, проникая в кровь углеводы и белки и устраняя избыток соли, минералов и других веществ. Адекватное увлажнение также сохраняет тело прохладным, когда температура поднимается и во время физической активности. Вода в организме человека предотвращает запоры и сохраняет кожу мягкой и эластичной. Легкие и рот нуждаются в воде, чтобы функционировать должным образом, в то время как суставы используют воду в качестве смазки.
Каждая клетка в теле зависит от воды, которая растворяет химические вещества, минералы и питательные вещества, чтобы сделать их пригодными для использования. Если крови не хватает воды, она может не течь свободно и нести достаточное количество кислорода в органы и ткани. Кожа может стать сухой и потрескавшейся, когда потребление воды падает ниже рекомендуемого уровня.
Вода в организме человека составляет около 70 процентов от общего веса мозга. В крови содержится около 80 процентов воды, а в легких — около 90 процентов воды.
Каждый день вода в организме человека теряется из-за мочи, пота и дыхания. Его необходимо заменять ежедневно, потому что организм не может хранить воду для последующего использования. Количество выделяемой воды зависит от уровня активности человека, температуры наружного воздуха, индивидуального обмена веществ и количества жидкости, потребляемой в еде и напитках. Очень активным людям и тем, кто живет в жарком климате, обычно требуется больше воды, потому что они часто производят больше пота.
Детские тела содержат больше воды, чем взрослые, и могут быстрее обезвоживаться. Пожилым людям может потребоваться увеличить потребление воды, потому что функции почек меняются с возрастом. Пожилые люди могут терять до 2,1 литра (2 литра) воды в день из-за нормальных функций организма.
Обезвоживание может стать серьезным риском для здоровья, вызывая почечную недостаточность. Симптомы включают темную, желтую мочу, головную боль и недостаток энергии. Губы и кожа могут стать сухими вместе с сухостью во рту. К тому времени, когда человек испытывает жажду, обезвоживание уже может существовать, что может помешать концентрации и способности выполнять умственные или физические задачи.
Большинство диет обеспечивают около половины необходимой воды в организме человека. Диетологи обычно рекомендуют пить шесть-восемь стаканов воды в день для поддержания здоровья. Эти уровни могут быть получены из супов, фруктов, чая и других продуктов. Пациентам, которые используют лекарства, которые увеличивают мочеиспускание, может потребоваться увеличить ежедневное потребление воды. Люди, страдающие от лихорадки, рвоты или диареи, также могут быстро терять жизненно важные жидкости.
ДРУГИЕ ЯЗЫКИ
Какова роль воды в жизни организмов
Количество атмосферных осадков обусловлено физико-географическими условиями, но для организмов важнейшим лимитирующим фактором является распределение осадков по сезонам года. В умеренных широтах их неравномерность может привести к засухе или переувлажнению, в тропиках — к чередованию влажных и сухих сезонов при постоянной почти круглый год температуре.[ …]
Влажность воздушной среды измеряется обычно в показателях относительной влажности, т.е. в виде процента реального давления водяного пара от давления насыщенного пара при той же температуре. Отсюда способность влажности изменять эффекты температуры: понижение влажности ниже некоторого предела при данной температуре ведет к иссушающему действию воздуха.[ …]
Иссушающее действие воздуха имеет наиболее важное экологическое значение для растений. Подавляющее большинство растений всасывает воду корневой системой из почвы.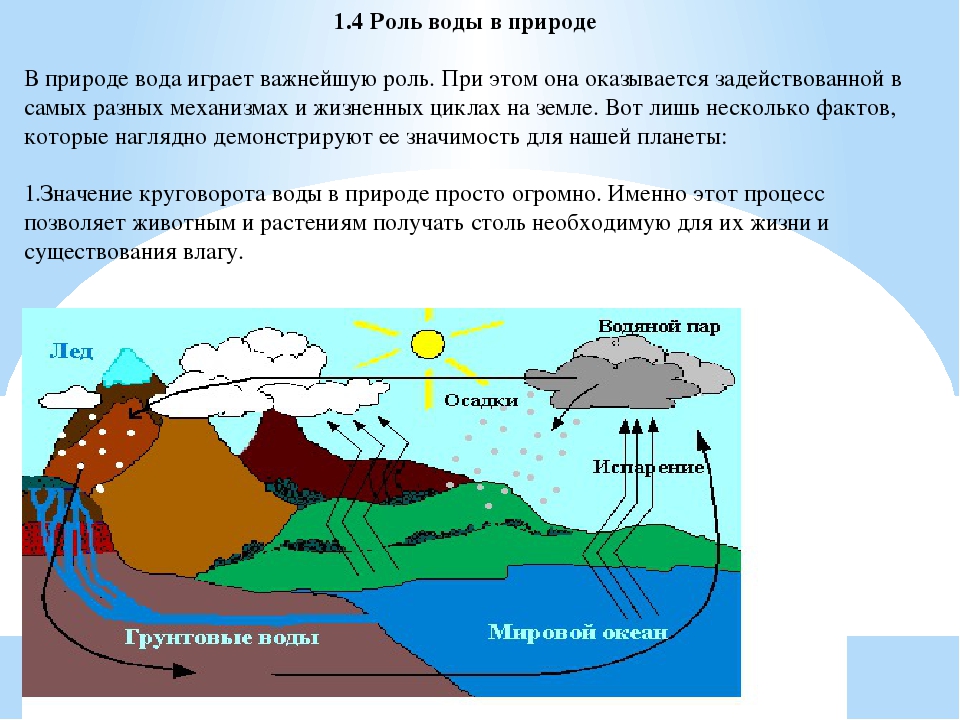 Иссушение почвы затрудняет всасывание. Адаптация растений к этим условиям — увеличение всасывающей силы и активной поверхности корней. Как только выбрана доступная вода в данном объеме, корни растут далее, вглубь и в стороны, и корневая система может достигнуть, например, у злаков длины 13 км на 1000 см3 почвы (без корневых волосков).[ …]
Иссушение почвы затрудняет всасывание. Адаптация растений к этим условиям — увеличение всасывающей силы и активной поверхности корней. Как только выбрана доступная вода в данном объеме, корни растут далее, вглубь и в стороны, и корневая система может достигнуть, например, у злаков длины 13 км на 1000 см3 почвы (без корневых волосков).[ …]
На фотосинтез клетками расходуется около 0,5% воды, а 97—99% ее уходит на транспирацию — испарение через листья. Эффективность транспирации — отношение прироста вещества (чистой продукции) к количеству транспириро-ванной воды (в граммах сухого вещества на 1000 см3 воды). Для большинства растений она равна двум, т.е. на получение грамма живого вещества тратится 500 г воды.[ …]
У животных по отношению к воде также выделяют свои экологические группы: гигрофилы (влаголюбивые) и ксеро-филы (сухолюбивые), а также промежуточную группу -ме-зофилы. Способы регуляции водного баланса у них поведенческие, морфологические и физиологические.[ …]
К поведенческим способам относятся перемещение в более влажные места, периодическое посещение водопоя, переход к ночному образу жизни и др. К морфологическим адаптациям — приспособления, задерживающие воду в теле: раковины наземных улиток, роговые покровы у рептилий и др. Физиологические приспособления направлены на образование метаболической воды, являющейся результатом обмена веществ и позволяющей обходиться без питьевой воды. Она используется насекомыми и такими животными, как овца, собака.[ …]
К морфологическим адаптациям — приспособления, задерживающие воду в теле: раковины наземных улиток, роговые покровы у рептилий и др. Физиологические приспособления направлены на образование метаболической воды, являющейся результатом обмена веществ и позволяющей обходиться без питьевой воды. Она используется насекомыми и такими животными, как овца, собака.[ …]
Значение и роль воды в жизни человека 3 класс
Трудно переоценить значение воды в нашей жизни, это настоящее природное богатство. Более половины нашей планеты занимают различные водоёмы. Вода вокруг нас может находиться в трёх состояниях: жидком – океаны, моря, реки, озёра, твёрдом – льды и снега, а также газообразном состоянии – туман, облака.
Да и сам человек на состоит из воды. Вода входит в состав крови и участвует в очищении организма. Недостаточное употребление жидкости может пагубно сказаться на состоянии здоровья человека, животного или птицы. И если без пищи мы можем обходиться до 40 дней, то без воды не более трёх суток.
И если без пищи мы можем обходиться до 40 дней, то без воды не более трёх суток.
С древних времён люди строили города и деревни по берегам водоёмов, ведь вода – это отличный помощник для человека. Реки, моря и океаны могут использоваться в качестве большой и удобной дороги. В любое время года, днём и ночью грузовые и пассажирские суда везут пассажиров и различные грузы. Тепло горячих источников используют в работе гидроэлектростанций. Приготовить обед, развести бетон для стройки, сделать бумагу, ткани, лекарства без воды невозможно. Заводам и фабрикам, сельскохозяйственным предприятиям также не обойтись без этого природного помощника. Не даром говорят – где вода, там и жизнь.
Воды вокруг нас очень много, но не вся она пригодна для жизнедеятельности. Для употребления в пищу, промышленности, сельского хозяйства необходима пресная вода, но её запасы на планете невелики, а из-за регулярного загрязнения и неэкономного потребления постоянно сокращаются.
Воду необходимо беречь. Каждый из нас должен помнить, что природные запасы воды ограничены. Необходимо контролировать загрязнение фабриками и заводами, повсеместно использовать очистные сооружения, не допускать попадания отходов с животноводческих ферм в водоёмы, а также экономно расходовать воду в быту. И тогда ещё многие века на нашей планете будет развиваться жизнь, люди будут путешествовать по морям и океанам, радоваться цветущим садам и многообразию животных и птиц.
Каждый из нас должен помнить, что природные запасы воды ограничены. Необходимо контролировать загрязнение фабриками и заводами, повсеместно использовать очистные сооружения, не допускать попадания отходов с животноводческих ферм в водоёмы, а также экономно расходовать воду в быту. И тогда ещё многие века на нашей планете будет развиваться жизнь, люди будут путешествовать по морям и океанам, радоваться цветущим садам и многообразию животных и птиц.
Значение воды в жизни человека
Интересно смогли бы люди жить на нашей планете, если бы на ней не было воды? Из чего бы состояло наше тело? Может, из воздуха или какой- то другой жидкости. Однако, все это лишь догадки. Попробуем разобраться в реальных фактах.
Вода — это жизнь. Очень мудрое высказывание. Вода — это не только один из химических элементов. Из воды состоит все, что нас окружает. Дом построен из кирпича, который лежит на цементе, замешанном на воде. Лужа на дороге, оставшаяся после дождя. Снег, которого мы ждем с нетерпением каждую зиму.
Вода обеспечивает жизнь всех живых существ. Животные и растения с её помощью утоляют жажду. Это позволяет ими хорошо расти. Люди с помощью неё готовят пищу, проводят уборку и стирку, моются, обслуживают автомобили и другую технику. Вода является необходимой средой обитания для многих живых существ. Например, рыбы, осьминоги, крабы, медузы, жуки водомерки – не смогли бы прожить без неё. Она для них — родной дом.
По воде ходят корабли и лодки. Они перевозят людей и грузы в те страны и на те острова, куда нельзя добраться на самолете, автомобиле или поезде. Благодаря воде в наших домах есть электричество. Ведь именно от неё работают гидроэлектростанции.
От воды зависит работа многих крупнейших фабрик и заводов. Где-то её используют для промывки оборудования, а где-то она — основной элемент изготовления некоторых товаров.
Вернувшись к вопросу, заданному выше, можно с уверенностью ответить, что без воды мы бы не смогли жить на этой планете.
3 класс
Значение воды в жизни человека
Интересные ответы
- Христофор Колумб — сообщение доклад
Христофор Колумб являлся известным мореплавателем, который родился и вырос на территории Испании. Именно он открыл Америку. Также известно, что Христофор был первым мореплавателем, который пересек
- Жизнь первобытных людей — доклад сообщение
Сейчас у человечества есть все условия для комфортной и спокойной жизни: пища, жилье, материальное обеспечение, энергия, разная техника и оружие. Но так в наше время, а раньше ничего этого не было
- Кислород сообщение доклад по химии 9 класс
Менделеев создал периодическую систему химических элементов, там он указал все возможные вещества, которые существуют на планете.
 В этой же таблице можно увидеть информацию о самом важном веществе в жизни всех живых существ – это кислород.
В этой же таблице можно увидеть информацию о самом важном веществе в жизни всех живых существ – это кислород. - Жизнь и творчество Марины Цветаевой
Имя Цветаевой стоит в одном ряду с такими поэтами, как Мандельштам, Ахматова. Она – поэт, своеобразный, талантливый и непосредственный.
- Жизнь и творчество Михаила Шолохова
В 1905 году 24 мая на Дону (в настоящее время Ростовская область) родился один из самых известных писателей советских времён, внесший большой вклад в литературу — Михаил Александрович Шолохов
Часто задаваемые вопросы о питьевой воде, сточных водах и коронавирусе (COVID-19)
Информация на английском языке
Ознакомьтесь с часто задаваемыми вопросами о питьевой воде, сточных водах и коронавирусе (COVID-19), а также смотрите основные ресурсы АООС США.
На этой странице:
Питьевая вода
Сточные воды и системы очистки стоков
Питьевая вода
Нужно ли кипятить воду, чтобы использовать ее для питья?
Кипячение воды не является обязательной мерой для профилактики COVID-19.
Безопасно ли мыть руки водой из-под крана?
АООС рекомендует американцам продолжать пользоваться водопроводной водой и пить ее как обычно. Согласно рекомендациям Центров по контролю и профилактике заболеваний США (CDC), частое мытье рук водой с мылом в течение не менее 20 секунд является эффективной профилактикой распространения COVID-19. См. рекомендации CDC по мытью рук (на английском языке.
Безопасно ли пить воду из-под крана?
АООС рекомендует американцам продолжать пользоваться водопроводной водой и пить ее как обычно. Всемирная организация здравоохранения (ВОЗ)ВЫХОД утверждает, что «вирус COVID-19 не был обнаружен в системах питьевого водоснабжения и, исходя из имеющихся на текущий момент данных, риск заражения им водных ресурсов является низким».1 Помимо этого, согласно данным CDC, предполагается, что COVID-19 передается от человека к человеку при тесном контакте. См. подробную информацию CDC о передаче COVID-19. Кроме того, в соответствии с требованиями АООС к питьевой воде, вода в коммунальных системах водоснабжения проходит специальную обработку для удаления или уничтожения любых патогенных микроорганизмов, включая вирусы.
Кроме того, в соответствии с требованиями АООС к питьевой воде, вода в коммунальных системах водоснабжения проходит специальную обработку для удаления или уничтожения любых патогенных микроорганизмов, включая вирусы.
1 Всемирная организация здравоохранения. 2020. Техническая сводка. Вода, канализация, гигиена и организация удаления отходов в условиях борьбы с COVID-19. Март.
Вебсайт: https://www.who.int/publications-detail/water-sanitation-hygiene-and-waste-management-for-covid-19. Код документа: WHO/2019-NcOV/IPC_WASH/2020.1
Нужно ли покупать бутилированную воду или запасаться питьевой водой?
АООС рекомендует населению продолжать пользоваться водопроводной водой и пить ее как обычно. В настоящее время нет оснований полагать, что COVID-19 присутствует в системах питьевого водоснабжения или как-то повлияет на надежность водоснабжения.
Какова роль АООС в обеспечении безопасности питьевой воды?
АООС установило нормативы, в которых прописаны требования к обработке воды, предназначенной для использования в системах коммунального водоснабжения, для предотвращения загрязнения питьевой воды воднопатогенными организмами, в том числе вирусами. Эти требования к обработке включают фильтрацию и обработку обеззараживающими средствами, такими как хлор, которые удаляют или убивают патогенные микроорганизмы до того, как они попадут в кран потребителя. Кроме того, Всемирная организация здравоохранения (ВОЗ) ВЫХОД отмечает, что «стандартные централизованные методы очистки воды с использованием фильтрации и обеззараживания должны блокировать активность вируса COVID-19».
Эти требования к обработке включают фильтрацию и обработку обеззараживающими средствами, такими как хлор, которые удаляют или убивают патогенные микроорганизмы до того, как они попадут в кран потребителя. Кроме того, Всемирная организация здравоохранения (ВОЗ) ВЫХОД отмечает, что «стандартные централизованные методы очистки воды с использованием фильтрации и обеззараживания должны блокировать активность вируса COVID-19».
АООС также продолжит координировать свои усилия с нашими федеральными партнерами, включая Центры по контролю и профилактике заболеваний (CDC), и продолжит оказывать техническую помощь и поддержку штатам по мере необходимости.
Что мне делать, если качество питьевой воды вызывает у меня сомнения?
Всемирная организация здравоохранения (ВОЗ)ВЫХОД утверждает, что «вирус COVID-19 не был обнаружен в системах питьевого водоснабжения и, исходя из имеющихся на текущий момент данных, риск заражения им водных ресурсов является низким».
Собственники жилья, водоснабжение которого осуществляет коммунальное предприятие, могут обратиться к своему поставщику за подробной информацией об используемых методах очистки воды. Методы очистки могут включать фильтрацию и обеззараживание, например хлором, с целью удаления или уничтожения патогенных микроорганизмов до того, как они попадут в кран потребителя.
Методы очистки могут включать фильтрацию и обеззараживание, например хлором, с целью удаления или уничтожения патогенных микроорганизмов до того, как они попадут в кран потребителя.
Собственники жилья с автономным водоснабжением из частных скважин, обеспокоенные возможным попаданием патогенных микроорганизмов, в том числе вирусов, в питьевую воду, могут рассмотреть возможность воспользоваться одним из существующих методов удаления бактерий, вирусов и других болезнетворных микроорганизмов, включая сертифицированные устройства для домашней очистки воды.
Сточные воды и системы очистки стоков
Могу я заразиться COVID-19 через сточные воды или канализацию?
Всемирная организация здравоохранения (ВОЗ)ВЫХОД утверждает, что «на сегодняшний день нет доказательств того, что вирус COVID-19 передается через канализационные системы с очисткой сточных вод или без таковой».
Моя система очистки стоков нейтрализует COVID-19?
Несмотря на то что системы децентрализованной очистки сточных вод (такие как септические резервуары) не обеспечивают обеззараживание, АООС предполагает, что правильно организованная система очистки стоков нейтрализует COVID-19, так же как и другие вирусы, часто встречающиеся в сточных водах. Кроме того, при правильной установке система очистки стоков располагается на безопасном расстоянии и в месте, специально оборудованном для предотвращения попадания стоков в водозаборную скважину.
Кроме того, при правильной установке система очистки стоков располагается на безопасном расстоянии и в месте, специально оборудованном для предотвращения попадания стоков в водозаборную скважину.
Станции очистки сточных вод нейтрализуют COVID-19?
Да, станции очистки сточных вод нейтрализуют вирусы и прочие патогенные микроорганизмы. Коронавирус, который вызывает COVID-19, относится к вирусам, особенно чувствительным к обеззараживанию. Ожидается, что стандартные процессы очистки и обеззараживания, практикуемые на станциях очистки сточных вод, будут эффективными.
Должны ли работники станций водоочистки принимать дополнительные меры предосторожности, чтобы защитить себя от вируса COVID-19?
Станции очистки сточных вод должны следить за тем, чтобы их сотрудники соблюдали установленные процедуры, исключающие непосредственный контакт со сточными водами. Это подразумевает использование мер инженерно-технического и административного контроля, безопасных методов работы и средств индивидуальной защиты, предусмотренных стандартами выполнения рабочих задач по обработке неочищенных сточных вод. Рекомендации по использованию каких-либо специальных средств защиты от COVID-19 для сотрудников, занятых на работах по очистке сточных вод, в том числе для работников очистных сооружений, отсутствуют.
Рекомендации по использованию каких-либо специальных средств защиты от COVID-19 для сотрудников, занятых на работах по очистке сточных вод, в том числе для работников очистных сооружений, отсутствуют.
Можно ли смывать дезинфицирующие салфетки в унитаз?
АООС настоятельно просит американцев не смывать в канализацию ничего, кроме туалетной бумаги. Дезинфицирующие салфетки и прочие предметы следует выбрасывать в мусорное ведро, а не в унитаз. Эти салфетки и другие посторонние предметы не разлагаются в канализационных системах или системах очистки стоков и могут повредить как внутреннюю канализационную систему вашего дома, так и коммунальную систему сбора сточных вод. Смытые в унитаз салфетки могут образовать засор в вашем туалете и/или привести к обратному ходу сточной воды через канализационные сливы вашего жилища или жилища соседей. Помимо этого, такие салфетки могут стать причиной серьезного повреждения трубопроводов, насосов и другого водоочистного оборудования. Обратный ход воды из канализации может представлять угрозу для здоровья населения и создавать проблемы в работе систем коммунального водоснабжения и водоотведения, отвлекая на себя ресурсы, задействованные в жизненно важной работе по сбору и очистке сточных вод нашей страны. Дезинфицирующие салфетки, влажные салфетки для малышей и бумажные полотенца НИ В КОЕМ СЛУЧАЕ НЕЛЬЗЯ смывать в унитаз.
Обратный ход воды из канализации может представлять угрозу для здоровья населения и создавать проблемы в работе систем коммунального водоснабжения и водоотведения, отвлекая на себя ресурсы, задействованные в жизненно важной работе по сбору и очистке сточных вод нашей страны. Дезинфицирующие салфетки, влажные салфетки для малышей и бумажные полотенца НИ В КОЕМ СЛУЧАЕ НЕЛЬЗЯ смывать в унитаз.
Какова роль воды в клетке человека
Буквально с самого детства каждый человек знает, что вода для нас играет очень важную роль. Гигиена, уборка, питье — каждый из этих неотъемлемых элементов жизни связан с водой. Постепенно изучая мир, ребенок узнает и о том, какова роль воды в клетке. Пожалуй, только с этого момента становится понятным, насколько велико ее значение: без воды немыслима сама жизнь. Благодаря своим свойствам она делает возможным функционирование сложных организмов.
Строение молекулы
Роль воды в жизни клетки напрямую связана с особенностями ее структуры. Всем известна формула главной жидкости нашего организма. Каждая молекула воды состоит из одного атома кислорода и двух атомов водорода. Соединяются они в единое целое благодаря полярным ковалентным связям, основанным на образовании общей электронной пары у двух атомов. Характерной особенностью молекул воды является ее электрическая асимметрия. Атом кислорода более электроотрицательный, он сильнее притягивает электроны атомов водорода. Следствие этого — смещение общих пар электронов в сторону атома кислорода.
Всем известна формула главной жидкости нашего организма. Каждая молекула воды состоит из одного атома кислорода и двух атомов водорода. Соединяются они в единое целое благодаря полярным ковалентным связям, основанным на образовании общей электронной пары у двух атомов. Характерной особенностью молекул воды является ее электрическая асимметрия. Атом кислорода более электроотрицательный, он сильнее притягивает электроны атомов водорода. Следствие этого — смещение общих пар электронов в сторону атома кислорода.
Диполь
То, какова роль воды в клетке, зависит от особенностей, присущих этому веществу. В результате смещения общей пары электронов она приобретает поляризованность. Для молекулы воды характерно наличие двух полюсов: каждый атом водорода обладает частично положительным зарядом, а кислорода — частично отрицательным. Вместе они создают нейтральную молекулу.
Таким образом, каждая структурная единица воды представляет собой диполь. Особенность строения молекулы определяет и характер связи между соседними структурами. Частично отрицательный атом кислорода притягивается атомами водорода других молекул. Между ними образуются так называемые водородные связи. Каждая молекула воды стремится связаться подобным образом с четырьмя своими соседками. Всеми названными нюансами строения определяется биологическая роль воды в клетке.
Частично отрицательный атом кислорода притягивается атомами водорода других молекул. Между ними образуются так называемые водородные связи. Каждая молекула воды стремится связаться подобным образом с четырьмя своими соседками. Всеми названными нюансами строения определяется биологическая роль воды в клетке.
Особенности
Водородные связи, характерные для молекул воды, определяют многие ее свойства. Соединения между атомами кислорода и водорода обладают особой прочностью, то есть для того, чтобы их разорвать, необходимо затратить внушительное количество энергии. В результате вода обладает высокой температурой кипения, а также плавления и парообразования. Среди подобных себе веществ вода — единственное вещество, присутствующее на Земле одновременно в трех агрегатных состояниях. То, какова роль воды в клетке, основано и на этой ее особенности.
Взаимодействие с гидрофильными веществами
Присущая частицам воды способность к образованию водородных связей позволяет основной жидкости организма растворять многие соединения. Такие вещества получили название гидрофильных, то есть «дружественных» воде. К ним относятся ионные соединения: соли, основания и кислоты. В число гидрофильных веществ входят и неионные соединения, обладающие полярностью. Их молекулы содержат заряженные группы. Это аминокислоты, сахара, простые спирты и некоторые другие соединения.
Такие вещества получили название гидрофильных, то есть «дружественных» воде. К ним относятся ионные соединения: соли, основания и кислоты. В число гидрофильных веществ входят и неионные соединения, обладающие полярностью. Их молекулы содержат заряженные группы. Это аминокислоты, сахара, простые спирты и некоторые другие соединения.
Роль воды в жизнедеятельности клетки сводится к созданию среды, необходимой для ускорения всех реакций. Раствор представляет собой такое состояние вещества, в котором все его молекулы могут двигаться гораздо свободнее, то есть значительно выше становится способность вступать в реакцию, чем в обычном виде.
Благодаря таким своим свойствам вода стала основной средой для протекания подавляющего большинства химических реакций. Более того, например, гидролиз и весь набор окислительно-восстановительных процессов осуществляются только при непосредственном участии главной жидкости клетки.
Реагент
Огромная роль воды в жизнедеятельности клетки неоспорима. Она участвует во всех важных процессах. Например, вода необходима для фотосинтеза. Один из его этапов, фотолиз воды, заключается в отделении атомов водорода и включении их в образующиеся органические соединения. При этом в атмосферу выделяется освободившийся кислород.
Она участвует во всех важных процессах. Например, вода необходима для фотосинтеза. Один из его этапов, фотолиз воды, заключается в отделении атомов водорода и включении их в образующиеся органические соединения. При этом в атмосферу выделяется освободившийся кислород.
Роль воды в клетке человека и животных связана с уже названным гидролизом, разрушением веществ с присоединением воды. Одной из важнейших реакций подобного рода в клетке является распад молекулы АТФ, происходящий с выделением энергии, которая используется для других жизненно важных процессов.
Взаимодействие с гидрофобными веществами
Некоторые белки, а также жиры и нуклеиновые кислоты не растворяются в воде совсем, или же этот процесс протекает очень тяжело. Такие вещества получили название гидрофобных, то есть «страшащихся» воды. Роль воды в клетке и организме связана и с взаимодействием ее с подобными соединениями.
Молекулы воды способны отделять гидрофобные вещества от самой жидкости. В результате образуются так называемые поверхности раздела. На них осуществляются многие химические реакции. Так, именно благодаря взаимодействию фосфолипидов, из которых состоит клеточная мембрана, с водой образуется липидный бислой.
На них осуществляются многие химические реакции. Так, именно благодаря взаимодействию фосфолипидов, из которых состоит клеточная мембрана, с водой образуется липидный бислой.
Теплоемкость
Биологическая роль воды в клетке заключается и в ее участии в терморегуляции. Теплоемкость воды достаточно высока. Это означает, что при поглощении внушительного количества тепловой энергии температура воды меняется незначительно. Такая ее характеристика способствует поддержанию постоянной температуры внутри клетки, что необходимо для нормального протекания многих процессов и поддержания постоянства внутренней среды.
Равномерное распределение тепла
Еще одна характерная особенность воды — теплопроводность. Она также способствует поддержанию постоянства внутренней среды. Вода способна переносить внушительное количество теплоты из участка организма, где она в переизбытке, к тем клеткам и тканям, которым ее не хватает.
Кроме того, терморегуляция осуществляется и за счет испарения воды. Охлаждение происходит из-за того, что при переходе из одного агрегатного состояния в другое должны разрушиться водородные связи. А для этого, как уже говорилось, требуются большие затраты энергии.
Охлаждение происходит из-за того, что при переходе из одного агрегатного состояния в другое должны разрушиться водородные связи. А для этого, как уже говорилось, требуются большие затраты энергии.
Гидростатический скелет
Роль воды в жизни клетки на этом не заканчивается. Основная жидкость организма обладает еще одним свойством: она практически не сжимается. Такая характеристика позволяет воде играть роль гидростатического скелета в клетке. Вода создает тургорное давление, тем самым определяя такие свойства клеток и тканей, как объемность и упругость. Легко понять, какова роль воды в клетке в этом смысле, если посмотреть на деревья. Привычная форма листьев создается за счет повышенного давления в клетках. Подобных примеров в органическом мире масса. Например, знакомая всем форма медуз или круглых червей поддерживается также за счет гидростатического скелета. Потеря воды клетками, соответственно, приводит к обратным процессам. Начинается изменение формы: листья увядают, плоды сморщиваются, кожа теряет упругость.
Участие в транспортировке веществ
Молекулы воды при помощи водородных связей способны соединяться не только друг с другом, но и с прочими веществами. В результате такого взаимодействия появляется поверхностное натяжение, играющее значительную роль в транспорте веществ в организме. Так, следствием когезии (сцепления молекул под действием силы притяжения, а в случае воды — при помощи водородных связей) является перемещение питательных веществ в капиллярах растений. Благодаря этому же свойству вода попадает из почвы через корневые волоски в растение.
Также сила поверхностного натяжения делает возможным капиллярный кровоток у животных и человека. Вода участвует в перемещении веществ и выведении из организма продуктов распада.
Получается, что ответ на вопрос «какая роль воды в клетке?» достаточно однозначный — она огромна. Благодаря основным свойствам молекулярного строения этой жидкости возможны все основные процессы, без которых жизнь немыслима. Вода способствует повышению реакционной способности веществ, поддерживает форму клеток и органов, участвует в их обеспечении всем необходимым, является частью многих химических реакций. Вода — источник жизни и это, определенно, не метафора. Все главные процессы обмена веществ связаны с ней, она же лежит в основе взаимодействия различных соединений. Именно из-за подобных свойств вода является тем веществом, которое ищут в первую очередь во время исследования других планет в попытке понять, пригодны ли они для жизни.
Вода — источник жизни и это, определенно, не метафора. Все главные процессы обмена веществ связаны с ней, она же лежит в основе взаимодействия различных соединений. Именно из-за подобных свойств вода является тем веществом, которое ищут в первую очередь во время исследования других планет в попытке понять, пригодны ли они для жизни.
Роль экосистем в глобальном круговороте воды
Экосистема обычно определяется как комплекс всех живых (растений, животных, микроорганизмов) и неживых (почва, климат) компонентов, взаимодействующих как функциональная единица в определенной области. Каждый компонент способствует поддержанию здорового состояния и производительности экосистемы в целом. Такие экосистемы, как леса, водно-болотные и лугопастбищные угодья, играют важную роль в глобальном круговороте воды. Признание этой роли и взаимодействия обоих компонентов имеет решающее значение для устойчивого управления водными ресурсами.
Часто постулируется, что экосистемы предоставляют целый ряд «услуг», которые можно классифицировать как: а) снабжение потребительскими товарами, такими как пища и вода; б) регулирование, включающее, в частности, очистку воды и предотвращение эрозии; в) среду обитания обеспечивающую жизненные циклы различных видов или поддерживающую генетическое разнообразие за счет качества и количества естественной растительности или субстрата для рыб, и г) культуру, которая подразумевает, например, эстетические, туристические и духовные услуги (TEEB, 2010).
Согласно проведенной в 2011 году оценке, общая экономическая ценность мировых экосистемных услуг составила 124,8 триллиона долл. США, в два раза превысив мировой валовый внутренний продукт за тот же год (Costanza and others, 2014). В настоящее время общепризнано, что различные экосистемы — как водные, так и экосистемы суши — находятся в состоянии упадка, в основном из-за последствий экономического развития. Соответствующей статистики предостаточно. С 1900 года мир потерял около 50 процентов всех водно-болотных угодий (WWDR 3, 2009). Изменения моделей землепользования привели к тому, что в период с 1997 по 2011 годы ежегодно терялись экосистемные услуги стоимостью от 4,3 до 20,2 триллиона долл. США. (Costanza and others, 2014) По оценкам, 20 процентов водоносных горизонтов мира подвергаются чрезмерной эксплуатации, что приводит, помимо прочего, к просадке грунта и интрузии соленых вод (Gleeson and others, 2012). Более чем на половину крупных речных систем мира неблагоприятное воздействие оказывают плотины (Nilsson and others, 2005). Неэффективное использование воды в растениеводстве вызвало засолонение 20 процентов общей площади орошаемых земель (FAO, 2011). Упадок экосистем приводит к ряду неблагоприятных последствий для человека, поскольку миллиарды людей проживают в регионах, испытывающих нехватку воды и (или) на территориях, характеризующихся низким качеством воды (Guppy and Anderson, 2017; Veolia and IFPRI, 2015).
Сегодня в научном дискурсе используются такие выражения как «платежи за экосистемные услуги», «экосистемный подход», «зеленая» и «серая» инфраструктура, «экологичные решения» и множество других терминов, прямо или косвенно связанных с понятием экосистем (Lautze, 2014). Этот дискурс отражает растущую обеспокоенность относительно состояния глобальных экосистем и более глубокое понимание той важной роли, которую экосистемы играют в развитии, включая развитие водных ресурсов.
В процессе модификации естественной (например, водной) экосистемы некоторые из изначально предоставляемых ею услуг и, соответственно, извлекаемых из нее выгод, теряются и заменяются выгодами от внедренных модификаций. Однако в этом процессе есть «переломный момент», когда сумма всех выгод от экосистемы достигает своего максимального значения, а дальнейшие изменения лишь уменьшают совокупность этих выгод (Acreman, 2001). На практике данный момент очень сложно определить — и, вероятно, это обстоятельство является одной из множества причин продолжающегося упадка экосистем.
Определение и количественная оценка услуг, предоставляемых экосистемами, также могут иметь большое значение в политическом контексте. Так, конфликт из-за водных ресурсов реки может рассматриваться как конфликт по поводу того, какая из сторон получит доступ к предоставляемым рекой услугам снабжения, а какая — его потеряет. Негативные последствия воздействия различных крупных и малых проектов развития водных ресурсов на доступность экосистемных услуг и связанные с ними социальные конфликты встречаются довольно часто — например, в контексте ирригации и охраны природы или производства гидроэлектроэнергии и поддержания среды обитания.
Экосистемные услуги, в том числе предоставляемые водными экосистемами, имеют решающее значение для выживания и существования бедных слоев населения сельских районов; их утрата может повлечь за собой увеличение масштабов нищеты. В качестве решения данной проблемы часто предлагается концепция платежей за экологические услуги. Город, расположенный ниже по течению реки, мог бы платить сельским общинам в верхнем течении за сохранение излишков воды за счет пополнения водоносного пласта с помощью регулируемых систем, что позволит снизить риск наводнений или сократить их масштабы (Pavelic and others, 2012), или за внедрение различных мер по сохранению почв, предназначенных для сокращения объемов наносов, переносимых в резервуары ниже по течению. Однако такие схемы довольно сложно реализовать на практике. Что еще более важно, сама концепция «экосистемных услуг» и связанная с ней идея о том, что на природу можно наклеить ценник, имеет своих противников (Kosoy and Corbera, 2010). Кроме того, вряд ли возможно компенсировать ущерб, наносимый экосистеме в процессе развития водных ресурсов — например, в случаях, когда места массовых посещений на водных объектах оказываются постоянно подтопленными или когда речное рыболовство становится невозможным из-за загрязнения воды или фрагментации рек.
Деградация экосистем также является важной причиной увеличения связанных с водой рисков и экстремальных ситуаций, таких как наводнения и засухи. Экосистемы обеспечивают природную («зеленую») инфраструктуру, выполняющую определенные функции уменьшения опасности бедствий и, следовательно, частично заменяющую или дополняющую «серую» (техногенную) инфраструктуру, предназначенную для тех же целей. Сочетание «зеленой» и «серой» инфраструктуры, например в контексте комплексного управления рисками, связанными с наводнениями и засухами, в отдельно взятом речном бассейне, может способствовать экономии средств по сравнению с использованием исключительно «серой» инфраструктуры (WWDR, 2018). Кроме того, «зеленая» инфраструктура выполняет функции и предоставляет преимущества, способные напрямую повысить производительность «серой» инфраструктуры и снизить риски для последней. Однако маловероятно, что экосистемы сами по себе смогут обеспечить такой же уровень снижения риска, как и «серая» инфраструктура, или полностью заменить ее в будущем. Поэтому ставка на одни лишь экосистемы представляется чрезмерно упрощенным подходом к проблематике смягчения последствий стихийных бедствий, связанных с водой, и может потенциально привести к разработке неэффективных стратегий (McCartney and Finlayson, 2017).
Существует целый ряд препятствий на пути к широкомасштабному внедрению экосистемно-ориентированных подходов в управлении водными ресурсами. Среди них — преобладание решений, связанных с «серой» инфраструктурой, в инструментарии многих государств, недоступность количественных данных об успешности применения на практике экосистемно-ориентированных подходов и отсутствие потенциала для их внедрения. Многие из вышеупомянутых концепций сложны, недостаточно развиты для практического применения или просто неизвестны специалистам-практикам и директивным органам. Таким образом, хотя научный дискурс по проблемам экосистем является довольно оживленным, на сегодняшний день он не отвечает текущим прикладным и политическим запросам.
Вместе с тем наблюдается сдвиг парадигмы, выражающийся в постепенном признании экосистем в качестве неотъемлемой части решений в области развития. Данный сдвиг находит отражение в международных многосторонних соглашениях по устойчивому развитию, таких как Повестка дня в области устойчивого развития на период до 2030 года (утверждена в 2015 году), Сендайская рамочная программа по снижению риска бедствий (принята 2015 году) и Парижское соглашение по климату (заключено в 2015 году). Явный акцент на экосистемы прослеживается по крайней мере в трех из 17 целей в области устойчивого развития (ЦУР), изложенных в Повестке дня в области устойчивого развития на период до 2030 года и подразумевается во многих других. ЦУР 6 представляет собой революционный шаг в деле всемирного развития водных ресурсов. Впервые в истории в ней рассматриваются не только проблемы всеобщего доступа к воде и санитарии, в том числе доставшиеся нам в наследство от предыдущих десятилетий, но и вопросы, связанные с эффективным управлением ресурсами, их рациональным использованием и с пресноводными экосистемами.
Задача 6.3 в рамках ЦУР 6 направлена на значительное улучшение качества воды во всем мире. Задача 6.4 ориентирована на эффективное использование воды различными секторами экономики. Одним из измеряемых показателей выполнения данной задачи является расчет дефицита воды в каждой стране, что позволяет оценить нагрузку на национальные возобновляемые ресурсы пресной воды. Дефицит воды определяется как общий объем пресной воды, отобранной за год всеми секторами экономики, поделенный на разницу между всеми возобновляемыми ресурсами пресной воды и экологическими потребностями в воде. Последний термин по сути определяется как вода, предназначенная для единственной цели — поддержания пресноводной экосистемы в здоровом состоянии (Smakhtin, Revenga and Döll, 2004). Такое явное признание потребностей экосистем в воде в контексте глобальной повестки дня в области развития отражает понимание того, что поддержание баланса между удовлетворением требований водной среды и использованием водных ресурсов для других нужд уже приобрело критическое значение во многих речных бассейнах мира в связи с продолжением роста населения и сопутствующего спроса на водные ресурсы.
Показатель выполнения задачи 6.6 был специально разработан для защиты связанных с водой экосистем, с тем чтобы они продолжали предоставлять экосистемные услуги ради благополучия человечества. Защитные меры распространяются на водно-болотные угодья, реки, водоносные горизонты и озера. Прослеживается явная связь между показателями выполнения задачи 6.6 и цели 6.4 (оценка нехватки воды).
Хотя это не утверждается напрямую, логично предположить, что достижение цели 6.5 — создание системы комплексного управления водными ресурсами (КУВР) — невозможно без обслуживания экосистем. В целях правильного применения принципов КУВР каждой стране или администрации бассейна необходимо будет, к примеру, знать потребные объемы воды для каждой экосистемы, с тем чтобы удерживать отбор воды из рек и водоносных горизонтов в приемлемых пределах.
Все целевые показатели ЦУР, связанные с экосистемами, являются добровольными и не выражаются в количественной форме. Многие из предлагаемых показателей представляют собой чрезвычайно упрощенные модели более масштабных или абстрактных задач. Соблюдение временных рамок Повестки дня в области устойчивого развития на период до 2030 года само по себе является нетривиальной задачей. Будущее покажет, удастся ли нам выполнить хотя бы часть из поставленных задач, или же придется и впредь цитировать мрачную статистику деградации экосистем. Впрочем, надежда на положительный исход, разумеется, остается.
Библиография
Acreman, Mike (2001). Ethical aspects of water and ecosystems. Water Policy, vol. 3, No. 3, pp. 257-265.
Costanza, Robert, and others (2014). Changes in the global value of ecosystem services. Global Environmental Change, vol. 26 (May), 152-158. С публикацией можно ознакомиться на веб-сайте: http://www.sciencedirect.com/science/article/pii/S0959378014000685.
Food and Agriculture Organization of the United Nations (FAO) (2011). The State of the World’s Land and Water Resources for Food and Agriculture: Managing systems at risk. London, Rome, Earthscan and FAO. С публикацией можно ознакомиться на веб-сайте: http://www.fao.org/nr/solaw/solaw-home/en/.
Gleeson, Tom, and others (2012). Water balance of global aquifers revealed by groundwater footprint. Nature, vol. 488 (9 August), pp. 197—200.
Guppy, Lisa, and Kelsey Anderson (2017). Water Crisis Report. United Nations University Institute for Water, Environment and Health, Hamilton, Canada. С публикацией можно ознакомиться на веб-сайте: http://inweh.unu.edu/wp-content/uploads/2017/11/Global-Water-Crisis-The-….
International Food Policy Research Institute (IFPRI) and VEOLIA (2015). The murky future of global water quality: New global study projects rapid deterioration in water quality. A White Paper. Washington, D.C. and Chicago, IL. С публикацией можно ознакомиться на веб-сайте: http://www.ifpri.org/publication/murky-future-global-water-quality-new-g….
Kosoy, Nicolás, and Esteve Corbera (2010). Payments for ecosystem services as commodity fetishism. Ecological Economics, vol. 69, No. 6 (April), pp. 1228-1236.
Lautze, Jonathan, ed. (2014). Key Concepts in Water Resource Management: A Review and Critical Evaluation. New York, Routledge and Earthscan.
McCartney, Matthew, and Max Finlayson (2017). Exaggerating the value of wetlands for natural disaster mitigation is a risky business. The Conversation, 2 February. С публикацией можно ознакомиться на веб-сайте: http://theconversation.com/exaggerating-the-value-of-wetlands-for-natura….
Nilsson, Christer, and others (2005). Fragmentation and flow regulation of the world’s large river systems. Science, vol. 308, No. 5720 (15 April), pp. 405-408.
Pavelic, Paul, and others, (2012). Balancing-out floods and droughts: opportunities to utilize floodwater harvesting and groundwater storage for agricultural development in Thailand. Journal of Hydrology, vols. 470—471 (12 November), pp. 55—64.
Smakhtin, Vladimir, Carmen Revenga, and Petra Döll (2004). A pilot global assessment of environmental water requirements and scarcity. Water International, vol. 29, No.3, pp. 307-317.
The Economics of Ecosystems and Biodiversity TEEB (2010). The Economics of Ecosystems and Biodiversity: Ecological and Economic Foundations. Pushpam Kumar, ed. Earthscan, London and Washington.
United Nations World Water Assessment Programme (2009). The United Nations World Water Development Report 3 (WWDR3): Water in a Changing World. The United Nations Educational, Scientific and Cultural Organization (UNESCO), Earthscan, Paris, London.
United Nations World Water Assessment Programme (forthcoming), The United Nations World Water Development Report 2018 (WWDR): Nature-based Solutions for Water. The United Nations Educational, Scientific and Cultural Organization (UNESCO), Paris.
Какова роль воды в жизни человека. Сферы использования
Муниципальное автономное общеобразовательное учреждение«Средняя школа №66»
Презентация
По технологии
На тему : » Какова роль воды в жизни человека.»
Выполнила ученица 11 класса
Зубарева К.Э
Проверила
Иванова С.Н
г.Хабаровск. 2021г.
План презентациии
1. Введение
2. Сферы использования воды
3. Почему вода так важна для человеческого организма
4.
5. Потеря воды
6.
7. Сколько нужно выпивать воды в день
8. В какое время пить воду
9. Можно ли заменять воду различными напитками
Вода — это самое
распространенное
неорганическое соединение
на земле. Вода существует в
природе в трех состояниях:
твердом, жидком и
газообразном виде. Но уже
сейчас выделяют более 20
состояний воды, из которых
только 14 — это вода в
замерзшем состоянии.
Сферы использования воды
Человек зависит от воды ежедневно и повсеместно. По сути, сферы ее
использования можно разделить на личную, бытовую и
производственную.
Сферах промышленности:
В металлургии, чистая вода используется в огромных количествах,
особенно, в производстве чугуна и стали.
В сфере производства соков, напитков, алкоголя, тоже необходима
специальная мягкая вода.
Для потребностей микробиологии, химии, фармацевтики и медицины
получают продукт сверхочистки.
Личная сфера
О роли воды в жизни
человека можно
судить на простом
примере – сам
человек в
большинстве своем
состоит из воды.
Почему вода так важна для человеческого
организма
Снижению массы тела
Повышению вязкости крови,
температуры тела, пульса и
Дефицит
воды
приводит к :
дыхания
Жажде
Тошноте, слабости,
головокружению, одышке
Снижению работоспособности.
Снижению физической
активности
Потеря воды
приводит :
2% от массы тела – ощущение
жажды
6% – полуобморок
10% – нарушение речи, зрения,
слуха, бред, галлюцинации и
потеря сознания
15-25% – необратимые
изменения в нервной , гибель
Избыток
воды
приводит к :
Ухудшению пищеварения
(разбавляется концентрация
желудочного сока)
Повышению нагрузки на сердце и
почки
Выведению минеральных
веществ
Быстрой утомляемости мышц
Судорогам
Сколько нужно выпивать воды в день ?
Правильно рассчитать норму
потребляемой жидкости можно
только индивидуально
в зависимости
от физиологических
особенностей человека, его
образа жизни и с учетом
времени года.
Также принимать во внимание
состояние здоровья человека
и медикаменты, которые
он принимает. Некоторые
из них, например мочегонные
препараты, вызывают
дополнительную потерю
жидкости.
В какое время пить воду?
Распределите количество питьевой жидкости равномерно
в течение всего дня для того, во-первых, чтобы тело
не обезвоживалось, во-вторых, чтобы не перегрузить организм.
Следует пить после пробуждения, до обеда или ужина, перед
тренировкой и после нее, а также незадолго до сна. Кроме того,
нужно выпить воды, когда хочется и когда вам кажется,
что вы голодны: возможно, на самом деле это жажда.
Можно ли заменять воду различными напитками
Действительно, овощные или фруктовые соки способны
пополнить запасы организма нужной влагой.
сладкие газированные напитки лишь способствуют
обезвоживанию организма
алкоголь, чай или кофе имеют мочегонное действие. Поэтому
после вышеперечисленных напитков вам всё равно потребуется
восполнить свой организм водой.
Спасибо за
внимание!
Роль воды на Земле — стенограмма видео и урока
Биологические процессы
Землю называли голубой планетой. Когда вы смотрите на Землю издалека, вы видите вот что: маленькое синее пятнышко. 71% поверхности Земли покрыто водой. И большинство млекопитающих, как и люди, на 55-75% состоят из воды. Растения также содержат большое количество воды.
Некоторые люди могут возразить, что жизнь на Земле зависит от воды именно потому, что ее здесь очень много.Возможно, жизни на других планетах это не понадобится. Но нам трудно даже представить, как бы без него могли существовать организмы. Это потому, что вода жизненно важна для биологических процессов, от химических реакций до переноса питательных веществ в крови и перемещения питательных веществ между клетками. Без воды нашему телу пришлось бы работать совершенно иначе. Растения нуждаются в воде аналогичным образом, и в случае небольших растений вода также создает напряжение в их стеблях, позволяя им стоять прямо и тянуться к солнечному свету.Это называется тургорным давлением .
Круговорот воды
Вода также играет важную роль в функционировании нашего мира в целом. Круговорот воды — это не буквально то, что заставляет мир вращаться, но все же это имеет большое значение. Вода испаряется из океанов, рек и озер и переносится через растения и деревья к их листьям. Газообразная вода, называемая водяным паром , затем поднимается с листьев растений, пока не станет достаточно холодной, чтобы образовать облака. Эти облака в конечном итоге выпускают воду в виде дождя или снега, и цикл продолжается.
Круговорот воды заставляет воду постоянно перемещаться с места на место, позволяя растениям по всему миру расти, а животным повсюду получать необходимую воду. Он создает погодные условия на Земле, которые имеют огромное влияние на жизнь здесь: от молний, вызывающих естественное горение и отрастание лесов, до снегопадов в полярных регионах и наводнений вокруг рек. Соленая вода менее полезна для млекопитающих, чем пресная, поэтому тот факт, что дождевая вода не содержит соли, очень важен.
Современное использование
Люди довели потребление воды до крайности. Мы используем воду для мытья, приготовления пищи, выращивания продуктов на фермерских полях, для производства продуктов в промышленности, для выработки электроэнергии (как при сжигании ископаемого топлива, особенно на гидроэлектростанциях), а также для отдыха, например, плавания. У нас так много способов использования воды, что средний американец расходует 150–250 галлонов каждый день! По этой причине даже в западном мире есть места, где не хватает воды.На планете, покрытой водой, хотя и соленой, это должно быть гораздо более шокирующим фактом, чем кажется.
Краткое содержание урока
Землю называют голубой планетой, потому что она покрыта водой. Так что, может быть, неудивительно, что вода жизненно важна на Земле. Вода содержит молекулы с двумя атомами водорода и одним кислородом, что может показаться неприятным, но без этого мы бы умерли. Это жизненно важно для всех человеческих начинаний.
В биологии человека и животных вода используется для транспортировки, выделения, химических реакций и многих других процессов.У небольших растений вода создает напряжение в их стеблях, позволяя им стоять прямо и достигать солнечного света. А в современной жизни мы используем установки для приготовления пищи, очистки, мытья, выращивания сельскохозяйственных культур, производства продуктов, выработки электроэнергии и других задач, которые невозможно перечислить. Хотя у нас много соленой воды, нехватка пресной воды является обычным явлением, потому что люди могут использовать сотни галлонов воды каждый день. К счастью, круговорот воды продолжает испарять морскую воду и проливать на нас пресную воду, по крайней мере, во влажных частях мира.
Роль воды в некоторых биологических процессах
Состояние внутриклеточной воды долгое время было предметом споров по двум причинам. Во-первых, эксперименты часто давали противоречивые результаты. Во-вторых, до сих пор не было веских оснований предполагать, что внутриклеточная вода должна значительно отличаться от основной воды. Коллективное поведение молекул воды предлагается здесь как термодинамически неизбежный механизм образования заметных зон аномальной воды.На сильно заряженной поверхности молекулы воды движутся вместе, образуя зону воды толщиной около 6 нм, которая слабо связана водородными связями, жидкая, реакционная и избирательно накапливает небольшие катионы, многовалентные анионы и гидрофобные растворенные вещества. На гидрофобной поверхности молекулы расходятся, и локальная вода становится прочно связанной, инертной и вязкой и накапливает большие катионы, одновалентные анионы и совместимые растворенные вещества. Белки и многие другие биополимеры имеют неоднородные поверхности, которые, таким образом, вызывают с помощью двух описанных механизмов неоднородные межфазные водные структуры, которые простираются на значительные расстояния от поверхности.Теперь становится очевидной причина многих противоречивых экспериментальных результатов. Средние значения свойств воды, измеренные в гелях, клетках или растворах белков, часто не сильно отличаются от тех же свойств нормальной воды, что не указывает на то, что они являются средними крайними значениями. Чтобы обнаружить действие этого явления, необходимо выборочно исследовать одну аномальную популяцию. Приведены примеры таких экспериментов. Показано, что такое коллективное поведение молекул воды составляет значительную биологическую силу, которая может быть эквивалентна давлению в 1000 атм (1.013 x 10 (5) кПа). Предполагается, что клетки избирательно накапливают ионы K + и совместимые растворенные вещества, чтобы избежать экстремальной структуры воды в своих водных отсеках, но что катионные насосы и другие ферменты используют различные свойства растворителя и реакционную способность воды для выполнения работы по транспорту или синтезу.
Двойственная роль воды в истоках жизни — Nascimento Vieira — 2020 — FEBS Letters
Вода необходима для всех известных форм жизни [[1]].В качестве растворителя для жизни он обеспечивает протоны (H + ) и гидроксильные группы (OH — ) для бесчисленных реакций, но создает центральную проблему, когда дело доходит до происхождения жизни: гидролиз. Молекулы воды диссоциируют химические связи и тем самым разбивают более крупные молекулы или полимеры на их мономерные компоненты. В свободном растворе реакции конденсации, приводящие к образованию воды, термодинамически неблагоприятны. И протоны, и гидроксид-ионы могут катализировать реакции гидролиза, что делает их сильно зависимыми от pH процессов [[2]].Молекулы воды могут легко расщеплять сложноэфирные и амидные связи и, таким образом, гидролизовать нуклеиновые кислоты и белки или влиять на период полужизни реагентов. При гидролизе OH — обычно заменяет другой фрагмент в молекуле (например, фосфатную, амино- или тиольную группу) путем нуклеофильного замещения. В метаболизме Escherichia coli , например, наиболее распространенным реагентом является H + , за которым следует вода, которая участвует в качестве субстрата или продукта в более чем 500 реакциях [[3]].
Клетки противодействуют гидролизу с помощью ряда механизмов, включая энергетический метаболизм [[4]].Основные полимеры клеток, белки и нуклеиновые кислоты подвержены гидролизу. На их синтез уходит около 80% энергетического бюджета анаэробной клетки [[5]]. Энергетический метаболизм постоянно поддерживает АТФ-зависимый синтез полимера, тем самым гарантируя, что скорость синтеза полимера выше, чем скорость гидролиза. Однако у зародыша жизни примерно 4 миллиарда лет назад, прежде чем полимеризация нуклеотидов, аминокислот или сахаров могла быть связана со сложным энергетическим метаболизмом, должны были существовать другие средства, позволяющие избежать естественной тенденции к гидролизу [[6, 7]] ].Например, в системах серпентинизации, таких как щелочные гидротермальные источники (см. Вставку 1 «Серпентинизация»), химически реактивная среда может обеспечивать постоянное поступление мономеров из простых неорганических соединений (CO 2 , карбонаты, водород) посредством взаимодействия породы и воды. [[8-11]], хотя точный источник этих мономеров является предметом споров [[12]].
Вставка 1. Серпентинизация
Серпентинизация — это геохимический процесс, который происходит, когда ультраосновные породы в верхней мантии взаимодействуют с морской водой, поступающей из трещин в коре [13].Основным газофазным продуктом этого процесса является молекулярный водород (H 2 ), образующийся в результате восстановления протонов воды минералами железа.
Верхняя часть мантии Земли состоит в основном из перидотита, который состоит в основном из пироксена (цепочечных силикатообразующих минералов) и оливина [[14]]. Оливин представляет собой силикат железа и магния, твердый раствор между форстеритом силиката магния (Mg 2 SiO 4 ) и фаялитом силиката железа (Fe 2 SiO 4 ).Ниже 400 ° C форстерит растворяется в воде [[15-18]]:- Mg 2 SiO 4 + 4 H + → 2 Mg 2+ + SiO 2 (водн.) + 2 H 2 O
- 3 Mg 2+ + 2 SiO 2 (водн.) + 5 H 2 O → Mg 3 Si 2 O 5 (OH) 4 + 6 H +
- Mg 2+ + 2 H 2 O → Mg (OH) 2 + 2 H +
- 3 Fe 2 SiO 4 + 2 H 2 O → 2 Fe 3 O 4 + 3 SiO 2 (водн.) + 2 H 2
Эта реакция также потребляет воду, но магнетит является второстепенным компонентом серпентинизации, хотя он является основным продуктом окисления Fe 2+ .Большая часть воды расходуется в результате реакций на змеевик и брусит. Равновесный pH гидротермального флюида почти нейтрален при температурах около 300 ° C, но увеличивается примерно до pH 11 при 50 ° C, потому что растворимость брусита увеличивается при более низких температурах, высвобождая растворенные ионы Mg 2+ и OH — [ [18]].
Содержание минералов в серпентинизированных системах сильно зависит от среды, в которой расположена каждая система.Если достаточное количество H 2 накапливается в окружающей среде, содержащей соединения, содержащие Ni 2+ , могут образовываться самородные сплавы NiFe, такие как аваруит (Ni 3 Fe) [[19, 20]].- (FeO) + 3 (NiO) + 4 H 2 → Ni 3 Fe + 4 H 2 O
Точно так же сульфиды железа или никеля могут образовываться в системах с более высокой долей H 2 S вместо H 2 [[19, 21]].Количество H 2 , образующееся в результате серпентинизации, зависит от температуры и соотношения вода: порода в реагирующем пласте. Например, при 100 ° C серпентинизация, начинающаяся с гарцбургита, ультраосновной оливинсодержащей породы, дает около 0,9 моль H 2 на кг породы при соотношении вода: порода 0,2 (превышение породы над водой), но увеличивается примерно до 130 моль H 2 по мере увеличения отношения вода: порода до 10 [[18]].
Серпентинизация — очень распространенный процесс и, вероятно, на ранней Земле было более распространенным явлением, чем сейчас [[16]].
Недавние открытия показывают поразительные параллели между первыми этапами биохимической фиксации CO 2 водородом (H 2 ) и фиксацией углерода в геохимических условиях, аналогичных условиям в серпентинизирующихся системах [[22]]. Формиат, ацетат и пируват органических кислот легко образуются из H 2 и CO 2 в присутствии H 2 O с помощью металлов и минеральных катализаторов, также присутствующих в системах серпентинизации [[22, 23]] .Реакции с участием ионов металлов между пируватом и глиоксилатом приводят к более сложным органическим кислотам, наблюдаемым в метаболизме, например фумарату, малату или α-кетоглутарату [[24]]. В присутствии восстановленных соединений азота, таких как аммиак [[25]] или гидроксиламин [[24]], пируват, оксалоацетат и ацетат могут реагировать с простыми аминокислотами аланином, аспарагиновой кислотой и глицином. Такие восстановленные соединения азота могут быть получены в гидротермальных условиях путем гидрирования диазота (N 2 ) на минеральных катализаторах [[26-28]].Гетероциклические мономеры в качестве азотистых оснований могут быть получены либо из формамида (который сам является продуктом реакции между муравьиной кислотой и аммиаком) [[29]], либо через реакцию конденсации аминокислот, путь ближе к биологическим путям [[30]] . Однако оба подхода требуют низкой активности воды. Хотя прямой синтез аминокислот или азотистых оснований, начиная с N 2 и CO 2 , связанный с серпентинизацией, еще не был продемонстрирован [[11, 12]], в условиях высокого давления и высоких температур, обеспечиваемых системами серпентинизации, активирующие N 2 , CO 2 и H 2 одновременно на минеральных поверхностях могут, в принципе, привести к образованию сложных биомолекул и мономеров, включая аминокислоты, кофакторы и нуклеиновые основания, которые могут способствовать образованию протометаболических автокаталитических сетей [[31]. ].Таким образом, синтез простых биологических органических веществ из H 2 и CO 2 с использованием гидротермальных катализаторов является легким [[22]], однако синтез более сложных биомолекул из H 2 , CO 2 и N 2 еще не сообщается.
Но даже если биомономеры могут быть образованы в системах серпентинизации, пока продукты полимеризации гидролизуются быстрее, чем они синтезируются, не возникнет молекулярной сложности, потому что образование сложных мономеров можно предотвратить гидролизом.Это требует более пристального внимания к активности воды в геохимических, биологических и первичных протометаболических условиях. В этой статье мы обращаемся к проблеме гидролиза в контексте происхождения на стыке геохимии и биохимии, рассматривая его механизмы и их контроль в условиях окружающей среды и клеток.
Гидролиз и активность воды в биологии
Содержание воды в цитозоле зависит от размера клетки и метаболизма, но может варьироваться от нескольких десятков до многих тысяч фемтолитров (10 −15 ) [[32]].Он состоит из связанной и объемной («свободной») воды, причем активность воды представляет собой мольную долю воды в объеме (см. Вставку 2 «Что такое активность воды?»). Цитозоль насыщен широким спектром молекул, что делает его переполненной средой с концентрациями до сотен г · л -1 аминокислот, пептидов, белков, нуклеиновых кислот, азотистых оснований, моносахаридов, сахаров и т. Д. [[33, 34]]. Например, концентрация аминокислот в цитозоле, как свободных, так и полимеризованных в виде белка, составляет около 550 г · л -1 [[5]].Количество и природа растворенных молекул в цитозоле обуславливают уникальные растворяющие свойства внутриклеточной воды, которые в конечном итоге также способствуют полимеризации биомолекул [[35, 36]]. Можно различать воду для гидратации (см. Вставку 3 «Вода для гидратации»), которая сильно абсорбируется белками и другими клеточными соединениями, и воду, которая имеет физические и химические свойства основной воды [[37]]. В кристаллизованных белках, например, около 40% веса кристаллов приходится на воду, смесь гидратной воды и основной воды [[37]].Две формы воды имеют очень разные свойства. Гидратационная вода имеет более высокую теплоемкость, менее подвижна и более упорядочена, чем объемная вода, поэтому они различаются по своей способности растворять различные соединения [[37]]. Для активности ферментов необходима гидратная вода, поскольку она стабилизирует третичные и четвертичные конформации за счет водородных связей, заряд-дипольных взаимодействий и гидрофобных (энтропийных) эффектов. Вкратце: гидратная вода сохраняет ферменты нетронутыми для катализа [[38, 39]].
Вставка 2. Что такое активность воды?
Активность воды — это мера «эффективной концентрации» воды в системе, также называемая «объемная вода». Когда объемные молекулы воды связываются с ионами, с поверхностями или иным образом захватываются, общая активность воды в системе снижается.
Простым способом определения активности воды является измерение давления водяного пара в водном растворе. Фундаментальные термодинамические соотношения показывают: где p w — давление водяного пара водного раствора.— давление пара чистой воды при том же внешнем давлении и температуре, что и у раствора
X w — мольная доля воды в растворе, а
f w — безразмерный коэффициент активности.
На активность воды особенно влияет сильное электростатическое взаимодействие частичных зарядов воды с ионами растворенных солей.Сильное взаимодействие приводит к сравнительно низкой активности воды. В случае достаточно разбавленного «идеального» раствора f w ≈ 1 и:В соответствии с этим соотношением относительное снижение давления пара растворителя равно мольной доле x 2 растворенного соединения, например соли в водном солевом растворе (эмпирический закон Рауля от 1890 г.) [[40] ].
Вставка 3. Вода гидратация
Термин гидратная вода используется в химии для обозначения воды в кристаллической структуре металлического комплекса или соли, которая не связана напрямую с катионом. Часто кристаллические свойства теряются, когда эта вода удаляется нагреванием. В биологическом контексте важность гидратации воды очевидна. Белки кристаллизуются с содержанием воды в решетке до 50%, что намного больше, чем неорганические соли [[37, 41]].Часто их ферментативная функция снижается, а их структура изменяется, если эта вода удаляется. Большая часть воды в биологических клетках — это вода гидратации [[37]]. В этой статье мы используем понятие гидратационной воды в более широком смысле, чем просто кристаллизационная вода, чтобы принять во внимание эффекты в биологических системах.
Под гидратной водой здесь понимается вся вода, которая не связана с колеблющейся сеткой объемной воды (чистая жидкая вода), но с другими частицами в водной фазе.Часто гидратная вода более прочная и связанная более упорядоченно, чем объемная вода [[42]], и поэтому демонстрирует существенно другую свободную энергию Гиббса [[43]]. Гидратационная вода может быть связана в первой или второй сольватной оболочке катиона или аниона растворенной соли, связана с заряженной боковой цепью (ами) аминокислот в белке, упорядочена с гидрофобными молекулами или химическими группами, связана с цепочка молекул воды в мембранном протеиновом канале, проводящая протоны или связанная с твердой поверхностью [[41]].Все эти взаимодействия можно классифицировать по их свободной энергии связи Гиббса, которая может быть довольно большой. Например, высокий вакуум в реакторе может быть получен только путем нагревания его стенок значительно выше 100 ° C в течение многих часов во время откачки (процесс, известный как отжиг), чтобы высвободить плотно прикрепленные монослои воды [[44]] .
Соли также могут оказывать огромное влияние на характеристики воды как растворителя [[45, 46]]. Натрий (Na + ), калий (K + ), магний (Mg 2+ ), фосфат (PO 4 3–) и хлорид (Cl — ) способствуют сворачиванию белков и ферментов. , структура и специфичность за счет создания in situ микросреды, в которой определенных ионов больше, чем в основной массе [[36, 47]].Эти микросреды регулируют активность воды посредством электростатического взаимодействия. Гидрофильные поверхности связаны с более высокой концентрацией воды, тогда как гидрофобные поверхности вызывают миграцию воды в другие места. Это сложное взаимодействие помогает повысить термостабильность макромолекул в их водном окружении [[48-50]]. Результирующая внутриклеточная динамика воды — также называемая биологической активностью воды — обеспечивает полимеризацию и сохранение энергии, поскольку ферменты контролируют опосредованные водой взаимодействия.Среди этих взаимодействий — гидрирование [[51, 52]], конденсация [[53, 54]] и гидролиз. Последний является центральным для энергетического метаболизма [[55, 56]], потому что эндергонические реакции могут быть связаны с высвобождающей энергию гидролитической реакцией, в частности гидролизом АТФ, тем самым облегчая эндергонические реакции в метаболизме. Например, полимеризация аминокислот является эндергонической и не происходит спонтанно в чистых водных (абиотических) системах [[57]]. Были введены индуцированное солью или управляемое влажно-сухим циклом образование пептидов [[58, 59]], гидротермальный синтез [[60]] или полимеризация в адсорбированной фазе, например, на минеральных поверхностях [[61, 62]]. как возможные механизмы, способствующие образованию пептидов в абиотическом контексте [[57]].
Однако в клетках полимеризация аминокислот требует переноса АМФ от АТФ, чтобы активировать аминокислоту для полимеризации через тРНК [[63-65]]. Перенос высвобождает пирофосфат (PP i ), который впоследствии гидролизуется, чтобы сделать активацию необратимой в физиологических условиях (ΔG 0 ‘= — 19,3 кДж · моль -1 ) [[65]]. Похожий механизм используется при конденсации нуклеотидов, когда пирофосфат высвобождается при образовании фосфодиэфирной связи между двумя нуклеотидами [[66]].Пирофосфат немедленно гидролизуется на две свободные фосфатные группы под действием пирофосфатаз [[65]], ферментов, которые используют ионы Mg 2+ для ускорения контролируемого гидролиза (показано на рис. 1) [[67]]. Ионы Mg 2+ также способствуют сборке нуклеиновых кислот, располагая нуклеотиды в правильной конформации [[68]]; другой Mg 2+ затем активирует гидроксильную группу на 3′-конце нуклеотида праймера, способствуя образованию последующей фосфодиэфирной связи [[69]].
Каталитический механизм гидролаз, содержащих Mg 2+ или Mn 2+ (гидролазы пирофосфатазного типа). Металлический комплекс, образованный карбоксильными группами кислых аминокислот и молекулами воды, может активировать как субстрат (участок показан красным), так и воду (участок, образующий ОН —, показан синим). По материалам [[67]].Полезность АТФ в биологии заключается в его способности гидролизоваться по фосфоангидридной связи, таким образом генерируя менее энергоемкий АДФ и неорганический PO 4 3– (P i ).Энергия, выделяемая при реакции АТФ на АДФ и P i , составляет 30,5 кДж · моль -1 и 45,6 кДж · моль -1 для реакции АТФ с АМФ и PP i [[65]] . Непрерывный цикл реакций гидролиза и конденсации молекул АТФ, АДФ, АМФ, PP i и P i позволяет использовать энергию макромолекул в метаболизме через реакции энергетического сочетания [[70, 71]]. Помимо АТФ, в биологии существует множество других молекул, способных передавать химическую энергию посредством реакций энергетического сочетания, таких как НАД, ацилтиоэфиры, аминоациловые эфиры и рибозильные фрагменты [[72-75]].
Ряд реакций в клетке включает контролируемый гидролиз во время разложения липидов, нуклеиновых кислот и белков. Ферментами, ответственными за эти реакции, являются гидролазы, которые составляют около одной трети всех известных ферментов, самый большой класс ферментов [[67]]. Подгруппы гидролаз используют кофакторы двухвалентных металлов, такие как Mg 2+ , марганец (Mn 2+ ), кобальт (Co 2+ ) и цинк (Zn 2+ ) [[67, 76-78]], все это также может иметь значение в контексте пребиотиков [[79–82]].Четыре гидролазы считаются особенно древними, все они используют металлические кофакторы, три из них функционируют без кофакторов, производных от нуклеотидов, таких как АТФ или НАД [[83]], что указывает на консервативный и, возможно, первичный механизм. К наиболее древним гидролазам относятся тиоэфиргидролазы (например, ацетил-CoA гидролаза), которые действуют с Mg 2+ или Mn 2+ в своих активных центрах [[78, 83]].
Молекулярные механизмы катализа в гидролазах достаточно хорошо изучены [[67]], хотя еще не известны подробно для каждой подгруппы семейства ферментов.На рис. 1 изображен механизм активного центра гидролазы, содержащего Mg 2+ или Mn 2+ , показывая, что кислотные аминокислоты имеют решающее значение для позиционирования ионов, так что они производят OH — из воды для осуществления целевого гидролиза. Как описано ранее, гидролиз пирофосфата делает возможной полимеризацию аминокислот и нуклеотидов. Примечательно, что Mg 2+ также может катализировать гидролиз сам по себе, без защитной среды ферментативного активного центра [[84]].В абиотических системах, где нет ферментативной активности, общая доступность солей и других заряженных молекул может регулировать скорость гидролиза и конденсации.
Гидролиз также является центральным аспектом метаболизма углерода [[85-87]]. Одним из примеров является участие воды во всех известных путях фиксации CO 2 , включая путь ацетил-CoA, который позволяет ацетогенам и метаногенам расти из H 2 и CO 2 [[88]]. Геномные реконструкции показывают, что последний универсальный общий предок (LUCA) следовал аналогичным путем, используя путь ацетил-КоА для углеродного и энергетического метаболизма [[89]].Как уже говорилось, недавние исследования показывают, что формиат, ацетат и пируват образуются в течение ночи из H 2 и CO 2 в воде с использованием только минеральных катализаторов в гидротермальных условиях [[22]]. Подобные абиотические пути недавно были показаны для промежуточных продуктов и продуктов обратного цикла лимонной кислоты [[24, 90]]. В этом отношении разрыв между такими гидротермальными условиями и химией реальной жизни, проявляющейся у современных автотрофов, сокращается. Таким образом, может также существовать связь между биохимией автотрофов и геохимией серпентинизирующих систем, когда речь идет о гидролизе.
В гидрогенотрофном метаногенезе первым шагом к производству метана является восстановление CO 2 до формилметанофурана (формил-MFR) с использованием ферредоксина в качестве донора электронов. Эта реакция катализируется формил-MFR дегидрогеназой. В ферментативном механизме молекула CO 2 направляется через гидрофобный канал в каталитическую камеру с вольфрамовым активным центром, в которую электроны притягиваются через длинную цепочку кластеров [4Fe-4S] [[91]].В каталитической камере CO 2 восстанавливается до формиата, гидрофильной молекулы. Формиат (или муравьиная кислота) диффундирует из активного центра через гидрофильный туннель к активному центру цинка, где он конъюгирован с MFR в виде карбамата [[91]] . Это окислительно-восстановительная реакция с участием электронов ферредоксина; вода образуется как вторичный продукт при образовании карбамата. То есть взаимодействие гидрофобных и гидрофильных поверхностей в сотрудничестве с металлическими катализаторами способствует контролируемым взаимодействиям вода-субстрат на начальной стадии фиксации CO 2 .Карбамат восстанавливается до формильной группы, связанной с MFR. Далее следует ступенчатое восстановление до метильной группы, связанной с MFR, до того, как группа будет перенесена на кофермент М. После последней стадии восстановления метильная группа высвобождается в виде CH 4 [[88]].
Общеизвестно, что ферменты имеют тенденцию исключать воду из активного центра и могут легко катализировать реакции против активности воды цитозоля. Вопрос о том, какие условия окружающей среды могли способствовать пребиотическому пути от CO 2 к органике и жизни, является более сложным.
Загадка гидролиза в исследовании происхождения жизни
Вода незаменима для жизни в том виде, в каком мы ее знаем. Но в то же время отщепление воды (конденсация, полимеризация) — одна из наиболее распространенных реакций метаболизма, лежащих в основе синтеза клеток [[53, 54]]. Обратная реакция, добавление воды, представляет собой гидролиз и может химически разрушать многие важные биомолекулы. Через гидролиз вода буквально работает против синтеза и накопления полимеров при зарождении жизни.
Хотя ферментативно опосредованный гидролиз может разрушить любой тип известной углеродной связи [[92]], современные биомолекулы защищены от случайного гидролиза их структурированным пространственным расположением гидрофобных / гидрофильных поверхностей и взаимодействием с неорганическими ионами и другими органическими молекулами [[37]. ]. Они способствуют созданию среды, в которой вода очень контролируемым и целенаправленным образом участвует в биохимических процессах. Конечно, современные биомолекулы в ходе эволюции подверглись постоянному отбору, чтобы удалить те, которые являются нестабильными, нерастворимыми или токсичными в клеточной среде.Однако у истоков жизни, на этапе пребиотической химии до появления генов и кодируемых белков, не было ни карманов для ферментов, ни сложных белков, ни упорядоченных мембран, ни ферментативно выработанного энергетического метаболизма, чтобы управлять постоянным химическим давлением реакций с участием воды. Следовательно, первичная полимеризация простых молекул в предшественников белков и нуклеиновых кислот посредством удаления воды, необходимого для жизни, происходила без помощи биологических механизмов, которые модулируют активность воды в живой клетке.Тем не менее, ниже мы увидим, что сама серпентинизация порождает неорганические механизмы, которые модулируют гомеостаз воды.
На первый взгляд, происхождение жизни и полностью водная химия не очень хорошо работают вместе, особенно если для протекания химических реакций требуются высокие температуры [[93, 94]]. Но в то же время цитозоль клетки также не является средой полностью водной химии. Итак, что-то не так с основной концепцией гидротермального происхождения или что-то не так с предположением, что гидротермальные условия обычно полностью связаны с водной химией? Внутри серпентинизирующихся систем есть определенные физико-химические участки, в которых наблюдается и даже поддерживается низкая активность воды (см. Вставку 2) при довольно умеренных температурах (100–200 ° C).Такие системы обеспечивают спектр условий, необходимых для перехода от соединений C 1 к сложной органике [[93, 94]]. Как и в клетках, свободная вода в правильной геохимической среде может быть связана как гидратная вода с помощью солей и других полярных молекул, снижая активность воды и, таким образом, способствуя синтезу более крупных молекул [[37, 93]]. Другой возможный способ стимулировать реакции, чувствительные к гидролизу, — это минеральные поверхности [[22, 27, 95-104]]. Минеральные поверхности обеспечивают разнообразие каталитических сред, позволяя проводить реакции на границе твердое тело – жидкость в водных условиях [[22, 23, 101, 104-106]].Комбинация высококаталитически активных минералов и низкой активности воды (обеспечиваемая высокими солевыми условиями или другими способами) может открыть множество возможных химических путей.
Современная среда с высоким содержанием соли и высокой температурой представляет собой экстремальные условия для жизни. Поскольку такие суровые условия, вероятно, преобладали на ранней Земле — особенно внутри ее коры — в то время, когда зародилась жизнь [[15, 107]], биологи давно подозревали, что современные экстремофилы могут иметь ключ к разгадке биологии первых клеток [[[ 108, 109]].Экстремофилы, обитающие в самых опасных для жизни местах Земли, могут дать ценную информацию о переходе от неживого к жизни. Галоархеи, например, могут выжить в кристаллах соли в течение очень долгих периодов времени, возможно, в течение геологических периодов времени, хотя сколько именно времени остается предметом предположений [[40, 110]]. Чтобы противодействовать осмотическому давлению солевой среды, некоторые галофилы переносят ионы K + в клетку [[40]]. Однако большинство других галофилов выбирают более энергоемкий путь для борьбы с высокими концентрациями солей путем синтеза осмолитов, таких как сахара, глицерин или производные аминокислот.При такой стратегии только организмы с очень эффективной скоростью метаболизма (высокий уровень синтеза АТФ) могут выжить в очень соленых условиях [[111]].
Соль может иметь интересные эффекты на трехмерную структуру белков в абиотических условиях. Было показано, например, что гомохиральные полипептиды лейцин-лизин (Leu-Lys) сворачиваются в виде случайных клубков в чистой воде [[112]]. Но в соли они образуют термостабильные и устойчивые к гидролизу бислои бета-листов с гидрофильными боковыми цепями Lys (положительно заряженная аминогруппа), направленными наружу в раствор соли, и гидрофобными боковыми цепями Leu (изобутильная группа) внутрь [[112]] .На структуру более крупных белков (140 аминокислот) также влияют высокие концентрации солей (до 2 мкм). Цепи кислотных аминокислот стабилизируются катионами солей, а бета-листы складываются так, чтобы указывать наружу. С простыми гидрофобными аминокислотами, такими как Leu, Ile (изолейцин) и Val (валин), указывающими внутрь, может быть сформировано гидрофобное ядро / карман, где возможные реакции полимеризации будут защищены от окружающей среды [[113, 114]]. Такие исследования показывают, как высокие концентрации соли — и, следовательно, среды с низкой активностью воды — могут обеспечивать динамические физико-химические условия, которые естественным образом модулируют структуры пребиотической химии, сохраняя при этом риск гидролиза ниже, чем в чисто водных средах.Эти условия возникают в результате действия простых ионных сил.
Были предложены различные механизмы для решения или обхода проблемы гидролиза в зародыше жизни. Наиболее часто встречающиеся из них вызывают существование циклов «влажный-сухой» [[59, 97, 106, 115, 116]], которые влекут за собой чередующиеся периоды гидролиза (высокая активность воды) и конденсации (отсутствие активности воды) для достижения полимеризация. Хотя такие циклы дают многообещающие результаты для синтеза нуклеотидов в лабораторных условиях [[115]], важно не только ограничивать среду происхождения за счет избегания воды, но также из соображений доступности углерода или энергии, основных предпосылок для микробной жизни.Недоизученной альтернативой влажно-сухим циклам могут быть границы раздела твердых фаз и водной фазы в геохимических системах, где активность воды постоянно низкая. Это было недавно предложено для гидротермальных осадочных слоев, где поровые пространства между вулканическими частицами могут быть заполнены силикагелями [[117]], что приводит к уменьшению количества свободной воды в геохимической системе. Конечно, активность воды — важная переменная в усилиях по обнаружению жизни за пределами Земли, поэтому активность воды имеет множество последствий для астробиологии (обсуждается во вставке 4).
Вставка 4. Значение активности воды для астробиологии
Активность воды напрямую связана с теориями и экспериментами, касающимися происхождения жизни. Поиск жизни на других планетах или лунах направляется поиском воды [[118]]. Когда дело доходит до поиска доказательств продолжающегося взаимодействия породы и воды в заметной величине, в последнее время в центре внимания исследований находятся спутники Сатурна, Энцелада и Титана. Миссия Кассини предоставила спектрометрические доказательства существования серпентинизации на Энцеладе [[119]].Его каменистая внутренняя часть покрыта несколькими километрами жидкой воды, которая в свою очередь покрыта несколькими километрами льда, образующего поверхность [[120, 121]]. Вода поддерживается в жидком состоянии из-за гравитации Сатурна, который постоянно месит маленький спутник диаметром примерно 500 км, чтобы генерировать тепло [[120, 121]]. На Южном полюсе Энцелада есть гейзеры, извергающие жидкую воду на сотни километров в космос [[120, 121]].
Во время миссии «Кассини» H 2 было измерено в шлейфах гейзера Энцелада [[122]].Присутствие H 2 , обнаружение силикатных наночастиц и моделей, предполагающих щелочной рН океана Энцелада, интерпретируется как свидетельство продолжающейся серпентинизации под ледяной корой Луны [[120, 122, 123]]. Шлейфы также содержат органические соединения. Это могут быть либо фрагменты полиароматических углеводородов, то есть продукты распада углерода, принесенного на Энцелад метеоритами [[124, 125]], либо продукты органического синтеза de novo , подпитываемого серпентинизацией [[126]].Хотя точный источник органических соединений в шлейфах до сих пор не ясен, взаимодействия породы и воды, похоже, имеют место на Энцеладе, а это означает, что в этом процессе нет ничего особенного, что ограничивало бы его распространение Землей. Если мы примем во внимание возможность того, что жизнь могла развиться в серпентинизирующихся системах, вместо того, чтобы исключить возможность a priori [[127]], последствия для астробиологии будут далеко идущими. Солнечный свет не будет иметь практически никакой роли в происхождении и, в свою очередь, расширит обитаемую зону в нашей солнечной системе и в недавно охарактеризованных солнечных системах до регионов, где солнечный свет не дает энергии.Химическая энергия серпентинизации потребует только водоредуцирующих пород и CO 2 для раскрытия.
В средах с очень низкой активностью воды для гидролиза может даже потребоваться катализ. Как упоминалось выше, двухвалентные ионы, такие как Mn 2+ и Mg 2+ , могут способствовать гидролизу как в активном центре гидролаз, так и в абиотических условиях (без ферментов). Таким образом, возможно, что такие ионы, которых довольно много в гидротермальных источниках / установках серпентинизации, могут обеспечить именно ту скорость гидролиза, которая необходима, если средняя активность воды в системе достаточно мала.В то же время различные солевые ионы действительно могут помочь снизить активность воды, связывая воду (гидратация). Таким образом, сложное взаимодействие солей, ионов, минералов, гелей, глин и воды, не говоря уже о самих органических соединениях, если они присутствуют, составляет водную загадку происхождения жизни.
Системы серпентинизации и водохозяйственная деятельность
Природные среды с низкой активностью воды не должны ограничиваться земными поверхностями, они могут существовать и существуют в серпентинизирующихся гидротермальных системах и, таким образом, могли иметь отношение к геохимическим условиям, в которых возникла жизнь.Конечно, низкая активность воды — не единственное требование, которому должна соответствовать такая обстановка. Неравновесные условия, углерод (клетки содержат примерно 50% углерода по сухому весу) [[128]], азот (клетки содержат 10% азота по сухому весу) [[129]], а также серу и фосфор, но, возможно, наиболее важно Изначально требовался непрерывный источник энергии. Системы серпентинизации объединяют углерод, энергию и электроны в форме CO 2 и H 2 в средах с низкой активностью воды [[130-133]].Серпентинизация — широко распространенное явление в современной океанической коре [[134, 135]]. Ультрабазитовые породы, содержащие силикат железа, вступают в реакцию с морской водой с выделением H 2 и в процессе превращаются в минералы серпентиновой группы («серпентинит», Mg 3 Si 2 O 5 (OH) 4 ). — отсюда и название серпентинизация. Одним из наиболее изученных участков серпентинизации является гидротермальное поле Лост-Сити, открытое недалеко от Срединно-Атлантического хребта в 2001 г. [[8]].На этом геологическом участке породы земной мантии, содержащие группу силикатов железа и магния, называемую оливином, из-за подъема магмы обнажены на морском дне, где они реагируют с морской водой с образованием H 2 [[136]].
Современные системы серпентинизации поддерживают градиенты температуры, pH и окислительно-восстановительного потенциала [[94]] и обеспечивают получение углерода (в основном в форме CO 2 / карбонатов), серы (H 2 S и сульфидных минералов) и в меньшей степени или в следовых количествах. также содержит азот и фосфат [[137]].Уникальной особенностью систем серпентинизации является непрерывное производство водорода (H 2 ) из воды, обеспечивающее окружающую среду постоянным притоком электронов, очень низким потенциалом средней точки [[138]] и химическим источником энергии [[139] -141]]. Производство H 2 влечет за собой также постоянное обновление железосодержащих минералов, которые могут действовать как катализаторы пребиотических реакций [[98, 99, 142, 143]], в том числе магнетита (Fe 3 O 4 ), a прямой продукт серпентинизации, сульфиды железа, такие как пирит (FeS 2 ) или грейгит (Fe 3 S 4 ) [[19, 21, 144]], и даже соединения самородных металлов, такие как аваруит (Ni 3 Fe) [[19]].Пребиотические реакции, катализируемые такими минералами, предположительно начались с реакции высвобождения энергии CO 2 и H 2 [[22]], которая сегодня все еще используется ацетогенами и метаногенами для роста [[11, 88, 133, 145- 149]].
А как насчет активности воды в системах серпентинизации? Она уменьшается, поскольку огромное количество морской воды потребляется во взаимодействиях между морской водой и оливином, и соленость в порах горных пород увеличивается [[150]]. Ультрабазиты, участвующие в процессе, изолируют морскую воду, что приводит к гидратации минералов (образованию гидроксидов) [[151]].Недавний эксперимент по серпентинизации in situ (при 280 ° C и 500 бар) предоставил важные механистические представления о взаимодействиях между породой и водой и о влиянии солености на свободную воду в порах минералов и, следовательно, на активность воды [[15]] . С помощью рамановской спектроскопии и микроскопии Lamadrid et al. [[15]] контролировали концентрацию солей и минералов в микропорах оливина. Образование серпентиновых минералов, брусита (Mg (OH) 2 ), магнетита (Fe 3 O 4 ) и H 2 , потребляет воду.По мере уменьшения содержания воды в порах во время серпентинизации увеличивается концентрация солей и минералов. В конечном итоге поры заполнены высококонцентрированным, «переполненным» гидротермальным флюидом с низкой активностью воды. Что Ламадрид и др. [[15]] описывает ситуацию, которая на удивление близка к тому, что наблюдается во внутриклеточных жидкостях. На геохимических микросайтах, которые они наблюдают [[15]], серпентинизация прекращается, как только активность воды становится слишком низкой (что означает, что соленость становится слишком высокой), и новая морская вода с более низкой соленостью должна диффундировать в систему, чтобы возобновить серпентинизацию.Объем породы увеличивается во время серпентинизации [[139]], что приводит к открытым трещинам и миграции морской воды в (микротрещины), что позволяет серпентинизации продолжаться. Этот сценарий колебания активности воды напоминает циклы «влажный – сухой», описанные выше. Ламадрид и др. [[15]] сообщают о разновидности саморегулирующейся системы, которая оттачивает низкую активность воды с экзергонической реакцией (образование H 2 ), которая прекращается, когда активность воды становится слишком низкой, и возобновляется только при добавлении воды. Химически доступность воды во время серпентинизации в очень малых масштабах неорганических компартментов микронного размера напоминает ионный гомеостаз в современных клетках на нескольких уровнях.
В неорганических порах ультраосновных пород сочетание поверхностного катализа минералов, низкой активности воды и непрерывного поступления энергии и углерода (в дополнение к азоту и другим питательным веществам) может, в принципе, привести к образованию сложных биомолекул. Такой устойчивый источник специфической «пищи» и энергии необходим для появления автокаталитических сетей, систем химических реакций, подобных метаболизму, которые в современных клетках проще, чем метаболизм, поскольку они поддерживают себя без ферментов [[78]].Считается, что такие реакционные системы являются промежуточными звеньями при переходе от неживых к живым системам [[152, 153]]. С геохимической точки зрения есть все основания полагать, что серпентинизация была очень распространенной реакцией на ранней Земле [[11, 16, 154, 155]]. Необходимые ингредиенты — морская вода и ультраосновные породы, которых на ранней Земле было практически неограниченное количество [[156]] . Радиоактивное изотопное датирование карбонатных структур и отложений в Лост-Сити показывает, что возраст этой серпентинизирующейся системы составляет не менее 30 000 лет.В массиве под Затерянным городом достаточно минералов, чтобы вызвать серпентинизацию еще на сотни тысяч, если не миллионы, лет [[139]]. Скалы из бывших серпентинизирующихся систем, сохранившиеся на глубине под Срединно-Атлантическим хребтом, где находится Лост-Сити, совсем недавно обнаружили синтезированные абиотически органические соединения, включая аминокислоты и более сложные молекулы [[157-159]]. Такие результаты подчеркивают потенциал систем серпентинизации пребиотического синтеза. В конечном итоге это означает, что системы серпентинизации, такие как щелочные гидротермальные источники, могут обеспечивать низкую активность воды.Многие неправильные представления о жерлах связаны с активностью воды и гидролизом, заблуждениями, которые предполагают химический состав свободного водного раствора в гидротермальных жерлах. [[127, 160, 161]].
На сегодняшний день каталитический и органический синтетический потенциал серпентинизирующих систем в сочетании с низкой активностью воды не исчерпан в достаточной степени в лабораторных экспериментах. Стоки активных участков, таких как гидротермальное поле Лост-Сити, регулярно контролируются, в основном показывая простые угольные кислоты, такие как формиат, метан и, возможно, ацетат, как абиотические продукты окислительно-восстановительных реакций, происходящих внутри пористой коры [[137, 141, 148, 162] ].Прямое наблюдение in situ реакций в системах серпентинизации в подводной коре представляет собой огромные технические проблемы. Но результаты прямых наблюдений могут быть столь же велики, поскольку текущие результаты показывают, что серпентинизирующие системы катализируют биомиметические реакции [[157-159]]. Проблема, однако, в том, что вентиляционные отверстия плотно заселены микробами и, возможно, содержат источники биологически полученного органического вещества, так что контролируемые лабораторные эксперименты в стерильных системах [[22-24]] необходимы в дополнение к исследованиям in situ и отбору химических проб.
Выводы и перспективы
Избегание постоянного гидролиза при сохранении доступа к химическим стадиям гидролиза имеет решающее значение для появления пребиотических химических сетей [[163]]. До сих пор большинство экспериментов по фиксации пребиотика CO 2 проводилось в водном растворе, который может блокировать гетерогенные минеральные катализаторы. Из промышленных процессов известно, что вода отравляет минеральные катализаторы за счет образования гидроксила на их поверхности, блокируя предполагаемые центры катализа [[164]].Это также объясняет, почему выходы всех экспериментов с водным CO 2 / H 2 обычно очень низки по сравнению с промышленными газофазными химическими процессами, такими как синтез Фишера-Тропша и Габера-Боша [[22, 23, 151, 164, 165]]. С другой стороны, исследования водяного пара в процессах гидрирования показали, что H 2 O, хотя и снижает выход промышленно значимых продуктов, включая метан и более крупные углеводороды, увеличивает процент оксигенатов C 1 –C 4 ‘ ‘- окисленные соединения углерода — возможно, включая органические кислоты, занимающие центральное место в метаболизме [[166]].Таким образом, ограниченное отравление водой может быть управляемой проблемой и, возможно, полезно, пока активность воды в целом низкая.
Гидролиз часто рассматривается как разрушительная сила в пребиотической химии [[93]]. Но в контексте механистических деталей мелкомасштабных геохимических реакций в серпентинизирующихся системах гидролиз становится неожиданной и потенциально мощной силой, которая может способствовать самоорганизации в пребиотической химии (рис. 2). Возможны две роли.Во-первых, в среде с постоянно низкой активностью воды гидролиз нарушается, превращая его из вездесущей проблемы в существенную реакцию, которая может быть опосредована двухвалентными ионами, как в современных гидролазах [[67, 84]]. Во-вторых, в условиях средней (не высокой) активности воды гидролиз может быть селективной движущей силой по отношению к сложным молекулам. В смоделированных гидротермальных условиях (высокая активность воды) минеральные катализаторы, восстановители и CO 2 могут генерировать восстановленные соединения углерода, включая 2-оксокислоты [[22, 23]], в течение ночи, в присутствии активированного азота аминокислоты также легко образуются [[[ 24, 25]].В метаболизме аминокислоты являются предшественниками азотистых гетероциклических соединений (кофакторов и азотистых оснований), исходным материалом и конечными продуктами протометаболических автокаталитических сетей [[31, 78, 153]]. При высоких концентрациях солей и низкой активности воды внутри пор серпентинизирующихся пород (от средней до низкой активности воды) пептиды могут образовываться из аминокислот даже при более высоких температурах [[114]]. Затем пептиды становятся еще более устойчивыми к гидролизу, когда они достигают длины, позволяющей образовывать альфа-спирали и бета-листы [[167]].В условиях устойчивого пептидного синтеза и устойчивого пептидного гидролиза начинается процесс отбора, посредством которого устойчивые к гидролизу пептиды могут накапливаться [[168, 169]], но не благодаря более быстрому синтезу, а скорее благодаря их более медленному гидролизу («выживаемость» из крепких ‘).
Системы серпентинизации, водные развлечения и происхождение. На рисунке схематично изображены гидратированные поры (связанная с породой вода, гидроксильные группы), внедренные в оливиновую матрицу серпентинизирующих систем.(А) Серпентинизация. H 2 синтезируется при взаимодействии воды и оливина (подробнее см.). Постоянно производятся каталитически активные минералы, включая магнетит (Fe 3 O 4 ), сульфиды железа (FeS 2 , Fe 3 S 4 ) и сплавы Ni, Fe (Ni 3 Fe). тогда как Fe 3 O 4 возникают в результате серпентинизации, а сульфиды и сплавы являются продуктами реакции ионов H 2 , H 2 S и Fe 2+ или Ni 2+ .(B) Химия минеральных поверхностей . С помощью таких минералов, как катализаторы, N 2 можно гидрогенизировать до аммиака [[26-28]], а CO 2 восстановить до углеродных соединений, таких как α-кетокарбоновые кислоты [[22-24]]. Последний может реагировать с активированным аммиаком до аминокислот [[24, 25]]. Теоретически на этой стадии можно было бы синтезировать и тиоэфиры, хотя это спорно [[172]]. (C) Автокаталитические сети. Продукты восстановления могут реагировать с множеством других N-содержащих углеродных соединений, таких как кофакторы или азотистые основания, особенно в условиях низкой активности воды (с высоким содержанием соли) [[29, 30]].Такие сложные мономеры будут подпитывать автокаталитические протометаболические сети [[31, 78, 153]]. (D) Полимеризация и складывание с помощью минералов . Из-за высоких концентраций солей и низкой активности воды внутри пор полимеры, такие как полипептиды, могут образовываться из аминокислот [[113, 114]]. Большинство свернутых белков могут достигать необходимой структурной точности для их каталитической функции без нуклеиновых кислот в качестве матриц, просто управляемых активностью воды и концентрацией соли [[112]]. Они могли концентрировать субстраты в своем защищенном интерьере.Здесь может происходить контролируемый гидролиз (например, через захваченные ионы Mg 2+ или Mn 2+ , как показано на рис.1) и реакции конденсации через кофакторы, полученные из минералов. Также возможна нацеленная фиксация CO 2 в таких белковых карманах с использованием аминокислот с нуклеофильными боковыми цепями и включенными переходными металлами, такими как Fe 2+ или Ni 2+ [[22, 23, 88, 173]] . Микропоры в древних серпентинизирующихся гидротермальных полях могли быть самыми ранними предшественниками биологических клеток.Все реакции, описанные на этом рисунке, могут впоследствии происходить в одной и той же микропоре, но для развития некоторых стадий могут потребоваться поры в разных физико-химических условиях. Поэтому следует учитывать хроматографические эффекты (разделение продуктов при перемещении между двумя разными порами).Таким образом, низкая активность воды может способствовать синтезу случайных пептидов, в то время как гидролитическое удаление наиболее лабильных из них будет способствовать получению неслучайных структур в области случайно синтезированных вариантов, возможно, без генетической инструкции.Такие пептиды обязательно должны иметь определенные структурные поверхности, следовательно, эквивалент нескольких активных центров [[170]], и, в свою очередь, могут отдавать предпочтение одним кинетически контролируемым реакциям по сравнению с другими, тем самым ускоряя самоорганизацию молекул. Синтез пребиотических пептидов требует постоянного источника аминокислот и энергии [[171]], в дополнение к подходящим поверхностям, чтобы катализировать полимеризацию [[57, 97]]. Серпентинизирующие системы могут обеспечить как в геологических временных масштабах, так и выживание самого прочного обогащения для неслучайных структур с собственными каталитическими свойствами в виде каталитически активных пептидов, которые в настоящее время служат в качестве элементов автокаталитических сетей, сохраняемых в микробном метаболизме [[78]].
Таким образом, мы описали, как сильно засоленные, серпентинизирующиеся, пористые горные породы могут обойти и, возможно, даже модулировать неконтролируемый гидролиз способом, аналогичным — похожим, но не связанным — с современным метаболизмом (Рис. 2). Могут ли эти процессы быть гомологичными, то есть сходными в силу общего происхождения, остается открытым вопросом для дальнейшего изучения.
Благодарности
Мы благодарим фонд VW (96_742), Deutsche Forschungsgemeinschaft (MA-1426 / 21-1) и Европейский исследовательский совет (ERC 666053) за финансирование.
Вклад авторов
MP написал рукопись с участием AV по гидролизу в биологии, вкладом KK по гидролизу в химическом контексте и серпентинизации, а также вкладом WFM в контексте происхождения жизни. KK исследовал и разработал блоки 1–3 и сформулировал вместе с MP и WFM схему, изображенную на рис. 2. MP адаптировал рис. 1, AV нарисовал рис. 2 с участием KK, WFM и MP. Проект AV и WFM Вставка 4.WFM редактировал и вносил свой вклад в рукопись.
Список литературы
- 1Westall F и Brack A (2018) Важность воды для жизни. Space Sci Rev. 214, 1-23.
- 2Speight JG (2018) Гидролиз. В «Механизмы реакции в экологической инженерии», стр. 203–229. CD & W Inc., Ларами, Вайоминг, США.
- 3Sousa FL, Hordijk W, Steel M и Martin WF (2015) Автокаталитические наборы в метаболизме E. coli . J Syst Chem 6, 4.
- 4Ereciflska M и Wilson DF (1982) Регулирование клеточного энергетического метаболизма. J Membr Biol 70, 1–14.
- 5Левер М.А., Роджерс К.Л., Ллойд К.Г., Оверманн Дж., Шинк Б., Тауер Р.К., Хелер Т.М. и Йоргенсен Б.Б. (2015) Жизнь в условиях экстремального ограничения энергии: синтез лабораторных и полевых исследований. FEMS Microbiol Rev 39, 688–728.
- 6 Таширо Т., Исида А., Хори М., Игису М., Койке М., Меджан П., Такахата Н., Сано И. и Комия Т. (2017) Ранние следы жизни в осадочных породах 3,95 млрд лет в Лабрадоре, Канада. Природа 549, 516–518.
- 7Ueno Y, Yamada K, Yoshida N, Maruyama S и Isozaki Y (2006) Данные флюидных включений для микробного метаногенеза в раннеархейскую эру. Природа 440, 516–519.
- 8Kelley DS, Karson JA, Blackman DK, Früh-Green GL, Butterfield DA, Lilley MD, Olson EJ, Schrenk MO, Roe KK, Lebon GT et al . (2001) Внеосевое гидротермальное жерловое поле около Срединно-Атлантического хребта на 30 ° северной широты. Nature 412, 145– 149.
- 9Früh-Green GL, Orcutt BN, Green SL, Cotterill C, Morgan S, Akizawa N, Bayrakci G, Behrmann J-H, Boschi C, Brazelton WJ и др. .(2017) Северные площадки. Proc Int Ocean Discov Программа 357.
- 10Klein F, Grozeva NG, Seewald JS (2019) Абиотический синтез метана и серпентинизация во флюидных включениях, содержащих оливин. Proc Natl Acad Sci 116, 17666–17672.
- 11McCollom TM и Seewald JS (2013) Серпентиниты, водород и жизнь. Элементы 9, 129–134.
- 12Ривес Е.П. и Фибиг Дж. (2020) Абиотический синтез метана и органических соединений в литосфере Земли. Элементы 16, 25–31.
- 13Кастинг Дж. Ф. и Холм Н. Г. (1992) От чего зависит объем Мирового океана? Earth Planet Sci Lett 109, 507– 515.
- 14Langmuir CH и Broecker W (2012) Как построить обитаемую планету.Princeton University Press, Нью-Джерси.
- 15Lamadrid HM, Rimstidt JD, Schwarzenbach EM, Klein F, Ulrich S, Dolocan A and Bodnar RJ (2017) Влияние активности воды на скорость серпентинизации оливина. Нац Коммуна 8, 16107.
- 16Sleep NH, Meibom A, Fridriksson T, Coleman RG и Bird DK (2004) H 2 -богатые флюиды от серпентинизации: геохимические и биотические последствия. Proc Natl Acad Sci USA 101, 12818–12823.
- 17Klein F, Bach W и McCollom TM (2013) Композиционный контроль генерации водорода во время серпентинизации ультраосновных пород. Lithos 178, 55–69.
- 18McCollom TM и Bach W (2009) Термодинамические ограничения на образование водорода во время серпентинизации ультраосновных пород. Geochim Cosmochim Acta 73, 856– 875.
- 19Klein F и Bach W. (2009) Фазовые отношения Fe-Ni-Co-O-S во взаимодействиях перидотит-морская вода. J Бензин 50, 37–59.
- 20Foustoukos DI, Bizimis M, Frisby C и Shirey SB (2015) Редокс-контроль минерализации Ni-Fe-PGE и фракционирования Re / Os во время серпентинизации абиссальных перидотитов. Geochim Cosmochim Acta 150, 11–25.
- 21Findlay AJ, Estes ER, Iii GWL, Gartman A, Yücel M, Kamyshny AK и Luther GW III, Jr (2019) Образование и перенос наночастиц железа и сульфидов в зарождающихся шлейфах гидротермальных источников. Нац Коммуна 10, 1597.
- 22Preiner M, Igarashi K, Muchowska K, Yu M, Varma SJ, Kleinermanns K, Nobu MK, Kamagata Y, Tüysüz H, Moran J et al .(2020) Водородзависимый геохимический аналог первичного углерода и энергетического метаболизма. Nat Ecol Evol 4, 534–542.
- 23Varma SJ, Muchowska KB, Chatelain P и Moran J (2018) Самородное железо восстанавливает CO 2 до промежуточных продуктов и конечных продуктов пути ацетил-КоА. Nat Ecol Evol 2, 1019–1024.
- 24Muchowska KB, Varma SJ and Moran J (2019) Синтез и распад универсальных метаболических предшественников, которым способствует железо. Природа 569, 104–107.
- 25Barge LM, Flores E, Baum MM, Vandervelde DG и Russell MJ (2019) Редокс-градиенты и градиенты pH управляют синтезом аминокислот в минеральных системах оксигидроксида железа. Proc Natl Acad Sci USA 116, 4828– 4833.
- 26Schoonen MAA and Xu Y (2003) Восстановление азота в условиях гидротермальных источников: значение для пребиотического синтеза соединений C-H-O-N. Астробиология 1, 133–142.
- 27Кандемир Т., Шустер М.Э., Сенишин А., Беренс М. и Шлёгль Р. (2013) Пересмотр процесса Габера-Боша: реальная структура и стабильность «аммиачного железа» в рабочих условиях. Angew Chemie — Int Ed 52, 12723–12726.
- 28Dörr M, Käßbohrer J, Grunert R, Kreisel G, Brand WA, Werner RA, Geilmann H, Apfel C, Robl C и Weigand W. (2003) Возможное пребиотическое образование аммиака из диазота на поверхностях сульфида железа. Angew Chemie — Int Ed 42, 1540–1543.
- 29Saladino R, Crestini C, Pino S, Costanzo G и Di Mauro E (2012) Формамид и происхождение жизни. Phys Life Rev. 9, 84–104.
- 30Heinz VB, Ried W. and Dose K (1979) Thermische Erzeugung von Pteridinen und Flavinen aus Aminosauregemischen. Angew Chemie 91, 510–511.
- 31Preiner M, Xavier JC, Vieira N, Kleinermanns K, Allen JF and Martin WF (2019) Катализаторы, автокатализ и происхождение метаболизма. Интерфейс Focus 9, 201.
- 32Delgado F, Cermak F, Hecht NC, Son VC и Li S (2013) Внутриклеточный водообмен для измерения сухой массы, массы воды и изменений химического состава живых клеток. PLoS One 8, 67590.
- 33Minton AP, Colclasure GC и Parker JC (1992) Модель роли макромолекулярного скопления в регуляции клеточного объема. Proc Natl Acad Sci USA 89, 10504– 10506.
- 34Ishihama Y, Schmidt T., Rappsilber J, Mann M, Hartl FU, Kerner MJ и Frishman D (2008) Профилирование содержания белка в цитозоле Escherichia coli . BMC Genom 9, 102.
- 35Groen J, Foschepoth D, te Brinke E, Boersma AJ, Imamura H, Heus HA и Huck WTS (2015) Ассоциативные взаимодействия в переполненных растворах биополимеров противодействуют эффектам истощения. J Anal Appl Pyrolysis 137, 13041–13048.
- 36Sarkar M, Smith AE, Pielak GJ и Baldwin RL (2013) Влияние восстановленного цитозоля на стабильность белка. Proc Natl Acad Sci USA 110, 19342–19347.
- 37Fulton AB (1982) Насколько переполнена цитоплазма? Ячейка 30, 345– 347.
- 38Rupley JA, Yang P-H и Tollin G (1980) Термодинамические и связанные с ними исследования взаимодействия воды с белками. Водный полимер , 127, 111–132.
- 39Pal SK и Zewail AH (2004) Динамика воды в биологическом распознавании. Chem Rev 104, 2099–2123.
- 40Grant WD, Danson MJ, Scott DJ, Halling PJ, Engberts JBFN, Ho MW и Berendsen HJC (2004) Жизнь при низкой активности воды. Philos Trans R Soc B Biol Sci 359, 1249–1267.
- 41Blake CCF, Pulford WCA, Artymiuk PJ и Huber R (1983) Рентгеновские исследования воды в кристаллах лизоцима. Дж Мол Биол 167, 693–723.
- 42Smith JD, Smith JD, Cappa CD, Wilson KR, Messer BM, Cohen RC и Saykally RJ (2013) Энергетика перестроек сети водородных связей в жидкой воде. Наука 306, 851–853.
- 43Hribar B, Southall NT, Vlachy V и Dill KA (2002) Как ионы влияют на структуру воды. J Am Chem Soc 124, 12302–12311.
- 44Розанов Л.М., Хабланян М.Х. (2002) Вакуумная техника Лондон; Тейлор и Фрэнсис Тейлор, Нью-Йорк.
- 45Cossins BP, Jacobson MP и Guallar V (2011) Новый взгляд на среду бактериального цитозоля. PLoS Comput Biol 7, 1002066.
- 46Spitzer J (2011) От воды и ионов к переполненным биомакромолекулам: in vivo структурирование прокариотической клетки. Microbiol Mol Biol Rev 75, 491–506.
- 47Spitzer J и Poolman B (2013) Насколько переполнена прокариотическая цитоплазма? FEBS Lett. 587, 2094–2098.
- 48Gi M (2012) Активность ферментов в многолюдной среде. PLoS One 7, 39418.
- 49Politou A и Temussi PA (2015) Пересмотр догмы: эффект исключения объема в молекулярном скоплении. Curr Opin Struct Biol 30, 1–6.
- 50Spitzer JJ и Poolman B (2005) Электрохимическая структура переполненной цитоплазмы. Trends Biochem Sci 30, 536– 541.
- 51Joó F, Balogh N, Horváth LI, Filep G, Horváth I и Vígh L (1991) Комплексные реакции гидрирования / окисления водорастворимого катализатора гидрирования палладия ди (ализаринмоносульфонат натрия) и детали гомогенного гидрирования липидов в изолированных биомембранах и живые клетки. Анальная биохимия 194, 34–40.
- 52Curtis W и Ordal EJ (1954) Гидрогеназа и водородный метаболизм в Micrococcus aerogenes. Дж. Бактериол 68, 351–361.
- 53Vagelos R (1964) Липидный обмен. Annu Rev Biochem 33, 139– 172.
- 54Calvin M (1974) Биополимеры: происхождение, химия и биология. Angew Chemie — Int Ed 13, 121–131.
- 55Дэвис Дж. М., Пул Р. Дж. И Сандерс Д. (1993) Расчетное изменение свободной энергии гидролиза неорганического пирофосфата и АТФ: очевидное значение. для неорганических пирофосфатных реакций промежуточного метаболизма. Biochim Biophys Acta — Bioenerg 1141, 29–36.
- 56Акола Дж. И Джонс Р.О. (2003) Гидролиз АТФ в воде — исследование с функциональной плотностью. J. Phys Chem B 107, 11774–11783.
- 57Lambert JF (2008) Адсорбция и полимеризация аминокислот на минеральных поверхностях: обзор. Orig Life Evol Biosph 38, 211–242.
- 58Rode BM (1999) Пептиды и происхождение жизни. Пептиды 20, 773–786.
- 59Forsythe JG, Yu S, Mamajanov I, Grover MA, Krishnamurthy R, Fernández FM and Hud NV (2015) Эфир-опосредованное образование амидной связи, обусловленное циклами влажный-сухой: возможный путь к полипептидам на пребиотической Земле. Angew Chemie — Int Ed 54, 9871–9875.
- 60Imai EI, Honda H, Hatori K, Brack A и Matsuno K (1999) Удлинение олигопептидов в моделируемой подводной гидротермальной системе. Наука 283, 831–833.
- 61Le Son H, Suwannachot Y, Bujdak J и Rode BM (1998) Соль-индуцированное образование пептидов из аминокислот в присутствии глин и родственных катализаторов. Inorganica Chim Acta 272, 89–94.
- 62Zaia DAM (2004) Обзор адсорбции аминокислот на минералах: было ли это важно для происхождения жизни? Аминокислоты 27, 113–118.
- 63Berg P и Ofengand EJ (1958) Ферментативный механизм связывания аминокислот с РНК. Proc Natl Acad Sci USA 44, 78–86.
- 64Ofengand EJ, Dieckmann M и Berg P (1961) Ферментативный синтез аминоацильных производных рибонуклеиновой кислоты. J Biol Chem 236, 1741–1747.
- 65Berg JM, Tymoczko JL, Gatto GJJ and Stryer L (2015) Biochemistry, 8th. В. Х. Фриман и компания, Нью-Йорк.
- 66Kottur J and Nair DT (2018) Гидролиз пирофосфата является внутренним и критическим этапом реакции синтеза ДНК. Nucleic Acids Res 46, 5875.
- 67 Варфоломеев С.Д., Гуревич К.Г. (2001) Активные центры ферментов: биоинформатика, архитектура и механизмы действия. Russ Chem Bull 50, 1709–1717.
- 68Яо Нью-Йорк и О’Доннелл М.Э. (2016) Эволюция репликационных машин. Crit Rev Biochem Mol Biol 51, 135–149.
- 69Deutscher MP и Kornberg A (1969) Ферментативный синтез дезоксирибонуклеиновой кислоты. J Biol Chem 244, 3019–3028.
- 70Jensen PR и Michelsen O (1992) Углеродный и энергетический метаболизм мутантов atp Escherichia coli . Дж. Бактериол 174, 7635–7641.
- 71, Мюллер М., Ментел М., Ван Хеллемонд Дж. Дж., Хенце К., Вуле С., Гулд С. Б., Ю. Р-Й, Ван ДерГизен М., Тиленс А. Г. и Мартин В. Ф. (2012) Биохимия и эволюция анаэробного метаболизма энергии у эукариот. Microbiol Mol Biol Rev 76, 444–495.
- 72Oppenheimer NJ (1994) Гидролиз НАД: химические и ферментативные механизмы. Mol Cell Biochem 138, 245– 251.
- 73Spencer AK, Greenspan AD и Cronan JE Jr. (1978) Тиоэстеразы I и II из Escherichia coli . Гидролиз тиоэфиров нативного ацилацильного белка-носителя. J Biol Chem 253, 5922–5926.
- 74Wolfenden R (1963) Механизм гидролиза аминоацильной РНК. Biochim Biophys Acta 47, 353.
- 75Lee HC и Aarhus R (1993) Широкое распространение фермента, катализирующего гидролиз циклической АДФ-рибозы. Биохимия . Biophys Acta — Protein Struct Mol Enzymol 1164, 68–74.
- 76 Варфоломеев С.Д. (2004) Каталитические центры ферментов: структурные парадоксы, феномен структурного единства и новые реакции. Mendeleev Commun 14, 185–188.
- 77Rack JGM, Ariza A, Drown BS и др. . (2018) (АДФ-рибозил) гидролазы: структурная основа различного распознавания и ингибирования субстрата. Cell Chem Biol 25, 1533–1546.e12.
- 78Xavier JC, Hordijk W, Kauffman SA, Steel M и Martin WF (2020) Автокаталитические химические сети в основе метаболизма. Proc Royal Soc B Biol Sci 287.
- 79Holm NG (2012) Значение Mg в пребиотической геохимии. Геобиология 10, 269–279.
- 80Belmonte L and Mansy SS (2016) Металлические катализаторы и происхождение жизни. Элементы 12, 413–418.
- 81Соарс АРМ, Андерсон Д.Р., Чандрашейкер В. и Линдси Дж. С. (2013) Каталитическая диверсификация при улавливании металлов в пребиотической модели образования тетрапиррольных макроциклов. Новый J Chem 37, 2716.
- 82Шунен М., Смирнов А. и Кон С. (2004) Взгляд на роль минералов в синтезе пребиотиков. AMBIO A J Hum Environ 33, 539–551.
- 83Голдман А.Д., Баросс Дж. А. и Самудрала Р. (2012) Ферментативные и метаболические возможности в раннем возрасте. PLoS One 7, e39912.
- 84Williams NH (2000) Катализируемый ионами магния гидролиз АТФ. J Am Chem Soc 122, 12023–12024.
- 85Prince RC, Amande TJ и McGenity TJ (2010) Прокариотические деструкторы углеводородов. В Справочнике по углеводородной и липидной микробиологии (Тиммис, К.Н., изд.), Стр. 1669–1692. Издательство Springer International, Берлин, Гейдельберг.
- 86Weeks A, Lund L and Raushel FM (2006) Туннелирование промежуточных продуктов в реакциях, катализируемых ферментами. Curr Opin Chem Biol 10, 465–472.
- 87Ragsdale SW (2008) Энзимология пути Вуда-Люнгдаля ацетогенеза. Ann N Y Acad Sci 1125, 129–36.
- 88Fuchs G (2011) Альтернативные пути фиксации углекислого газа: понимание ранней эволюции жизни? Annu Rev Microbiol 65, 631–658.
- 89 Weiss MC, Sousa FL, Mrnjavac N, Neukirchen S, Roettger M, Nelson-Sathi S и Martin WF (2016) Физиология и среда обитания последнего универсального общего предка. Нат Микробиол 1, 16116.
- 90Muchowska KB, Varma SJ, Chevallot-Beroux E, Lethuillier-Karl L, Li G и Moran J (2017) Металлы продвигают последовательности обратного цикла Кребса. Nat Ecol Evol 1, 1716–1721.
- 91Wagner T, Ermler U and Shima S (2016) Метаногенный восстанавливающий и фиксирующий фермент CO 2 является бифункциональным и содержит 46 кластеров [4Fe-4S]. Наука 354, 114–117.
- 92Timm DE, Mueller HA, Bhanumoorthy P, Harp JM и Bunick GJ (1999) Кристаллическая структура и механизм гидролазы углерод-углеродной связи. Строение 7, 1023– 1033.
- 93Pace NR (1991) Происхождение жизни лицом к лицу с физическим окружением. Ячейка 65, 531–533.
- 94Baross JA и Hoffman SE (1985) Подводные гидротермальные источники и связанные с ними градиентные среды как места происхождения и эволюции жизни. Orig Life Evol Biosph 15, 327–345.
- 95Wächtershäuser G (1988) До ферментов и матриц: Теория поверхностного метаболизма. Microbiol Rev 52, 452– 484.
- 96Bernal JD (2002) Физическая основа жизни. Proc Phys Soc Sect A 62, 537–558.
- 97Erastova V, Degiacomi MT, Fraser DG и Greenwell HC.Контроль химического состава поверхности минералов для определения происхождения пребиотических пептидов. Nat Commun 1–9.
- 98Vincent L, Berg M, Krismer M, Saghafi ST, Cosby J, Sankari T., Vetsigian K, Ii HJC and Baum DA (2019) Выбор химической экосистемы на минеральных поверхностях показывает долгосрочную динамику, согласующуюся со спонтанным возникновением взаимного катализа. Жизнь 9, 80.
- 99Хазен Р.М., Сверженский Д.А. (2010) Минеральные поверхности, геохимические сложности и происхождение жизни. Колд Спринг Харб Перспект Биол 2, a002162.
- 100McCollom TM и Seewald JS (2003) Экспериментальное исследование гидротермальной реакционной способности органических кислот и кислотных анионов: II. Уксусная кислота, ацетат и валериановая кислота. Geochim Cosmochim Acta 67, 3645– 3664.
- 101Chen QW и Bahnemann DW (2000) Восстановление диоксида углерода магнетитом: значение для первичного синтеза органических молекул [11]. J Am Chem Soc 122, 970–971.
- 102Santos-Carballal D, Roldan A, Dzade NY и De LeeuwNH (2018) Реакционная способность CO 2 на поверхности магнетита (Fe 3 O 4 ), грейгита (Fe 3 S 4 ) и макинавит (FeS). Philos Trans R Soc A 376, 20170065.
- 103 Ролдан А., Холлингсворт Н., Роффи А., Ислам Х.Ю., Гудолл Дж.Б.М., Кэтлоу CRA, Дарр Дж. А., Брасс В., Санкар Г., Холт КБ и др. .(2015) Биологически активная конверсия CO 2 с помощью катализаторов из сульфида железа в устойчивых условиях. Chem Commun 51, 7501–7504.
- 104 Гуан Г., Кида Т., Ма Т., Кимура К., Абэ Э и Йошида А. (2003) Восстановление водного CO 2 при температуре окружающей среды с использованием композитов на основе нуль-валентного железа. Грин Хим 5, 630.
- 105Huber C и Wächtershäuser G (1997) Активированная уксусная кислота путем фиксации углерода на (Fe, Ni) S в изначальных условиях. Наука 276, 245– 248.
- 106Fontecilla-Camps JC (2019) Геохимическая преемственность и замена катализатора / кофактора в возникновении и эволюции жизни. Angew Chemie — Int Ed 58, 42–48.
- 107 Wiegel J и Adams MWW (ред.) (1998) Термофилы: ключи к молекулярной эволюции и происхождению жизни.Тейлор и Фрэнсис, Лондон.
- 108Singh RP, Buttar HK, Kaur R and Manchanda G (2020) Многогранная жизнь микробов: выживание в различных средах. В «Универсальность микробов в разнообразных средах» (Р.П. Сингх, Дж. Манчанда, И. К. Маурья и Ю. Вей, ред.), Стр. 3–12. Springer Singapore, Сингапур.
- 109Штеттер К.О. (2006) Гипертермофилы в истории жизни. Philos Trans R Soc B 361, 1837–1843.
- 110Roedder E (1984) Жидкости в соли. Am Mineral 69, 413–439.
- 111Oren A (2011) Высокие термодинамические пределы микробной жизни. Environ Microbiol 13, 1908–1923.
- 112Barbier B и Brack A (1992) Конформационно-контролируемый гидролиз полирибонуклеотидов последовательными основными полипептидами. J Am Chem Soc 114, 3511–3515.
- 113Longo LM, Lee J и Blaber M (2013) Упрощенный дизайн белка, предвзятый для пребиотических аминокислот, дает складываемый галофильный белок. Proc Natl Acad Sci USA 110, 2135– 2139.
- 114Longo LM and Blaber M (2014) Конструкция пребиотических белков поддерживает галофильное происхождение складываемых белков. Front Microbiol 4, 2013–2015.
- 115Becker S, Schneider C, Dejmek M, Carell T, Okamura H и Crisp A (2018) Циклы влажно-сушки обеспечивают параллельное происхождение канонических и неканонических нуклеозидов путем непрерывного синтеза. Нац Коммуна 9, 163.
- 116 Tucker MC, Srinivasan V, Ross PN и Weber AZ.(2013) Производительность и цикл проточной ячейки окислительно-восстановительного потенциала железа / водорода с различными солями католита. J Appl Electrochem 43, 637–644.
- 117Westall F, Hickman-Lewis K, Hinman N, Gautret P, Campbell KA, Bréhéret JG, Foucher F, Hubert A, Sorieul S, Dass AV et al . (2018) Гидротермально-осадочный контекст происхождения жизни. Астробиология 18, 259–293.
- 118Landis GA.(2001) Марсианская вода: есть ли на Марсе сохранившиеся галобактерии? Астробиология 1, 161–164.
- 119Мэтсон Д.Л., Кастильо Дж. С., Лунин Дж. И Джонсон ТВ (2007) Шлейф Энцелада: Составное свидетельство горячего интерьера. Икар 187, 569–573.
- 120Hsu H-W, Postberg F, Sekine Y, Shibuya T., Kempf S, Horányi M, Juhász A, Altobelli N, Suzuki K, Masaki Y и др. .(2015) Текущая гидротермальная деятельность на Энцеладе. Природа 519, 207–210.
- 121 Шибуя Т., Постберг Ф., Хсу Х-В, Сузуки К., Масаки Ю., Куватани Т., Мори М., Хонг ПК, Йошизаки М., Тачибана С. и др. . (2015) Высокотемпературные взаимодействия воды и породы и гидротермальные условия в хондритоподобном ядре Энцелада. Nat Commun 6, 1–8.
- 122 Уэйт Дж. Х., Глейн С. Р., Перриман Р. С., Теолис Б. Д., Маги Б. А., Миллер Г., Граймс Дж., Перри М. Е., Миллер К. Э., Букет А и др. .(2017) Кассини находит молекулярный водород в плюме Энцелада: свидетельство гидротермальных процессов. Наука 356, 155– 159.
- 123Glein CR, Baross JA и Waite JH (2015) pH океана Энцелада. Geochim Cosmochim Acta 162, 202– 219.
- 124 Постберг Ф., Хаваджа Н., Абель Б., Чоблет Дж., Глейн С.Р., Гудипати М.С., Хендерсон Б.Л., Хсу Х.В., Кемпф С., Кленнер Ф. и др. .(2018) Высокомолекулярные органические соединения из глубин Энцелада. Природа 558, 564– 568.
- 125Alexander CMOD, Cody GD, De Gregorio BT, Nittler LR and Stroud RM (2017) Природа, происхождение и модификация нерастворимого органического вещества в хондритах, главном источнике углерода и азота Земли. Chem Erde 77, 227–256 .
- 126Khawaja N, Postberg F, Hillier J, Klenner F, Kempf S, Reviol R, Zou Z and Srama R (2019) Маломассивные азотные, кислородсодержащие и ароматические соединения в ледяных зернах Энчелады. Пн Не R Astron Soc 489, 5231– 5243.
- 127Deamer D и Damer B (2017) Может ли жизнь начаться на Энцеладе? Взгляд из гидротермальной химии. Астробиология 17, 834–839.
- 128Bratbak G and Dundas I (1984) Оценка содержания сухого вещества бактерий и биомассы. Appl Environ Microbiol 48, 755–757.
- 129Vrede K, Heldal M, Norland S и Bratbak G (2002) Элементный состав (C, N, P) и объем клеток экспоненциально растущего и ограниченного питательными веществами бактериопланктона. Appl Environ Microbiol 68, 2965–2971.
- 130Holm NG (1992) Почему гидротермальные системы предлагаются в качестве вероятной среды для происхождения жизни? В морских гидротермальных системах и происхождении жизни (Н.Г. Холм, изд.), стр. 5–14. Springer, Dordrecht.
- 131Nisbet E and Sleep NH (2001) Среда обитания и природа ранней жизни. Природа 409, 1083– 1091.
- 132Frost RB и Beard JS (2007) Об активности кремнезема и серпентинизации. J Petrol 48, 1351–1368.
- 133Martin WF и Russell MJ (2007) О происхождении биохимии в щелочном гидротермальном источнике. Philos Trans R Soc B Biol Sci 362, 1887–1925.
- 134Früh-Green GL, Connolly JAD, Plas A, Kelley DS и Grobety B. (2004) Серпентинизация океанических перидотитов: последствия для геохимических циклов и биологической активности. В Подводной биосфере на Срединно-океанических хребтах Серия геофизических монографий 144 (У. Д. Уилкок, Э. Ф. Делонг, Д. С. Келли, Д. А. Баросс и К. С. Крейг), стр. 119–136. Американский геофизический союз 10.1029 / 144GM08.
- 135Holm NG, Oze C, Mousis O, Waite JH и Guilbert-Lepoutre A (2015) Серпентинизация и формирование H 2 и CH 4 на небесных телах (планетах, лунах, кометах). Астробиология 15, 587–600.
- 136Schrenk MO, Kelley DS, Bolton SA и Baross JA (2004) Низкое разнообразие архей связано с геохимическими процессами на дне гидротермального поля Лост-Сити, Срединно-Атлантический хребет. Environ Microbiol 6, 1086– 1095.
- 137Lang SQ и Brazelton WJ (2020) Обитаемость морских серпентинитовых недр: тематическое исследование гидротермального поля Лост-Сити. Philos Trans R Soc A 378, 20180429.
- 138Boyd ES, Amenabar MJ, Poudel S, Templeton AS и Boyd ES (2020) Биоэнергетические ограничения происхождения автотрофного метаболизма. Philos Trans R Soc A 378, 201.
- 139 Келли Д.С., Карсон Дж. А., Фрю-Грин Г. Л., Йоргер Д. Р., Шэнк Т. М., Баттерфилд Д. А., Хейс Дж. М., Шренк МО, Олсон Э. Дж., Проскуровски Г. и др. . (2005) Экосистема с серпентинитами: гидротермальное поле затерянного города. Наука 307, 1428–1434.
- 140Проскуровски Г., Лилли М.Д., Сивальд Дж.С., Фру х-Грин Гл, Олсон Э.Дж., Луптон Дж.Э., Сильва С.П. и Келли Д.С. (2008) Абиогенная добыча углеводородов на гидротермальном месторождении Лост-Сити. Наука 319, 319–607.
- 141Lang SQ, Баттерфилд Д.А., Шульте М., Келли Д.С. и Лилли М.Д. (2010) Повышенные концентрации формиата, ацетата и растворенного органического углерода, обнаруженные на гидротермальном поле Лост-Сити. Geochim Cosmochim Acta 74, 941–952.
- 142Huber C, Eisenreich W и Wächtershäuser G (2010) Синтез α-амино и α-гидроксикислот в вулканических условиях: последствия для происхождения жизни. Tetrahedron Lett 51, 1069– 1071.
- 143Camprubi E, Jordan SF, Vasiliadou R and Lane N (2017) Катализ железа в происхождении жизни. IUBMB Life 69, 373–381.
- 144Russell MJ и Hall AJ (1997) Возникновение жизни из пузырьков моносульфида железа на подводном гидротермальном фронте окислительно-восстановительного потенциала и pH. J. Geol Soc London 154, 377–402.
- 145Shock EL и Helgeson HC (1988) Расчет термодинамических и транспортных свойств водных частиц при высоких давлениях и температурах: алгоритмы корреляции для ионных частиц и уравнения состояния для прогнозов до 5 kb и 1000 ° C. Geochim Cosmochim Acta 52, 2009– 2036.
- 146Shock EL (1990) Геохимические ограничения происхождения органических соединений в гидротермальных системах. Orig Life Evol Biosph 20, 331–367.
- 147Konn C, Charlou JL, Holm NG и Mousis O (2015) Производство метана, водорода и органических соединений в гидротермальных жерлах Срединно-Атлантического хребта, расположенных в ультрабазитах. Астробиология 15, 381– 399.
- 148Schrenk MO, Brazelton WJ and Lang SQ (2013) Серпентинизация, углерод и глубокая жизнь. Рев Минеральная геохимия 75, 575–606.
- 149Martin W, Baross J, Kelley D and Russell MJ (2008) Гидротермальные источники и происхождение жизни. Nat Rev Microbiol 6, 805–814.
- 150Preiner M, Xavier J, Sousa F, Zimorski V, Neubeck A, Lang S, Greenwell H, Kleinermanns K, Tüysüz H, McCollom T et al .(2018) Серпентинизация: соединение геохимии, древнего метаболизма и промышленной гидрогенизации. Жизнь 8, 41.
- 151Miller HM, Mayhew LE, Ellison ET, Kelemen P, Kubo M и Templeton AS (2017) Производство водорода при низкой температуре во время экспериментальной гидратации частично серпентинизированного дунита. Geochim Cosmochim Acta 209, 161–183.
- 152Кауффман С.А. (1986) Автокаталитические наборы белков. J Theor Biol 119, 1–24.
- 153Steel M, Hordijk W и Xavier JC (2019) Автокаталитические сети в биологии: структурная теория и алгоритмы. J R Интерфейс Soc 16, 20180808.
- 154Russell MJ, Hall AJ and Martin WF (2010) Серпентинизация как источник энергии в зародыше жизни. Геобиология 8, 355–371.
- 155Etiope G и Sherwood Lollar B (2013) Абиотический метан на Земле. Rev Geophys 51, 276–299.
- 156Занле К.Дж., Арндт Н., Кокелл С., Халлидей А., Нисбет Э., Селсис Ф. и Сон NH (2007) Появление обитаемой планеты. Space Sci Rev. 129, 35–78.
- 157Ménez B, Pisapia C, Andreani M, Jamme F, Vanbellingen QP, Brunelle A, Richard L., Dumas P и Réfrégiers M и др. .(2018) Абиотический синтез аминокислот в глубинах океанической литосферы. Природа 564, 59–63.
- 158Sforna MC, Brunelli D, Pisapia C, Pasini V, Malferrari D and Ménez B (2018) Абиотическое образование конденсированного углеродистого вещества в гидратирующей океанической коре. Нац Коммуна 9, 5049.
- 159Андреани М. и Менез Б. (2019) Новые взгляды на абиотический органический синтез и переработку во время гидротермальных изменений океанической литосферы.In Deep Carbon (Б. Н. Оркатт, И. Дэниэл и Р. Дасгупта, ред.), Стр. 447–479. Издательство Кембриджского университета, Кембридж.
- 160 Беннер С. А., Ким Х. Дж. И Карриган М. А. (2012) Асфальт, вода и пребиотический синтез рибозы, рибонуклеозидов и РНК. Acc Chem Res 45, 2025–2034.
- 161Chandru K, Gilbert A, Butch C, Aono M и Cleaves HJ (2016) Абиотическая химия тиолированных производных ацетата и происхождение жизни. Sci Rep 6, 1–11.
- 162Charlou JL, Donval JP, Fouquet Y, Jean-Baptiste P и Holm N (2002) Геохимия высоких H 2 и CH 4 выходных флюидов, выходящих из ультраосновных пород на гидротермальном поле Рейнбоу (36 ° 14 ′ с.ш., МАР). Chem Geol 191, 345–359.
- 163Xavier JC, Hordijk W., Kauffman SA, Steel M и Martin WF.(2019) Автокаталитические химические сети в эволюции предшествовали белкам и РНК. BioRxiv [ПРЕПЕЧАТАТЬ].
- 164Porosoff MD, Yan B и Chen JG (2016) Каталитическое восстановление CO 2 с помощью H 2 для синтеза CO, метанола и углеводородов: проблемы и возможности. Energy Environ Sci 9, 62–73.
- 165Leigh GJ (2004) Haber – Bosch и другие производственные процессы.В «Катализаторы для фиксации азота: нитрогеназы, соответствующие химические модели и коммерческие процессы» (Б. Е. Смит, Р. Л. Ричардс и В. Е. Ньютон, ред.), Стр. 33–54. Дордрехт: Springer.
- 166Satterfield CN, Hanlon RT, Tung SE, Zou Zmiln и Papaefthymiou GC (1986) Влияние воды на катализируемый железом синтез Фишера-Тропша. Ind Eng Chem Prod Res Dev 25, 407–414.
- 167Brack A (1987) Избирательное появление и выживание ранних полипептидов в воде. Orig Life 17, 367–379.
- 168Wolfenden R (2011) Контрольные скорости реакций, стабильность биологических молекул в воде и эволюция каталитической силы ферментов. Annu Rev Biochem 80, 645–667.
- 169Radzicka A and Wolfenden R (1996) Скорость некаталитического гидролиза пептидной связи в нейтральном растворе и сродство протеаз к переходному состоянию. J Am Chem Soc 118, 6105–6109.
- 170Токурики Н. и Тауфик Д.С. (2009) Динамизм и эволюционируемость белков. Наука 324, 203–207.
- 171Danger G, Plasson R и Pascal R (2012) Пути образования и эволюции пептидов в пребиотической среде. Chem Soc Rev 41: 5416–5429.
- 172Reeves EP, Mcdermott JM и Seewald JS (2014) Происхождение метантиола в гидротермальных флюидах срединно-океанического хребта. Proc Natl Acad Sci U S A 111, 5474– 5479.
- 173Ragsdale SW и Pierce E (2008) Ацетогенез и путь Вуд-Люнгдал фиксации CO 2 . Biochim Biophys Acta 1784, 1873–1898.
Роль воды в биоматериалах
Исследование взаимодействия белков плазмы с синтетическими полимерами методом кругового дихроизма
ACS Polym. Prepr., 20 (1) (1979), pp. 581-584
Сравнение эмпирических силовых полей белков для моделирования адсорбционного поведения структурированных пептидов LK на функционализированных поверхностях
Biointerphases, 7 (1) (2012), pp. 1-19
Гемосовместимость: влияние структурированной воды
Пер. Являюсь. Soc. Артиф. Междунар. Органы, 26 (1980), стр. 294-298
Соответствие окружающей среде
The Macmillan Company, New York, NY (1913)
Адсорбция воды и смачивание металла поверхности
Surf. Sci. Rep., 64 (9) (2009), pp. 381-451
Взаимодействие гидрофобной и гидрофильной личности -собранные монослои с водой по данным спектроскопии генерации суммарной частоты
Chem.Phys. Lett., 494 (4–6) (2010), pp. 193-197
Vmd — визуальная молекулярная динамика
J. Mol. Graph., 14 (1) (1996), pp. 33-38
Вода и гидрогели
J. Biomed. Матер. Res., 7 (1973), pp. 509-522
Кластеры воды: разгадывая загадки жидкости, по одной молекуле за раз
Proc.Natl. Акад. Sci., 98 (19) (2001), pp. 10533-10540
Роль воды H- дисбаланс связей в переходах субстрата B-ДНК и распознавание пептидов, выявленное с помощью FTIR-спектроскопии с временным разрешением
J. Am. Chem. Soc., 133 (15) (2011), стр. 5834-5842
Исследование дискретной и континуальной моделей поведения воды в гидрогелевых контактных линзах
Eye Contact Lens, 31 (6) (2005), стр.270-278
Влияние ионов на структуру воды: создание и разрушение структуры
Chem. Rev., 109 (2009), pp. 1346-1370
Специфические ионные эффекты на структуру и динамику воды за пределами первой гидратной оболочки
Angew. Chem., 50 (2) (2011), стр. 352-353
Структурные изменения воды в гидрогеле во время дегидратации
J. Chem. Phys., 130 (3) (2009), с. 034501
Унифицированное описание температурно-зависимых перегруппировок водородных связей в жидкой воде
Proc. Natl. Акад. Sci. США A, 102 (40) (2005), стр. 14171-14174
Влияние структуры воды на совместимость с кровью: термический анализ воды в поли (мет) акрилате
J. Biomed. Матер. Res., 68A (2004), стр. 684-695
Гидрофобный эффект и организация живого вещества
Science, 200 (4345) (1978), стр. 1012-1018
О роли молекул воды на границе раздела биологических систем и полимеров
J.Биоматер. Sci. Polym. Ed., 21 (14) (2010), pp. 1831-1848
Гидрофобный эффект
Phys. Chem. Chem. Phys., 5 (15) (2003), с. 3085
Химия анионов и осмолитов Гофмайстера
Annu. Rev. Phys. Chem., 61 (1) (2010), стр. 63-83
Произошла ошибка при настройке вашего пользовательского файла cookie
Этот сайт использует файлы cookie для повышения производительности.Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт.
Настройка вашего браузера для приема файлов cookie
Существует множество причин, по которым cookie не может быть установлен правильно. Ниже приведены наиболее частые причины:
- В вашем браузере отключены файлы cookie. Вам необходимо сбросить настройки своего браузера, чтобы он принимал файлы cookie, или чтобы спросить вас, хотите ли вы принимать файлы cookie.
- Ваш браузер спрашивает вас, хотите ли вы принимать файлы cookie, и вы отказались.Чтобы принять файлы cookie с этого сайта, нажмите кнопку «Назад» и примите файлы cookie.
- Ваш браузер не поддерживает файлы cookie. Если вы подозреваете это, попробуйте другой браузер.
- Дата на вашем компьютере в прошлом. Если часы вашего компьютера показывают дату до 1 января 1970 г., браузер автоматически забудет файл cookie. Чтобы исправить это, установите правильное время и дату на своем компьютере.
- Вы установили приложение, которое отслеживает или блокирует установку файлов cookie.Вы должны отключить приложение при входе в систему или проконсультироваться с системным администратором.
Почему этому сайту требуются файлы cookie?
Этот сайт использует файлы cookie для повышения производительности, запоминая, что вы вошли в систему, когда переходите со страницы на страницу. Чтобы предоставить доступ без файлов cookie потребует, чтобы сайт создавал новый сеанс для каждой посещаемой страницы, что замедляет работу системы до неприемлемого уровня.
Что сохраняется в файле cookie?
Этот сайт не хранит ничего, кроме автоматически сгенерированного идентификатора сеанса в cookie; никакая другая информация не фиксируется.
Как правило, в cookie-файлах может храниться только информация, которую вы предоставляете, или выбор, который вы делаете при посещении веб-сайта. Например, сайт не может определить ваше имя электронной почты, пока вы не введете его. Разрешение веб-сайту создавать файлы cookie не дает этому или любому другому сайту доступа к остальной части вашего компьютера, и только сайт, который создал файл cookie, может его прочитать.
Роль воды во взаимодействии хозяина и гостя
Коллективные переменные от флуктуаций равновесия с Deep-LDA
В этой работе нас в основном интересует вычисление разности свободной энергии Δ G между связанным состоянием (B), в котором лиганд находится в самой позе связывания свободной энергии и в несвязанном состоянии (U), когда лиганд сольватирован в воде и может свободно диффундировать.Чтобы получить резюме, способное фиксировать поведение воды, мы используем недавно разработанный метод машинного обучения Deep-LDA 29 .
Deep-LDA — это нелинейная эволюция проверенного временем метода классификации линейного дискриминантного анализа (LDA) 37 . В LDA берется два набора данных, в нашем случае конфигурации, посещенные в коротких несмещенных симуляциях в B и U, и определяется набор из N d дескрипторов d , которые могут различать эти два.Цель LDA — найти линейную комбинацию дескрипторов s = w T d , которая лучше всего разделяет два набора данных, w — это N d — размерный вектор. {\ mathrm {T}} \). w , которое максимизирует это соотношение, является направлением, которое оптимально различает два состояния и дает наилучшую разделенную проекцию данных в одномерном пространстве s . Было показано, что полученная таким образом переменная хорошо работает как CV во многих случаях, особенно если использовать ее вариант Harmonic LDA 38,39 .
В Deep-LDA применяется аналогичная парадигма с тем ключевым отличием, что LDA выполняется при нелинейном преобразовании дескрипторов.Нелинейность вводится нейронной сетью (см. Рис. 2), входом которой является набор из N d дескрипторов d , а на выходе — N h компонентов последнего скрытый слой h . LDA выполняется для компонентов h , так что после определения соответствующих S w и S b , NN оптимизируется с использованием \ ({\ mathcal {J}} ({\ boldsymbol {w}}) \) как функция потерь.{\ mathrm {T}} {{{\ mathbf {h}}}}. $$
(2)
Рис. 2: Схема архитектуры Deep-LDA, используемой в этой работе.Дескрипторы d подаются в NN, который генерирует s как линейную комбинацию последнего скрытого слоя NN h и собственного вектора LDA w . CV Deep-LDA тогда составляет с w = с + с 3 .
Deep-LDA — это мощный классификатор, который стремится сжимать данные до очень четких распределений, которые не подходят для расширенных приложений выборки.Чтобы решить эту проблему, мы сглаживаем распределения, применяя следующее кубическое преобразование s w = s + s 3 , в духе того, что было сделано в исх. 40 . Полученная таким образом CV будет использоваться для описания поведения воды в наших моделированиях.
Включение воды в модель
Выбор дескрипторов d имеет первостепенное значение, поскольку подразумевает физику, которую мы хотим описать.В нашем случае нас интересует роль воды в процессе связывания. Для этого мы выбираем два набора точек, вокруг которых вычисляем координационное число воды. Один набор расположен на лиганде, а другой фиксируется вдоль оси хозяина z через равные промежутки времени (см. Рис. 1 и дополнительные методы).
Первый набор координационных чисел {L i } описывает водную сольватацию вокруг лиганда и по духу аналогичен переменным сольватации лиганда, которые использовались в прошлом 5,28 .Второй {V i } вместо этого нацелен на захват водной структуры внутри и снаружи связывающего кармана без какой-либо явной ссылки на лиганд. Важно, чтобы дескрипторы захватывали все молекулы воды, которые способствуют сольватации хозяина и гостя. Отсутствие некоторых из них создало бы неполную картину сольватации, что, в свою очередь, привело бы к ошибкам классификации Deep-LDA и неэффективной систематической ошибке.
Набор дескрипторов {L i , V i } дает информацию о структуре воды и ее нелокальных изменениях в малом и среднем масштабе во время процесса связывания-развязывания.Его эффективность заключается не в индивидуальном действии каждого дескриптора, а в его коллективной способности улавливать согласованные движения множества тел хозяина, гостя и молекул воды. Использование этих дескрипторов — один из элементов новизны нашего подхода и один из ключей к его успеху.
Связывание свободных энергий из расширенного моделирования выборки
Мы выполняем моделирование OPES для оценки свободных энергий связывания всех шести лигандов на рис. 1. Мы используем Deep-LDA CV s w вместе со вторым CV s z , которая представляет собой проекцию центра масс лиганда на ось связывания z .В контексте связывания лиганда использование последнего является естественным выбором 5,36 , поскольку он имеет четкую физическую интерпретацию и помогает отличить B от U. Кроме того, мы используем воронкообразный потенциал сдерживания 4 , чтобы стимулировать лиганд, чтобы найти свой путь обратно к сайту связывания, как только он окажется в растворе. Энтропийная поправка к свободной энергии из-за ограничения воронки может быть вычислена аналитически (см. Уравнение 4 в дополнительных методах) и принимается во внимание при вычислении свободных энергий связи Δ G .Мы отсылаем заинтересованного читателя к дополнительным методам для получения более подробной информации.
Комбинированное использование этих двух CV приводит к эффективной выборке, что отражается в большом количестве событий связывания-развязывания в единицу времени (см., Например, дополнительный рис. 18). Мы заметили явное улучшение по сравнению с более стандартным набором CV 36 , а именно s z , и косинус угла θ между осью связывания z и ориентацией лиганда (см. Инжир.17). Введение CV на водной основе в расширенное моделирование выборки позволяет системе достичь режима, при котором она без гистерезиса диффундирует из одного метастабильного состояния в другое, обеспечивая высокую точность оценки средних по ансамблю физических величин. Это позволяет значительно уменьшить планки ошибок без увеличения времени вычислений по сравнению с тем, что указано в литературе 34 .
Выполнение расширенного моделирования выборки позволяет получить равновесное распределение P ( с ) любой коллективной переменной с 14 .Здесь мы сосредоточимся на поверхности свободной энергии (FES), определяемой как \ ({\ rm {FES}} (s) = — {k} _ {{\ rm {B}}} T \, \ mathrm {log} \ , P (s) \), где k B — постоянная Больцмана, а T — температура системы. В контексте связывания лиганда обычно рассматривают FES как функцию расстояния хозяин-гость s z . Для каждого из шести лигандов мы вычисляем FES и оцениваем ошибки с помощью анализа среднего по блоку. Эти результаты представлены на рис.3, в котором мы также оцениваем надежность CV Deep-LDA, показывая результаты, соответствующие трем различным раундам обучения Deep-LDA.
Рис. 3: Поверхности свободной энергии в проекции на расстояние хозяин-гость.Для каждого из шести лигандов мы вычисляем свободную энергию по переменной s z , используя стандартную формулу повторного взвешивания, подобную зонтичной выборке, чтобы восстановить несмещенное распределение 13 . Заштрихованные области указывают на ошибки, расчет которых подробно описан в дополнительных методах.{c} \), а соответствующие FES обозначены соответственно штриховыми, пунктирными и штрих-пунктирными линиями. Для ясности кривые, относящиеся к одному и тому же лиганду, но с разными CV, сдвинуты на 1 ккал моль -1 , тогда как сдвиг между кривыми разных лигандов составляет 5 ккал моль -1 .
Затем мы приводим значения свободной энергии связи Δ G с поправкой на наличие воронки в таблице 1. На рис. 4 мы сравниваем их с экспериментальными значениями и теоретическими расчетами, выполненными на той же модели, но с разными методами отбора проб. 35,36 .Мы оцениваем качество наших оценок с помощью показателей, используемых в обзорной статье SAMPL5 32 , и получаем среднеквадратичную ошибку 0,68 ккал моль -1 , коэффициент детерминации Пирсона 0,93, наклон линейной регрессии 1,21 и коэффициент корреляции Кендалла 0,87. За некоторыми исключениями, мы соответствуем результатам SAMPL5 (см. Рис. 4 и дополнительные таблицы 1 и 2). Однако шкала ошибок значительно снижается по всему набору исследованных лигандов.
Таблица 1 Связанные свободные энергии. Рис. 4: Сравнение свободных энергий связи с экспериментами и другими расчетами.В и мы наносим на график значение Δ G , полученное в результате моделирования Deep-LDA (синие крестики) для каждого лиганда, в сравнении с экспериментальными значениями и показываем соответствующую линейную аппроксимацию. В b мы сообщаем об их различии с экспериментальными значениями и сравниваем их с другими результатами расчетов, выполненными с использованием той же установки моделирования.Результаты из исх. 36 обозначены красными кружками, из исх. 34 с зелеными бриллиантами, а от исх. 35 в желтых квадратах.
Чтобы проверить общность нашей процедуры, мы исследуем взаимодействие шести лигандов с хозяином OAH, также изученным в тесте SAMPL5. Результаты согласуются с данными, приведенными в исх. 34,35,36 и на дополнительных рисунках. 31–57 и Таблицы 9–16 мы предоставляем полный отчет. В качестве дополнительной проверки нашего метода и роли воды мы также выполняем моделирование OAMe хозяина с шестью лигандами, используя модель воды TIP4P / EW 41 вместо модели TIP3P 42 .Хотя процесс связывания / развязывания не изменился, мы обнаружили, что свободные энергии связывания зависят от выбранной модели воды. По модулю сдвига примерно 1,3 ккал / моль -1 , два набора результатов достаточно хорошо коррелируют друг с другом и с экспериментами. Для количественной оценки этих утверждений см. Дополнительные рис. 59–78 и таблицы 19–26. Причина этого изменения может быть связана с различной растворимостью лиганда в двух водных моделях и с различным взаимодействием хозяин-вода.
Случай G4
Использование Deep-LDA CV s w позволяет нам получить не только точные значения свободной энергии связывания, но и детальное представление о поведении воды в процессе связывания. Мы проиллюстрируем здесь случай с G4, гостем, который демонстрирует наиболее сложное поведение, и отсылаем заинтересованного читателя к дополнительным рис. 5–30 и таблицы. 3–8 для подробного анализа всех остальных лигандов.
На рис. 5 показаны ФЭС G4 и цилиндрически усредненная плотность воды в метастабильных состояниях.Мы обнаруживаем, что система представляет две связывающие позы B и B1. Самая низкая поза связывания свободной энергии B такая же, как и найденная в экспериментах, и не содержит воды. Наше моделирование обнаружило вторую позу связывания B1, которая отличается от B наличием молекулы воды в центре полости. Эта вторая поза на ≈ 2 k B T выше по свободной энергии, и поэтому она занята с гораздо меньшей вероятностью.
Рис. 5: Связывание FES лиганда G4 с исследованием присутствия воды в посещенных состояниях.Мы показываем двумерный FES лиганда G4 относительно s z и Deep-LDA CV s w . Различные соседние цвета соответствуют разнице свободной энергии 1 k B T ≈ 0,6 ккал моль −1 . Мы выделяем некоторые соответствующие состояния, в которых мы проводим простое моделирование молекулярной динамики (МД) для измерения присутствия воды. Приведены гистограммы плотности атомов кислорода воды в цилиндрических координатах z , r .Каждая гистограмма нормализована значением плотности в верхнем правом углу, а более темные цвета соответствуют областям с более высокой плотностью воды. Положение лиганда на этих графиках является иллюстративным.
Когда лиганд выходит из кармана, до того, как он полностью сольватируется, он может пройти через два промежуточных короткоживущих состояния I и I1. В I полость сухая, и лиганд может свободно вращаться перед входом в полость. В I1 лиганд снова находится перед входом в хозяин, но его вращение способствует конфигурациям, в которых атом брома лиганда направлен в сторону полости, образуя линейное расположение, где вода в центре полости соединяется другой водой с Br . — анион (см. Дополнительный рис.21). Мы подчеркиваем, что ни B1, ни я, ни I1 не участвовали в обучении Deep-LDA.
Способность Deep-LDA CV s w улавливать нелокальные структурные изменения воды является основной причиной нашей способности изучать FES системы и ее метастабильные состояния на этом уровне детализации. Например, использование CV, которые концентрируются исключительно на положении лиганда относительно сайта связывания, такого как s z отдельно, явно приведет к неполной картине.Фактически, B и B1 (и аналогично I и I1) не могут быть правильно различены с помощью s z , и без наличия смещения, изменяющего сольватацию полости, ограничивающей шкалой времени моделирования было бы движение воды. в и из кармана. Более того, локальные CV, которые описывают только среднюю сольватацию лиганда, могут лишь частично учитывать эти нелокальные эффекты.
Анализ роли воды
Мы можем получить более глубокое представление о роли воды, исследуя зависимость Deep-LDA CV от дескрипторов {L i , V i }.Это можно сделать, проанализировав релевантность дескрипторов в действии s w , и для этого мы используем метод производного ранжирования, проиллюстрированный в исх. 29 . Здесь мы разделяем роль дескрипторов в связанных и несвязанных состояниях и сообщаем результаты для лиганда G4 на фиг. 6 (см. Дополнительный рисунок 22 для анализа всех метастабильных состояний G4).
Рис. 6. Относительные веса дескрипторов для гостя G4.В соответствии с рейтингом на основе производных финансовых инструментов исх. 29 , мы показываем относительный вес, который имеет каждый дескриптор в Deep-LDA CV в связанном и несвязанном состояниях гостевого G4. Мы показываем средний вес по трем различным CV Deep-LDA, которые мы тренировали. Дескрипторы V 1 , V 2 , которые измеряют количество молекул внутри кармана, очерчены, чтобы отметить значительное изменение их вклада между двумя состояниями.
В обоих состояниях B и U веса распределяются по широкому диапазону дескрипторов, указывая на тот факт, что Deep-LDA CV способен улавливать сложное нелокальное действие воды.Однако разные дескрипторы по-разному действуют в двух состояниях. В состоянии B дескрипторы V 4 , V 5 , которые связаны с молекулами воды, находящимися в непосредственной близости от входа в хозяин, имеют больший вес. Это указывает на то, что колебания в этой части водной системы должны быть усилены для выхода лиганда.
Напротив, в состоянии U дескрипторы, которые приобретают больший вес, — это L 4 , который измеряет сольватацию вокруг атома брома лиганда, и V 1 , V 2 , которые контролируют количество вода, содержащаяся в полости для связывания.Для связывания лиганда должны происходить колебания в сторону сухого состояния полости. Такие флуктуации могут происходить с небольшой, но не маловероятной вероятностью также в голосостоянии (см. Дополнительный рис. 2). Еще большие флуктуации наблюдались экспериментально в работе [5]. 33 в связанной системе. Мы ожидаем, что эти колебания будут важной частью процесса реакции во многих системах хост-гость.
Нелокальное действие Deep-LDA CV, таким образом, отражается в релевантности, данной различным дескрипторам на основе воды, в зависимости от того, находится ли система в связанном или несвязанном состоянии.При увеличении выборки этого CV эта нелокальность определяет коллективное движение воды, которое способствует возникновению событий связывания / развязывания.
Местные органы власти играют важную роль в защите качества воды: Часть 1
Государственные и федеральные постановления помогают защищать водные ресурсы, но не выполняют всю работу. Местное самоуправление также играет важную роль — часто превентивную функцию.
Местные органы власти играют очень важную роль в защите поверхностных и грунтовых вод, питьевой воды и водно-болотных угодий, часто заполняя пробелы в государственных и федеральных постановлениях.Если местное самоуправление не сделает этого с местным зонированием, эти пробелы могут не быть устранены. Существуют различные законы штата и федеральные законы, направленные на защиту качества воды. Но полагаться только на законы штата нельзя.
“. . . на государственном уровне [законов] недостаточно; они, как правило, притупляют, но не останавливают деградацию берега, и защищают не целые экосистемы, а только ресурсы, находящиеся на определенных участках »согласно Заполнение пробелов: варианты защиты окружающей среды для местных органов власти (Кэтрин А.Ardizone et al. , Департамент качества окружающей среды штата Мичиган, 2003 г.).
Органы местного самоуправления профилактические с зонированием; характеристика зонирования, которая не всегда содержится в государственных законах. Часто законы штата сосредотачиваются только на одной посылке или являются реакцией на уже возникшую проблему. Кроме того, в книге Заполняя пробелы перечислено, какие аспекты защиты окружающей среды не регулируются на федеральном уровне и уровне штата, а также пробелы в этих нормах, указывая на важную роль местных органов власти.
Ни один уровень правительства не может быть эффективным сам по себе. Это требует совместных усилий. Один из способов визуализировать это — расположить в центре местные органы власти, а в кругу вокруг них находятся государственные и федеральные программы регулирования окружающей среды, группы водоразделов и землевладельцы.
Однако есть два предостережения в отношении участия местных властей в охране водных ресурсов. Во-первых, чтобы быть наиболее эффективным, нужно решать проблему в той же географии, что и рассматриваемая тема.Это означает, что местные органы власти должны координировать свои действия и объединяться для защиты такого ресурса, как вода, чтобы действия охватывали весь водораздел или водосборник подземных вод. В противном случае он выполняет только часть работы.
Во-вторых, в ледниковой геологии Мичигана подземные воды, поверхностные воды (озера и ручьи) и водно-болотные угодья взаимосвязаны. Это означает, что вода (и загрязнители в этой воде) перемещаются туда и обратно между всеми тремя: заболоченными территориями, поверхностными и грунтовыми водами. Таким образом, местный подход должен учитывать все три.В противном случае человек выполняет только часть работы.
Предотвращение загрязнения подземных вод посредством зонирования часто осуществляется с помощью стандартов обзора плана участка в постановлении о зонировании, ресурсе, разработанном Расширением Мичиганского государственного университета, который требует вторичной локализации и ограничения использования сухих колодцев. Предотвращение загрязнения питьевой воды / подземных вод также является частью программы защиты устьев скважин штата Мичиган. Это упреждающая попытка определить исторические и существующие возможные источники загрязнения в районе общественной водозаборной скважины, чтобы сообщество могло отслеживать эти проблемы.Кроме того, община использует зонирование, противопожарные инспекции и другие стимулы, чтобы предотвратить загрязнение в будущем в районе колодца. Эти стратегические мероприятия изложены в местном плане защиты устья скважины.
Упреждающая защита водно-болотных угодий и поверхностных вод (озер, рек) часто является проблемой, связанной с обращением с береговой линией: отступами, поясами / буферами растительности и плотностью застройки (размер участка и непроницаемая поверхность). Какой размер растительного пояса и насколько велико отступление, будет определяться в первую очередь домашним заданием.Это будет зависеть от того, какова цель, от того, какую проблему вы пытаетесь решить. Это будет зависеть от результатов просмотра первичной информации о размере и форме озера в районе (морфологии), типах почв (веб-исследование почвы), уклонах, информации о наводнениях и данных из Системы управления информацией о поверхностных водах штата Мичиган. Этот тип информации может быть получен из таких мест, как агентства регионального планирования, данные окружной географической информационной системы (ГИС), государственные агентства, районы охраны почв и центры водоразделов.
Стандарты, используемые или принятые в постановление о зонировании, должны основываться на этом домашнем задании и соответствовать обоснованным научным стандартам и будут зависеть от целей. Например, целью может быть защита воды от питательных веществ и других стоков. Или цели могут заключаться в защите эстетики ресурса или в защите естественной среды обитания. В зависимости от того, чего вы пытаетесь достичь, появятся разные стандарты.
Один из примеров набора стандартов был представлен в серии семинаров МГУ по расширению береговой линии в 2015 году:
Минимальные стандарты прибрежной зоны для озера с канализационной системой (Департамент природных ресурсов Миннесоты)
Класс озера | Lakeshore | Без берега озера | ||||
Ширина лота | Площадь участка | Снижение конструкции | Береговая зона воздействия | Ширина лота | Площадь участка | |
Природный экологический | 125 футов | 40 000 квадратных футов | 150 футов | 75 футов | 125 футов | 20000 квадратных футов |
Рекреационный девелопмент | 75 футов | 29000 квадратных футов | 75 футов | 37.5 футов | 75 футов | 15000 квадратных футов |
Общее развитие | 74 футов | 15000 квадратных футов | 50 футов | 25 футов | 75 футов | 10 000 квадратных футов |
Минимальные стандарты прибрежной зоны для озера без канализации (Департамент природных ресурсов Миннесоты)
Класс озера | Lakeshore | Без берега озера | ||||
Ширина лота | Площадь участка | Снижение конструкции | Береговая зона воздействия | Ширина лота | Площадь участка | |
Природный экологический | 200 футов | 80000 квадратных футов | 150 футов | 75 футов | 200 футов | 80000 квадратных футов |
Рекреационный девелопмент | 150 футов | 40 000 квадратных футов | 100 футов | 50 футов | 150 футов | 45000 квадратных футов |
Общее развитие | 100 футов | 20000 квадратных футов | 75 футов | 37.5 футов | 150 футов | 40 000 квадратных футов |
Другой способ взглянуть на это — изучить различные нормативные акты, основанные на том, является ли их целью защита качества воды, эстетика или защита среды обитания. Приведенная ниже таблица была разработана на основе пилотного проекта GEM в округе Манисти в 1995 году. Она основана на интенсивном объеме исследований, проведенных Институтом исследований водных ресурсов МГУ, и рассматривает почвы округа, литологию колодцев, движение грунтовых вод и различные источники экспертной оценки. исследовательская работа.Эти цифры относятся к озерам, рекам и водно-болотным угодьям.
Защита качества воды от биогенных веществ, стоков | Защита территорий, вызывающих особую озабоченность: нетронутые реки, места обитания рыб, особые и уникальные природные условия. | Охрана среды обитания, экологических коридоров | |
Буферная полоса (без или с минимальным использованием удобрений | от 5 до 10 футов | 20 футов (Отчет Лейкленда № 12) (с фильтром) | От 33 до 400 футов (птицы) 97 футов (избегать ударов при лесозаготовках) Достаточно, чтобы река оставалась в тени (рыба) |
Минимальный размер посылки: нет общественной канализации | 15000 квадратных футов | 40 000 квадратных футов | 80000 квадратных футов |
Минимальный размер участка: водопровод и канализация | 12000 квадратных футов | 29000 квадратных футов | 40 000 квадратных футов |
Минимальная ширина участка на набережной | 100 футов | 100-300 футов | 150-300 футов |
Откат для построек и непроницаемых поверхностей | 50 футов от поверхности воды или края заболоченного участка | 50 футов от берега края буфера | 50 футов от берега края буфера |
Устранение источников питательных веществ и бактерий (дренажное поле, хранилище навоза, компостная куча) (Запретить использование сухого колодца или аналогичного устройства) | 100 футов от поверхности воды или края заболоченного участка | 100 футов от поверхности воды или края заболоченного участка | 100 футов от поверхности воды или края заболоченного участка |
Устранение источников питательных веществ и бактерий (дренажное поле, хранилище навоза, компостная куча) (Запретить использование сухого колодца или аналогичного устройства) | 100 футов от поверхности воды или края заболоченного участка | 100 футов от поверхности воды или края заболоченного участка | 100 футов от поверхности воды или края заболоченного участка |
Дело в том, что используемые стандарты будут зависеть от целей и задач, а также исходных исходных данных.Эта информация будет включена в генеральный план сообщества. Участие общественности в принятии генерального плана также поможет определить, что будет политически приемлемым, и определить ограничения, которые могут наложить существующие разработки.
В результате более практичным идеалом может быть следующее:
- 50-футовое отступление от уреза воды
- Отступление 100-футового септика и других источников питательных веществ от кромки воды
- Буферная полоса 35–50 футов (Биологическая станция UofM или Совет водораздела Митта) (комбинация местных деревьев и кустарников: удаление невозможно, кроме мертвых, больных, инвазивных; ограниченная обрезка и удаление для просмотра; ограничения на использование пестицидов и удобрений)
- Изменение береговой линии на 25% или менее
- 10% непроницаемая поверхность в пределах 500 футов от береговой линии (стандарт для почв: 10-40%)
Вы нашли эту статью полезной?
Расскажите, пожалуйста, почему
Представлять на рассмотрение . В этой же таблице можно увидеть информацию о самом важном веществе в жизни всех живых существ – это кислород.
В этой же таблице можно увидеть информацию о самом важном веществе в жизни всех живых существ – это кислород.