Сокращение потребления соли
Наращивание производства пищевых продуктов все более глубокой переработки, быстрая урбанизация и изменение образа жизни меняют тенденции в области питания. Доступность и ценовая приемлемость продуктов, прошедших глубокую технологическую переработку, повышаются. Во всем мире население потребляет все больше высококалорийной пищи со значительным содержанием насыщенных жиров, трансжиров, сахаров и соли. Соль является основным источником натрия, при этом установлена связь между повышенным потреблением натрия и гипертонией, а также увеличением риска сердечно-сосудистых заболеваний и инсульта.
Одновременно, по мере отхода от привычных схем питания снижается потребление ключевых составляющих здорового рациона — фруктов, овощей и пищевых волокон (в частности, цельных злаков). Фрукты и овощи содержат калий, способствующий снижению кровяного давления.
Роль переработанных пищевых продуктов как источника соли в рационе объясняется тем, что содержание соли в них особенно высоко (в случае готовых блюд, мясопродуктов, таких как бекон, ветчина и сырокопченая колбаса, сыров, соленых снеков, лапши быстрого
приготовления и т.
Вместе с тем многие производители меняют рецептуру своей продукции для сокращения содержания соли, и потребителям рекомендуется обращать внимание на этикетки продуктов и выбирать продукты с низким содержанием натрия.
Рекомендации по снижению потребления соли
- Взрослые. ВОЗ рекомендует взрослым потреблять менее 5 г соли в день (чуть меньше одной чайной ложки) (1).
- Дети. Для детей в возрасте от двух до 15 лет ВОЗ рекомендует корректировать рекомендованное максимальное потребление соли в сторону уменьшения исходя из их потребностей в энергии по сравнению с взрослыми. Эта рекомендация в отношении детей не
охватывает период исключительно грудного вскармливания (0–6 месяцев) или период прикорма при продолжающемся грудном вскармливании (6–24 месяца).

- Вся потребляемая соль должна быть йодированной, т.е. обогащенной йодом, который имеет важнейшее значение для здорового развития головного мозга у плода и у детей младшего возраста и общего укрепления психических функций у всех людей.
Информация о соли, натрии и калии
- Натрий является важнейшим биогенным элементом, необходимым для поддержания объема плазмы крови и водно-щелочного баланса, передачи нервных импульсов и нормального функционирования клеток.
- Избыток натрия сопровождается негативными последствиями для здоровья, в том числе повышением кровяного давления.
- Основные источники потребления натрия в пище определяются культурными особенностями и кулинарными предпочтениями населения.
- Натрий естественным образом содержится в целом ряде продуктов питания, таких как молоко, мясо и морепродукты. Он нередко встречается в большом количестве в переработанных пищевых продуктах, таких как хлебобулочные изделия, мясопродукты и снеки, а
также во вкусовых добавках к пище (например, соевом и рыбном соусах).

- Натрий содержится также в глутамате натрия, который используется в качестве пищевой добавки во многих регионах мира.
- Калий — важнейший микроэлемент, необходимый для поддержания общего объема жидкостей в организме, кислотного и водно-электролитного баланса и нормального функционирования клеток.
- Калий содержится в самых разнообразных необработанных пищевых продуктах, особенно фруктах и овощах.
- Установлено, что увеличение потребления калия снижает систолическое и диастолическое давление у взрослых людей.
Как сократить потребление соли с продуктами питания
Государственная политика и стратегии должны обеспечивать создание условий, позволяющих населению потреблять достаточное количество безопасных и питательных продуктов, составляющих основу здорового рациона, к которым относятся продукты с низким содержанием
соли. Оздоровление привычек в области питания является обязанностью не только общества, но и каждого человека. Эта задача должна решаться с учетом характеристик и культурных особенностей населения и с участием целого ряда секторов.
Можно выделить следующие ключевые стратегии общего характера по сокращению потребления соли:
- политика государства, в том числе надлежащая налоговая политика и регулирование, обеспечивающие поставку производителями и розничными предприятиями более здоровых продуктов питания и расширение ассортимента доступной и недорогой здоровой пищевой продукции;
- взаимодействие с частным сектором для обеспечения поставок и повышения доступности продуктов с низким содержанием соли;
- информирование и расширение прав и возможностей потребителей методами социального маркетинга и мобилизации для повышения их осведомленности о необходимости сокращать потребление соли;
- создание благоприятных предпосылок для сокращения потребления соли за счет инициатив в области местной политики и содействие формированию «сред здорового питания», в частности на уровне школ, общин и городов;
- мониторинг потребления соли населением, источников соли в рационе питания, а также уровня осведомленности, установок и поведения людей в отношении этой проблемы для учета полученных данных при принятии решений о мерах политики.

Потребление соли дома можно сократить, если:
- не солить блюда во время их приготовления;
- не держать на обеденном столе солонку;
- ограничить потребление соленых снеков;
- выбирать продукты с низким содержанием натрия.
Сокращению потребления соли способствует целый ряд других практических мер местного уровня:
- включение вопросов сокращения потребления соли в программы обучения работников пищевой промышленности и общественного питания;
- изъятие солонок и соевого соуса со столов на предприятиях общественного питания; размещение уведомлений о том, что определенная продукция содержит много натрия на упаковке или на полках магазинов;
- предоставление специальных рекомендаций в отношении питания посетителям учреждений здравоохранения;
- разъяснительная работа о необходимости сокращения потребления соли и ограниченном ее использовании при приготовлении пищи;
- разъяснительная работа с детьми и создание для детей обстановки, способствующей формированию у них привычки к низкосолевому рациону уже в молодом возрасте.

Действия пищевой промышленности должны включать в себя:
- постепенное сокращение содержания соли в продукции с течением времени, с тем чтобы потребители привыкли к ее вкусу постепенно, не переходя на альтернативную продукцию;
- пропаганду преимуществ употребления продуктов питания с пониженным содержанием соли в рамках информационных мероприятий для потребителей на предприятиях общественного питания и в магазинах;
- сокращение содержания соли в пищевых продуктах и блюдах, предлагаемых ресторанами и службами питания, и указание содержания натрия в них.
Заблуждения о сокращении потребления соли
- «В жаркий и влажный день человек потеет, и в его пище должно быть больше соли». Потея, организм теряет совсем немного соли, поэтому даже в условиях жары и высокой влажности лишняя соль не нужна; однако важное значение имеет обильное питье.
- Морская соль не «полезнее» промышленно произведенной лишь потому, что «создана природой».
 Независимо от происхождения соли, негативные последствия для здоровья вызывает содержащийся в ней натрий.
Независимо от происхождения соли, негативные последствия для здоровья вызывает содержащийся в ней натрий. - Добавление соли при приготовлении пищи — не основной источник потребляемой соли. Во многих странах примерно 80% соли в рационе потребляется в составе промышленно переработанных пищевых продуктов.
- Чтобы придать пище приятный вкус, не обязательно использовать соль. Вкусовые рецепторы человека адаптируются не сразу, но, привыкнув к пониженному потреблению соли, он с большей вероятностью будет получать удовольствие от пищи и чувствовать более широкий диапазон вкусов.
- «Пища без соли кажется пресной». Поначалу это может быть и так, однако вскоре вкусовые рецепторы адаптируются к уменьшению содержания соли, и человек привыкает ценить менее соленую, но более выраженную во вкусовом отношении пищу.
- «Пища, в которой много соли, соленая на вкус». Некоторые продукты питания с высоким содержанием соли не имеют выраженного соленого вкуса, потому что он сочетается с другими, маскирующими соленость ингредиентами, например, сахарами.
 Чтобы выяснить содержание натрия в продуктах питания, необходимо обращать внимание на этикетки.
Чтобы выяснить содержание натрия в продуктах питания, необходимо обращать внимание на этикетки. - «Беспокоиться о количестве потребляемой соли стоит только пожилым людям». Избыточное потребление соли может приводить к повышению кровяного давления у лиц любого возраста.
- «Сокращение потребления соли может плохо повлиять на мое здоровье». Потреблять слишком мало соли очень трудно, потому что она содержится в большом количестве повседневных продуктов питания.
Деятельность ВОЗ
В руководствах ВОЗ о потреблении натрия и калия определены предельные значения их потребления без ущерба для здоровья. В руководствах также описываются меры по оздоровлению питания и профилактике НИЗ у взрослых и детей.
В 2004 г. Всемирная ассамблея здравоохранения приняла Глобальную стратегию по питанию, физической активности и здоровью. Она содержит призыв к правительствам, ВОЗ, международным партнерам, частному сектору и гражданскому обществу принимать меры в
поддержку здорового питания и физической активности на глобальном, региональном и местном уровнях.
В 2010 г. Всемирная ассамблея здравоохранения одобрила свод рекомендаций в отношении маркетинга продуктов питания и безалкогольных напитков, ориентированного на детей. Рекомендации служат странам ориентиром при выработке новых и укреплении существующих мер политики по уменьшению негативных последствий маркетинга вредных для здоровья продуктов питания для детей. ВОЗ также содействует разработке модели профилей питательных веществ, которая может использоваться странами в качестве инструмента при выполнении рекомендаций, касающихся маркетинга.
В 2011 г. мировые лидеры взяли на себя обязательство сокращать негативное воздействие нездорового питания на людей. Данное обязательство было провозглашено в Политической декларации Совещания высокого уровня Генеральной Ассамблеи по профилактике НИЗ и борьбе с ними.
В 2012 г. Всемирная ассамблея здравоохранения утвердила шесть глобальных целей в области питания, включающих сокращение числа детей, страдающих задержкой роста, истощением и ожирением, повышение показателей грудного вскармливания и уменьшение числа
случаев анемии и низкой массы тела при рождении.
В 2013 г. Всемирная ассамблея здравоохранения согласовала девять глобальных добровольных целей в области профилактики НИЗ и борьбы с ними, которые, в частности, предусматривают прекращение распространения диабета и ожирения, а также сокращение потребления соли на 30% к 2025 г. Глобальный план действий по профилактике неинфекционных заболеваний и борьбе с ними на 2013–2020 гг. содержит руководящие указания и набор вариантов политики для достижения этих целей государствами-членами, ВОЗ и другими учреждениями ООН.
В мае 2014 г., ввиду быстрого роста распространенности ожирения среди младенцев и детей, ВОЗ учредила комиссию по ликвидации детского ожирения. Комиссия подготовила доклад за 2015 г., в котором уточнила, какие подходы и действия с большой вероятностью будут наиболее эффективны в условиях различных стран мира.
(1) Эти рекомендации применимы ко всем лицам, независимо от того, страдают ли они повышенным кровяным давлением (включая беременных и кормящих грудью женщин), за исключением лиц, которые страдают заболеваниями или принимают лекарства, которые могут
приводить к снижению уровня натрия или резкому накоплению воды в организме, либо лиц, нуждающихся в специальной диете под наблюдением врача (например, пациентов с сердечной недостаточностью или диабетом первого типа). Для этих подгрупп населения может
быть установлена специфическая взаимосвязь между потреблением натрия и показателями здоровья (Руководство ВОЗ о потреблении натрия для взрослых и детей, 2012 г.).
Для этих подгрупп населения может
быть установлена специфическая взаимосвязь между потреблением натрия и показателями здоровья (Руководство ВОЗ о потреблении натрия для взрослых и детей, 2012 г.).
Калий биологическая функция — Справочник химика 21
Для нормального роста и вьшолнения биологических функций человеку и животным кроме витаминов необходим также целый ряд неорганических элементов. Эти элементы можно разделить на два класса макроэлементы и микроэлементы. Макроэлементы, к которым относятся кальций, магний, натрий, калий, фосфор, сера и хлор, требуются организму в относительно больших количествах (порядка нескольких граммов в сутки). Часто они выполняют более чем одну функцию. Например, кальций служит структурным компонентом неорганического вещества костей гидроксиапатита, состав которого можно приблизительно описать формулой [Саз (РО гЗз. Вместе [c.294]Макроэлементами в живом веществе являются кислород, водород, углерод, азот, кальций, сера, фосфор, калий, магний, железо, кремний, натрий, хлор и алюминий.
 Их роль в живых организмах различна. Первые десять элементов (их названия выделены в перечне полужирным шрифтом) жизненно необходимы для животных и для растений. Натрий и хлор, безусловно, нужны всем животным и полезны для некоторых видов растений. Биологические функции кремния и алюминия изучены недостаточно. Все макроэлементы живого вещества располагаются в верхней части периодической системы. Большинство из них входит в состав второго и третьего периодов. [c.142]
Их роль в живых организмах различна. Первые десять элементов (их названия выделены в перечне полужирным шрифтом) жизненно необходимы для животных и для растений. Натрий и хлор, безусловно, нужны всем животным и полезны для некоторых видов растений. Биологические функции кремния и алюминия изучены недостаточно. Все макроэлементы живого вещества располагаются в верхней части периодической системы. Большинство из них входит в состав второго и третьего периодов. [c.142] Натрий и калий в живой клетке. Несмотря на большое сходство химических свойств натрия и калия, их биологические функции различны. В плазме клеток велико содержание катионов К+, но относительно мало катионов Ма+, и наоборот, во внеклеточном растворе много Ма+, но мало К+. Концентрация калия внутри клетки превышает концентрацию вне клеток в 10 раз и более. Катион калия связан с внутриклеточной активностью, а катион натрия участвует в процессах на внешней поверхности клетки и эти два катиона не могут заменить друг друга. Катион К+ является важным активатором более чем 60 ферментов внутри клетки. Катион Ма+ не действует на К+-зависимые ферменты. Катион Na+ также активирует несколько ферментов, а К+ не способен их активировать. [c.277]
Катион К+ является важным активатором более чем 60 ферментов внутри клетки. Катион Ма+ не действует на К+-зависимые ферменты. Катион Na+ также активирует несколько ферментов, а К+ не способен их активировать. [c.277]
Утверждение, что калий-натриевый градиент играет роль буфера протонного потенциала, позволяет понять не только биологическую функцию этого градиента, но и причину, которая в течение многих лет препятствовала выяснению его значения для жизнедеятельности клетки. Мысль о буферной роли калий-натриевого градиента не могла родиться, прежде чем был открыт протонный потенциал и было доказано, что он служит конвертируемой формой энергии. Все эти годы проблема калия и натрия просто ждала своего часа. [c.173]
В животных организмах калий необходим для нормальной ра боты мышечных клеток и нервной системы. Нормальный ритм ра боты организма, в частности ритм сокращения сердца, поддержи вается при определенном соотношении концентраций ионов калия и натрия. Оценивая роль ионов калия и натрия в развивающихся системах — клетках и организмах, — приходится констатировать, что не химическое сходство, казалось бы такое очевидное, а довольно тонкие различия между ионами стали основой для того распределения биохимических функций, которое необходимо для действия биологических систем связи и регулирования. [c.153]
Оценивая роль ионов калия и натрия в развивающихся системах — клетках и организмах, — приходится констатировать, что не химическое сходство, казалось бы такое очевидное, а довольно тонкие различия между ионами стали основой для того распределения биохимических функций, которое необходимо для действия биологических систем связи и регулирования. [c.153]
Различная адсорбируемость солей калия и натрия почвенным комплексом привела к разделению ионов ионы натрия оказались в водах морей и океанов, а ионы калия закрепились в почве и, естественно, вошли как важнейший компонент в метаболические процессы растений. Различная способность ионов калия и натрия проходить через биологические мембраны обусловила и специфические функции этих ионов в передаче нервного импульса. [c.153]
Аккумулятивная функция Сущность этой функции заключается в накоплении в форме ГВ важнейших элементов питания живых организмов, органических соединений, несущих энергетические запасы или непосредственно необходимых и усваиваемых микроорганизмами или растениями, а также элементов, не участвующих в биологических процессах Такое накопление происходит не только в почвах, но также в природных водах, донных отложениях, где ГВ служат источниками энергии и питания для биоты Именно в форме ГВ в почвах накапливается до 90% всего азота, половина и более фосфора, серы [451] В этой же форме аккумулируются и сохраняются длительное время калий, кальций, магний, железо и практически все необходимые микроорганизмам микроэлементы В составе ГВ идентифицируются такие элементы, как Н , РЬ, N1, 2п, Си и Аи, которые они очень эффективно сорбируют [c.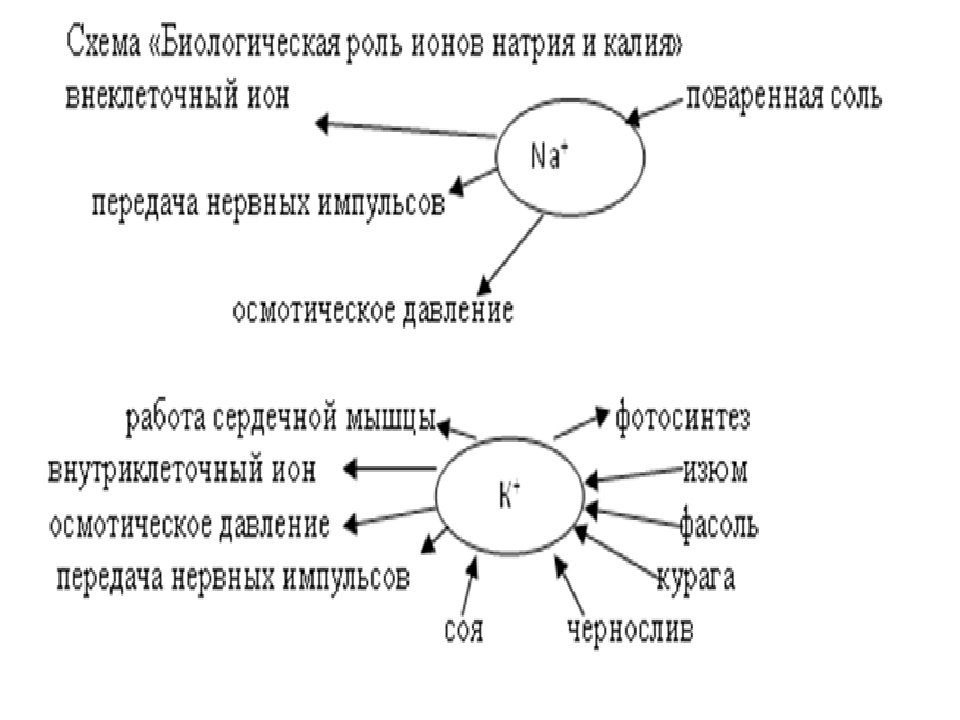 350]
350]
В природе с белками связано относительно небольшое число металлов. Если рассматривать также ферменты, активируемые металлами, то к этому списку элементов следует добавить лишь натрий, калий и магний. Биологическая роль иона металла в белке характеризуется высокой специфичностью. И тем не менее в зависимости от типа белка один и тот же ион металла осуществляет различные функции разнообразие выполняемых функций является, очевидно, следствием ограничений, накладываемых белковым окружением. В связи с этим биологическая специфичность функций металла имеет, по-видимому,- стереохимическую природу. Основная тема обзора — значение структурных и стереохимических данных и сведений о строении координационных центров металл —лиганд для выяснения функциональной роли металлов в ферментативных процессах — не требует, таким образом, дополнительного обоснования. [c.16]
Липиды играют важную биологическую роль они являются источником энергии для животного организма, при окислении в организме 1 г жира выделяется 9,3 кал. Они хорошие растворители биологически активных веществ (например, витаминов), необходимы для осуществления нормальных функций животного организма. Жировая ткань образует мягкую изолирующую прослойку, защищая внутренние органы и все тело от толчков, ударов и переохлаждения. [c.267]
Они хорошие растворители биологически активных веществ (например, витаминов), необходимы для осуществления нормальных функций животного организма. Жировая ткань образует мягкую изолирующую прослойку, защищая внутренние органы и все тело от толчков, ударов и переохлаждения. [c.267]
Важное биологическое значение имеют и некоторые щелочные и щелочноземельные элементы. По сравнению с переходными элементами они связываются менее прочно, и поэтому более легко и свободно перемещаются. Функция натрия и калия в клеточных мембранах связана с нервными импульсами. Магний и кальций участвуют в процессе превращения химической энергии в работу мышц. Определенную функцию в биохимических процессах выполняют и некоторые неметаллы [51]. [c.601]
Остальные из названных выше элементов металлы. Каковы же их функции Какая роль, например, магния, для чего нужны организму калий и натрий, каковы функции ионов кобальта, сделавшие его необходимым для нормальной работы организма Не всегда удается дать исчерпывающие ответы на подобные вопросы. В дальнейшем мы изложим те сведения о роли ионов металлов в ферментных системах, которые могут считаться надежно установленными. Природа экономно использует металлы — их содержание в организмах невелико и ион каждого вида выполняет различные функции. Чаще всего они связаны с усилением действия биологических катализаторов или образованием специфических активных групп катализаторов — металлосодержащих ферментов. Известно, что металлы, как правило, входят в состав организмов в виде комплексных соединений. Так, железо с азотсодержащими веществами образует сложный комплекс — гем. Гем вступает во взаимодействие с белками, и в зависимости от того, с каким белком он соединился, получающееся вещество приобретает различные свойства. В одном случае получается превосходный переносчик кислорода — гемоглобин, в другом — фермент, разлагающий перекись водорода,— каталаза, в третьем — фермент пероксидаза и т. д. [c.10]
В дальнейшем мы изложим те сведения о роли ионов металлов в ферментных системах, которые могут считаться надежно установленными. Природа экономно использует металлы — их содержание в организмах невелико и ион каждого вида выполняет различные функции. Чаще всего они связаны с усилением действия биологических катализаторов или образованием специфических активных групп катализаторов — металлосодержащих ферментов. Известно, что металлы, как правило, входят в состав организмов в виде комплексных соединений. Так, железо с азотсодержащими веществами образует сложный комплекс — гем. Гем вступает во взаимодействие с белками, и в зависимости от того, с каким белком он соединился, получающееся вещество приобретает различные свойства. В одном случае получается превосходный переносчик кислорода — гемоглобин, в другом — фермент, разлагающий перекись водорода,— каталаза, в третьем — фермент пероксидаза и т. д. [c.10]
Ионы кальция, магния, калия и натрия регулируют многие биологические процессы они влияют на функции ферментов и играют роль в передаче нервного возбуждения. Между ними наблюдается антагонизм эффект избыточного количества калия подавляется увеличением концентрации натрия. [c.19]
Между ними наблюдается антагонизм эффект избыточного количества калия подавляется увеличением концентрации натрия. [c.19]
Растворимые соединения бария токсичны. Это объясняется тем, что вследствие близости ионных радиусов Ва + и катион бария может замещать катион калия в биологически активных соединениях, не выполняя его функцию. [c.307]
Спинномозговая жидкость. Функции механическая защита мозга, удаление продуктов метаболизма из мозга, транспорт биологически активных веществ. Общий объем СМЖ — 150 мл, плотность — 1,006—1,008, pH — 7,31, содержание белков — 200—400 мг/л, глюкозы — 2,5-4,44 ммоль/л, натрия — 138-150, калия — 2,7—3,9 ммоль/л. Равновесие между глюкозой крови и глюкозой СМЖ устанавливается за 4 ч. При спинномозговой пункции требуется одновременная оценка уровня глюкозы в крови и СМЖ. Белки проникают в СМЖ из плазмы крови путем пиноцитоза через эндотелий капилляров. [c.457]
В лейкопластах образуются крахмал и некоторые другие вещества клетки. В хромопластах, окрашенных в желтый, красный или оранжевый цвет, накапливаются биологически важные вещества— каротиноиды. Хлоропласты являются органами первичного синтеза углеводов — фотосинтеза. Они устроены очень сложно. Это округлые или овальные тельца, ярко-зеленого цвета, размером в несколько микрометров. Внутри них находятся очень мелкие зерна— граны, окрашенные в ярко-зеленый цвет. Хлоропласты состоят из хлорофилла, белков, липидов, каротиноидов и некоторого количества РНК- Из элементов, кроме магния, входящего в молекулу хлорофилла, в них обнаружены калий, кальций, марганец и др. Главная функция хлоропластов — биосинтез глюкозы, который идет при использовании солнечной энергии. [c.26]
В хромопластах, окрашенных в желтый, красный или оранжевый цвет, накапливаются биологически важные вещества— каротиноиды. Хлоропласты являются органами первичного синтеза углеводов — фотосинтеза. Они устроены очень сложно. Это округлые или овальные тельца, ярко-зеленого цвета, размером в несколько микрометров. Внутри них находятся очень мелкие зерна— граны, окрашенные в ярко-зеленый цвет. Хлоропласты состоят из хлорофилла, белков, липидов, каротиноидов и некоторого количества РНК- Из элементов, кроме магния, входящего в молекулу хлорофилла, в них обнаружены калий, кальций, марганец и др. Главная функция хлоропластов — биосинтез глюкозы, который идет при использовании солнечной энергии. [c.26]
В зависимости от химического состава ПАВ мицеллы могут быть неионными, катионными, анионными или амфотерными. Физические свойства ряда детергентов приведены в табл. 1. Наиболее широко применяемые неионные детергенты содержат полиоксиэти-леновую или полиоксипропиленовую цепь, связанную, как правило, со спиртами или фенолами имеющими длинную углеводородную цепь. К неионным ПАВ относятся также эфиры сахаров, жирные алканоламины, жирные окиси аминов. Все эти вещества довольно трудно получить в виде индивидуальных химических соединений, однако отсутствие ионов в мицеллах, которые они образуют, делает их особенно полезными в качестве детергентов и эмульгаторов и позволяет упростить теоретическое рассмотрение структуры таких мицелл. ККМ неионных ПАВ обычно в 100 раз меньше, чем ККМ ионогенных детергентов, содержащих сравнимые по величине гидрофобные группы. Поэтому масса мицелл неионных детергентов существенно больше, чем масса мицелл ионогенных ПАВ. Анионные детергенты обычно содержат длинную углеводородную цепь и карбоксилатную, сульфатную или сульфонатную группу. В качестве противоионов выступают натрий, калий, литий или водород. Длинноцепочечные четвертичные амины или пиридипы с бромид-, хлорид- или иодид-ионом в качестве противоиона образуют группу катионных ПАВ. Степень нейтрализации заряда противоионами в слое Штерна у катионных мицелл несколько меньше (это связано с некоторым экранированием заряда четвертичной аммониевой группы), поэтому их структура более компактна по сравнению с анионными мицеллами.
К неионным ПАВ относятся также эфиры сахаров, жирные алканоламины, жирные окиси аминов. Все эти вещества довольно трудно получить в виде индивидуальных химических соединений, однако отсутствие ионов в мицеллах, которые они образуют, делает их особенно полезными в качестве детергентов и эмульгаторов и позволяет упростить теоретическое рассмотрение структуры таких мицелл. ККМ неионных ПАВ обычно в 100 раз меньше, чем ККМ ионогенных детергентов, содержащих сравнимые по величине гидрофобные группы. Поэтому масса мицелл неионных детергентов существенно больше, чем масса мицелл ионогенных ПАВ. Анионные детергенты обычно содержат длинную углеводородную цепь и карбоксилатную, сульфатную или сульфонатную группу. В качестве противоионов выступают натрий, калий, литий или водород. Длинноцепочечные четвертичные амины или пиридипы с бромид-, хлорид- или иодид-ионом в качестве противоиона образуют группу катионных ПАВ. Степень нейтрализации заряда противоионами в слое Штерна у катионных мицелл несколько меньше (это связано с некоторым экранированием заряда четвертичной аммониевой группы), поэтому их структура более компактна по сравнению с анионными мицеллами. Катионные мицеллы обладают несколько большей солюбилизующей способностью в отношении неполярных субстратов, чем анионные мицеллы, образованные ПАВ того же молекулярного веса. Амфотерные мицеллы образованы цвиттер-ионными молекулами, у которых тип диссоциации определяется pH раствора [45, 46]. Природные фосфатиды и липиды, такие, как лецитин и соли желчных кислот, также образуют мицеллы и определяют многие важные биологические функции in vivo и in vitro [20, 47—51]. [c.228]
Катионные мицеллы обладают несколько большей солюбилизующей способностью в отношении неполярных субстратов, чем анионные мицеллы, образованные ПАВ того же молекулярного веса. Амфотерные мицеллы образованы цвиттер-ионными молекулами, у которых тип диссоциации определяется pH раствора [45, 46]. Природные фосфатиды и липиды, такие, как лецитин и соли желчных кислот, также образуют мицеллы и определяют многие важные биологические функции in vivo и in vitro [20, 47—51]. [c.228]
Хорошо известно, что ионы кальция поступают в цитоплазму в ответ на нервную стимуляцию и что именно они вызывают различные ответные реакции в организме, такие, например, как мышечное сокращение. Весьма вероятно, что в результате присоединения ионов Са- к специфическим центрам связывания (как это имеет место, например, в каль-ций-связывающем белке карпа) в молекуле происходят конформационные изменения, инициирующие биологические ответные реакции. Кальций-связывающий белок содержит интересную систему внутренних полярных групп, связанных между собой специфическим образом с помощью водородных связей (рис. 4-5, ). Присоединение ионов кальция может вызывать перестройку этих внутренних связей (гл. 2, разд. Б.7) и изменять тем самым характер взаимодействия этого белка (функция которого точно не известна) с другим белком (ср., например, с действием тропонина С, разд. Е.1). В других кальций-связывающих центрах в белках содержатся остатки у-карбоксиглутаминовой кислоты, способной образовывать хелатные комплексы (дополнение 10-Г). [c.270]
4-5, ). Присоединение ионов кальция может вызывать перестройку этих внутренних связей (гл. 2, разд. Б.7) и изменять тем самым характер взаимодействия этого белка (функция которого точно не известна) с другим белком (ср., например, с действием тропонина С, разд. Е.1). В других кальций-связывающих центрах в белках содержатся остатки у-карбоксиглутаминовой кислоты, способной образовывать хелатные комплексы (дополнение 10-Г). [c.270]
Каждая клетка состоит из огромного числа атомов и молекул. Попробуем разобраться, насколько они универсальны и какие функции выполняют в клетках Оказалось, что из периодической системы элементов всего лишь шесть биоэлементов используются для построения подавляющего числа биологически значимых молекул углерод С, ьшслород О, водород Н, сера 8, азот N и фосфор Р. Еще 16 микроэлементов присутствуют в клетках в различных количествах и соотношениях. К ним относятся железо Ре, медь Си, цинк Zn, марганец Мп, кобальт Со, иод I, молибден Мо, ванадий V, никель N1, хром Сг, фтор Р, селен 8е, кремний 81, олово 8п, бор В, мышьяк Аз и пять ионов натрий Na , калий К , магний Mg , кальций Са » , хлор С1 . Каков бы ни был принцип отбора атомов для процессов жизнедеятельности, он не связан с их распространенностью в природе. Например, из галогенов только хлор и иод выбраны природой, хотя фтор и бром обладают не меньшей доступностью. По-видимому, в основу отбора положен принцип пригодности и целесообразности. Например, шесть основных биоэлементов имеют набор свойств, достаточный для построения почти всех необходимых для клетки молекул. [c.6]
Каков бы ни был принцип отбора атомов для процессов жизнедеятельности, он не связан с их распространенностью в природе. Например, из галогенов только хлор и иод выбраны природой, хотя фтор и бром обладают не меньшей доступностью. По-видимому, в основу отбора положен принцип пригодности и целесообразности. Например, шесть основных биоэлементов имеют набор свойств, достаточный для построения почти всех необходимых для клетки молекул. [c.6]
Биология и медицина. Начало биологическим применениям стеклянных электродов с металлической функцией ( катион-чувствительных ) положили работы Эйзенмана с сотрудниками (1957 г.). Результаты работы, проведенной под руководством Эйзенмана, дали возможность биологам получать данные об активности ионов калия и натрия непосредственно с места их действия (in situ) в биологических процессах. В этих работах подчеркивается и другая сторона вопроса для ряда биологических явлений (возникновение биопотенциалов, клеточная проницаемость и связанные с ней процессы нервного возбуждения, кажущаяся специфичность многих клеток и тканей по отношению к ионам К ) физико-химические закономерности оказываются во многом сходными с теми, которые имеют важное значение в функционировании стеклянных и мембранных электродов. Это повышает интерес и значимость самой ионообменной теории стеклянного электрода. [c.331]
Это повышает интерес и значимость самой ионообменной теории стеклянного электрода. [c.331]
Если смешать соответствующие фосфолипиды и белки и нанести эту смесь на поверхность воды, то спонтанно образуются мембраноподобные структуры, сходные по толщине с биологическими мембранами. Исследование таких искусственных мембран, приготовленных из белков и липидов природных мембран, дает нам возможность лучше понять структуру и функцию биологических мембран. Искусственные мембраны обнаруживают разную проницаемость для разных ионов в зависимости от природы белков и липидов, входящих в их состав. Чрезвычайно-интересные эффекты можно наблюдать при добавлении к искусственным мембранам некоторых антибиотиков. Валиномицин, например, благодаря своей структуре (т. е. определенным размерам и заряду молекулы) оказывается способным притягивать и удерживать ионы калия, но не притягивает ионов натрия (рис. 2.5). Если добавить валиномицин к искусственной мембране, отделяющей растворы с ионами К+ и Ка+ от чистой воды. [c.28]
[c.28]
Этот последний член семейства ГР—ПРЛ— ХС не выполняет у человека строго определенной функции. При биологических испытаниях он проявляет лактогенную и лютеотропную активность, а его метаболические эффекты качественно сходны с действием гормона роста, включая торможение поглощения глюкозы, стимуляцию высвобождения свободных жирных кислот и глицерола, усиление задержки азота и кальция (несмотря на повыщение выделения кальция с мочой), а также снижение мочевой экскреции фосфора и калия. ХС может поддерживать рост развивающегося плода, однако и в тех случаях, когда ни у плода, ни в плаценте нет генов группы ГР—ХС (кроме генов ГР-Ы и ХС-Ь), внутриутробное развитие плода и рост младенца в неонатальном периоде протекают нормально. Поскольку [c.177]
Структурная и молекуля1рная организация биологических мембран. Эта проблема — одна из актуальнейших в современной биологии. Ее решение позволит не только адекватно представить структурную и функциональную организацию клетки, но и активно воздействовать на нее. Мембраны образуют большие площади и играют универсальную регуляторную роль. Функции биологических мембран многообразны активный транспорт веществ, общая н избирательная диффузия небольших молекул и рюнов, регулирование транспорта ионов и продуктов метаболизма внутри клеток, преобразование световой энергии в химическую энергию АТФ и энергии биологического окисления в химическую энергию макроэргических фосфорных связей. Мембраны поддерживают неравномерное распределение ионов (например, калия, натрия, хлора) между протопластом и окружающей средой и обусловливают появление разности биоэлектрических потенциалов. [c.65]
Мембраны образуют большие площади и играют универсальную регуляторную роль. Функции биологических мембран многообразны активный транспорт веществ, общая н избирательная диффузия небольших молекул и рюнов, регулирование транспорта ионов и продуктов метаболизма внутри клеток, преобразование световой энергии в химическую энергию АТФ и энергии биологического окисления в химическую энергию макроэргических фосфорных связей. Мембраны поддерживают неравномерное распределение ионов (например, калия, натрия, хлора) между протопластом и окружающей средой и обусловливают появление разности биоэлектрических потенциалов. [c.65]
Сдать анализ на калий, натрий, хлор
Метод определения Ион-селективный, ионселективные электроды (непрямой метод).
Исследуемый материал Сыворотка крови
Доступен выезд на дом
Онлайн-регистрацияСинонимы: Электролиты в сыворотке крови. Electrolyte Panel; Serum electrolyte test; lytes; Sodium, Potassium, Chloride; Na/K/Cl; CMP, BMP.
Electrolyte Panel; Serum electrolyte test; lytes; Sodium, Potassium, Chloride; Na/K/Cl; CMP, BMP.
Краткая характеристика определяемых веществ (Калий, Натрий, Хлор)
Калий (К+) – основной катион внутриклеточной жидкости.
Калий (К+) участвует в создании и поддержании электрического мембранного потенциала клеток. Регулирует внутриклеточное осмотическое давление, стимулирует активность ферментов гликолиза, участвует в метаболизме белков и гликогена, играет важную роль в формировании потенциала действия в нервных и мышечных клетках и проведении нервных импульсов, обладает иммуномодулирующей активностью.
Концентрация калия в плазме (сыворотке) зависит от равновесия следующих процессов: поступления калия извне, распределения в организме и выведения (почками, потовыми железами, через кишечник и т. п.). Депо калия в организме не существует. Поэтому даже при небольших изменениях концентрации калия внутри клеток значительно изменяется его концентрация в плазме.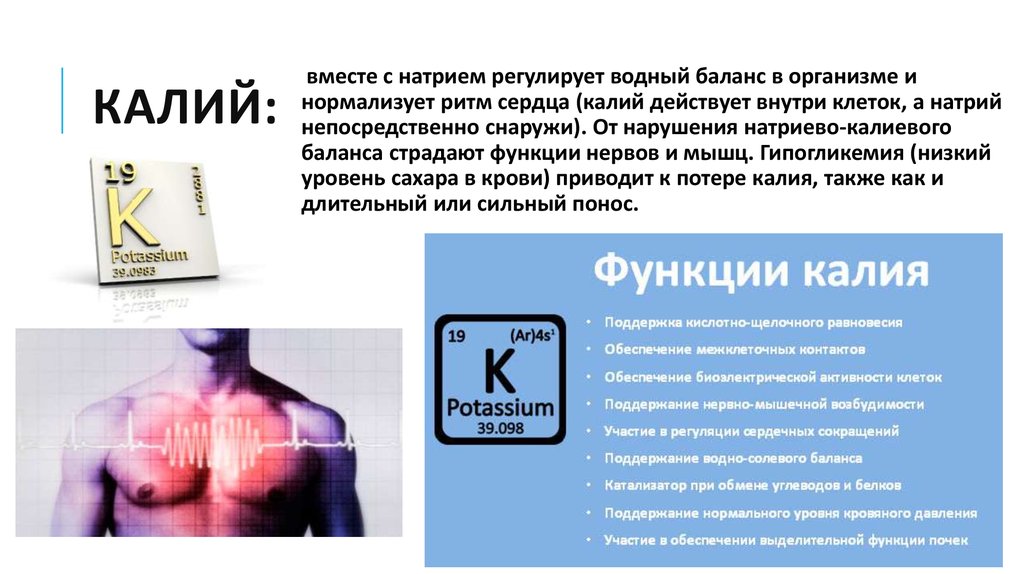 Захват калия клетками стимулируется инсулином, также захват калия клетками усиливается под действием катехоламинов, альдостерона.
Захват калия клетками стимулируется инсулином, также захват калия клетками усиливается под действием катехоламинов, альдостерона.
Натрий (Na+) – основной катион внеклеточного пространства.
Натрий (Na+) является важнейшим осмотически активным компонентом внеклеточного пространства, с которым связана регуляция объема внеклеточной жидкости. 96% общего количества натрия в организме содержится вне клеток. Он участвует в проведении возбуждения в нервных и мышечных клетках, в формировании щелочного резерва крови и транспорте ионов водорода.
Хлор (Сl-) – основной анион внеклеточной жидкости и желудочного сока.
Ионы хлора играют важную роль в поддержании кислотно-щелочного состояния, осмотического давления и баланса воды в организме. В биологических средах находится преимущественно в состоянии аниона-хлорида Cl-. Содержится в плазме, лимфе, ликворе.
С какой целью определяют уровень Калия, Натрия, Хлора в сыворотке крови
Натрий, калий, хлор входят в число основных электролитов плазмы. Тест используют для выявления нарушений электролитного баланса при различных патологических состояниях и в контроле лечения.
Тест используют для выявления нарушений электролитного баланса при различных патологических состояниях и в контроле лечения.
Что может повлиять на результат теста «Калий (К+, Potassium), Натрий (Na+, Sodium), Хлор (Сl-, Chloride)»
КалийИзменения рН крови приводят к изменению содержания К+ в клетках: при ацидозе он выходит из клеток в плазму, при алкалозе поступает внутрь клеток. При гиперкалиемии отмечаются желудочковая тахикардия, фибрилляция желудочков и даже асистолия. При гипокалиемии развиваются мышечная слабость, снижение рефлексов, гипотония, нарушения в проводящей системе сердца, непроходимость кишечника, полиурия.
Натрий
Концентрация натрия в плазме (сыворотке) зависит от равновесия следующих процессов: поступления натрия, распределения его в организме и выведения почками, потовыми железами. Основными регуляторами обмена натрия в организме являются ренин-ангиотензин-альдостероновая система, АДГ (вазопрессин), предсердный натрийуретический гормон.
Хлор
Баланс ионов хлора в организме осуществляется наличием равновесия между процессами поступления хлора с пищей, распределением в организме и выведением его с мочой, потом и калом. Изменение концентрации ионов натрия ведет за собой изменение концентрации хлорид-аниона. При потере хлоридов развивается алкалоз, при избыточном потреблении – ацидоз.
№AN39ISE, Электролиты (натрий, калий, хлор): показатели, норма
НАТРИЙ
Натрий является важным катионом внеклеточной жидкости организма. Всасывание натрия происходит в тонком кишечнике с помощью механизмов активного транспорта. При гипотензии натрий может быть почти полностью абсорбирован в толстом отделе кишечника. Натрий свободно фильтруется почками, и почти весь отфильтрованный натрий реабсорбируется. В начальном отделе проксимальных извитых канальцев почек натрий реабсорбируется вместе с глюкозой, фосфатом, аминокислотами и бикарбонатом, в то время как реабсорбция натрия в дистальном отделе происходит совместно с хлором. Натрий также активно реабсорбируется в толстом восходящем отделе петли Генле.
Натрий также активно реабсорбируется в толстом восходящем отделе петли Генле.
Функция натрия в организме заключается в поддержании нормального кровяного давления, объема крови и функционирования мышц и нервов. Концентрация натрия в плазме находится в пределах узкого диапазона. Баланс данного катиона в крови зависит от потребления натрия с пищей и водой и выведения его с мочой. Лишь небольшое количество натрия теряется с фекалиями и пóтом, но при некоторых заболеваниях или физиологических состояниях, в зависимости от вида животного, эти пути выделения могут стать более значимыми.
Регуляция содержания натрия в крови неразрывно связана с регуляцией водного баланса организма. Вода составляет примерно 60% от массы тела, около трети ее находится во внутриклеточной жидкости и одна треть — во внеклеточной жидкости. Примерно одна четверть внеклеточной жидкости находится в сосудистой сети, в то время как три четверти присутствуют в интерстиции. Водный баланс между различными жидкостными пространствами зависит от осмотического давления, и натрий, наряду со связанным с ним анионами, является основным фактором, определяющим внеклеточную осмолярность. Калий-натриевый насос обеспечивает стабильность градиента ионов относительновнутренней и внешней поверхностей клеточной мембраны, но натрий может свободно проходить через стенки кровеносных сосудов по градиенту концентрации, уравновешивая концентрационную разницу между интерстициальным и сосудистым пространствами. Концентрация натрия в сыворотке крови не обязательно отражает его содержание в организме, поскольку этот показатель отражает количество натрия по отношению к общему количеству воды в организме. Если общее содержание воды в организме очень высокое (состояние гипоосмолярности) или очень низкое (состояние гиперосмолярности), то измеренная концентрация натрия в сыворотке крови может быть в пределах нормы, даже если общее содержание катиона в организме нарушено. Рецепторы в стенках сосудов определяют изменения осмолярности и кровяного давления, в результате чего изменяется реабсорбция или выделение натрия и воды почками. Увеличение осмолярности плазмы всего на 1–2% будет улавливаться осморецепторами в гипоталамусе, что приведет к секреции вазопрессина (антидиуретического гормона) из задней доли гипофиза.
Калий-натриевый насос обеспечивает стабильность градиента ионов относительновнутренней и внешней поверхностей клеточной мембраны, но натрий может свободно проходить через стенки кровеносных сосудов по градиенту концентрации, уравновешивая концентрационную разницу между интерстициальным и сосудистым пространствами. Концентрация натрия в сыворотке крови не обязательно отражает его содержание в организме, поскольку этот показатель отражает количество натрия по отношению к общему количеству воды в организме. Если общее содержание воды в организме очень высокое (состояние гипоосмолярности) или очень низкое (состояние гиперосмолярности), то измеренная концентрация натрия в сыворотке крови может быть в пределах нормы, даже если общее содержание катиона в организме нарушено. Рецепторы в стенках сосудов определяют изменения осмолярности и кровяного давления, в результате чего изменяется реабсорбция или выделение натрия и воды почками. Увеличение осмолярности плазмы всего на 1–2% будет улавливаться осморецепторами в гипоталамусе, что приведет к секреции вазопрессина (антидиуретического гормона) из задней доли гипофиза. С другой стороны, снижение объема крови на 10%, воспринимаемое рецепторами, приводит к высвобождению вазопрессина независимо от осмолярности. Вазопрессин усиливает реабсорбцию воды в собирательных канальцах почек, тем самым восполняя количество жидкости в сосудистом русле. При повышении кровяного давления или увеличении объема крови импульсы от барорецепторов, расположенных в предсердиях и сосудах, поступают в гипоталамус и ингибируют высвобождение вазопрессина. При этом уменьшается реабсорбция натрия в дистальных отделах нефрона. Клетки юкстагломерулярного аппарата почек по сути являются барорецепторами, которые реагируют на низкое кровяное давление. Эти клетки активируют ренин-ангиотезин-альдостероновую систему (РААС) путем секреции ренина. Ренин расщепляет ангиотензиноген до ангиотензина I, который затем преобразуется в ангиотензиноген II с помощью ангиотензин-превращающего фермента (АПФ). Ангиотензин II вызывает высвобождение альдостерона из надпочечников, повышает секрецию вазопрессина, а также стимулирует центры жажды.
С другой стороны, снижение объема крови на 10%, воспринимаемое рецепторами, приводит к высвобождению вазопрессина независимо от осмолярности. Вазопрессин усиливает реабсорбцию воды в собирательных канальцах почек, тем самым восполняя количество жидкости в сосудистом русле. При повышении кровяного давления или увеличении объема крови импульсы от барорецепторов, расположенных в предсердиях и сосудах, поступают в гипоталамус и ингибируют высвобождение вазопрессина. При этом уменьшается реабсорбция натрия в дистальных отделах нефрона. Клетки юкстагломерулярного аппарата почек по сути являются барорецепторами, которые реагируют на низкое кровяное давление. Эти клетки активируют ренин-ангиотезин-альдостероновую систему (РААС) путем секреции ренина. Ренин расщепляет ангиотензиноген до ангиотензина I, который затем преобразуется в ангиотензиноген II с помощью ангиотензин-превращающего фермента (АПФ). Ангиотензин II вызывает высвобождение альдостерона из надпочечников, повышает секрецию вазопрессина, а также стимулирует центры жажды. Альдостерон действует на собирательные трубочки кортикального слоя почки, повышая реабсорбцию натрия. Реабсорбция натрия в сочетании либо с секрецией калия (еще одна очень важная функция альдостерона), либо с реабсорбцией хлора служит для поддержания электронейтральности.
Альдостерон действует на собирательные трубочки кортикального слоя почки, повышая реабсорбцию натрия. Реабсорбция натрия в сочетании либо с секрецией калия (еще одна очень важная функция альдостерона), либо с реабсорбцией хлора служит для поддержания электронейтральности.
При оценке концентрации натрия в сыворотке крови следует принять во внимание общее содержание воды в организме животного. Увеличение концентрации натрия в сыворотке крови возможно за счет увеличения содержания натрия, уменьшения количества воды или в результате комбинации показателей. И наоборот, уменьшение концентрации натрия в сыворотке крови возможно за счет снижения содержания натрия, повышения количества воды или в результате комбинации этих факторов.
Гипернатриемия чаще всего ассоциируется с дисбалансом воды в организме. Это может произойти из-за снижения потребления воды или при ее потере, превышающей потерю электролитов (например, при развитии центрального или нефрогенного несахарного диабета). Снижение потребления воды может быть связано с отсутствием доступа к воде, нарушением ответа на жажду или физической неспособностью пить. Потеря воды может происходить через кожу или с дыханием, а также через почки или желудочно-кишечный тракт. Во многих случаях потеря воды сопровождается также потерей электролитов, например, как случается при рвоте, диарее (осмотической диарее) или увеличении диуреза. У таких животных развивается гиповолемия. При абсолютной потере воды или недостаточном потреблении воды общее содержание натрия в организме остается нормальным, а вода из внутриклеточного пространства поступает в межклеточное пространство, поддерживая объем плазмы (изоволюмическая гипернатриемия). Избыток поступления натрия является редкой причиной гипернатриемии, обычно также отмечается одновременное ограничение поступления воды или неспособность почек к концентрации мочи. Снижение экскреции натрия также может привести к избытку катиона в организме, что возможно в редких случаях гиперальдостеронизма.
Снижение потребления воды может быть связано с отсутствием доступа к воде, нарушением ответа на жажду или физической неспособностью пить. Потеря воды может происходить через кожу или с дыханием, а также через почки или желудочно-кишечный тракт. Во многих случаях потеря воды сопровождается также потерей электролитов, например, как случается при рвоте, диарее (осмотической диарее) или увеличении диуреза. У таких животных развивается гиповолемия. При абсолютной потере воды или недостаточном потреблении воды общее содержание натрия в организме остается нормальным, а вода из внутриклеточного пространства поступает в межклеточное пространство, поддерживая объем плазмы (изоволюмическая гипернатриемия). Избыток поступления натрия является редкой причиной гипернатриемии, обычно также отмечается одновременное ограничение поступления воды или неспособность почек к концентрации мочи. Снижение экскреции натрия также может привести к избытку катиона в организме, что возможно в редких случаях гиперальдостеронизма. У таких животных развивается гиперволемия. Если избыток натрия присутствует во внеклеточной жидкости, то вода из клеток будет переходить во внеклеточное пространство, а клетки становятся обезвоженными.
У таких животных развивается гиперволемия. Если избыток натрия присутствует во внеклеточной жидкости, то вода из клеток будет переходить во внеклеточное пространство, а клетки становятся обезвоженными.
Гипонатриемия может развиться или в результате потери натрия, которая превышает потерю воды, или при увеличении воды в организме. Гипонатриемия связана с гипоосмолярностью, за исключением случаев псевдогипонатриемии или случаев транслокационной гипонатриемии, при которых снижение концентрации натрия в крови происходит за счет увеличения содержания других осмотически активных веществ. При псевдогипонатриемии снижение концентрации натрия возникает в результате увеличения содержания липидов или белков и не сопровождается истинным снижением осмолярности крови.
Транслокационная гипонатриемия развивается из-за присутствия в крови других веществ, вызывающих гиперосмолярность (например, глюкозы), которые плохо проходят через клеточные мембраны. Осмотически активные вещества в крови будут «тянуть» на себя воду из внутриклеточного пространства, способствуя дегидратации клеток. При этом концентрация содержащегося в крови натрия снижается из-за разведения. Транслокационную гипонатриемию не будут вызывать вещества, которые легко проникают через клеточные мембраны (например, мочевина).
При этом концентрация содержащегося в крови натрия снижается из-за разведения. Транслокационную гипонатриемию не будут вызывать вещества, которые легко проникают через клеточные мембраны (например, мочевина).
Гипоосмолярная гипонатриемия возникает из-за повышенного содержания воды или пониженного содержание натрия в крови. Повышенное содержание воды в крови отмечается в случаях нарушения почечной экскреции свободной воды или разбавленной мочи или если потребление воды превышает максимальную почечную выделительную способность. Избыточное потребление воды встречается редко, но может возникать при психогенной полидипсии. При избыточном потреблении воды осмолярность мочи и плазмы будет низкой.
Снижение почечной экскреции свободной воды в ответ на гиповолемию может привести к увеличению общего объема воды в организме. Это происходит в результате накопления жидкости в полостях тела, что может быть связано с застойной сердечной недостаточностью, циррозом печени или нефротическим синдромом. Выделение вазопрессина в ответ на развивающуюся гиповолемию приводит к увеличению реабсорбции воды. Нарушение почечной экскреции воды в результате развития почечной недостаточности также может привести к гиперволемической гипонатриемии.
Выделение вазопрессина в ответ на развивающуюся гиповолемию приводит к увеличению реабсорбции воды. Нарушение почечной экскреции воды в результате развития почечной недостаточности также может привести к гиперволемической гипонатриемии.
Гиповолемия обычно сопровождается потерей натрия из организма. Потеря натрия редко возникает без потери воды. Для развития гипонатриемии должна быть потеря гипертонической жидкости (выделение натрия больше, чем воды), либо потеряизотонической или гипотонической жидкости, что приводит к снижению объема внеклеточной жидкости, которое стимулирует жажду и задержку воды почками, «разбавляя» тем самым, остальные жидкости организма.
Гиповолемическая, гипоосмолярная гипонатриемия возможна в результате расстройств со стороны желудочно-кишечного тракта (рвота, диарея), почек (гипоадренокортицизм, продолжительный диурез) и интерстициального пространства (выпоты в полости тела). Первичный гипоадренокортицизм (болезнь Аддисона) связан с дефицитом альдостерона, что приводит к снижению почечной реабсорбции натрия и удержанию калия в собирательных трубочках коркового слоя почек.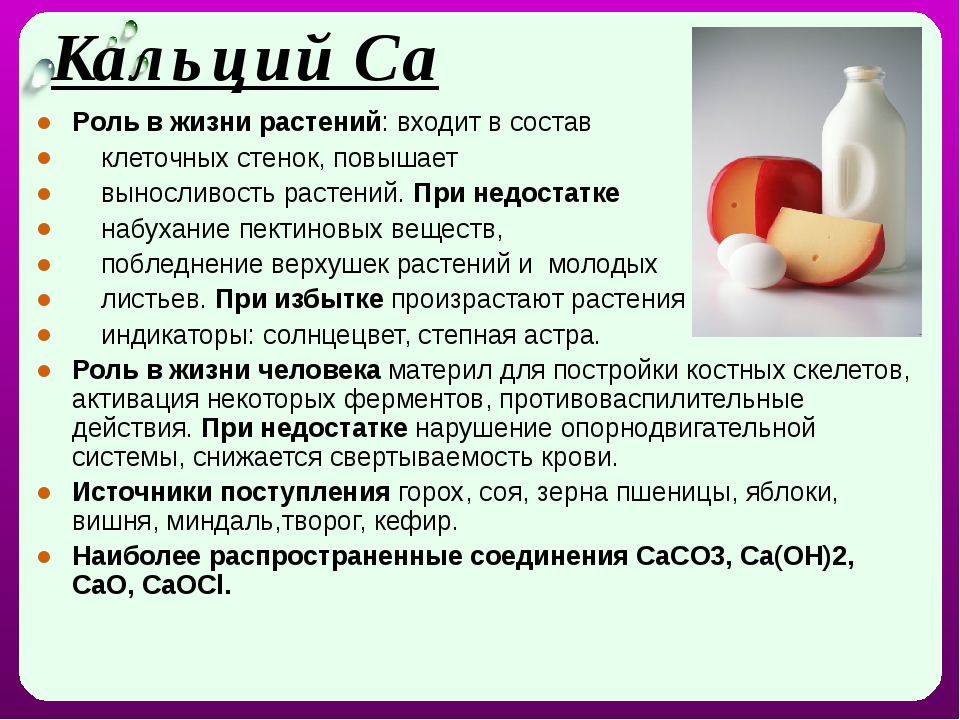 Следует учитывать, что в перечисленных состояниях у животного может не выявляться изменение концентрации натрия в крови, несмотря на то, что присутствует обезвоживание или гиперволемия, если произошла потеря только изотонической жидкости или было достигнуто равновесие концентраций. Гиповолемия не только стимулирует высвобождение вазопрессина, но вызывает активацию РААС, что приводит к задержке натрия в организме.
Следует учитывать, что в перечисленных состояниях у животного может не выявляться изменение концентрации натрия в крови, несмотря на то, что присутствует обезвоживание или гиперволемия, если произошла потеря только изотонической жидкости или было достигнуто равновесие концентраций. Гиповолемия не только стимулирует высвобождение вазопрессина, но вызывает активацию РААС, что приводит к задержке натрия в организме.
КАЛИЙ
Калий является основным внутриклеточным катионом, который играет важную роль в мембранном потенциале покоя клеток. В клетках содержится около 95–98% от общего содержания калия в организме, при этом 60–75% находится в миоцитах. Разность потенциалов между внутренней и внешней сторонами мембраны, а также поддержание высокой концентрации калия внутри клетки достигается благодаря работе Na/K-насоса при участии молекул АТФ. Калий всасывается в желудке и тонком отделе кишечника. В почках калий не реабсорбируется, поэтому от поступления калия с пищей будет зависеть его содержание в организме.
Клинические признаки, связанные с изменениями концентрации калия в сыворотке крови, проявляются в виде дисфункции сердечной и скелетных мышц.
Гиперкалиемия может оказать опасное для жизни воздействие на сердечную проводимость, поэтому сывороточная концентрация калия поддерживается в узких пределах. Кроме того, калий имеет большое значение для нормальной функции ферментных систем, контролирующих синтез ДНК, гликогена и белков.
Содержание общего количества калия в организме представляет собой баланс между калием, попавшем в организм (100%), и выведенным почками (около 90–95%) и через толстый отдел кишечника (около 5–10%). Концентрация калия во внеклеточном пространстве (сыворотке) также зависит от перемещения катиона между вне- и внутриклеточным пространствами. Менее 5% от общего содержания калия в организме находится во внеклеточном пространстве. Поэтому концентрация калия в сыворотке крови не полностью отражает общее содержание калия в организме.
Гиперкалиемия развивается в результате повышения нагрузки калия, снижения его экскреции или перемещения калия из внутриклеточного пространства во внеклеточное. Увеличение потребления калия вряд ли приведет к гиперкалиемии, если при этом не будет одновременного снижения почечной экскреции калия. Увеличение нагрузки калия может возникнуть ятрогенным путем и привести к летальному исходу, если ошибочно были назначены жидкости, содержащие высокую концентрацию калия. Развитие ренальных или постренальных заболеваний мочевыводящих путей, приводящих к снижению почечной экскреции калия, становится частой причиной гиперкалиемии. При олигурической и анурической стадиях почечной недостаточности почки неспособны удалить избыток калия из организма. Гиперкалиемия также наступает при постренальных патологиях, нарушающих отток мочи.
Альдостерон способствует увеличению концентрации натрия и снижению уровня калия в сыворотке крови путем увеличения реабсорбции натрия и экскреции калия в собирательных трубочках коркового слоя почек. Снижение секреции альдостерона (гипоадренокортицизм) обычно сопровождается гиперкалиемией и гипонатриемией. Почечная экскреция калия уменьшается (с повышением его концентрации в сыворотке крови) при снижении скорости тока жидкости в канальцах, которое может быть результатом гиповолемии (нарушения со стороны ЖКТ, образование выпотов). Гиповолемия с развитием гипонатриемии и гиперкалиемии более выражена при неоднократном образовании выпотов и дренировании полостей.
Снижение секреции альдостерона (гипоадренокортицизм) обычно сопровождается гиперкалиемией и гипонатриемией. Почечная экскреция калия уменьшается (с повышением его концентрации в сыворотке крови) при снижении скорости тока жидкости в канальцах, которое может быть результатом гиповолемии (нарушения со стороны ЖКТ, образование выпотов). Гиповолемия с развитием гипонатриемии и гиперкалиемии более выражена при неоднократном образовании выпотов и дренировании полостей.
К желудочно-кишечным заболеваниям, которые чаще всего связаны с гиперкалиемией, относится трихоцефалез при значительной степени инвазии. Перемещение калия между вне- и внутриклеточной жидкостью играет большую роль в поддержании постоянной концентрации калия в сыворотке крови. Выход калия из клеток с развитием гиперкалиемии может быть вызван поступлением ионов водорода и хлора в клетки, что происходит при метаболическом ацидозе. Так как инсулин играет важную роль в переносе калия из внеклеточного пространства во внутриклеточное, то его дефицит может привести к гиперкалиемии. Поскольку калий в высокой концентрации находится в клетках, то обширное повреждение тканей или клеток (синдром лизиса опухоли, рабдомиолиз или тяжелая травма), как правило, сопровождается развитием гиперкалиемии, особенно в случаях одновременного снижения почечной экскреции.
Поскольку калий в высокой концентрации находится в клетках, то обширное повреждение тканей или клеток (синдром лизиса опухоли, рабдомиолиз или тяжелая травма), как правило, сопровождается развитием гиперкалиемии, особенно в случаях одновременного снижения почечной экскреции.
Псевдокалиемия развивается вследствие нарушения техники взятия крови, при тромбоцитозе, лейкоцитозе и гемолизе. При этом будут отсутствовать клинические признаки гиперкалиемии и предрасполагающие факторы ее развития. В тромбоцитах содержится большое количество калия, который высвобождается при их активации. Свертывание крови, следовательно, может привести к повышению в сыворотке крови концентрации калия, особенно если присутствует тромбоцитоз. Референсные интервалы калия для сыворотки крови немного выше, чем для плазмы. Гемолиз приводит к выходу калия из эритроцитов. Количество калия в эритроцитах изменяется в зависимости от вида животного и даже породы. Лошади, свиньи и крупный рогатый скот имеют более высокое содержание калия в эритроцитах, по сравнению с кошками и собаками, за исключением японских пород собак (акита-ину и др. ).
).
Гипокалиемия является одним из наиболее распространенных нарушений электролитного баланса у пациентов в критическом состоянии, несмотря на то, что окончательная причина этого изменения не всегда может быть установлена. Гипокалиемия может быть результатом снижения потребления калия с пищей, увеличения его экскреции, потерей через ЖКТ (рвота, диарея), перемещения этого катиона между внутри- и внеклеточным пространством, или, что бывает чаще, комбинации всех этих причин. Снижение потребления калия может способствовать развитию гипокалиемии, но, как правило, не является причиной самой по себе. Гипокалиемия может быть вызвана ятрогенным путем при назначении растворов с низким содержанием калия. Гипокалиемия, связанная с хронической почечной недостаточностью, чаще встречается у кошек.
Ацидоз дистальных почечных канальцев, постобструкционный диурез, диабетический кетоацидоз и применение диуретиков (не калийсберегающих) — все это может привести к увеличению экскреции калия и гипокалиемии. Альдостерон вызывает реабсорбцию натрия (с пассивной абсорбцией хлора) в дистальных отделах нефрона и секрецию калия. Альдостерон также повышает активность Na/K-АТФазы в дистальных извитых канальцах, усиливая секрецию калия в дистальной части нефрона. Однако гиперальдостеронизм является редкой причиной развития гипокалиемии. Значительное перемещение калия из внеклеточного пространства во внутриклеточное также может привести к гипокалиемии, что возникает в результате переизбытка инсулина, инфузии глюкозы или при развитии метаболического алкалоза. Катехоламины, высвобождаемые в результате боли, сепсиса или травмы, также способны вызвать сдвиг калия путем перемещения его внутрь клетки.
Альдостерон вызывает реабсорбцию натрия (с пассивной абсорбцией хлора) в дистальных отделах нефрона и секрецию калия. Альдостерон также повышает активность Na/K-АТФазы в дистальных извитых канальцах, усиливая секрецию калия в дистальной части нефрона. Однако гиперальдостеронизм является редкой причиной развития гипокалиемии. Значительное перемещение калия из внеклеточного пространства во внутриклеточное также может привести к гипокалиемии, что возникает в результате переизбытка инсулина, инфузии глюкозы или при развитии метаболического алкалоза. Катехоламины, высвобождаемые в результате боли, сепсиса или травмы, также способны вызвать сдвиг калия путем перемещения его внутрь клетки.
ХЛОР
Хлор является основным анионом внеклеточной жидкости организма и, подобно натрию, имеет большое значение в транспортировке электролитов и воды. Хлор также служит в качестве сопряженного аниона в метаболизме кислот и оснований. Для поддержания электронейтральности хлор либо движется в том же направлении, что и положительно заряженные ионы натрия, либо обменивается с отрицательно заряженными ионами бикарбоната.
Гомеостаз хлора в основном регулируется почками и в незначительной степени ЖКТ. Попавший с пищей хлор всасывается в тощей кишке, дистальном отделе толстого отдела кишечника совместно с натрием, в подвздошной кишке. Облегченный транспорт хлора в подвздошной кишке и толстом кишечнике является движущей силой для натрия и реабсорбции воды. В почках около 50–60% отфильтрованного хлора реабсорбируется в проксимальных канальцах. Реабсорбция хлора под влиянием альдостерона осуществляется в дистальных отделах нефрона, а с помощью активного транспорта хлор реабсорбируется в толстом восходящем отделе петли Генле.
При оценке содержания хлора в сыворотке крови важно сопоставлять уровень хлора с уровнем натрия и кислотно-основным состоянием животного. Если отклоненияконцентрации хлора пропорциональны отклонениям концентрации натрия, то принципы изменений аналогичны тем, которые были рассмотрены при гипонатриемии или гипернатриемии. Если изменение концентрации хлора оказывается больше, чем изменение концентрации натрия, следует учитывать концентрацию бикарбоната и результаты анализа газов крови.
Гиперхлоремия обычно сопровождается потерей воды. Однако гиперхлоремия может быть связана со снижением уровня бикарбоната в крови. Потеря бикарбоната может возникать в результате нарушений со стороны желудочно-кишечного тракта (диарея, гиперсаливация у крупного рогатого скота, рвота содержимым кишечника, как в случае кишечной непроходимости). Потеря бикарбоната через почки происходит при проксимальном или дистальном тубулярном ацидозе. В ответ на респираторный алкалоз ослабляется механизм сохранения бикарбоната в почках, что приводит к удержанию хлора и развитию гиперхлоремии.
Гипохлоремия. Метаболический алкалоз приводит к большему снижению концентрации хлора в крови, чем снижению концентрации натрия. В процессе секреции соляной кислоты в желудке содержание хлора в сыворотке крови снижается, а количество бикарбонатаувеличивается. Эти изменения, как правило, обратимы, когда из кишечника абсорбируются ионы водорода и хлора, а также вода. Если желудочное содержимое теряется в результате рвоты или обструкции пилорического отдела, а также функциональной обструкции, концентрация хлора в сыворотке крови будет оставаться низкой, а уровень бикарбоната будет повышенным. Содержание хлора в сыворотке будет снижаться, когда уровень бикарбоната будет возрастать в ответ на развитие хронического респираторного ацидоза.
Содержание хлора в сыворотке будет снижаться, когда уровень бикарбоната будет возрастать в ответ на развитие хронического респираторного ацидоза.
Таким образом, подводя итог роли хлора в поддержании буферной системы крови и кислотно-щелочного баланса, можно сказать, что повышенное содержание хлора в сыворотке крови связано с метаболическим ацидозом, в то время как гипохлоремия связана с метаболическим алкалозом.
ПРЕАНАЛИТИКА
Для получения более точных результатов животные перед исследованием должны находиться на голодной диете не менее 12 часов. Образец стабилен неделю при хранении +2С…+8С и в течение года сохраняет стабильность при замораживании (-17С…-23С).
Нарушение преаналитики может привести к искажению результатов, например, при гемолизе образца или задержке отделения сыворотки от эритроцитарной массы после взятия крови.
ИНТЕРПРЕТАЦИЯ
Результаты исследования содержат информацию исключительно для врачей. Диагноз ставится на основании комплексной оценки различных показателей, дополнительных сведений и зависит от методов диагностики.
Диагноз ставится на основании комплексной оценки различных показателей, дополнительных сведений и зависит от методов диагностики.
Единицы измерения: ммоль/л.
Натрий, хлор
Оценка дегидратации
Пропорциональная потеря NaCl и воды (в некоторых случаях при диарее и заболеваниях почек). Концентрация [Na] и [Cl] в крови не изменяется, происходит увеличение гематокрита и содержание общего белка в сыворотке крови.* Осмолярность плазмы практически не изменяется, вода не перемещается из внутриклеточного пространства во внеклеточное, поэтому объем внеклеточной жидкости уменьшается.
Гипертоническая дегидратация (внеклеточная жидкость становится гипертонической)
Потеря воды больше потери NaCl (несахарный диабет, снижение потребления воды или отсутствие доступа к ней, гипертермия или учащенное дыхание, осмотический диурез, диарея).
Увеличение концентрации [Na] и [Cl] в крови, увеличение гематокрита и содержание общего белка в сыворотке крови.
 * В результате повышения осмолярности плазмы вода для поддержания объема внеклеточной жидкости перемещается из области внутриклеточного пространства во внеклеточное пространство. Развивается клеточный эксикоз.
* В результате повышения осмолярности плазмы вода для поддержания объема внеклеточной жидкости перемещается из области внутриклеточного пространства во внеклеточное пространство. Развивается клеточный эксикоз.Гипотоническая дегидратация (гипотония внеклеточной жидкости)
Потеря NaCl превышает потерю воды (секреторная диарея, рвота, выпоты, сильное потоотделение у лошадей).
Снижение концентрации [Na] и [Cl] в крови, увеличение гематокрита и содержание общего белка в сыворотке крови.* Осмолярность плазмы снижается, вода перемещается из внеклеточного пространства во внутриклеточное. Развивается отек клеток (внутриклеточная гипергидратация), усугубляя дефицит жидкости во внеклеточном пространстве.
- Величина общего белка в сыворотке крови и/или гематокрита может не увеличиваться, если отмечается одновременная потеря белка и/или анемия.
Референсные значения:
Натрий
Собаки: 142–155 ммоль/л.
Кошки: 142–158 ммоль/л.
Хорьки: 146–160 ммоль/л.
Повышение уровня:
Псевдогипернатриемия (дегидратация, использование антикоагулянтов, содержащих натрий).
Отсутствие доступа к воде, гиподипсия.
Несахарный диабет.
Гипертермия, лихорадочное состояние.
Потеря гипотонической жидкости (гиповолемия).
Осмотический диурез.
Применение диуретиков.
Хроническая почечная недостаточность (ХПН).
Неолигурическая острая почечная недостаточность.
Постобструктивный диурез.
Расстройства ЖКТ (рвота, диарея, обструкция тонкого отдела кишечника).
Выпоты.
Термические ожоги.
Гиперволемия.
Введение гипертонических растворов.
Гиперадренокортицизм.
Понижение уровня:
Псевдогипонатриемия (выраженная гиперпротеинемия, гиперлипемия).
Транслокационная гипонатриемия.
Гипергликемия.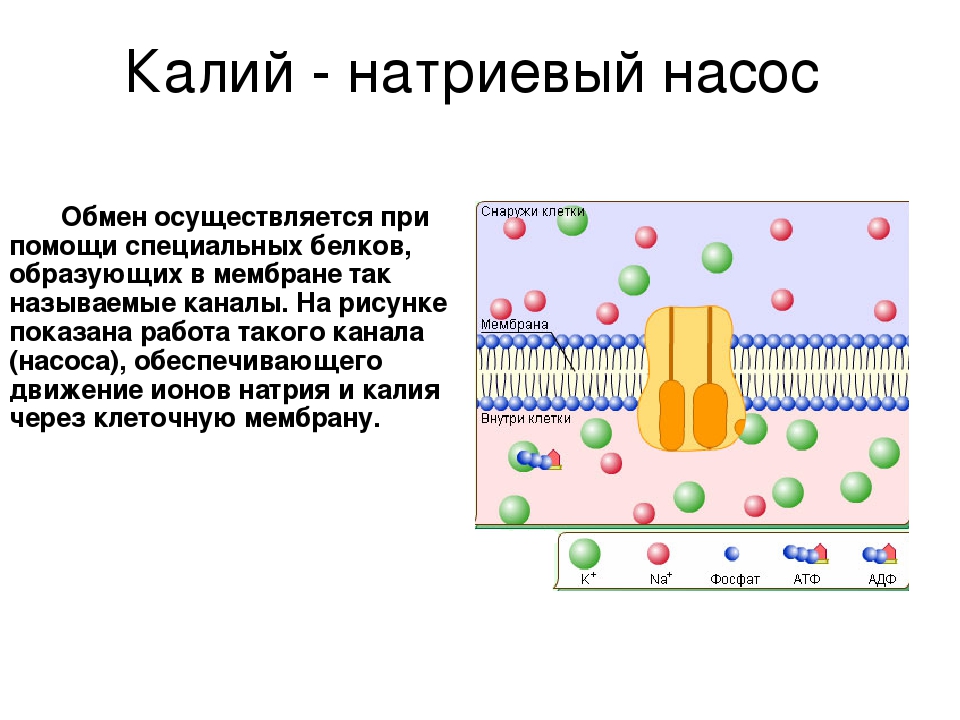
Снижение выделения воды почками (по разным причинам).
Усиленное потребление воды, превышающее выделительную способность почек.
Калий
Собаки: 4–5,7 ммоль/л.
Кошки: 4–5,5 ммоль/л.
Хорьки: 4,5–6,4 ммоль/л — альбиносы; 4,3–5,3 ммоль/л — темные.
Повышение уровня:
Псевдогиперкалиемия (гемолиз, тромбоцитоз, лейкоцитоз, беременность у собак, дефицит фосфофруктокиназы у собак).
Повышенное потребление калия с пищей, ятрогенная причина.
Снижение выделения калия с мочой (нарушение оттока мочи, анурическая или олигурическая стадия почечной недостаточности, выпоты, нарушения со стороны ЖКТ, гипоадренокортицизм, повторное дренирование выпотов, гипоренинемический гипоальдостеронизм).
Диабетический кетоацидоз.
Обширный некроз тканей (рабдомиолиз, синдром распада опухоли, травма).
Гипоадренокортицизм.
Метаболический ацидоз.
Понижение уровня:
Псевдогипокалиемия (выраженная липемия).
Снижение поступления калия с пищей, ятрогенная причина.
Повышенная потеря через ЖКТ (рвота, диарея).
Повышенная потеря через почки (ХПН у кошек, постобструктивный диурез, сахарный диабет, назначение (не калийсберегающих) диуретиков, гиперадренокортицизм, гипомагниемия, гипертиреоз у кошек, дистальный канальцевый ацидоз, проксимальный канальцевый ацидоз после лечения гидрокарбонатом, первичный гиперальдостеронизм).
Транслокационная гипокалиемия (введение инсулина или глюкозы, метаболический алкалоз, гипокалиемический периодический паралич беременных кошек, действие катехоламинов).
Хлор
Собаки: 98–118 ммоль/л.
Кошки: 108–125 ммоль/л.
Повышение уровня:
Псевдогиперхлоремия (выраженный хилез, действие некоторых лекарственных препаратов).
Превышение потребления хлора над экскрецией.
Дегидратация.
Несахарный диабет.
Действие кортикостероидов.
Почечный канальцевый ацидоз.
Гипоальдостеронизм.
Хронический респираторный алкалоз.
Почечная недостаточность.
Понижение уровня:
Псевдогипохлоремия (гиперпротеинемия, хилез).
Хронический респираторный ацидоз.
Кетонурия.
Полиурическая стадия почечной недостаточности.
Развитие отеков, ожоги.
Потеря через ЖКТ.
Выпоты.
Гиперадренокортицизм.
Застойная сердечная недостаточность.
Введение натрия бикарбоната.
Применение петлевых или тиазидных диуретиков.
Роль электролитов в организме животных
Электролиты – это
минеральные соединения, которые способны проводить электрический заряд. Большинство
физиологических процессов, происходящих в организме, без участия электролитов
невозможно.
Находясь в тканях и крови организма в виде растворов солей, они помогают перемещению питательных веществ в клетки и выводу продуктов обмена веществ из клеток, поддерживают в них водный баланс и необходимый уровень кислотности. Электролиты обеспечивают поддержание гомеостаза, участвуют в метаболизме, играют важную роль в развитии костной ткани, необходимы для обеспечения сократительной способности мышечных волокон, а также для их расслабления. К основным электролитам крови относятся калий, магний, натрий, кальций, фосфор, хлориды, железо.
Натрий – главный внеклеточный элемент, помогающий организму активно расти и развиваться. Он обеспечивает транспорт питательных веществ к клеткам организма, участвует в генерации нервных импульсов, обладает спазмолитическим действием, активизирует пищеварительные ферменты и регулирует обменные процессы.
Хлориды – электролит крови, нормализующий водно-солевой обмен. Он помогает выровнять уровень кровяного давления, уменьшить отечность тканей, активизировать процесс пищеварения, улучшить функционирование гепатоцитов.
Калий поддерживает на должном уровне водный баланс, стимулирует сокращения миокарда, защищает кровеносные сосуды, в силу чего препятствует развитию кислородного голодания, способствует выведению шлаков, нормализует работу сердца, оказывает положительное влияние на иммунитет.
Кальций – электролит, отвечающий за нормальную работу свертывающей и сердечно-сосудистой систем, регуляцию обмена веществ, укрепление нервной системы, построение и обеспечение прочности костной ткани, поддержание стабильного ритма сердца.
Магний – жизненно важный электролит. Он нормализует сокращение миокарда и улучшает работу центральной нервной системы. Магний предотвращает развитие холецистита и мочекаменной болезни.
Железо – электролит, обеспечивающий перенос и доставку кислорода к клеточным элементам и тканям. В результате кровь насыщается кислородом, нормализуется процесс клеточного дыхания и образования красных кровяных телец в костном мозге. Железо поступает в организм извне, всасывается в кишечнике и разносится с током крови по всему организму.
Железо поступает в организм извне, всасывается в кишечнике и разносится с током крови по всему организму.
Фосфор – микроэлемент, который необходим для осуществления липидного обмена, синтеза ферментов, распада углеводов. С его участием формируется зубная эмаль, протекает процесс образования костей, передача нервных импульсов. Фосфор поступает в организм с пищей, всасывается в ЖКТ только вместе с кальцием.
Содержание электролитов в крови часто нарушается у животных при отсутствии сбалансированного рациона или в случаях развития патологических процессов в организме. Расшифровкой полученных лабораторных результатов занимаются только ветеринарные специалисты.
В диагностическом отделе ФГБУ «Кемеровская МВЛ» проводится биохимический анализ крови по 23 показателям. Материалом для исследования уровня электролитов служит сыворотка крови. Следует отметить, что гемолизированная сыворотка крови не пригодна для исследования.
ФГБУ «Кемеровская МВЛ»
Калий — ОВУМ – медицинская лаборатория в Кемерοво
Описание
Калий — основной внутриклеточный катион, 98% калия содержится внутри клеток, а 2% во внеклеточной жидкости, включая плазму крови.
Калий участвует в создании и поддержании мембранного заряда клеток, играет важную роль в проведении нервных импульсов, механизмах возбуждения нервных и мышечных волокон, регулирует внутриклеточное осмотическое давление, участвует в обменах белков и гликогена, иммунологических реакциях.
Концентрация калия зависит от его поступления с пищей, баланса внутри- и внеклеточной жидкости, уровня выведения почками, в меньшей степени через кишечник и с потом. Обмен калия тесно связан с обменом натрия, регулируется гормоном альдостероном. На концентрацию калия влияют многие диуретики, изменение рН крови, введение инсулина.
Гиперкалиемия вызывает риск остановки сердца.
Гипокалиемия может вызывать нарушения ритма сердца, слабость мышц, атонию кишечника, ослабление рефлексов, гипотонию.
Показания к определению калия:
1.Контроль уровня калия при острой и хронической почечной недостаточности.
2.Контроль уровня калия при нарушениях ритма сердца.
3.Диагностика и мониторинг лечения надпочечниковой недостаточности.
4.Мониторинг терапии диуретиками.
Референтные интервалы калия в крови: 3,3-5,5 ммоль/л
Правила подготовки
- Необходимо исключить факторы, влияющие на результаты исследований: физическую нагрузку (бег, подъем по лестнице, подъем тяжестей), тепловые процедуры (посещение бани, сауны), эмоциональное возбуждение.
- Перед забором крови следует отдохнуть 10-15 минут в приемной, успокоиться.
- Исключить прием алкоголя за 1-2 дня до исследования.
- За 1 час до исследования исключить курение.
- Кровь не следует сдавать после рентгенографии, физиотерапевтических воздействий, после проведения диагностических или лечебных процедур.

- Анализ сдают натощак. «Натощак» — это когда между последним приемом пищи и взятием крови проходит не менее 8 ч (желательно — не менее 12 ч). Можно только пить воду. Накануне исследования следует избегать пищевых перегрузок.
- При исследовании крови учитывают влияние принимаемых лекарственных препаратов. Если прием лекарственного средства обязателен и исследование проводится на фоне приема препарата, об этом необходимо делать отметку на направлении
Биологи из МГУ исследовали состав, свойства и функции белка миокина
Сотрудники биологического факультета МГУ имени М.В. =Ломоносова изучили механизм транскрипции и секреции миокинов в скелетной мускулатуре. Результаты исследования ученых были опубликованы в журнале Biochemical and Biophysical Research Communication.
Миокины — это белки, которые образуются в организме в ответ на мышечное сокращение. Они регулируют деятельность костной и жировой тканей, головного мозга, молочных желез, а также органов пищеварения. Образование миокинов состоит из двух этапов: транскрипции, то есть переписывания информации с генов ДНК на информационную РНК, и трансляции — непосредственной сборки молекул миокина.
Образование миокинов состоит из двух этапов: транскрипции, то есть переписывания информации с генов ДНК на информационную РНК, и трансляции — непосредственной сборки молекул миокина.
«Впервые было показано изменение соотношения внутриклеточных концентраций натрия и калия в клетках мускулатуры мыши при их электростимуляции, что подтверждает возможность использования данной in vitro модели для изучения процессов ионного транспорта в работающей мускулатуре», — рассказал Кирилл Данилов, один из авторов статьи, сотрудник биологического факультета МГУ.
Ионы калия и натрия играют важную роль в клетках мышц. Ионы (частицы, обладающие электрическим зарядом, в данном случае — заряженные положительно калий и натрий) формируют электрический потенциал мембран клеток. За счет ионного транспорта, то есть проникновения через мембрану внутрь клетки или выхода из нее натрия и калия, возникает разность потенциалов снаружи и внутри мембраны. Вследствие такого обмена ионами осуществляется проведение возбуждения в мышечных волокнах.
При проведении атомно-абсорбционной спектроскопии (ААС), вестерн-блоттинга и электростимуляции ученые исследовали процесс образования миокина, его структуру и значение для организма человека. ААС — это способ определения химического состава образца. С помощью вестерн-блоттинга можно распознать особый тип белка в сложных веществах. При воздействии на мышцы электрическими импульсами вызывается интенсивный переход ионов калия и натрия через мембрану клетки.
«Полученные в данной работе данные позволяют оптимизировать дальнейшее использование модели и проведение экспериментов по транскрипции белка. Это поможет раскрыть механизм регуляции транскрипции на клеточном уровне в скелетной мускулатуре, в частности транскрипции миокинов, обладающих большим терапевтическим потенциалом», — пояснил ученый.
Физические нагрузки способствуют процессу активной транскрипции миокинов, которые ускоряют метаболические процессы, связанные с повышенной нагрузкой на мышечную ткань. Таким образом, объяснив процесс образования в организме этих белков, врачи смогут проводить коррекции различных расстройств, которые связаны со сложной адаптацией организма к физическим нагрузкам после тяжелых травм.
Таким образом, объяснив процесс образования в организме этих белков, врачи смогут проводить коррекции различных расстройств, которые связаны со сложной адаптацией организма к физическим нагрузкам после тяжелых травм.
Исследование выполнено совместно с учеными из Сколковского института науки и технологий, а также Томского государственного университета.
Исследование выполнено при поддержке гранта Российского научного фонда (РНФ).
Рассказать об открытии можно, заполнив следующую форму.
Роль калия | SpringerLink
Раздел
- 2 Цитаты
- 269 Загрузки
Abstract
Калий — один из основных минералов крови или электролитов, необходимых как для клеточной, так и для электрической функции. Калий — это первичный положительный ион или катион, обнаруженный в клетках, где содержится более 90% всех запасов калия в организме. Наряду с натрием калий регулирует водный баланс и кислотно-щелочной баланс в крови и тканях, а также играет важную роль в передаче электрических импульсов в сердце. Активный транспорт калия в клетки и из них имеет решающее значение для сердечно-сосудистой и нервной функций. Когда калий проникает в клетку, он вызывает обмен натрия и калия через клеточную мембрану.В нервных клетках это создает электрический потенциал, который позволяет проводить нервные импульсы. Когда калий покидает клетку, он восстанавливает реполяризацию клетки, что позволяет нервному импульсу развиваться. Этот градиент электрического потенциала способствует сокращению мышц и регулирует сердцебиение. Нормальный уровень калия в сыворотке составляет от 3,6 до 5,0 ммоль / л. Если уровень общего калия в организме снижается всего на 1% (35 ммоль), возникает серьезный дисбаланс внутриклеточного и внеклеточного калия.
Калий — это первичный положительный ион или катион, обнаруженный в клетках, где содержится более 90% всех запасов калия в организме. Наряду с натрием калий регулирует водный баланс и кислотно-щелочной баланс в крови и тканях, а также играет важную роль в передаче электрических импульсов в сердце. Активный транспорт калия в клетки и из них имеет решающее значение для сердечно-сосудистой и нервной функций. Когда калий проникает в клетку, он вызывает обмен натрия и калия через клеточную мембрану.В нервных клетках это создает электрический потенциал, который позволяет проводить нервные импульсы. Когда калий покидает клетку, он восстанавливает реполяризацию клетки, что позволяет нервному импульсу развиваться. Этот градиент электрического потенциала способствует сокращению мышц и регулирует сердцебиение. Нормальный уровень калия в сыворотке составляет от 3,6 до 5,0 ммоль / л. Если уровень общего калия в организме снижается всего на 1% (35 ммоль), возникает серьезный дисбаланс внутриклеточного и внеклеточного калия. Этот дисбаланс изменяет электрофизиологические свойства клеточной мембраны и оказывает пагубное воздействие на генерацию импульсов и их проведение по всему сердцу [1].
Этот дисбаланс изменяет электрофизиологические свойства клеточной мембраны и оказывает пагубное воздействие на генерацию импульсов и их проведение по всему сердцу [1].
Ключевые слова
Застойная сердечная недостаточность Диуретическая терапия Сыворотка Уровень калия Потребление калия Добавки калияЭти ключевые слова были добавлены машиной, а не авторами. Этот процесс является экспериментальным, и ключевые слова могут обновляться по мере улучшения алгоритма обучения.
Это предварительный просмотр содержимого подписки,
войдите в, чтобы проверить доступ.
Предварительный просмотр
Невозможно отобразить предварительный просмотр. Скачать превью PDF.
Список литературы
1.
Podrid PJ. Калиевые и желудочковые аритмии. Am J Cardiol 1990; 65: 33E – 44E.
PubMedCrossRefGoogle Scholar2.
Gennari FJ. Гипокалиемия. N Engl J Med 1998; 339: 451–58.
PubMedCrossRefGoogle Scholar3.

Cohn JN, Kowey PR, Whelton PK, Prisant M. Новые рекомендации по замещению калия в клинической практике: современный обзор Национального совета по применению калия в клинической практике.Arch Intern Med 2000; 160: 2429–36.
PubMedCrossRefGoogle Scholar4.
Tannen RL. Калиевые нарушения. В: Кокко Дж. П., Таннен Р. Л., редакторы. Жидкости и электролиты, 3
рдизд. Филадельфия, Пенсильвания: WB Saunders, 1996: Глава 3.
Google Scholar5.
Купер Х.А., Дрис Д.Л., Дэвис К.Э., Шен Ю.Л., Домански М.Дж. Диуретики и риск смерти от аритмии у пациентов с дисфункцией левого желудочка. Тираж 1999 г .; 100: 1311–15.
PubMedCrossRefGoogle Scholar6.
Khaw K-T, Barrett-Connor E. Диетический калий и смертность, связанная с инсультом: 12-летнее проспективное популяционное исследование. N Engl J Med 1987; 316: 235–40.
PubMedCrossRefGoogle Scholar7.
Belanger CF, Hennekens CH, Rosner B, Speizer FE.
PubMedGoogle Scholar Исследование здоровья медсестер. Am J Nurs 1978; 78: 1039–40.
Исследование здоровья медсестер. Am J Nurs 1978; 78: 1039–40.8.
Совместная исследовательская группа INTERSALT. INTERSALT: Международное исследование экскреции электролитов и артериального давления: результаты суточной экскреции натрия и калия с мочой.BMJ 1988; 297: 319–28.
CrossRefGoogle Scholar9.
Whelton PK, He J, Cutler JA, et al. Влияние перорального калия на артериальное давление: метаанализ рандомизированных контролируемых клинических исследований. JAMA 1997; 277: 1624–32.
PubMedCrossRefGoogle Scholar10.
Nolan J, Batin PD, Andrews R, et al. Проспективное исследование вариабельности сердечного ритма и смертности при хронической сердечной недостаточности: результаты оценки сердечной недостаточности в Соединенном Королевстве и оценка исследования риска (UK-heart).Тираж 1998 г .; 98: 1510–16.
PubMedCrossRefGoogle Scholar11.
Grobbee DE, Hoes AW. Несберегающие калий диуретики и риск внезапной сердечной смерти.
PubMedGoogle Scholar J Hypertens 1995; 13: 1539–45.
J Hypertens 1995; 13: 1539–45.12.
Duke M. Гипокалиемия, индуцированная тиазидом: связь с острым инфарктом миокарда и фибрилляцией желудочков. JAMA 1978; 239 (1) 43–45.
PubMedCrossRefGoogle Scholar13.
Kowey PR.Неопубликованные данные.
Google Scholar
Информация об авторских правах
© Springer Science + Business Media New York 2002
Авторы и аффилированные лица
Нет данных о членстве
Как калий попадает в клетки?
Сбалансированное калийное хозяйство имеет решающее значение для выживания как людей, так и бактерий. Поскольку бактерии подвержены гораздо большим колебаниям условий окружающей среды, контролируемое потребление калия часто представляет собой особую проблему.Поскольку клеточная мембрана непроницаема для ионов калия, она должна перемещаться через определенные мембранные транспортные белки.
С одной стороны, калиевые каналы обеспечивают быстрый, но пассивный приток ионов калия. Это прекращается, как только достигается электрохимическое равновесие между клеткой и окружающей средой. Для достижения более высоких внутриклеточных концентраций калий активно транспортируется в клетку через калиевые насосы, при этом энергия расходуется в форме АТФ.
Это прекращается, как только достигается электрохимическое равновесие между клеткой и окружающей средой. Для достижения более высоких внутриклеточных концентраций калий активно транспортируется в клетку через калиевые насосы, при этом энергия расходуется в форме АТФ.
Поскольку оба семейства белков — каналы и насосы — выполняют очень разные функции, они всегда описывались как отдельные друг от друга. Этому, однако, противоречит наблюдение, что KdpFABC, высокоаффинная, активная система бактерий, поглощающая калий, не представляет собой простой насос, а состоит из четырех различных белков. Один из них происходит от типичного насоса, а другой напоминает калиевый канал.
Инга Хенельт, доцент кафедры биохимии в Университете Гете, и ее коллега Кристина Паулино из Университета Гронингена, Нидерланды, поэтому решили поближе взглянуть на мембранный белок KdpFABC через микроскоп, или, точнее, криоэлектрон. микроскоп.Результат их удивил: «Все предыдущие гипотезы были ошибочными», — утверждает Инга Хенельт. «Несмотря на то, что перед нами были все данные, нам потребовалось время, чтобы понять, каким образом калий проходит через комплекс в клетку».
«Несмотря на то, что перед нами были все данные, нам потребовалось время, чтобы понять, каким образом калий проходит через комплекс в клетку».
Во-первых, канальный белок связывает калий и транспортирует его через первый туннель к помпе. По прибытии первый, обращенный наружу туннель закрывается, а второй, обращенный внутрь туннель, открывается. Этот туннель также проходит между обоими белками и в конечном итоге заканчивается внутри клетки.«Этот комплекс по сути сочетает в себе лучшие качества обоих семейств белков», — объясняет Шарлотт Сток, докторант исследовательской группы Инге Хэнельт. «Каналоподобный белок связывает калий, сначала очень специфично и с высоким сродством, в то время как помпа обеспечивает активный транспорт, который может обогащать калий в клетке в 10 000 раз».
Данные, недавно опубликованные в журнале Nature Communications , впечатлили ученых тем, насколько разнообразным может быть перенос через мембраны.«Мы узнали, что при исследовании различных белков мембранного транспорта мы не должны полагаться на кажущиеся неопровержимыми механизмы, но должны быть готовы к сюрпризам», — резюмирует Инга Хенельт.
###
Публикация: Charlott Stock, Lisa Hielkema, Igor Tascon, Dorith Wunnicke, Gert T. Oostergetel, Mikel Azkargorta, Cristina Paulino, Inga Hänelt, Крио-ЭМ структуры KdpFABC предполагают механизм транспорта K + через два межсубъединичных полуканала, в : Nature Communications , 10.1038 / s41467-018-07319-2
Изображение можно скачать по адресу: http: // www.
Подпись: Наружные и внутренние открывающиеся структуры KdpFABC в клеточной мембране. Предоставлено: исследовательская группа Инги Ханельт.
Дополнительная информация: д-р Инга Хенельт, Институт биохимии, факультет 14, кампус Ридберг, телефон: +49 69 798-29262, [email protected].
Текущие новости науки, образования и общества в GOETHE-UNI онлайн (http: // www.
Университет Гете — это научно-исследовательский университет в европейском финансовом центре Франкфурта. Университет был основан в 1914 году за счет частных средств, в основном еврейских спонсоров, и с тех пор добился новаторских достижений в области социальных наук, социологии и экономики. медицина, квантовая физика, исследования мозга и трудовое право. 1 января 2008 года он получил уникальный уровень автономии, вернувшись к своим историческим корням как «университет-основатель».Сегодня он входит в десятку лучших по внешнему финансированию и входит в тройку крупнейших университетов Германии с тремя кластерами передового опыта в области медицины, наук о жизни и гуманитарных наук. Вместе с Техническим университетом Дармштадта и Майнцским университетом он выступает в качестве партнера межгосударственного стратегического альянса Рейн-Майн университетов. Интернет: http: // www.
Университет был основан в 1914 году за счет частных средств, в основном еврейских спонсоров, и с тех пор добился новаторских достижений в области социальных наук, социологии и экономики. медицина, квантовая физика, исследования мозга и трудовое право. 1 января 2008 года он получил уникальный уровень автономии, вернувшись к своим историческим корням как «университет-основатель».Сегодня он входит в десятку лучших по внешнему финансированию и входит в тройку крупнейших университетов Германии с тремя кластерами передового опыта в области медицины, наук о жизни и гуманитарных наук. Вместе с Техническим университетом Дармштадта и Майнцским университетом он выступает в качестве партнера межгосударственного стратегического альянса Рейн-Майн университетов. Интернет: http: // www.
Издатель: Президент Университета Гете Редактор: Доктор Энн Харди, референт отдела научных коммуникаций, PR и коммуникаций, Theodor-W.-Adorno-Platz 1, 60323 Франкфурт-на-Майне, тел . : (069) 798-13035, факс: (069) 798-763 12531
: (069) 798-13035, факс: (069) 798-763 12531
Заявление об ограничении ответственности: AAAS и EurekAlert! не несут ответственности за точность выпусков новостей, размещенных на EurekAlert! участвующими учреждениями или для использования любой информации через систему EurekAlert.
Внутренний баланс калия — переход в клетки
Калий является чрезвычайно важным электролитом в организме и играет жизненно важную роль в поддержании мембранного потенциала покоя клеток.Даже небольшое изменение внеклеточной концентрации K + может значительно деполяризовать или гиперполяризовать клетки, что, помимо прочего, имеет большое значение для сердечной функции.
Концепция поддержания внутреннего баланса K + относится к его движению между внеклеточной жидкостью (ECF) и внутриклеточной жидкостью (ICF) . Нормальные концентрации K + находятся между 3,5-5,0 ммоль / л в ECF и между 120-150 ммоль / л внутриклеточно.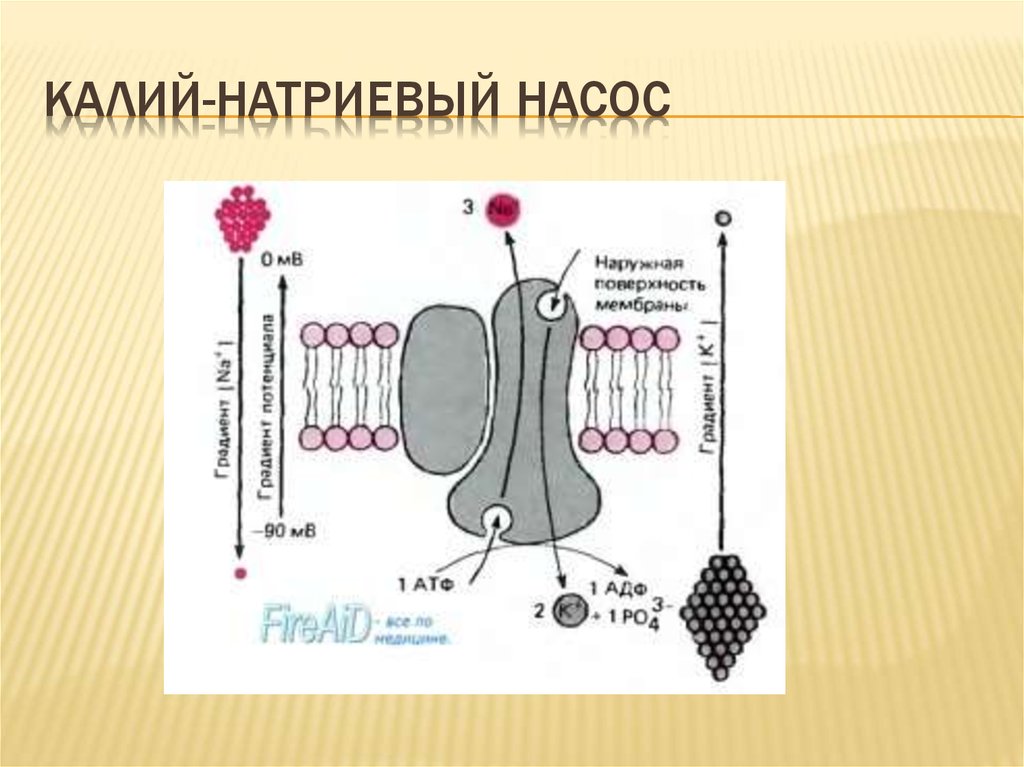 98% K + в организме хранится внутриклеточно.
98% K + в организме хранится внутриклеточно.
Механизмы замещения K
+ в ячейкиУвеличение [K + ] в ECF будет способствовать перемещению K + в клетки вниз по градиенту его концентрации. Однако внутренний баланс K + не так прост, и необходимо учитывать другие факторы.
Когда мы едим, инсулин секретируется поджелудочной железой в ответ на повышение концентрации K + в крови.Это увеличивает активность Na + / K + -АТФаза , таким образом перемещая избыток K + в клетки. Этот гомеостатический механизм помогает предотвратить опасное повышение [K + ] после еды. Другие гормоны, которые действуют на каналы Na + / K + -АТФазы, включают альдостерон и катехоламины .
Алкалоз также вызывает снижение ECF [K + ]. Это связано с тесной взаимосвязью [K + ] с pH ECF. Уменьшение концентрации ионов H + (т.е. увеличение pH) приведет к переносу ионов H + из клеток. Это вызывает обратный сдвиг K + в клетки, тем самым снижая концентрацию K + в ECF. И наоборот, увеличение концентрации ионов H + (ацидоз) заставляет H + перемещаться в клетки, вытягивая K + наружу.
Уменьшение концентрации ионов H + (т.е. увеличение pH) приведет к переносу ионов H + из клеток. Это вызывает обратный сдвиг K + в клетки, тем самым снижая концентрацию K + в ECF. И наоборот, увеличение концентрации ионов H + (ацидоз) заставляет H + перемещаться в клетки, вытягивая K + наружу.
Механизмы выдвижения K
+ из ячеекНизкая концентрация ECF K + способствует перемещению K + из клеток вниз по градиенту его концентрации.
Во время упражнения скелетные мышцы сокращаются, вызывая чистый выброс K + из этих клеток. Это приводит к увеличению ECF [K + ] пропорционально интенсивности упражнений. Гиперкалиемия предотвращается за счет поглощения K + другими несокращающимися клетками.
Кроме того, упражнения вызывают выброс катехоламинов , например адреналин, который увеличивает захват K + другими клетками через каналы Na + / K + -ATPase , как упоминалось ранее. При прекращении упражнений это может привести к кратковременной гипокалиемии.
Ацидоз также вызывает повышение концентрации ECF K + . Лизис клеток также вызовет высвобождение внутриклеточного K + в ECF.Если тоничность плазмы увеличивается, вода покидает клетки, чтобы компенсировать это. Это увеличит внутриклеточную концентрацию K + , заставляя его покинуть клетку и войти в ECF вниз по градиенту концентрации.
Рис. 2. Диаграмма, показывающая движение калия из клеток. [/ caption][старт-клиника]
Клиническая значимость — гипокалиемия
Гипокалиемия определяется как внеклеточная [K + ] <3. 5 ммоль / л . Обычно это происходит из-за нарушения внутреннего баланса или повышенной потери калия из почек или из других источников. Проблема с внутренним балансом — метаболический алкалоз (например, диабетический кетоацидоз). Это связано с тем, что, когда концентрация ионов H + в ECF низкая, они переносятся из клеток в обмен на K + , что приводит к гипокалиемии. Чрезмерная потеря калия происходит из-за почечной или непочечной потери. Потеря K + через почки может происходить при использовании определенных типов диуретиков или при наличии осмотического диуреза в результате сахарного диабета. Диарея и рвота — два примера непочечных потерь K + .
5 ммоль / л . Обычно это происходит из-за нарушения внутреннего баланса или повышенной потери калия из почек или из других источников. Проблема с внутренним балансом — метаболический алкалоз (например, диабетический кетоацидоз). Это связано с тем, что, когда концентрация ионов H + в ECF низкая, они переносятся из клеток в обмен на K + , что приводит к гипокалиемии. Чрезмерная потеря калия происходит из-за почечной или непочечной потери. Потеря K + через почки может происходить при использовании определенных типов диуретиков или при наличии осмотического диуреза в результате сахарного диабета. Диарея и рвота — два примера непочечных потерь K + .
Клинические особенности гипокалиемии
Слабость мышц — изменения мембранного потенциала в состоянии покоя могут изменить возбудимость скелетных мышц. Это может затруднить сокращение мышц, что приведет к их слабости.
Паралитическая кишечная непроходимость — на гладкую мускулатуру кишечника также могут влиять изменения мембранного потенциала покоя, потенциально вызывая паралитическую кишечную непроходимость.Здесь перистальтика кишечника замедляется или полностью останавливается, что может привести к непроходимости кишечника.
Несахарный нефрогенный диабет — гипокалиемия также может привести к тому, что почки перестают реагировать на антидиуретический гормон (АДГ). В результате нефроны имеют пониженную способность реабсорбировать воду.
На сердечную функцию также влияет из-за увеличения химического градиента K + . Это, в свою очередь, делает сердечные клетки более возбудимыми. Связанные с этим изменения ЭКГ включают:
- Малые или инвертированные зубцы T
- Выраженные зубцы U
- Депрессия сегмента ST (при тяжелой гипокалиемии)
Лечение
Гипокалиемию можно лечить с помощью i. v. или оральная заместительная терапия K + . Однако более конкретные методы лечения могут варьироваться в зависимости от причины гипокалиемии. Например, если причиной является повышенная активность минералокортикоидов, можно использовать щадящие диуретики K + , такие как амилорид или спиронолактон.
v. или оральная заместительная терапия K + . Однако более конкретные методы лечения могут варьироваться в зависимости от причины гипокалиемии. Например, если причиной является повышенная активность минералокортикоидов, можно использовать щадящие диуретики K + , такие как амилорид или спиронолактон.
Гиперкалиемия
Гиперкалиемия — это когда в ЭКФ вне клеток и в крови слишком много K + . Чтобы узнать об этом больше, нажмите здесь.
Рис. 3. Изменения ЭКГ при гипокалиемии.[/подпись][окончание клинической]
Как транспортируется калий? | Здоровое питание
Калий действует в организме как минерал и электролит. Как минерал, он способствует развитию и функционированию тканей и органов. Как электролизер, он помогает проводить электричество и обеспечивает правильную нервную проводимость, сокращение мышц и работу сердца. Хотя молекулы калия действуют как одинокие следопыты в кровотоке — перемещаясь свободно и независимо, — им необходимы либо активные, либо пассивные силы, чтобы входить и выходить из клеток.
Где это находится
Большая часть ионов калия в организме остается внутри клеток. Фактически, калий — это самый распространенный положительно заряженный ион внутри клеточных стенок. Оставшееся количество калия можно найти в кровотоке. Положительные ионы также находятся в пищеварительном тракте — они абсорбируются из тонкого кишечника после употребления с пищей, а также удаляются из организма после фильтрации через почки и толстую кишку.
Каналы и заряды
Определенные калиевые каналы расположены вдоль клеточных стенок.Ионы калия входят и выходят из клетки только по этим каналам. Эти каналы открываются и закрываются при изменении мембранного потенциала. Мембранный потенциал — это разность напряжений внутри и снаружи клетки. Жидкость вне клеток содержит большое количество положительно заряженных ионов натрия и отрицательно заряженных ионов хлора, тогда как жидкость внутри клетки содержит большое количество положительно заряженных ионов калия и отрицательно заряженных белков.
Пассивные силы
Три отдельные силы пассивно влияют на движение калия по каналам клеток.Поскольку внутри клетки обычно находится большое количество ионов калия, возникает химический градиент, который выталкивает калий из клетки, чтобы восстановить баланс химической концентрации. Но как только ионы калия выталкиваются из клетки, они автоматически возвращаются обратно в клетку — положительный заряд молекулы притягивается к отрицательному заряду белков внутри клетки, создавая электрический градиент. Химический и электрический градиенты борются друг с другом, поскольку они побуждают калий двигаться в противоположных направлениях — это создает электрохимический градиент.В конечном итоге этот электрохимический градиент определяет, сколько ионов калия фактически перемещается по калиевым каналам. Ионы калия будут продолжать поступать в ячейку и выходить из нее до тех пор, пока не будет установлен уровень равновесия.
Натрий-калиевый насос
Химические, электрические и электрохимические градиенты представляют собой пассивные силы, позволяющие калию свободно перемещаться по каналам в зависимости от градиентов. Но калий также переносится через активную силу — натриево-калиевый насос.Эти насосы разбросаны по клеточным мембранам, вкраплены между пассивными ионными каналами и требуют для работы молекул энергии. Поскольку ионы натрия постоянно просачиваются в ячейку, основная функция насоса — поддерживать баланс между электрическими зарядами внутри и снаружи ячейки. Когда слишком много ионов натрия просочилось в ячейку, насос выбрасывает три отрицательно заряженных иона натрия из ячейки и переносит два положительно заряженных иона калия в ячейку.
Но калий также переносится через активную силу — натриево-калиевый насос.Эти насосы разбросаны по клеточным мембранам, вкраплены между пассивными ионными каналами и требуют для работы молекул энергии. Поскольку ионы натрия постоянно просачиваются в ячейку, основная функция насоса — поддерживать баланс между электрическими зарядами внутри и снаружи ячейки. Когда слишком много ионов натрия просочилось в ячейку, насос выбрасывает три отрицательно заряженных иона натрия из ячейки и переносит два положительно заряженных иона калия в ячейку.
Ссылки
Биография писателя
Криста Шихан — дипломированная медсестра и профессиональный писатель.Она работает в отделении интенсивной терапии новорожденных (NICU), и ее предыдущий опыт медсестры включает гериатрию, легочные заболевания и уход на дому. Ее профессиональные писательские работы сосредоточены в основном на вопросах физического здоровья, фитнеса, питания и позитивных изменений образа жизни.
Калий (K) в анализе крови
Обзор теста
Тест на калий проверяет количество калия в крови. Калий является одновременно электролитом и минералом. Это помогает сохранить воду (количество жидкости внутри и вне клеток тела) и электролитный баланс в организме.Калий также важен для работы нервов и мышц.
Калий является одновременно электролитом и минералом. Это помогает сохранить воду (количество жидкости внутри и вне клеток тела) и электролитный баланс в организме.Калий также важен для работы нервов и мышц.
Уровень калия часто меняется в зависимости от уровня натрия. Когда уровень натрия повышается, уровень калия понижается, а когда уровень натрия понижается, уровень калия повышается. На уровень калия также влияет гормон альдостерон, который вырабатывается надпочечниками.
Уровень калия может зависеть от того, как работают почки, pH крови, количество потребляемого калия, уровень гормонов в вашем теле, сильная рвота и прием определенных лекарств, таких как диуретики и добавки калия.Некоторые методы лечения рака, которые разрушают раковые клетки, также могут повысить уровень калия.
Многие продукты богаты калием, включая бананы, апельсиновый сок, шпинат и картофель. В сбалансированной диете достаточно калия для нужд организма. Но если у вас низкий уровень калия, вашему организму может потребоваться некоторое время, чтобы начать удерживать калий.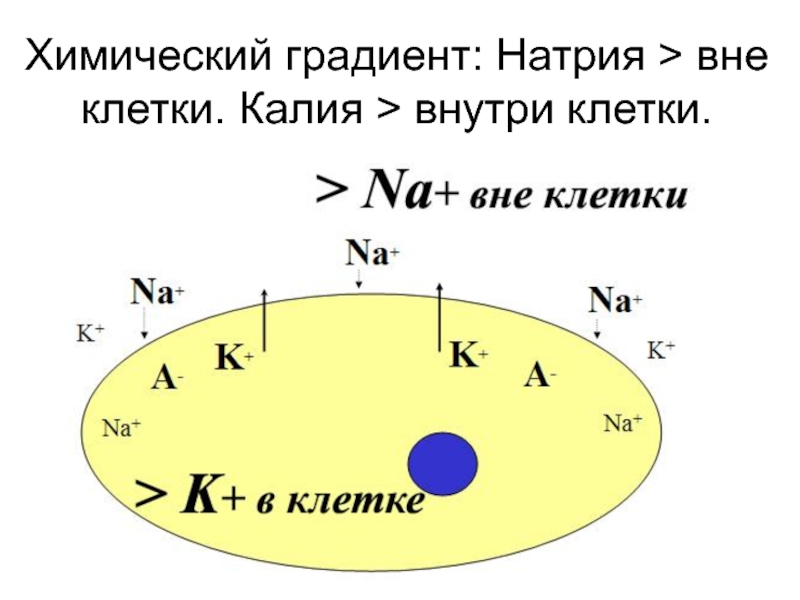 Тем временем калий по-прежнему выводится с мочой, поэтому в конечном итоге уровень калия в организме может быть очень низким, что может быть опасно.
Тем временем калий по-прежнему выводится с мочой, поэтому в конечном итоге уровень калия в организме может быть очень низким, что может быть опасно.
Слишком высокий или слишком низкий уровень калия может быть серьезным. Аномальный уровень калия может вызывать такие симптомы, как мышечные судороги или слабость, тошнота, диарея, частое мочеиспускание, обезвоживание, низкое кровяное давление, спутанность сознания, раздражительность, паралич и изменения сердечного ритма.
Другие электролиты, такие как натрий, кальций, хлорид, магний и фосфат, можно проверять в образце крови одновременно с анализом крови на калий.
Почему это делается
Анализ крови на калий сдают по номеру:
- Проверяйте уровни у людей, получающих лечение такими лекарствами, как диуретики, и у людей, находящихся на диализе почек.
- Проверьте, работает ли лечение слишком низкого или слишком высокого уровня калия.

- Проверьте людей с высоким кровяным давлением, у которых могут быть проблемы с почками или надпочечниками.
- Проверьте влияние дополнительного питания (общего парентерального питания [TPN]) на уровень калия.
- Проверьте, не вызывают ли определенные виды лечения рака слишком много клеток (лизис клеток). Синдром лизиса клеток вызывает очень высокий уровень некоторых электролитов, в том числе калия.
Как подготовить
В общем, вам ничего не нужно делать до этого теста, если только ваш врач не скажет вам об этом.
Как это делается
Медицинский работник с помощью иглы берет образец крови, обычно из руки.
Часы
Каково это
При взятии пробы крови игла может вообще ничего не чувствовать. Или вы можете почувствовать укол или ущипнуть.
Риски
Вероятность возникновения проблемы из-за этого теста очень мала. При заборе крови на месте может образоваться небольшой синяк.
При заборе крови на месте может образоваться небольшой синяк.
Результаты
Тест на калий проверяет количество калия в крови. Калий — это электролит и минерал.
Нормальные значения, перечисленные здесь, называемые контрольным диапазоном, являются лишь ориентировочными. Эти диапазоны варьируются от лаборатории к лаборатории, и ваша лаборатория может иметь другой диапазон от нормального.Отчет вашей лаборатории должен содержать диапазон, который использует ваша лаборатория. Кроме того, ваш врач оценит ваши результаты на основе вашего здоровья и других факторов. Это означает, что значение, выходящее за пределы нормальных значений, перечисленных здесь, может быть нормальным для вас или вашей лаборатории.
Уровень калия в крови также меняется с возрастом.
Результаты готовы за 1 день.
На уровень калия могут влиять многие состояния. Врач обсудит с вами любые отклонения от нормы, которые могут быть связаны с вашими симптомами и состоянием здоровья в прошлом.
Высокие значения
- Высокий уровень калия в крови может быть вызван повреждением почек. Это мешает почкам нормально выводить калий из крови.
- Высокий уровень калия в крови также может быть вызван условиями, при которых калий перемещается из клеток организма в кровь. Эти состояния включают тяжелые ожоги, тяжелые травмы, сердечный приступ и диабетический кетоацидоз.
- Прием слишком большого количества добавок калия также может вызвать высокий уровень калия в крови.
- Слишком много кислоты (pH) в крови повышает уровень калия, заставляя калий в клетках тела «просачиваться» из клеток в кровь.
- Некоторые лекарства, такие как антагонисты альдостерона и ингибиторы ангиотензинпревращающего фермента (АПФ), могут вызывать высокий уровень калия.
Низкие значения
- Низкий уровень калия в крови может быть вызван высоким уровнем альдостерона (гиперальдостеронизм), вырабатываемым надпочечниками.

- Другие состояния, которые могут вызывать низкий уровень калия в крови, включают тяжелые ожоги, муковисцидоз, расстройство, связанное с употреблением алкоголя, синдром Кушинга, обезвоживание, недоедание, рвоту, диарею и некоторые заболевания почек, такие как синдром Барттера. Синдром Барттера — это состояние, характеризующееся увеличением определенных клеток почек. Это чаще встречается у детей и может быть связано с аномально низким ростом (карликовостью). Причина синдрома Барттера до конца не известна.
- Лекарства, такие как диуретики, являются частой причиной низкого уровня калия.
Список литературы
Цитаты
- Пагана К.Д., Пагана Т.Дж. (2010). Руководство Мосби по диагностическим и лабораторным испытаниям , 4-е изд. Сент-Луис: Мосби Эльзевьер.
Кредиты
Текущий по состоянию на:
23 сентября 2020 г.
Автор: Healthwise Staff
Медицинский обзор:
Адам Хусни, доктор медицины, семейная медицина,
E.Грегори Томпсон, врач-терапевт,
Мартин Дж. Габика, врач, семейная медицина,
По состоянию на: 23 сентября 2020 г.
Автор: Здоровый персонал
Медицинский обзор: Адам Хусни, доктор медицины, семейная медицина, Э. Грегори Томпсон, врач, терапевт, Мартин Дж. Габика, доктор медицины, семейная медицина,
Регулирование гомеостаза калия | Американское общество нефрологии
Abstract
Калий является наиболее распространенным катионом во внутриклеточной жидкости, и поддержание правильного распределения калия через клеточную мембрану имеет решающее значение для нормального функционирования клеток. Долгосрочное поддержание гомеостаза калия достигается за счет изменения почечной экскреции калия в ответ на изменение потребления. Понимание механизма и регулирующих влияний, управляющих внутренним распределением и почечным клиренсом калия при нормальных обстоятельствах, может обеспечить основу для подхода к расстройствам калия, обычно встречающимся в клинической практике. В этой статье рассматриваются ключевые аспекты нормальной регуляции метаболизма калия, и она предназначена для использования в качестве легко доступного обзора для хорошо информированных врачей, а также в качестве ресурса для обучения стажеров и студентов-медиков.
Долгосрочное поддержание гомеостаза калия достигается за счет изменения почечной экскреции калия в ответ на изменение потребления. Понимание механизма и регулирующих влияний, управляющих внутренним распределением и почечным клиренсом калия при нормальных обстоятельствах, может обеспечить основу для подхода к расстройствам калия, обычно встречающимся в клинической практике. В этой статье рассматриваются ключевые аспекты нормальной регуляции метаболизма калия, и она предназначена для использования в качестве легко доступного обзора для хорошо информированных врачей, а также в качестве ресурса для обучения стажеров и студентов-медиков.
Введение
Калий играет ключевую роль в поддержании функции клеток. Почти все клетки обладают Na + -K + -ATPase, которая перекачивает Na + из клетки и K + в клетку и приводит к градиенту K + через клеточную мембрану (K + из > K + из ), который частично отвечает за поддержание разности потенциалов на мембране. Эта разность потенциалов имеет решающее значение для функции клеток, особенно в возбудимых тканях, таких как нервы и мышцы.Организм разработал многочисленные механизмы защиты сыворотки K + . Эти механизмы служат для поддержания правильного распределения K + в организме, а также для регулирования общего содержания K + в организме.
Эта разность потенциалов имеет решающее значение для функции клеток, особенно в возбудимых тканях, таких как нервы и мышцы.Организм разработал многочисленные механизмы защиты сыворотки K + . Эти механизмы служат для поддержания правильного распределения K + в организме, а также для регулирования общего содержания K + в организме.
Внутренний баланс K
+ Почки в первую очередь отвечают за поддержание общего содержания K + в организме путем согласования потребления K + с выделением K + . Регулировка почечной экскреции K + происходит в течение нескольких часов; следовательно, изменения во внеклеточной концентрации K + первоначально буферизируются перемещением K + внутрь или из скелетных мышц.Регулирование распределения K + между внутриклеточным и внеклеточным пространством упоминается как внутренний баланс K + . Наиболее важными факторами, регулирующими это движение в нормальных условиях, являются инсулин и катехоламины (1).
После еды постпрандиальное высвобождение инсулина не только регулирует концентрацию глюкозы в сыворотке, но и перемещает диетические K + в клетки, пока почки не выведут нагрузку K + , восстанавливая гомеостаз K + .Эти эффекты опосредованы связыванием инсулина с рецепторами клеточной поверхности, что стимулирует захват глюкозы в тканях, чувствительных к инсулину, за счет встраивания белка-переносчика глюкозы GLUT4 (2,3). Повышение активности Na + -K + -ATPase опосредует захват K + (рис. 1). У пациентов с метаболическим синдромом или ХБП поглощение глюкозы, опосредованное инсулином, нарушено, но клеточное поглощение K + остается нормальным (4,5), демонстрируя дифференциальную регуляцию опосредованного инсулином поглощения глюкозы и поглощения K + .
Рисунок 1. Клеточная модель иллюстрирует β 2 -адренергические и инсулино-опосредованные регуляторные пути для поглощения K + . β 2 -Адренергический агент и инсулин оба приводят к захвату K + за счет стимуляции активности насоса Na + -K + -АТФазы в основном в скелетных мышцах, но они делают это через разные сигнальные пути. β 2 -Адренергическая стимуляция приводит к увеличению активности насоса через цАМФ и протеинкиназу А (PKA) -зависимый путь.Связывание инсулина с его рецептором приводит к фосфорилированию субстратного белка рецептора инсулина (IRS-1), который, в свою очередь, связывается с фосфатидилинозитид-3-киназой (PI3-K). Взаимодействие IRS-1 – PI3-K приводит к активации 3-фосфоинозитид-зависимой протеинкиназы-1 (PDK1). Стимулирующий эффект инсулина на поглощение глюкозы и поглощение K + в этой точке расходятся. Akt-зависимый путь отвечает за встраивание в мембрану переносчика глюкозы GLUT4, тогда как активация атипичной протеинкиназы C (aPKC) приводит к встраиванию в мембрану насоса Na + -K + -ATPase (см.
β 2 -Адренергический агент и инсулин оба приводят к захвату K + за счет стимуляции активности насоса Na + -K + -АТФазы в основном в скелетных мышцах, но они делают это через разные сигнальные пути. β 2 -Адренергическая стимуляция приводит к увеличению активности насоса через цАМФ и протеинкиназу А (PKA) -зависимый путь.Связывание инсулина с его рецептором приводит к фосфорилированию субстратного белка рецептора инсулина (IRS-1), который, в свою очередь, связывается с фосфатидилинозитид-3-киназой (PI3-K). Взаимодействие IRS-1 – PI3-K приводит к активации 3-фосфоинозитид-зависимой протеинкиназы-1 (PDK1). Стимулирующий эффект инсулина на поглощение глюкозы и поглощение K + в этой точке расходятся. Akt-зависимый путь отвечает за встраивание в мембрану переносчика глюкозы GLUT4, тогда как активация атипичной протеинкиназы C (aPKC) приводит к встраиванию в мембрану насоса Na + -K + -ATPase (см. 3).
3).
Катехоламины регулируют внутреннее распределение K + , при этом α -адренергических рецепторов нарушают и β -адренергические рецепторы способствуют проникновению в клетки K + . β 2 -индуцированная рецептором стимуляция захвата K + опосредуется активацией насоса Na + -K + -ATPase. Эти эффекты играют роль в регулировании клеточного высвобождения K + во время упражнений (6).
В нормальных условиях упражнения связаны с перемещением внутриклеточного K + в интерстициальное пространство скелетных мышц.Увеличение интерстициального K + может достигать 10–12 мМ при тяжелых физических нагрузках. Накопление K + является фактором, ограничивающим возбудимость и сократительную силу мышц, что приводит к развитию утомления (7,8). Кроме того, увеличение интерстициального K + играет роль в быстрой вазодилатации, что позволяет увеличить кровоток в тренирующих мышцах (9). Во время упражнений высвобождение катехоламинов посредством стимуляции β 2 ограничивает рост внеклеточной концентрации K + , который в противном случае происходит в результате нормального высвобождения K + сокращающимися мышцами.Хотя механизм, вероятно, будет многофакторным, истощение всего тела K + может притупить накопление K + в интерстициальном пространстве, ограничивая приток крови к скелетным мышцам и объясняя связь гипокалиемии с рабдомиолизом.
Во время упражнений высвобождение катехоламинов посредством стимуляции β 2 ограничивает рост внеклеточной концентрации K + , который в противном случае происходит в результате нормального высвобождения K + сокращающимися мышцами.Хотя механизм, вероятно, будет многофакторным, истощение всего тела K + может притупить накопление K + в интерстициальном пространстве, ограничивая приток крови к скелетным мышцам и объясняя связь гипокалиемии с рабдомиолизом.
Изменения тонуса плазмы и кислотно-щелочные нарушения также влияют на внутренний баланс K + . Гипергликемия приводит к перемещению воды из внутриклеточного во внеклеточное пространство. Это движение воды способствует истечению K + из ячейки в процессе увлечения растворителем.Кроме того, сокращение клеток вызывает повышение внутриклеточной концентрации K + , создавая более благоприятный градиент концентрации для оттока K + .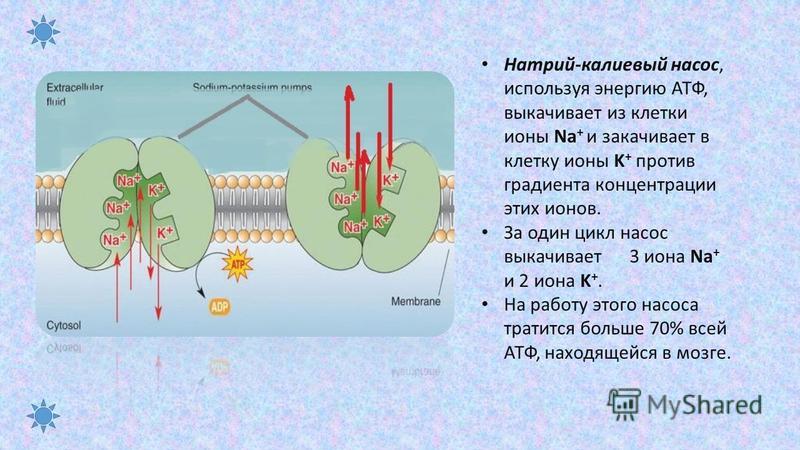 Минеральный ацидоз, но не органический ацидоз, может быть причиной сдвига клеток в K + . Как недавно было рассмотрено, общий эффект ацидемии, вызывающий потерю K + из клеток, обусловлен не прямым обменом K + -H + , а, скорее, явной связью, возникающей в результате эффектов ацидоза. на транспортерах, которые обычно регулируют pH клеток в скелетных мышцах (10) (рис. 2).
Минеральный ацидоз, но не органический ацидоз, может быть причиной сдвига клеток в K + . Как недавно было рассмотрено, общий эффект ацидемии, вызывающий потерю K + из клеток, обусловлен не прямым обменом K + -H + , а, скорее, явной связью, возникающей в результате эффектов ацидоза. на транспортерах, которые обычно регулируют pH клеток в скелетных мышцах (10) (рис. 2).
Влияние метаболического ацидоза на внутренний баланс K + в скелетных мышцах . (A) При метаболическом ацидозе, вызванном неорганическими анионами (минеральный ацидоз), снижение внеклеточного pH снижает скорость обмена Na + -H + (NHE1) и подавляет скорость поступления Na + -3HCO 3 cotransport (NBCe1 и NBCe2). Результирующее падение внутриклеточного Na + снизит активность Na + -K + -АТФазы, вызывая чистую потерю клеточного K + .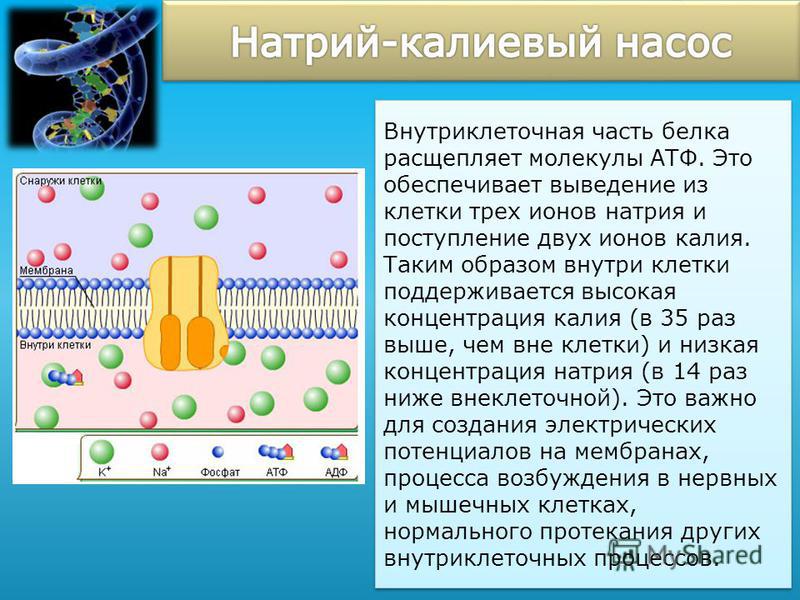 Кроме того, падение внеклеточной концентрации HCO 3 увеличит движение внутрь Cl — за счет обмена Cl-HCO —, дополнительно увеличивая отток K + за счет совместного транспорта K + -Cl —. (B) Потеря K + из клетки намного меньше по величине при метаболическом ацидозе, вызванном органическим ацидозом. В этом случае наблюдается сильный поток внутрь органического аниона и H + через переносчик монокарбоксилата (MCT; MCT1 и MCT4).Накопление кислоты приводит к большему падению внутриклеточного pH, тем самым стимулируя движение внутрь Na + посредством обмена Na + -H + и котранспорта Na + -3HCO 3 . Накопление внутриклеточного Na + поддерживает активность Na + -K + -АТФазы, тем самым сводя к минимуму любые изменения во внеклеточной концентрации K + .
Кроме того, падение внеклеточной концентрации HCO 3 увеличит движение внутрь Cl — за счет обмена Cl-HCO —, дополнительно увеличивая отток K + за счет совместного транспорта K + -Cl —. (B) Потеря K + из клетки намного меньше по величине при метаболическом ацидозе, вызванном органическим ацидозом. В этом случае наблюдается сильный поток внутрь органического аниона и H + через переносчик монокарбоксилата (MCT; MCT1 и MCT4).Накопление кислоты приводит к большему падению внутриклеточного pH, тем самым стимулируя движение внутрь Na + посредством обмена Na + -H + и котранспорта Na + -3HCO 3 . Накопление внутриклеточного Na + поддерживает активность Na + -K + -АТФазы, тем самым сводя к минимуму любые изменения во внеклеточной концентрации K + .
Внутриклеточный K + служит резервуаром для ограничения падения внеклеточных концентраций K + , происходящего при патологических условиях, когда происходит потеря K + из организма. Эффективность этого эффекта продемонстрировали призывники, проходящие летнюю подготовку (11). Эти субъекты были в состоянии поддерживать почти нормальную концентрацию K + в сыворотке, несмотря на ежедневную потерю K + пота на уровне> 40 ммоль и 11-дневный кумулятивный дефицит K + на уровне примерно 400 ммоль.
Эффективность этого эффекта продемонстрировали призывники, проходящие летнюю подготовку (11). Эти субъекты были в состоянии поддерживать почти нормальную концентрацию K + в сыворотке, несмотря на ежедневную потерю K + пота на уровне> 40 ммоль и 11-дневный кумулятивный дефицит K + на уровне примерно 400 ммоль.
Исследования на крысах с использованием метода зажима K + позволили понять роль скелетных мышц в регулировании внеклеточной концентрации K + (12).При использовании этого метода инсулин вводится с постоянной скоростью, и одновременно вводится K + со скоростью, предназначенной для предотвращения любого падения концентрации K + в плазме. Предполагается, что вводимое количество K + равно количеству K + , попадающему во внутриклеточное пространство скелетных мышц.
У крыс, лишенных K + в течение 10 дней, концентрация K + в плазме снизилась с 4,2 до 2,9 ммоль / л. Инсулино-опосредованное исчезновение K + снизилось более чем на 90% по сравнению с контрольными значениями.Это снижение поглощения K + сопровождалось снижением активности и экспрессии мышечной Na + -K + -АТФазы более чем на 50%, что позволяет предположить, что снижение активности помпы может быть причиной снижения эффекта инсулина. Это снижение поглощения мышцами K + в условиях истощения K + может ограничивать чрезмерное падение внеклеточной концентрации K + , которое происходит в условиях стимуляции инсулином. Одновременно снижение экспрессии и активности помпы способствует способности скелетных мышц буферизовать снижение внеклеточных концентраций K + , отдавая некоторые компоненты своих внутриклеточных запасов.
Инсулино-опосредованное исчезновение K + снизилось более чем на 90% по сравнению с контрольными значениями.Это снижение поглощения K + сопровождалось снижением активности и экспрессии мышечной Na + -K + -АТФазы более чем на 50%, что позволяет предположить, что снижение активности помпы может быть причиной снижения эффекта инсулина. Это снижение поглощения мышцами K + в условиях истощения K + может ограничивать чрезмерное падение внеклеточной концентрации K + , которое происходит в условиях стимуляции инсулином. Одновременно снижение экспрессии и активности помпы способствует способности скелетных мышц буферизовать снижение внеклеточных концентраций K + , отдавая некоторые компоненты своих внутриклеточных запасов.
Есть различия между скелетными и сердечными мышцами в ответе на хроническое истощение K + . Хотя скелетная мышца легко отдает K + , чтобы минимизировать падение концентрации K + в плазме, содержание K + в сердечной ткани остается относительно хорошо сохраненным. В отличие от снижения активности и экспрессии Na + -K + -АТФазы в скелетных мышцах, размер пула сердечной Na + -K + -АТФазы увеличивается у животных с дефицитом K + .Это различие объясняет более высокую общую способность клиренса K + после острого введения внутривенного KCl крысам, получавшим диету без K + в течение 2 недель, по сравнению с контрольными группами, содержащими K + (13, 14). Сердечная мышца накапливает значительное количество K + в условиях острой нагрузки. При выражении на основе веса сердечная емкость для поглощения K + сравнима с емкостью скелетных мышц в условиях истощения K + и может фактически превышать емкость скелетных мышц в контрольных условиях.
В отличие от снижения активности и экспрессии Na + -K + -АТФазы в скелетных мышцах, размер пула сердечной Na + -K + -АТФазы увеличивается у животных с дефицитом K + .Это различие объясняет более высокую общую способность клиренса K + после острого введения внутривенного KCl крысам, получавшим диету без K + в течение 2 недель, по сравнению с контрольными группами, содержащими K + (13, 14). Сердечная мышца накапливает значительное количество K + в условиях острой нагрузки. При выражении на основе веса сердечная емкость для поглощения K + сравнима с емкостью скелетных мышц в условиях истощения K + и может фактически превышать емкость скелетных мышц в контрольных условиях.
Почечная обработка калия
Калий свободно фильтруется клубочками. Основная часть отфильтрованного K + реабсорбируется в проксимальном канальце и петле Генле, так что менее 10% отфильтрованной нагрузки достигает дистального нефрона. В проксимальном канальце абсорбция K + в основном пассивна и пропорциональна Na + и воде (Рисунок 3). Реабсорбция K + в толстой восходящей конечности Генле происходит как по трансклеточным, так и по парацеллюлярным путям.Трансклеточный компонент опосредуется транспортом K + на апикальной мембране Na + -K + -2Cl — котранспортером (рис. 4). Секреция K + начинается в раннем дистальном извитом канальце и постепенно увеличивается вдоль дистального нефрона в кортикальный собирательный проток (Рис. 5). Большая часть мочевого K + может быть объяснена электрогенной секрецией K + , опосредованной основными клетками в начальном собирательном канале и кортикальном собирательном канале (Рисунок 6).На апикальной поверхности дистального нефрона также присутствует электронейтральный механизм котранспорта K + и Cl — (15). В условиях истощения K + происходит реабсорбция K + в собирательном канале.
В проксимальном канальце абсорбция K + в основном пассивна и пропорциональна Na + и воде (Рисунок 3). Реабсорбция K + в толстой восходящей конечности Генле происходит как по трансклеточным, так и по парацеллюлярным путям.Трансклеточный компонент опосредуется транспортом K + на апикальной мембране Na + -K + -2Cl — котранспортером (рис. 4). Секреция K + начинается в раннем дистальном извитом канальце и постепенно увеличивается вдоль дистального нефрона в кортикальный собирательный проток (Рис. 5). Большая часть мочевого K + может быть объяснена электрогенной секрецией K + , опосредованной основными клетками в начальном собирательном канале и кортикальном собирательном канале (Рисунок 6).На апикальной поверхности дистального нефрона также присутствует электронейтральный механизм котранспорта K + и Cl — (15). В условиях истощения K + происходит реабсорбция K + в собирательном канале.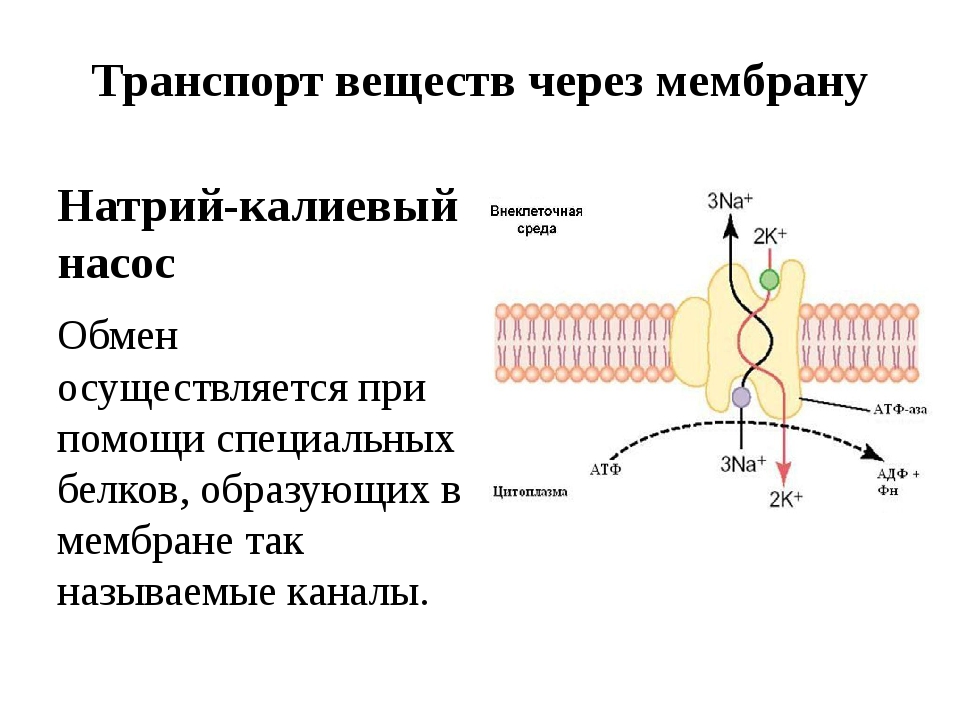 Этот процесс опосредуется повышающей регуляцией в апикально расположенной H + -K + -АТФазы на интеркалированных клетках (16) (рис. 7).
Этот процесс опосредуется повышающей регуляцией в апикально расположенной H + -K + -АТФазы на интеркалированных клетках (16) (рис. 7).
Клеточная модель для транспорта K + в проксимальном канальце .Реабсорбция K + в проксимальном канальце в основном происходит через параклеточный путь. Активная реабсорбция Na + вызывает реабсорбцию чистой жидкости через проксимальный каналец, что, в свою очередь, вызывает реабсорбцию K + через механизм увлечения растворителем. По мере того как жидкость течет по проксимальному канальцу, напряжение в просвете смещается от слегка отрицательного до слегка положительного. Сдвиг трансэпителиального напряжения обеспечивает дополнительную движущую силу, способствующую диффузии K + через межклеточный путь с низким сопротивлением.Экспериментальные исследования показывают, что может быть небольшой компонент трансцеллюлярного транспорта K + ; однако значение этого пути неизвестно. Поглощение K + через насос Na + -K + -ATPase может выходить из базолатеральной мембраны через проводящий путь или соединяться с Cl —. Апикально расположенный канал K + функционирует для стабилизации отрицательного потенциала клетки, в частности, в условиях сопряженного с Na + котранспорта глюкозы и аминокислот, который имеет деполяризующий эффект на напряжение клетки.
Поглощение K + через насос Na + -K + -ATPase может выходить из базолатеральной мембраны через проводящий путь или соединяться с Cl —. Апикально расположенный канал K + функционирует для стабилизации отрицательного потенциала клетки, в частности, в условиях сопряженного с Na + котранспорта глюкозы и аминокислот, который имеет деполяризующий эффект на напряжение клетки.
Модель ячейки для транспорта K + в толстой восходящей ветви Генле . Реабсорбция K + происходит как с помощью параклеточного, так и трансцеллюлярного механизмов. Базолатеральный насос Na + -K + -ATPase поддерживает низкий уровень внутриклеточного Na + , обеспечивая тем самым благоприятный градиент для управления апикально расположенным котранспортером Na + -K + -2Cl — (пример вторичного активного транспорта). Апикально расположенный почечный наружный медуллярный канал K + (ROMK) обеспечивает путь для рециркуляции K + из клетки в просвет и обеспечивает адекватное поступление K + для поддержания Na + -K + -2Cl — котранспорт. Это движение через ROMK создает положительное для просвета напряжение, обеспечивая движущую силу для пассивной реабсорбции K + через параклеточный путь. Часть K + , попадающая в клетку через котранспортер, покидает клетку через базолатеральную мембрану, обеспечивая трансцеллюлярную реабсорбцию K + .K + может покидать клетку по токопроводящему пути или при котранспорте с Cl — . ClC-Kb является основным путем оттока Cl — через базолатеральную мембрану.
Апикально расположенный почечный наружный медуллярный канал K + (ROMK) обеспечивает путь для рециркуляции K + из клетки в просвет и обеспечивает адекватное поступление K + для поддержания Na + -K + -2Cl — котранспорт. Это движение через ROMK создает положительное для просвета напряжение, обеспечивая движущую силу для пассивной реабсорбции K + через параклеточный путь. Часть K + , попадающая в клетку через котранспортер, покидает клетку через базолатеральную мембрану, обеспечивая трансцеллюлярную реабсорбцию K + .K + может покидать клетку по токопроводящему пути или при котранспорте с Cl — . ClC-Kb является основным путем оттока Cl — через базолатеральную мембрану.
Клеточная модель для транспорта K + в дистальном извитом канальце (DCT) . В ранней DCT захват Na + в просвете опосредуется апикально расположенным тиазид-чувствительным котранспортером Na + -Cl — . Транспортер получает энергию от базолатеральной Na + -K + -АТФазы, которая поддерживает низкую внутриклеточную концентрацию Na + , обеспечивая тем самым благоприятный градиент для входа Na + в клетку посредством вторичного активного транспорта. Котранспортер в изобилии экспрессируется в DCT1, но постепенно снижается в DCT2. ROMK экспрессируется через DCT и в кортикальный собирательный проток. Экспрессия эпителиального канала Na + (ENaC), который опосредует чувствительное к амилориду всасывание Na + , начинается в DCT2 и устойчиво экспрессируется в нижних соединительных канальцах и кортикальном собирательном канале.DCT2 является началом альдостерон-чувствительного дистального нефрона (ASDN), что определяется наличием как минералокортикоидного рецептора, так и фермента 11 β -гидроксистероиддегидрогеназы II. Этот фермент поддерживает рецептор минералокортикоидов свободным, чтобы связывать альдостерон только за счет метаболизма кортизола до кортизона, последний из которых не имеет сродства к рецептору.
Транспортер получает энергию от базолатеральной Na + -K + -АТФазы, которая поддерживает низкую внутриклеточную концентрацию Na + , обеспечивая тем самым благоприятный градиент для входа Na + в клетку посредством вторичного активного транспорта. Котранспортер в изобилии экспрессируется в DCT1, но постепенно снижается в DCT2. ROMK экспрессируется через DCT и в кортикальный собирательный проток. Экспрессия эпителиального канала Na + (ENaC), который опосредует чувствительное к амилориду всасывание Na + , начинается в DCT2 и устойчиво экспрессируется в нижних соединительных канальцах и кортикальном собирательном канале.DCT2 является началом альдостерон-чувствительного дистального нефрона (ASDN), что определяется наличием как минералокортикоидного рецептора, так и фермента 11 β -гидроксистероиддегидрогеназы II. Этот фермент поддерживает рецептор минералокортикоидов свободным, чтобы связывать альдостерон только за счет метаболизма кортизола до кортизона, последний из которых не имеет сродства к рецептору. Электрогенно-опосредованный транспорт K + начинается в DCT2 с комбинированным присутствием ROMK, ENaC и чувствительности к альдостерону.Электронейтральный K + -Cl — cotransport присутствует в DCT и сборном канале. Условия, вызывающие низкую концентрацию Cl — в просвете, увеличивают секрецию K + по этому механизму, который происходит при доставке плохо реабсорбируемых анионов, таких как сульфат, фосфат или бикарбонат.
Электрогенно-опосредованный транспорт K + начинается в DCT2 с комбинированным присутствием ROMK, ENaC и чувствительности к альдостерону.Электронейтральный K + -Cl — cotransport присутствует в DCT и сборном канале. Условия, вызывающие низкую концентрацию Cl — в просвете, увеличивают секрецию K + по этому механизму, который происходит при доставке плохо реабсорбируемых анионов, таких как сульфат, фосфат или бикарбонат.
Клетка, которая отвечает за секрецию K + в начальном собирательном канале и кортикальном собирательном канале, является основной клеткой .Эта клетка обладает базолатеральной Na + -K + -АТФазой, которая отвечает за активный транспорт K + из крови в клетку. Результирующая высокая концентрация K + в клетке обеспечивает благоприятный градиент диффузии для перемещения K + из клетки в просвет. Помимо установления высокой внутриклеточной концентрации K + , активность этого насоса снижает внутриклеточную концентрацию Na + , тем самым поддерживая благоприятный градиент диффузии для перемещения Na + из просвета в клетку.Оба движения Na + и K + через апикальную мембрану происходят через четко определенные каналы Na + и K + .
Помимо установления высокой внутриклеточной концентрации K + , активность этого насоса снижает внутриклеточную концентрацию Na + , тем самым поддерживая благоприятный градиент диффузии для перемещения Na + из просвета в клетку.Оба движения Na + и K + через апикальную мембрану происходят через четко определенные каналы Na + и K + .
Реабсорбция HCO 3 в дистальном нефроне опосредуется апикальной секрецией H + интеркалированной α клеткой . Два транспортера секретируют H + , вакуолярную H + -АТФазу и H + -K + -АТФазу.H + -K + -ATPase использует энергию, полученную в результате гидролиза АТФ, для секреции H + в просвет и реабсорбции K + электронейтральным образом. Активность H + -K + -АТФазы увеличивается при истощении K + и, таким образом, обеспечивает механизм, с помощью которого истощение K + усиливает секрецию как собирательного протока H + , так и секрецию K + . абсорбция.
Активность H + -K + -АТФазы увеличивается при истощении K + и, таким образом, обеспечивает механизм, с помощью которого истощение K + усиливает секрецию как собирательного протока H + , так и секрецию K + . абсорбция.
В большинстве гомеостатических условий доставка K + в дистальный нефрон остается небольшой и довольно постоянной.Напротив, скорость секреции K + дистальным нефроном варьируется и регулируется в соответствии с физиологическими потребностями. Клеточные детерминанты секреции K + в основной клетке включают внутриклеточную концентрацию K + , люминальную концентрацию K + , разность потенциалов (напряжений) на просветной мембране и проницаемость просветной мембраны для K + . Условия, которые увеличивают концентрацию клеточного K + , уменьшают концентрацию K + в просвете или делают просвет более электроотрицательным, увеличивают скорость секреции K + . Условия, которые увеличивают проницаемость просветной мембраны для K + , увеличивают скорость секреции K + . Двумя основными детерминантами секреции K + являются минералокортикоидная активность и дистальная доставка Na + и воды.
Условия, которые увеличивают проницаемость просветной мембраны для K + , увеличивают скорость секреции K + . Двумя основными детерминантами секреции K + являются минералокортикоидная активность и дистальная доставка Na + и воды.
Альдостерон является основным минералокортикоидом у человека и влияет на несколько клеточных детерминант, описанных выше, что приводит к стимуляции секреции K + . Во-первых, альдостерон увеличивает внутриклеточную концентрацию K + , стимулируя активность Na + -K + -АТФазы в базолатеральной мембране.Во-вторых, альдостерон стимулирует реабсорбцию Na + через просветную мембрану, что увеличивает электроотрицательность просвета, тем самым увеличивая электрический градиент, способствующий секреции K + . Наконец, альдостерон оказывает прямое воздействие на просветную мембрану, увеличивая проницаемость K + (17).
Второй основной детерминант, влияющий на секрецию K + , — это скорость дистальной доставки Na + и воды. Повышенная дистальная доставка Na + стимулирует дистальную абсорбцию Na + , что делает просвет просвета более отрицательным и, таким образом, увеличивает секрецию K + .Повышенная скорость потока также увеличивает секрецию K + . Когда K + секретируется в собирательный проток, концентрация K + в просвете повышается, что снижает градиент диффузии и замедляет дополнительную секрецию K + . При более высоких скоростях потока в просвете такое же количество секреции K + будет разбавлено большим объемом, так что повышение концентрации K + в просвете будет меньше. Таким образом, увеличение дистальной доставки Na + и воды стимулирует секрецию K + , снижая концентрацию K + в просвете и делая потенциал просвета более отрицательным.
Повышенная дистальная доставка Na + стимулирует дистальную абсорбцию Na + , что делает просвет просвета более отрицательным и, таким образом, увеличивает секрецию K + .Повышенная скорость потока также увеличивает секрецию K + . Когда K + секретируется в собирательный проток, концентрация K + в просвете повышается, что снижает градиент диффузии и замедляет дополнительную секрецию K + . При более высоких скоростях потока в просвете такое же количество секреции K + будет разбавлено большим объемом, так что повышение концентрации K + в просвете будет меньше. Таким образом, увеличение дистальной доставки Na + и воды стимулирует секрецию K + , снижая концентрацию K + в просвете и делая потенциал просвета более отрицательным.
Две популяции каналов K + были идентифицированы в клетках кортикального собирательного протока. Почечный наружный медуллярный канал K + (ROMK) считается основным K + -секреторным путем. Этот канал характеризуется низкой проводимостью и высокой вероятностью открытия в физиологических условиях. Канал maxi-K + (также известный как канал K + [BK] с большой проводимостью) характеризуется большой проводимостью одного канала и покоем в базовом состоянии и активацией в условиях повышенного потока (18).В дополнение к увеличенной доставке Na + и разбавлению просвета концентрации K + , рекрутирование каналов maxi-K + способствует зависящему от потока увеличению секреции K + . Почечные каналы K + являются предметом обширных обзоров (19–21).
Этот канал характеризуется низкой проводимостью и высокой вероятностью открытия в физиологических условиях. Канал maxi-K + (также известный как канал K + [BK] с большой проводимостью) характеризуется большой проводимостью одного канала и покоем в базовом состоянии и активацией в условиях повышенного потока (18).В дополнение к увеличенной доставке Na + и разбавлению просвета концентрации K + , рекрутирование каналов maxi-K + способствует зависящему от потока увеличению секреции K + . Почечные каналы K + являются предметом обширных обзоров (19–21).
Эффект увеличения канальцевого кровотока для активации каналов maxi-K + может быть опосредован изменениями внутриклеточной концентрации Ca 2+ (22). Канал активирован Ca 2+ , и резкое увеличение потока увеличивает внутриклеточные концентрации Ca 2+ в основной клетке.Было высказано предположение, что центральная ресничка (структура, присутствующая в основных клетках) может способствовать передаче сигналов повышенного потока в повышенную внутриклеточную концентрацию Ca 2+ . В культивируемых клетках изгиб первичных ресничек приводит к временному увеличению внутриклеточного Ca 2+ , эффект блокируется антителами к полицистину 2 (23). Хотя он присутствует почти во всех сегментах нефрона, канал maxi-K был идентифицирован как медиатор индуцированной потоком секреции K + в дистальном отделе нефрона и кортикальном собирательном канале (24).
В культивируемых клетках изгиб первичных ресничек приводит к временному увеличению внутриклеточного Ca 2+ , эффект блокируется антителами к полицистину 2 (23). Хотя он присутствует почти во всех сегментах нефрона, канал maxi-K был идентифицирован как медиатор индуцированной потоком секреции K + в дистальном отделе нефрона и кортикальном собирательном канале (24).
Развитие гипокалиемии при синдроме Барттера II типа иллюстрирует важность каналов maxi-K + в почечной экскреции K + (25). У пациентов с синдромом Барттера II типа имеется мутация потери функции в ROMK, которая проявляется клиническими особенностями заболевания в перинатальном периоде. ROMK обеспечивает путь для рециркуляции K + через апикальную мембрану в толстой восходящей конечности Генле. Эта рециркуляция создает положительный для просвета потенциал, который управляет параклеточной реабсорбцией Ca 2+ и Mg 2+ и обеспечивает просвет K + котранспортеру Na + -K + -2Cl — ( Рисунок 4).
Мутации в ROMK уменьшают реабсорбцию NaCl и жидкости в толстой конечности, имитируя петлевой диуретический эффект, вызывающий истощение объема. Несмотря на увеличение дистальной доставки Na + , истощение K + не наблюдается постоянно, потому что ROMK также является основным K + -секреторным путем для регулируемой экскреции K + в собирательный проток. Фактически, в перинатальном периоде у младенцев с этой формой синдрома Барттера часто наблюдается преходящая гиперкалиемия, связанная с потерей функции ROMK в собирательном канале.Однако со временем у этих пациентов развивается гипокалиемия в результате увеличения секреции K + , опосредованной потоком, через каналы maxi-K + . Исследования на модели синдрома Барттера типа II на мышах с дефицитом ROMK согласуются с этим механизмом (26). Преходящая гиперкалиемия, наблюдаемая в перинатальном периоде, вероятно, связана с тем фактом, что каналы ROMK функционально экспрессируются раньше, чем каналы maxi-K + в ходе развития.
В связи с этим растущие младенцы и дети находятся в состоянии положительного баланса K + , который коррелирует с ростом и увеличением количества клеток.На ранних этапах развития способность дистального нефрона секретировать K + ограничена из-за нехватки как апикально расположенных каналов ROMK, так и maxi-K + каналов. Увеличение секреторной способности K + по мере созревания изначально является результатом повышенной экспрессии ROMK. Несколькими неделями позже развивается экспрессия канала maxi-K + , позволяющая происходить опосредованной потоком секреции K + (рассмотрено в ссылке 27). Ограничение дистальной секреции K + является канально-специфическим, поскольку электрохимический градиент, благоприятствующий секреции K + , определяемый активностью Na + -K + -АТФазы и реабсорбцией Na + , составляет не ограничивая.Кроме того, увеличение скорости потока сопровождается соответствующим увеличением реабсорбции Na + и внутриклеточной концентрации Ca 2+ в дистальном отделе нефрона, несмотря на отсутствие стимулирующего эффекта на секрецию K + (28). Активность H + — K + -АТФазы, которая связывает реабсорбцию K + с секрецией H + в интеркалированных клетках, одинакова у новорожденных и взрослых. Реабсорбция K + через этот насос, в сочетании со сниженной экспрессией K + -секреторных каналов, помогает поддерживать состояние положительного баланса K + во время соматического роста после рождения.Эти особенности дистального воздействия K + развивающейся почкой являются вероятным объяснением высокой частоты неолигурической гиперкалиемии у недоношенных детей (29).
Другим физиологическим состоянием, характеризующимся периодом положительного баланса K + , является беременность, при которой сохраняется приблизительно 300 мэкв K + (30). Высокий уровень циркулирующего прогестерона может играть роль в этой адаптации за счет стимулирующего воздействия на транспорт K + и H + с помощью H + -K + α 2 изоформы -АТФазы в дистальных отделах нефрона. (31).
В дополнение к стимуляции каналов maxi-K + было показано, что усиленный канальцевый ток стимулирует абсорбцию Na + через эпителиальный канал Na + (ENaC) в собирательном канале. Это увеличение абсорбции происходит не только из-за увеличения доставки Na + , но также, по-видимому, является результатом механочувствительных свойств, присущих каналу. Повышенный поток создает напряжение сдвига, которое активирует ENaC за счет увеличения вероятности открытия канала (32,33).
Была выдвинута гипотеза, что биомеханическая регуляция почечного канальцевого транспорта Na + и K + в дистальных отделах нефрона могла развиваться как реакция на защиту от внезапного увеличения внеклеточной концентрации K + , которое происходит в ответ на прием пищи. K + -богатых рационов, типичных для ранних позвоночных (22). Согласно этой гипотезе, увеличение СКФ после приема пищи, богатой белком, приведет к увеличению дистального кровотока, активируя ENaC, увеличивая внутриклеточную концентрацию Ca 2+ и активируя каналы maxi-K + .Эти события будут усиливать секрецию K + , тем самым обеспечивая буфер для защиты от развития гиперкалиемии.
У пациентов с ХБП потеря массы нефрона уравновешивается адаптивным увеличением секреторной скорости K + в оставшихся нефронах, так что гомеостаз K + обычно хорошо сохраняется до тех пор, пока СКФ не упадет ниже 15-20 мл / мин (34). Считается, что природа адаптивного процесса аналогична адаптивному процессу, который происходит в ответ на высокое потребление K + с пищей у нормальных субъектов (35).Хроническая нагрузка K + у животных увеличивает секреторную способность дистального нефрона, и, следовательно, почечная экскреция K + значительно увеличивается для любого заданного уровня K + в плазме. Повышенная секреция K + в этих условиях происходит в связи со структурными изменениями, характеризующимися клеточной гипертрофией, повышенной плотностью митохондрий и пролиферацией базолатеральной мембраны в клетках дистального отдела нефрона и основных клетках собирательного канала.Повышенные сывороточные K + и минералокортикоиды независимо инициируют процесс амплификации, который сопровождается повышением активности Na + -K + -ATPase.
Aldosterone Paradox
В условиях истощения объема активация ренин-ангиотензиновой системы приводит к увеличению высвобождения альдостерона. Повышение уровня циркулирующего альдостерона стимулирует удержание в почках Na + , способствуя восстановлению объема внеклеточной жидкости, но происходит без заметного воздействия на почечную секрецию K + .В условиях гиперкалиемии высвобождение альдостерона опосредуется прямым воздействием K + на клетки клубочковой зоны. Последующее увеличение циркулирующего альдостерона стимулирует почечную секрецию K + , восстанавливая концентрацию K + в сыворотке до нормального уровня, но делает это без сопутствующей задержки Na + в почках.
Способность альдостерона сигнализировать почкам о стимулировании удержания соли без секреции K + при истощении объема и стимулировать секрецию K + без удержания соли при гиперкалиемии была названа парадоксом альдостерона (36).Частично эту способность можно объяснить взаимной взаимосвязью между скоростью потока мочи и дистальной доставкой Na + с уровнями циркулирующего альдостерона. В условиях истощения объема проксимальное поглощение соли и воды увеличивается, что приводит к снижению дистальной доставки Na + и воды. Хотя уровни альдостерона увеличиваются, почечная экскреция K + остается довольно постоянной, потому что стимулирующий эффект повышенного альдостерона уравновешивается уменьшенной доставкой фильтрата к дистальному нефрону.В условиях увеличенного объема внеклеточной жидкости дистальная доставка фильтрата увеличивается в результате снижения реабсорбции жидкости в проксимальных канальцах. И снова почечная экскреция K + остается относительно постоянной в этих условиях, потому что уровни циркулирующего альдостерона подавлены. Только при патофизиологических условиях повышенный уровень Na + в дистальных отделах и доставка воды сочетаются с повышенным уровнем альдостерона. Почечная атрофия K + будет происходить в этом случае (37) (Рисунок 8).
Рисунок 8.В нормальных условиях доставка Na + к дистальному отделу нефрона обратно пропорциональна уровню альдостерона в сыворотке . По этой причине почечная экскреция K + не зависит от изменений объема внеклеточной жидкости. Гипокалиемия, вызванная почечным истощением K + , может быть объяснена патофизиологическими изменениями, которые приводят к сочетанию повышенной дистальной доставки Na + и эффектов альдостерона или альдостерона.При приближении к гипокалиемии, вызванной почечным истощением K + , необходимо определить, является ли первичным заболеванием повышение активности минералокортикоидов или увеличение дистальной доставки Na + . EABV — эффективный объем артериальной крови.
Почечная секреция K + также остается стабильной при изменениях скорости потока, вызванных колебаниями циркулирующего вазопрессина. В связи с этим вазопрессин оказывает стимулирующее действие на почечную секрецию K + (38,39).Это калиуретическое свойство может служить противодействием тенденции к удержанию K + в условиях антидиуреза, когда в противном случае могло бы произойти падение в дистальных канальцах секреции K + , зависящее от низкой скорости потока. Напротив, подавление эндогенного вазопрессина приводит к снижению активности дистального K + -секреторного механизма, тем самым ограничивая чрезмерные потери калия в условиях полной гидратации и водного диуреза.
Хотя обратная зависимость между уровнями альдостерона и дистальной доставкой соли и воды служит для сохранения почечной экскреции K + независимо от статуса объема, недавние обзоры предложили более сложный механизм, основанный на отсутствии лизина [K] 4 (WNK4 ) протеинкиназа в дистальном отделе нефрона (40,41).WNK4 является одним из четырех членов семейства серин-треониновых киназ, каждая из которых кодируется другим геном и характеризуется атипичным размещением каталитического остатка лизина, который присутствует в большинстве других протеинкиназ. Инактивирующие мутации в WNK4 приводят к развитию псевдогипоальдостеронизма II типа (PHAII; синдром Гордона). Это заболевание наследуется по аутосомно-доминантному типу и характеризуется гипертонией и гиперкалиемией (42). Уровень циркулирующего альдостерона низкий, несмотря на наличие гиперкалиемии.Тиазидные диуретики особенно эффективны при лечении гипертонии и гиперкалиемии (43).
WNK4 дикого типа снижает поверхностную экспрессию тиазид-чувствительного котранспортера Na + -Cl —, а также стимулирует клатрин-зависимый эндоцитоз ROMK в собирательном канале (44,45). Инактивирующая мутация WNK4, отвечающая за PHAII, приводит к увеличению активности котранспортера и дополнительно стимулирует эндоцитоз ROMK. Чистый эффект заключается в увеличении реабсорбции NaCl в сочетании с уменьшением секреции K + .Мутировавший WNK4 также увеличивает проницаемость для Cl — в параклетках, вызванную повышенным фосфорилированием клаудинов, белков плотных контактов, участвующих в регуляции транспорта ионов в параклетках (46). Помимо увеличения удерживания Na + , это изменение проницаемости дополнительно ухудшает секрецию K + , потому что отрицательное напряжение в просвете, которое обычно служит движущей силой для секреции K + , рассеивается.
Поскольку развитие гипертонии и гиперкалиемии в результате PHAII-мутированного белка WNK4 можно рассматривать как преувеличенную реакцию на уменьшение объема внеклеточной жидкости (задержка соли без увеличения секреции K + ), было предложено, что дикий тип WNK4 может действовать как молекулярный переключатель, определяющий баланс между почечной реабсорбцией NaCl и секрецией K + (45,47).В условиях истощения объема переключение будет изменено способом, напоминающим мутант PHAII, так что реабсорбция NaCl увеличивается, но секреция K + дополнительно ингибируется. Однако, когда повышенная концентрация K + в сыворотке происходит в отсутствие истощения объема, изменения WNK4 приводят к максимальной почечной секреции K + без удержания Na + .
Ангиотензин II (AII) появился как важный модулятор этого переключателя.В условиях истощения объема повышаются уровни AII и альдостерона (Рисунок 9). В дополнение к эффектам, ведущим к усилению реабсорбции NaCl в проксимальном канальце, AII активирует котранспортер Na + -Cl — зависимым от WNK4 образом, и он в первую очередь располагается в начальной части дистального извитого канальца (DCT ; DCT1) (48,49). AII также активирует ENaC, который обнаружен в чувствительном к альдостерону дистальном нефроне (ASDN), состоящем из второго сегмента DCT (DCT2), соединительного канальца и собирательного канала (50).Активация ENaC под действием AII дополняет активацию альдостерона (51). Таким образом, AII и альдостерон действуют совместно, стимулируя удерживание Na + . В то же время, AII ингибирует ROMK с помощью как WNK4-зависимых, так и независимых механизмов (52,53). Этот ингибирующий эффект на ROMK наряду со снижением доставки Na + в собирательный проток, вызванный стимуляцией AII реабсорбции Na + в проксимальном нефроне, и DCT1 позволяет одновременно сохранять Na + без потери K + .
Рисунок 9.Парадокс альдостерона относится к способности почки стимулировать задержку NaCl с минимальной секрецией K + в условиях истощения объема и максимизировать K + секрецию без Na + удержание при гиперкалиемии . При истощении объема (левая панель) повышенные уровни циркулирующего ангиотензина II (AII) стимулируют котранспортер Na + -Cl — на ранней стадии DCT.В ASDN AII вместе с альдостероном стимулируют ENaC. В этом последнем сегменте AII оказывает ингибирующее действие на ROMK, тем самым обеспечивая механизм максимального сохранения соли и минимизации почечной секреции K + . Когда гиперкалиемия или повышенное потребление K + с пищей происходит с нормоволемией (правая панель), низкие уровни циркулирующего AII или прямые эффекты K + приводят к ингибированию активности котранспорта Na + -Cl — наряду с повышенной активностью РОМК.В результате доставка Na + в ENaC оптимизирована для связанной электрогенной секреции K + через ROMK. Как обсуждается в тексте, без лизина [K] 4 (WNK4) белки интегрально участвуют в сигналах, вызывающих парадокс. Следует подчеркнуть, что белки WNK являются частью сложной сигнальной сети, которая еще полностью не выяснена. Заинтересованного читателя отсылаем к нескольким недавним обзорам и достижениям по этой теме (48,51,91–93).
Гиперкалиемия, или увеличение потребления K + с пищей, может увеличивать почечную секрецию K + независимо от изменения активности минералокортикоидов и без сохранения объема.Этот эффект был продемонстрирован на крысах Wistar, получавших диету с очень низким содержанием NaCl и K + в течение нескольких дней и получавшую фармакологическую дозу дезоксикортикостерона для обеспечения постоянного и неизменного эффекта минералокортикоидов (54,55). После введения KCl в брюшную полость были отмечены две отдельные фазы. В первые 2 часа наблюдалось значительное увеличение скорости почечной экскреции K + , что в значительной степени было вызвано увеличением концентрации K + в кортикальном собирательном канале.Во время этой ранней фазы поток через собирающий канал увеличился лишь незначительно, предполагая, что изменения в концентрации K + в значительной степени были вызваны увеличением секреторной способности K + собирательного канала. Этот эффект согласуется с известными эффектами диетической добавки K + на увеличение плотности каналов как ROMK, так и maxi-K + (56).
В последующие 4 часа почечная экскреция K + оставалась высокой, но во время этой второй фазы калиурез в основном объяснялся повышенным потоком через собирательный проток.Повышенный кровоток был приписан ингибирующему эффекту повышенной интерстициальной концентрации K + на реабсорбцию NaCl в восходящей восходящей конечности Генле, эффект, подтвержденный исследованиями микроперфузии в прошлом (57,58). По-видимому, важна синхронизация двух фаз, потому что более высокие потоки будут наиболее эффективны в продвижении калиуреза только после установления повышенной плотности каналов. Хотя более ранние исследования согласуются с уменьшением всасывания Na + в толстой конечности и проксимальном нефроне после увеличения потребления K + , ингибирующим эффектам в этих сегментах с высокой емкостью не хватает точности и времени, необходимых для обеспечения доставки ниже по потоку Na + подходит для максимального стимулирования секреции K + и в то же время не является чрезмерным, предрасполагающим к истощению объема, особенно в условиях диеты с низким содержанием Na + (57–59).
Характер DCT с низкой пропускной способностью и его расположение непосредственно выше по потоку от ASDN делают этот сегмент более вероятным местом для изменений в диетическом потреблении K + , чтобы модулировать транспорт Na + и гарантировать, что доставка Na + — это именно то количество, которое необходимо для поддержания гомеостаза K + , не вызывая нежелательных эффектов на объем. В связи с этим повышенное потребление K + с пищей приводит к ингибирующему эффекту на транспорт Na + в этом сегменте, и это происходит за счет воздействия на WNK1, другого члена семейства киназ WNK (60,61).WNK1 повсеместно экспрессируется по всему телу в множественных сплайсированных формах. Напротив, более короткий транскрипт WNK1, лишенный аминоконцевых 1–437 аминокислот длинного транскрипта, высоко экспрессируется в почках, но не в других тканях, и его называют почко-специфическим WNK1 (KS-WNK1). KS-WNK1 ограничен DCT и частью соединительного протока и функционирует как физиологический антагонист действия длинного WNK1. Изменения соотношения KS-WNK1 и длинного WNK1 в ответ на диетический K + вносят вклад в физиологическую регуляцию почечной экскреции K + (62–65).
В нормальных условиях длинный WNK1 предотвращает способность WNK4 ингибировать активность котранспортера Na + -Cl — в DCT. Таким образом, повышенная активность длинного WNK1 приводит к чистому увеличению реабсорбции NaCl. Диетическая нагрузка K + увеличивает количество KS-WNK1. Повышенный KS-WNK1 противодействует ингибирующему эффекту длинного WNK1 на WNK4. Чистый эффект заключается в ингибировании котранспорта Na + -Cl — в DCT и увеличении доставки Na + в более дистальные части канальца.Кроме того, увеличенный KS-WNK1 противодействует эффекту длинного WNK1 для стимуляции эндоцитоза ROMK. Кроме того, KS-WNK1 оказывает стимулирующее действие на ENaC. Таким образом, увеличение KS-WNK1 в ответ на диетическую загрузку K + способствует секреции K + за счет комбинированных эффектов увеличения доставки Na + за счет подавления котранспорта Na + -Cl — в DCT, повышенная электрогенная реабсорбция Na + через ENaC и большее количество ROMK.
Повышенные уровни альдостерона в ответ на диету с высоким содержанием K + приводят к эффектам, которые дополняют эффекты KS-WNK1 (66,67). Сывороточная и глюкокортикоид-зависимая протеинкиназа (SGK1) является непосредственной транскрипционной мишенью связывания альдостерона с рецептором минералокортикоидов. Активация SGK1 приводит к фосфорилированию WNK4, что приводит к потере способности WNK4 ингибировать ROMK и ENaC (66,68). Альдостерон-индуцированная активация SGK1 также ведет к увеличению экспрессии и активности ENaC, вызывая фосфорилирование убиквитин протеинлигазы Nedd4–2.Фосфорилированный Nedd4–2 приводит к меньшему извлечению ENaC из апикальной мембраны (69). Следует подчеркнуть, что отсутствие AII является критическим фактором в способности высокого потребления K + вызывать изменения, необходимые для облегчения секреции K + без чрезмерной реабсорбции Na + .
Роль в гипертонии
Изменения в KS-WNK1 и длинном WNK1, которые происходят в ответ на потребление K + с пищей, влияют на почечную обработку Na + таким образом, что это может иметь значение для наблюдаемой взаимосвязи между K + в рационе потребление и гипертония.Эпидемиологические исследования установили, что потребление K + обратно пропорционально распространенности гипертонии (70). Кроме того, добавки K + и предотвращение гипокалиемии снижают АД у пациентов с гипертонией. Напротив, АД увеличивается у пациентов с гипертонией, находящихся на диете с низким содержанием K + . Это повышение АД связано с повышенной реабсорбцией Na + почками (71).
K + дефицит увеличивает соотношение длинных WNK1 и KS-WNK1. Длинный WNK1 связан с повышенным извлечением ROMK, таким образом обеспечивая соответствующий ответ для ограничения секреции K + .Однако длинный WNK1 также приводит к стимулирующему эффекту на активность ENaC, а также к высвобождению ингибирующего эффекта WNK4 на реабсорбцию Na + , опосредованную котранспортером NaCl в DCT (72,73). Эти эффекты предполагают, что снижение секреции K + в условиях дефицита K + будет происходить за счет увеличения удерживания Na + .
Сохранение в почках K + и Na + в условиях дефицита K + можно рассматривать как эволюционную адаптацию, потому что диетический дефицит K + и Na + , вероятно, имел место вместе у ранних людей (74) .Однако такой эффект потенциально пагубен в наших нынешних условиях, потому что в ходе эволюции наблюдалось значительное увеличение соотношения потребления Na + с пищей по сравнению с K + . Эффекты повышенного отношения WNK1 к KS-WNK1 в почках в условиях современной диеты с высоким содержанием Na + / низким содержанием K + могут быть центральными в патогенезе солочувствительной гипертензии (75).
Энтерический датчик K
+Имеются данные, подтверждающие существование энтеральных датчиков растворенных веществ, способных реагировать на пищевые Na + , K + и фосфат, которые сигнализируют почкам о быстром изменении экскреции или реабсорбции ионов. (76–78).У экспериментальных животных и с использованием протоколов для поддержания идентичной концентрации K + в плазме калийуретический ответ на нагрузку K + выше при приеме в пищу по сравнению с внутривенным вливанием (79). Эти исследования показывают, что потребление K + с пищей через внутренний механизм восприятия может сигнализировать об увеличении почечной экскреции K + независимо от изменений концентрации K + в плазме или альдостерона (см. Ссылку 80).
Хотя точный механизм передачи сигналов неизвестен, недавние исследования показывают, что почечный ответ может быть вызван быстрым и почти полным дефосфорилированием котранспортера Na + -Cl — в DCT, вызывая снижение активности переносчика и , таким образом, улучшая доставку Na + в ASDN (81,82).В этих исследованиях доставка в желудок K + привела к дефосфорилированию котранспортера в течение нескольких минут независимо от альдостерона и на основании исследований in vitro , независимо от изменений во внеклеточной концентрации K + . Связанное во времени увеличение почечной экскреции K + является результатом более благоприятной электрохимической движущей силы, вызванной нисходящим сдвигом реабсорбции Na + от DCT к ENaC в ASDN, а также увеличением канала maxi-K + K + секреция, вызванная усилением кровотока.Этот быстрый натрийуретический ответ на увеличение потребления с пищей K + согласуется с эффектом снижения АД рационов с высоким содержанием K + , обсуждавшимся ранее.
Циркадный ритм секреции K
+В течение 24-часового периода экскреция K + с мочой изменяется в зависимости от изменений активности и колебаний потребления K + , вызванных интервалом между приемами пищи. Однако даже когда потребление и активность K + равномерно распределены в течение 24-часового периода, остается циркадный ритм, в результате которого экскреция K + ниже ночью и в ранние утренние часы, а затем увеличивается днем (83 –86).Этот циркадный паттерн является результатом изменений внутриканальцевой концентрации K + в собирательном канале, в отличие от изменений скорости потока мочи (87).
В дистальном нефроне мышей циркадный ритм существует для транскриптов генов, которые кодируют белки, участвующие в секреции K + (88). Экспрессия гена ROMK выше в периоды активности, тогда как экспрессия H + -K + -ATPase выше во время покоя, что соответствует периодам, когда почечная экскреция K + больше и меньше, соответственно (89 ).Изменения уровня альдостерона в плазме могут играть определенную роль, поскольку в надпочечниках описан циркадный ритм синтеза и секреции глюкокортикоидов. Кроме того, экспрессия часовых генов в клетках дистального нефрона предполагает, что функция водителя ритма, регулирующая транспорт K + , может быть внутренним компонентом почек, способным работать независимо от внешнего воздействия.
Клиническое значение этой ритмичности в K + и других секрециях электролитов не известно.Данные свидетельствуют о том, что нарушение регуляции циркадных ритмов может способствовать отсутствию снижения АД в ночное время с возможным развитием стойкой гипертензии, а также ускорением ХБП и сердечно-сосудистых заболеваний (85, 90).
- Авторские права © 2015 Американского общества нефрологов
Флуоресцентные индикаторы Na + и K + для визуализации функций клеток | Abcam
Na + индикаторы с первого взглядаСуществует большая разница в концентрации ионов натрия внутри и вне клетки (5-40 мМ внутриклеточно; 120-450 мМ внеклеточно, в зависимости от организма).Этот градиент концентрации важен для поглощения питательных веществ, регулирования концентраций других внутриклеточных ионов и растворенных веществ, а также для генерации и передачи электрических импульсов в возбудимых клетках. Низкая внутриклеточная концентрация натрия требует использования чувствительных красителей, способных регистрировать любые небольшие отклонения. Поскольку внутриклеточная концентрация калия обычно выше, чем концентрация натрия (более 100 мМ), индикаторы Na + должны избирательно реагировать на Na +, а не на K +.
Индикатор | Возбуждение (нм) | Эмиссия (нм) | K d (мМ) |
| Ион NaTRIUM Зеленый — TMA Salt / AM | 20 |
Форма ацетоксиметилового (AM) эфира, впервые представленная в 1981 г.Tsien1, 2 неинвазивен и является наиболее популярным методом
загрузки флуоресцентных ионных индикаторов в клетки. Функции фенольных и карбоновых кислот в молекуле дериватизируются в виде сложных эфиров AM
. Эти сложные эфиры делают молекулу достаточно гидрофобной, чтобы проникать через мембрану. Попав внутрь клетки, неспецифические эстеразы
, обнаруженные почти во всех типах клеток, гидролизуют сложные эфиры обратно до полианионной формы, необходимой для водорастворимости;
удержание в ячейке; и для обнаружения ионов.
Ion NaTRIUM Green — TMA + Salt
Ion NaTRIUM Green — это флуоресцентный индикатор с видимой длиной волны и полезным динамическим диапазоном для измерения концентраций Na + в цитозоле. Краситель возбуждается видимым светом. Хотя Ion NaTRIUM Green максимально возбуждает на длине волны 517 нм, его исключительная яркость обеспечивает возбуждение при стандартных настройках 488 нм. Более того, он хорошо работает для двухфотонного возбуждения ближним инфракрасным светом. Ion NaTRIUM Green также отличается стойкостью к фотообесцвечиванию и утечкам.
Соль ТМА представляет собой водорастворимую солевую форму Ion NaTRIUM Green, доступную для целей калибровки или для инвазивной загрузки, такой как микроинъекция в клетки или загрузка через цельноклеточный патч-электрод, а также для калибровки красителя in vitro. .
Ion NaTRIUM Green — AM
Форма ацетоксиметилового (AM) эфира Ion NaTRIUM Green неинвазивна и является наиболее популярным методом загрузки флуоресцентных ионных индикаторов в клетки. Функции фенольных и карбоновых кислот молекулы дериватизируются в виде сложных эфиров AM.Эти сложные эфиры делают молекулу достаточно гидрофобной, чтобы проникать через мембрану. Попав внутрь клетки, неспецифические эстеразы, обнаруженные почти во всех типах клеток, гидролизуют сложные эфиры до полианионной формы, необходимой для водорастворимости, удержания в клетке и восприятия ионов. Загрузка обычно выполняется в бессывороточной культуральной среде с эфиром AM в конечной концентрации в диапазоне от 1 до 10 мкМ.
K
+ индикаторы с первого взгляда| индикатор | Возбуждение (нм) | Эмиссия (нм) | K d (мМ) | Ион Калий Зеленый 4833 51736 | 91718 |
| PBFI | 340/390 | 500 | 5 |
Ион калиевый зеленый
Ион калиевый зеленый — флуоресцентный индикатор с полезным K d для измерения + цитозамещения. концентрация.Он легко заряжается и возбуждается видимым светом. Несмотря на то, что он не является логометрическим, его большой динамический диапазон флуоресценции позволяет обнаруживать даже небольшие изменения в концентрации K + . Оптимальное возбуждение происходит на длине волны 517 нм, но индикатор также может возбуждаться на обычной длине волны 488 нм. Ионно-калиевый зеленый хорошо работает с двухфотонным возбуждением в ближней инфракрасной области спектра, и, хотя он не полностью устойчив к фотообесцвечиванию, он более устойчив, чем другие красители. Как и его аналог Na + , он полезен для конфокальной микроскопии, проточной цитометрии и скрининга.
PBFI
K d PBFI для K + сильно зависит от присутствия Na + со значением 5,1 мМ в отсутствие Na + и 44 мМ в растворах с комбинированная концентрация Na + и K + 135 мМ (что приблизительно соответствует физиологической ионной силе). Хотя селективность PBFI для K + меньше, чем у индикаторов Ca 2+ , таких как Fura-2, ее достаточно для определения физиологических концентраций K + в присутствии других одновалентных катионов.Спектральный отклик PBFI при связывании иона позволяет измерять коэффициент возбуждения, и этот индикатор можно использовать с теми же оптическими фильтрами и оборудованием, что и для Fura-2.
Na
+ ионофорыИонофоры способствуют транспорту ионов Na + через липидные мембраны, в результате чего Na + может течь из отсека с более высокой концентрацией Na + через мембрану в отсек с более низкими концентрациями Na +. Эти ионофоры можно использовать для уравновешивания внутриклеточных и внеклеточных концентраций Na +.
Натриевая соль монензина — Na + -селективный карбоксильный ионофор
K
+ ионофорыВалиномицин
Валиномицин — природная липидорастворимая молекула, которая связывает ионы калия (K + ) и облегчает их перенос через липидные бислои. Он демонстрирует 10000-кратную селективность для K + по сравнению с Na + . Валиномицин — мощный антибиотик. Он обычно используется в качестве агента, вызывающего апоптоз, а также может использоваться для калибровки потенциометрических ответов в мембранных экспериментах с участием потенциально чувствительных красителей.
Нигерицин
Нигерицин селективен как для K + , так и для ионов водорода (H + ). Поэтому его обычно используют при калибровке флуоресценции цитозольных индикаторов pH.
Nonactin
Моновалентный катион-ионофор, проявляющий селективность в отношении K + и NH 4 + (K + = NH 4 + > Na + > Mg 2+ > Li + >> Ca 2+ ).Индуцирует транспорт катионов через искусственные мембраны.
.



 Независимо от происхождения соли, негативные последствия для здоровья вызывает содержащийся в ней натрий.
Независимо от происхождения соли, негативные последствия для здоровья вызывает содержащийся в ней натрий. Чтобы выяснить содержание натрия в продуктах питания, необходимо обращать внимание на этикетки.
Чтобы выяснить содержание натрия в продуктах питания, необходимо обращать внимание на этикетки.

 Исследование здоровья медсестер. Am J Nurs 1978; 78: 1039–40.
Исследование здоровья медсестер. Am J Nurs 1978; 78: 1039–40. J Hypertens 1995; 13: 1539–45.
J Hypertens 1995; 13: 1539–45.
