Клеточный иммунитет — Википедия
Материал из Википедии — свободной энциклопедии
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 24 октября 2018; проверки требует 1 правка. Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 24 октября 2018; проверки требует 1 правка.Клеточный иммунитет (англ. Cell-mediated immunity) — такой тип иммунного ответа, в котором не участвуют ни антитела, ни система комплемента. В процессе клеточного иммунитета активируются макрофаги, натуральные киллеры, антиген-специфичные цитотоксические Т-лимфоциты, и в ответ на антиген выделяются цитокины.[1]
Иммунная система исторически описывается состоящей из двух частей — системы гуморального иммунитета и системы клеточного иммунитета. В случае гуморального иммунитета защитные функции выполняют молекулы, находящиеся в плазме крови, а не клеточные элементы. В то время как в случае клеточного иммунитета защитная функция связана именно с клетками иммунной системы. Лимфоциты кластера дифференцировки CD4 или Т-хелперы осуществляют защиту против различных патогенов.
Система клеточного иммунитета выполняет защитные функции следующими способами:
- путём активации антиген-специфических цитотоксичных Т-лимфоцитов, которые могут вызывать апоптоз соматических клеток, демонстрируя на поверхности эпитопы чужеродных антигенов, например, клеток, заражённых вирусами, содержащими бактерии и клеток опухолей, демонстрирующих опухолевые антигены;
- путём активации макрофагов и натуральных киллеров, которые разрушают внутриклеточные патогены;
- путём стимулирования секреции цитокинов, которые оказывают влияние на другие клетки иммунной системы, принимающие участие в адаптивном иммунном ответе и врождённом иммунном ответе.[2]
Клеточный иммунитет направлен преимущественно против микроорганизмов, которые выживают в фагоцитах и против микроорганизмов, поражающие другие клетки. Система клеточного иммунитета особенно эффективна против клеток, инфицированных вирусами, и принимает участие в защите от грибов, простейших, внутриклеточных бактерий и против клеток опухолей. Также система клеточного иммунитета играет важную роль в отторжении тканей.
- ↑ Мейл Д., Бростофф Дж., Рот Д.Б., Ройтт А. Иммунология = Immunology, 7th edition, Elsevier, 2006. — 1. — Москва: Логосфера, 2007. — 568 с. — ISBN 9785986510105.
- ↑ Bruce Alberts, Alexander Johnson, Julian Lewis, Martin Raff, Keith Roberts, Peter Walter. Molecular Biology of the Cell. — 5. — Garland Science, 2008. — 1392 с. — ISBN 0815341059.
Иммунная система — Википедия
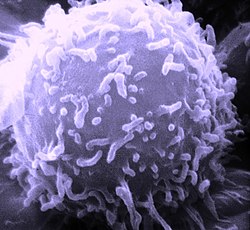
Имму́нная систе́ма — система органов, существующая у позвоночных животных и объединяющая органы и ткани, которые защищают организм от заболеваний, идентифицируя и уничтожая опухолевые клетки и патогены. Иммунная система распознаёт множество разнообразных возбудителей — от вирусов до паразитических червей — и отличает их от биомолекул собственных клеток. Распознавание возбудителей усложняется их адаптацией и эволюционным развитием новых методов успешного инфицирования организма-хозяина.
Конечной целью иммунной системы является уничтожение чужеродного агента, которым может оказаться болезнетворный микроорганизм, инородное тело, ядовитое вещество или переродившаяся клетка самого организма. Этим достигается биологическая индивидуальность организма.
В иммунной системе развитых организмов существует множество способов обнаружения и удаления чужеродных агентов: этот процесс называется иммунным ответом. Все формы иммунного ответа можно разделить на врождённые и приобретённые реакции. Основное различие между ними в том, что приобретённый иммунитет высокоспецифичен по отношению к конкретному типу антигенов и позволяет быстрее и эффективнее уничтожать их при повторном столкновении. Антигенами называют молекулы, воспринимаемые как чужеродные агенты и вызывающие специфические реакции организма. Например, у перенёсших ветрянку, корь, дифтерию людей часто возникает пожизненный иммунитет к этим заболеваниям. В случае аутоиммунных реакций антигеном может служить молекула, произведённая самим организмом.
Некоторые вещества, вырабатываемые иммунной системой, активно влияют на работу центральной нервной системы[1].
Защитные механизмы, направленные на распознавание и обезвреживание возбудителей, существуют даже у прокариот: например, ряд бактерий обладает ферментными системами, которые предотвращают заражение бактерии вирусом. Другие базовые иммунные механизмы развились в процессе эволюции у древних эукариот и сохранились у их современных потомков, в том числе у растений и животных. К таким механизмам относятся антимикробные пептиды, дефензины, рецепторы распознавания специфических последовательностей и система комплемента.
Короткие фрагменты РНК, которые избирательно синтезируются только в клетках половых органов (открыты в 2000-х годах), способны подавлять активность транспозонов (могут вызывать мутации при перемещении по геному) и передаются по материнской линии потомству. Потомство дрозофил получает в комплекте с ДНК такой молекулярный переключатель, который подавляет активность вредных генетических элементов[2].
Более сложные механизмы развились относительно недавно, в ходе эволюции позвоночных[3].
Иммунная система у позвоночных (например, у человека) состоит из множества видов белков, клеток, органов и тканей, взаимодействия между которыми сложны и динамичны. Благодаря такой усовершенствованной иммунной реакции система позвоночных со временем приспосабливается, и распознавание конкретных чужеродных веществ или клеток становится более эффективным. В процессе адаптации создаётся иммунологическая память, которая позволяет ещё более эффективно защищать организм при следующей встрече с этими возбудителями. Такой вид приобретённого иммунитета лежит в основе методик вакцинации.
У теплокровных сохранение гомеостаза уже обеспечивается двумя иммунными механизмами (разными по времени эволюционного появления): температура (общее воздействие) и антитела (избирательное воздействие).
Иммунная система человека и других позвоночных представляет собой комплекс органов и клеток, способных выполнять иммунологические функции. Прежде всего иммунный ответ осуществляют лейкоциты. Бо́льшая часть клеток иммунной системы происходит из кроветворных тканей. У взрослых людей развитие этих клеток начинается в костном мозге. Лишь Т-лимфоциты дифференцируются внутри тимуса (вилочковой железы). Зрелые клетки расселяются в лимфоидных органах и на границах с окружающей средой, около кожи или на слизистых оболочках.
Организм животных, обладающих механизмами приобретённого иммунитета, производит множество разновидностей специфических иммунных клеток, каждая из которых отвечает за какой-то определённый антиген. Наличие большого количества разновидностей иммунных клеток необходимо для того, чтобы отражать атаки микроорганизмов, способных мутировать и изменять свой антигенный состав. Значительная часть этих клеток завершает свой жизненный цикл, так и не приняв участие в защите организма, например, не встретив подходящих антигенов.
Иммунная система защищает организм от инфекции в несколько этапов, при этом с каждым этапом повышается специфичность защиты. Самая простая линия защиты представляет собой физические барьеры, которые предотвращают попадание возбудителей инфекции — бактерий и вирусов — в организм. Если возбудитель проникает через эти барьеры, промежуточную неспецифическую реакцию на него осуществляет врождённая иммунная система. Врождённая иммунная система обнаруживается у всех растений и животных[4]. На случай, когда возбудители успешно преодолевают воздействие врождённых иммунных механизмов, у позвоночных существует третий уровень защиты — приобретённая иммунная защита. Эта часть иммунной системы адаптирует свою реакцию во время инфекционного процесса, чтобы улучшить распознавание чужеродного биологического материала. Такой улучшенный ответ сохраняется после уничтожения возбудителя в виде иммунологической памяти. Она позволяет механизмам приобретённого иммунитета развивать более быструю и более сильную ответную реакцию при каждом появлении такого же возбудителя [5].
| Врождённый иммунитет | Приобретённый иммунитет |
|---|---|
| Реакция неспецифична | Специфическая реакция, привязанная к чужеродному антигену |
| Столкновение с инфекцией приводит к немедленной максимальной реакции | Между контактом с инфекцией и максимальным ответом латентный период |
| Клеточные и гуморальные звенья | |
| Не обладает иммунологической памятью | Столкновение с чужеродным агентом приводит к иммунологической памяти |
| Обнаруживается практически у всех форм жизни | Обнаружена только у некоторых организмов |
Как врождённый, так и приобретённый иммунитет зависят от способности иммунной системы отличать свои молекулы от чужих. В иммунологии под своими молекулами понимают те компоненты организма, которые иммунная система способна отличить от чужеродных[6]. Напротив, чужими называют молекулы, которые распознаются как чужеродные. Один из классов «чужих» молекул называют антигенами (термин произошёл от сокращения англ. antibody generators — «вызывающие антитела») и определяют как вещества, связываемые со специфическими иммунными рецепторами и вызывающие иммунный ответ[7].
Организмы защищены от инфекций рядом механических, химических и биологических барьеров. Примерами механических барьеров, служащих первым этапом защиты от инфекции, могут служить восковое покрытие многих листьев растений, экзоскелет членистоногих, скорлупа яиц и кожа [8]. Однако организм не может быть полностью отграничен от внешней среды, поэтому существуют и другие системы, защищающие внешние сообщения организма — дыхательную, пищеварительную и мочеполовую системы. Эти системы можно разделить на постоянно действующие и включающиеся в ответ на вторжение. Пример постоянно действующей системы — крохотные волоски на стенках трахеи, называемые ресничками, которые совершают быстрые движения, направленные вверх, удаляя частицы пыли, пыльцу растений или другие мелкие инородные объекты, чтобы они не могли попасть в лёгкие. Аналогичным образом, изгнание микроорганизмов осуществляется при помощи промывного действия слёз и мочи. Слизь, секретируемая в дыхательную и пищеварительную систему, служит для связывания и обездвиживания микроорганизмов[9]
Если постоянно действующих механизмов оказывается недостаточно, то включаются «аварийные» механизмы очистки организма, такие как кашель, чихание, рвота и диарея.
Помимо этого, существуют химические защитные барьеры. Кожа и дыхательные пути выделяют антимикробные пептиды, например бета-дефензины[10]. Такие ферменты, как лизоцим и фосфолипаза A, содержатся в слюне, слезах и грудном молоке, и также обладают антимикробным действием[11][12]. Выделения из влагалища служат химическим барьером после начала менструаций, когда они становятся слабокислыми. Сперма содержит дефензины и цинк для уничтожения возбудителей[13][14]. В желудке соляная кислота и протеолитические ферменты служат мощными химическими защитными факторами в отношении попавших с пищей микроорганизмов.
В мочеполовом и желудочно-кишечном трактах существуют биологические барьеры, представленные дружественными микроорганизмами — комменсалами. Приспособившаяся к обитанию в этих условиях неболезнетворная микрофлора конкурирует с патогенными бактериями за пищу и пространство, и, в ряде случаев, изменяя условия обитания, в частности pH или содержание железа[15]. Это снижает вероятность достижения болезнетворными микробами достаточных для возникновения патологии количеств. Поскольку большая часть антибиотиков неспецифически воздействует на бактерии, и, зачастую, не затрагивает грибы, антибактериальная терапия может приводить к чрезмерному «разрастанию» грибковых микроорганизмов, что вызывает такие заболевания, как молочница (кандидоз)[16]. Есть убедительные сведения, подтверждающие, что введение пробиотической флоры, например чистых культур лактобацилл, которые содержатся, в частности, в йогурте и других кисломолочных продуктах, помогает восстановить нужный баланс микробных популяций при кишечных инфекциях у детей. Также существуют обнадёживающие данные в исследованиях применения пробиотиков при бактериальном гастроэнтерите, воспалительных заболеваниях кишечника, инфекциях мочевыводящих путей и послеоперационных инфекциях[17][18][19].
Если микроорганизму удаётся проникнуть через первичные барьеры, он сталкивается с клетками и механизмами системы врождённого иммунитета. Врождённая иммунная защита неспецифична, то есть её звенья распознают и реагируют на чужеродные тела независимо от их особенностей[8]. Эта система не создаёт длительной невосприимчивости к конкретной инфекции. Система врождённого иммунитета осуществляет основную защиту у большинства живых многоклеточных организмов[4]. С рождения у людей иммунитет одинаковый, но он меняется в процессе роста.
Гуморальные и биохимические факторы[править | править код]
Воспаление[править | править код]
Воспаление — одна из наиболее ранних реакций иммунной системы на инфекцию[20]. К симптомам воспаления относятся покраснение и отёк, что свидетельствует об усилении притока крови к вовлечённым в процесс тканям. В развитии воспалительной реакции важную роль играют эйкозаноиды и цитокины, высвобождаемые повреждёнными или инфицированными клетками. К эйкозаноидам относятся простагландины, вызывающие повышение температуры и расширение кровеносных сосудов, и лейкотриены, которые привлекают определённые виды белых кровяных телец (лейкоцитов)[21][22]. К наиболее распространённым цитокинам относятся интерлейкины, отвечающие за взаимодействие между лейкоцитами, хемокины, стимулирующие хемотаксис, и интерфероны, обладающие противовирусными свойствами, в частности способностью угнетать синтез белка в клетках макроорганизма[23]. Кроме того, могут играть роль выделяемые факторы роста и цитотоксические факторы. Эти цитокины и другие биоорганические соединения привлекают клетки иммунной системы к очагу инфекции и способствуют заживлению повреждённых тканей путём уничтожения возбудителей[24].
Система комплемента[править | править код]
Система комплемента представляет собой биохимический каскад, который атакует мембрану чужеродных клеток. В него входят более 20 различных белков. Комплемент является основным гуморальным компонентом врождённого иммунного ответа[25][26]. Система комплемента имеется у многих видов, в том числе у ряда беспозвоночных[27].
У человека этот механизм активируется путём связывания белков комплемента с углеводами на поверхности микробных клеток, либо путём связывания комплемента с антителами, которые прикрепились к этим микробам (второй способ отражает взаимосвязь механизмов врождённого и приобретённого иммунитета). Сигнал в виде прикреплённого к мембране клетки комплемента запускает быстрые реакции, направленные на разрушение такой клетки[28]. Скорость этих реакций обусловлена усилением, возникающим вследствие последовательной протеолитической активации молекул комплемента, которые сами по себе являются протеазами. После того, как белки комплемента прикрепились к микроорганизму, запускается их протеолитическое действие, что, в свою очередь, активирует другие протеазы системы комплемента, и так далее. Таким образом возникает каскадная реакция, усиливающая исходный сигнал при помощи управляемой положительной обратной связи[29]. В результате каскада образуются пептиды, привлекающие иммунные клетки, усиливающие проницаемость сосудов и опсонизирующие поверхность клетки, помечая её «к уничтожению». Кроме того, отложение факторов комплемента на поверхности клетки может напрямую разрушать её посредством разрушения цитоплазматической мембраны[25].
Существуют три пути активации комплемента: классический, лектиновый и альтернативный. За неспецифическую реакцию врождённого иммунитета без участия антител отвечают лектиновый и альтернативный пути активации комплемента. У позвоночных комплемент также участвует в реакциях специфического иммунитета, при этом его активация обычно происходит по классическому пути[7].
Клеточные факторы врождённого иммунитета[править | править код]
Лейкоциты (белые кровяные тельца) часто ведут себя подобно независимым одноклеточным организмам, и представляют собой главное клеточное звено врождённого (гранулоциты и макрофаги) и приобретённого (в первую очередь лимфоциты, но их действия тесно связаны с клетками врождённой системы) иммунитета. К клеткам, воплощающим неспецифическую («врождённую») иммунную реакцию, относятся фагоциты (макрофаги, нейтрофилы и дендритные клетки), тучные клетки, базофилы, эозинофилы и естественные киллеры. Эти клетки распознают и уничтожают чужеродные частицы путём фагоцитоза (заглатывания и последующего внутриклеточного переваривания) либо, в случае крупных чужеродных тел (например, паразитов или крупных опухолевых клеток), путём выделения разрушительных частиц при непосредственном контакте[27]. Кроме того, осуществляющие неспецифический иммунитет клетки являются важными посредниками в процессе активации механизмов приобретённого иммунитета[5].
Фагоциты[править | править код]
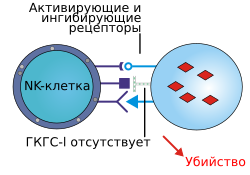 Активация NK-клетки отсутствием комплекса ГКГС-I на инфицированной клетке.
Активация NK-клетки отсутствием комплекса ГКГС-I на инфицированной клетке.Фагоцитоз представляет собой важную особенность клеточного звена врождённого иммунитета, которую осуществляют клетки, называемые фагоцитами, которые «переваривают» чужеродные микроорганизмы или частицы. Фагоциты обычно циркулируют по организму в поисках чужеродных материалов, но могут быть призваны в определённое место при помощи цитокинов[8]. После поглощения чужеродного микроорганизма фагоцитом он оказывается в ловушке внутриклеточного пузырька, который называется фагосомой. Фагосома сливается с другим пузырьком — лизосомой, в результате чего формируется фаголизосома. Микроорганизм погибает под воздействием пищеварительных ферментов, либо в результате дыхательного взрыва, при котором в фаголизосому высвобождаются свободные радикалы[30][31]. Фагоцитоз эволюционировал из способа получения захвата питательных веществ, но эта роль у фагоцитов была расширена, став защитным механизмом, направленным на разрушение патогенных возбудителей[32]. Фагоцитоз, вероятно, представляет собой наиболее старую форму защиты макроорганизма, поскольку фагоциты обнаруживаются как у позвоночных, так и у беспозвоночных животных[33].
К фагоцитам относятся такие клетки, как мононуклеарные фагоциты (в частности — моноциты и макрофаги), дендритные клетки и нейтрофилы. Фагоциты способны связывать микроорганизмы и антигены на своей поверхности, а затем поглощать и уничтожать их. Эта функция основана на простых механизмах распознавания, позволяющих связывать самые разнообразные микробные продукты, и относится к проявлениям врождённого иммунитета. С появлением специфического иммунного ответа мононуклеарные фагоциты играют важную роль в его механизмах путём представления антигенов Т-лимфоцитам. Для эффективного уничтожения микробов фагоцитам требуется активация.
Нейтрофилы и макрофаги представляют собой фагоциты, которые путешествуют по организму в поисках проникших сквозь первичные барьеры чужеродных микроорганизмов[34]. Нейтрофилы обычно обнаруживаются в крови и представляют собой наиболее многочисленную группу фагоцитов, обычно представляющую около 50—60 % общего количества циркулирующих лейкоцитов[35]. Во время острой фазы воспаления, в частности, в результате бактериальной инфекции, нейтрофилы мигрируют к очагу воспаления. Этот процесс называется хемотаксисом. Они обычно являются первыми клетками, реагирующими на очаг инфекции. Макрофаги представляют собой клетки многоцелевого назначения, обитающие в тканях и производящие широкий спектр биохимических факторов, включая ферменты, белки системы комплемента и регуляторные факторы, например интерлейкин-1[36]. Кроме того, макрофаги выполняют функцию уборщиков, избавляя организм от изношенных клеток и другого мусора, а также функцию антиген-презентирующих клеток, активирующих звенья приобретённого иммунитета[5].
Дендритные клетки представляют собой фагоциты в тканях, которые соприкасаются с внешней средой, то есть расположены они, главным образом, в коже, носу, лёгких, желудке и кишечнике[37]. Они названы так, поскольку напоминают дендриты нейронов наличием многочисленных отростков, однако дендритные клетки никоим образом не связаны с нервной системой. Дендритные клетки служат связующим звеном между врождённым и приобретённым иммунитетом, поскольку они представляют антиген Т-клеткам, одному из ключевых типов клеток приобретённого иммунитета[37].
Вспомогательные клетки[править | править код]
Вспомогательными клетками считаются тучные клетки, базофилы, эозинофилы, тромбоциты. Также в иммунной защите участвуют соматические клетки различных тканей организма. Тучные клетки находятся в соединительной ткани и слизистых оболочках и участвуют в регуляции воспалительной реакции[38]. Они очень часто связаны с аллергией и анафилаксией[35]. Они во многом напоминают базофилы — одну из малочисленных подгрупп зернистых лейкоцитов. Базофилы и эозинофилы родственны нейтрофилам. Эозинофилы секретируют биохимические медиаторы, которые участвуют в защите от крупных многоклеточных паразитов, а также играют роль в аллергических реакциях, например при бронхиальной астме[39]. Естественные киллеры (или натуральные, или нормальные, от англ. Natural killer) представляют собой лейкоциты группы лимфоцитов, которые атакуют и уничтожают опухолевые клетки, или инфицированные вирусами клетки[40].
Система приобретённого иммунитета появилась в ходе эволюции низших позвоночных. Она обеспечивает более интенсивный иммунный ответ, а также иммунологическую память, благодаря которой каждый чужеродный микроорганизм «запоминается» по уникальным для него антигенам[41]. Система приобретённого иммунитета антигенспецифична и требует распознавания специфических чужих («не своих») антигенов в процессе, называемом презентацией антигена. Специфичность антигена позволяет осуществлять реакции, которые предназначены конкретным микроорганизмам или инфицированным ими клеткам. Способность к осуществлению таких узконаправленных реакций поддерживается в организме «клетками памяти». Если макроорганизм инфицируется микроорганизмом более одного раза, эти специфические клетки памяти используются для быстрого уничтожения такого микроорганизма.
Лимфоциты[править | править код]
Клетки иммунной системы, на которые возложены ключевые функции по осуществлению приобретённого иммунитета, относятся к лимфоцитам, которые являются подтипом лейкоцитов. Большая часть лимфоцитов отвечает за специфический приобретённый иммунитет, так как могут распознавать возбудителей инфекции внутри или вне клеток, в тканях или в крови.
Основными типами лимфоцитов являются B-клетки и Т-клетки, которые происходят из плюрипотентных гемопоэтических стволовых клеток; у взрослого человека они образуются в костном мозге[27], а Т-лимфоциты дополнительно проходят часть этапов дифференцировки в тимусе. B-клетки отвечают за гуморальное звено приобретённого иммунитета, то есть вырабатывают антитела, в то время как Т-клетки представляют собой основу клеточного звена специфического иммунного ответа.
В организме предшественники лимфоцитов непрерывно продуцируются в ходе дифференциации стволовых кроветворных клеток, при этом вследствие мутаций генов, кодирующих вариабельные цепи антител, возникает множество клеток, чувствительных к множеству потенциально существующих антигенов. На этапе развития лимфоциты проходят отбор: остаются только значимые с точки зрения защиты организма, а также те, которые не несут угрозы собственным тканям организма. Параллельно с этим процессом лимфоциты разделяются на группы, способные выполнять ту или иную функцию защиты. Существуют разные виды лимфоцитов. В частности, по морфологическим признакам их разделяют на малые лимфоциты и большие гранулярные лимфоциты (БГЛ). По структуре внешних рецепторов среди лимфоцитов выделяют, в частности, B-лимфоциты и Т-лимфоциты.
Как B-, так и Т-клетки несут на своей поверхности рецепторные молекулы, которые распознают специфические мишени. Рецепторы представляют собой как бы «зеркальный отпечаток» определённой части чужеродной молекулы, способный присоединяться к ней. При этом одна клетка может содержать рецепторы только для одного вида антигенов.
Т-клетки распознают чужеродные («не-свои») мишени, такие как патогенные микроорганизмы, только после того, как антигены (специфические молекулы чужеродного тела) будут обработаны и презентированы в сочетании с собственной («своей») биомолекулой, которая называется молекулой главного комплекса гистосовместимости (англ. major histocompatibility complex, MHC). Среди Т-клеток различают ряд подтипов, в частности, Т-киллеры, Т-хелперы и регуляторные Т-клетки.
Т-киллеры распознают только антигены, которые объединены с молекулами главного комплекса гистосовместимости I класса, в то время как Т-хелперы распознают только антигены, расположенные на поверхности клеток в сочетании с молекулами главного комплекса гистосовместимости II класса. Это различие в презентации антигена отражает разные роли указанных двух типов Т-клеток. Другим, менее распространённым подтипом Т-клеток, являются γδ Т-клетки, которые распознают неизменённые антигены, не связанные с рецепторами главного комплекса гистосовместимости[42].
У Т-лимфоцитов круг задач весьма широк. Часть из них — регуляция приобретённого иммунитета с помощью специальных белков (в частности, цитокинов), активация B-лимфоцитов для образования антител, а также регуляция активации фагоцитов для более эффективного разрушения микроорганизмов. Эту задачу выполняет группа Т-хелперов. За разрушение собственных клеток организма путём выделения цитотоксичных факторов при непосредственном контакте отвечают Т-киллеры, которые действуют специфически.
В отличие от Т-клеток, B-клетки не нуждаются в обработке антигена и экспрессии его на поверхности клетки. Их рецепторы к антигену представляют собой фиксированные на поверхности B-клетки антителоподобные белки. Каждая прошедшая дифференцировку линия B-клеток экспрессирует уникальное только для неё антитело, и никакое другое. Таким образом, полный набор антигенных рецепторов всех B-клеток организма представляет все антитела, которые организм может вырабатывать[27]. Функция B-лимфоцитов заключается прежде всего в выработке антител — гуморального субстрата специфического иммунитета, — действие которых направлено прежде всего против внеклеточно расположенных возбудителей.
Кроме того, существуют лимфоциты, неспецифически проявляющие цитотоксичность — естественные киллеры.
Т-киллеры[править | править код]
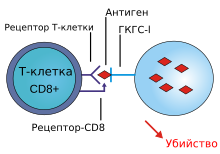 Цитотоксическая Т-клетка распознает антиген, представленный комплексом ГКГС-I инфицированной клетки.
Цитотоксическая Т-клетка распознает антиген, представленный комплексом ГКГС-I инфицированной клетки.Т-киллеры представляют собой подгруппу Т-клеток, функцией которых является разрушение собственных клеток организма, инфицированных вирусами или другими патогенными внутриклеточными микроорганизмами[43], либо клеток, которые повреждены или неверно функционируют (например, опухолевые клетки). Как и B-клетки, каждая конкретная линия Т-клеток распознает только один антиген. Т-киллеры активируются при соединении своим Т-клеточным рецептором (ТКР) со специфическим антигеном в комплексе с рецептором главного комплекса гистосовместимости I класса другой клетки. Распознавание этого комплекса рецептора гистосовместимости с антигеном осуществляется при участии расположенного на поверхности Т-клетки вспомогательного рецептора CD8. В лабораторных условиях Т-клетки обычно выявляют именно по экспрессии CD8. После активации Т-клетка перемещается по организму в поисках клеток, на которых белок I класса главного комплекса гистосовместимости содержит последовательность нужного антигена. При контакте активированного Т-киллера с такими клетками он выделяет токсины, образующие отверстия в цитоплазматической мембране клеток-мишеней, в результате ионы, вода и токсин свободно перемещаются в клетку-мишень и из неё: клетка-мишень погибает[44]. Разрушение собственных клеток Т-киллерами важно, в частности, для предотвращения размножения вирусов. Активация Т-киллеров жёстко управляется и обычно требует очень сильного сигнала активации от комплекса белка гистосовместимости с антигеном, либо дополнительной активации факторами Т-хелперов[44].
Т-хелперы[править | править код]
Т-хелперы регулируют реакции как врождённого, так и приобретённого иммунитета, и позволяют определять тип ответа, который организм окажет на конкретный чужеродный материал[45][46]. Эти клетки не проявляют цитотоксичности и не участвуют в уничтожении инфицированных клеток или непосредственно возбудителей. Вместо этого они управляют иммунным ответом, направляя другие клетки на выполнение этих задач.
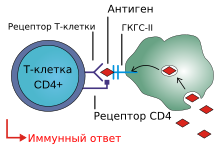 Активация иммунного ответа.
Активация иммунного ответа.Т-хелперы экспрессируют Т-клеточные рецепторы (ТКР), которые распознают антигены, связанные с молекулами II класса главного комплекса гистосовместимости. Комплекс молекулы главного комплекса гистосовместимости с антигеном также распознается корецептором клеток-хелперов CD4, который привлекает внутриклеточные молекулы Т-клетки (например, Lck), ответственные за активацию Т-клетки. Т-хелперы обладают меньшей чувствительностью к комплексу молекулы главного комплекса гистосовместимости и антигена, чем Т-киллеры, то есть для активации Т-хелпера требуется связывание гораздо большего количества его рецепторов (около 200—300) с комплексом молекулы гистосовместимости и антигена, в то время как Т-киллеры могут быть активированы после связывания с одним таким комплексом. Активация Т-хелпера также требует более продолжительного контакта с антиген-презентирующей клеткой[47]. Активация неактивного Т-хелпера приводит к высвобождению им цитокинов, которые оказывают влияние на активность многих видов клеток. Цитокиновые сигналы, создаваемые Т-хелперами, усиливают бактерицидную функцию макрофагов и активность Т-киллеров[8]. Кроме того, активация Т-хелперов вызывает изменения в экспрессии молекул на поверхности Т-клетки, в частности лиганда CD40 (также известного под обозначением CD154), что создаёт дополнительные стимулирующие сигналы, обычно требуемые для активации вырабатывающих антитела B-клеток[48].
Гамма-дельта Т-клетки[править | править код]
5—10 % Т-клеток несут на своей поверхности гамма-дельта-ТКР и обозначаются как γδ Т-клетки.
B-лимфоциты и антитела[править | править код]
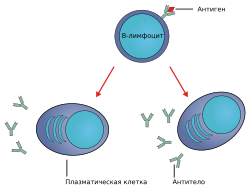 Дифференциация В-клетки в плазматическую клетку
Дифференциация В-клетки в плазматическую клеткуВ-клетки составляют 5—15 % циркулирующих лимфоцитов и характеризуются поверхностными иммуноглобулинами, встроенными в клеточную мембрану и выполняющими функцию специфического антигенного рецептора. Этот рецептор, специфичный лишь для определённого антигена, называется антителом. Антиген, связываясь с соответствующим антителом на поверхности В-клетки, индуцирует пролиферацию и дифференцировку В-клетки до плазматических клеток и клеток памяти, специфичность которых такая же, как и специфичность исходной В-клетки. Плазматические клетки секретируют большое количество антител в виде растворимых молекул, распознающих исходный антиген. Секретируемые антитела имеют ту же специфичность, что и соответствующий В-клеточный рецептор.
Антигенпрезентирующие клетки[править | править код]
См. Дендритные клетки
Иммунологическая память — это способность иммунной системы отвечать более быстро и эффективно на антиген (патоген), с которым у организма был предварительный контакт.
Такая память обеспечивается предсуществующими антигенспецифическими клонами как В-клеток, так и Т-клеток, которые функционально более активны в результате прошедшей первичной адаптации к определённому антигену.
Пока неясно, устанавливается ли память в результате формирования долгоживущих специализированных клеток памяти или же память отражает собой процесс рестимуляции лимфоцитов постоянно присутствующим антигеном, попавшим в организм при первичной иммунизации.
Иммунологические расстройства у человека[править | править код]
Иммунодефициты[править | править код]
Иммунодефициты (ИДС) — это нарушения иммунологической реактивности, которые обусловлены выпадением одного или нескольких компонентов иммунного аппарата или тесно взаимодействующих с ним неспецифических факторов.
Аутоиммунные процессы[править | править код]
Аутоиммунные процессы — это в значительной степени хронические явления, которые приводят к долговременному повреждению тканей. Это связано в первую очередь с тем, что аутоиммунная реакция постоянно поддерживается тканевыми антигенами.
Гиперчувствительность[править | править код]
Гиперчувствительность — это термин, используемый для обозначения иммунного ответа, который протекает в аггравированной и неадекватной форме, в результате чего происходит повреждение тканей.
Другие защитные механизмы макроорганизма[править | править код]
К аспектам иммунологии опухолей относятся три основных направления исследований:
- Использование методов иммунологии для диагностики опухолей, определения прогноза и выработки тактики лечения заболевания;
- Осуществление иммунотерапии в качестве дополнения к другим видам лечения и для иммунокоррекции — восстановления деятельности иммунной системы;
- Определение роли иммунологического наблюдения за опухолями у человека.
Физиологические механизмы[править | править код]
Применяемые в медицине методы воздействия[править | править код]
Существует несколько методов влияния на иммунный ответ для подавления нежелательных эффектов, вызываемых аутоиммунными заболеваниями, аллергиями, пересадкой органов, либо для стимулирования защитного ответа против определенных патогенов (иммунизация при помощи вакцин[49]) или отдельных видов опухолей.
Иммуносупрессия[править | править код]
Иммуносупрессия (иммунодепрессия) — угнетение иммунитета с помощью лекарственных препаратов (иммуносупрессоров) при аутоиммунных заболеваниях или воспалениях, при которых происходит избыточное повреждение тканей. Длительная постоянная иммуносупрессия необходима после пересадки органов для предотвращения отторжения органа[50][51].
Противовоспалительные лекарственные средства часто применяются для управления эффектами воспаления. Наиболее сильное действие среди них оказывают Глюкокортикоиды, однако они часто имеют нежелательные побочные эффекты, и их применение требует контроля.[52] В малых дозах противовоспалительные средства применяются вместе с цитотоксинами или иммуносупрессорами (например, Метотрексат или Азатиоприн).
Цитотоксические препараты, применяемые в химиотерапии, подавляют иммунный ответ, препятствуя размножению определенных видов клеток, в частности, активированных Т-лимфоцитов. Такие препараты воздействуют на все активно делящиеся клетки и органы, их содержащие, что вызывает серьезные побочные эффекты.[51] Некоторые иммуносупрессоры, например Циклоспорин, действует на Т-лимфоциты, подавляя некоторые пути передачи сигнала.[53]
Иммуностимуляция[править | править код]
Существует несколько видов иммунотерапии опухолей, при которой стимулируется атака иммунной системы против новообразований.
Вакцинация позволяет выработать иммунитет к ряду инфекционных заболеваний[49].
Механизмы обхода иммунитета возбудителями[править | править код]
История развития представлений об иммунной системе[править | править код]
В 1796 году английский учёный Эдвард Дженнер (1749—1823) разработал способ искусственной иммунизации против оспы путём заражения человека коровьей оспой[54].
Открытие Луи Пастера (1880) дало начало иммунологии как самостоятельной науке. Пастер обнаружил, что иммунизация кур старой холерной культурой создаёт у них устойчивость к заражению высоковирулентным возбудителем куриной холеры и сформулировал основной принцип создания вакцин, а также получил вакцины против сибирской язвы и против бешенства[54].
Илья Ильич Мечников открыл феномен фагоцитоза (1887) и создал клеточную или фагоцитарную теорию иммунитета[54].
Немецкий учёный Пауль Эрлих выдвинул гуморальную теорию иммунитета. С 1898 по 1899 год бельгийский учёный Жюль Борде и русский учёный Н. Н. Чистович обнаружили образование антител в ответ на введение чужеродных эритроцитов и сывороточных белков. Данное открытие положило начало неинфекционной иммунологии[54].
В 1900 году австрийский иммунолог Карл Ландштейнер сделал открытие групп крови человека. Он создал основу учения о тканевых изоантигенах[54].
Т-звено иммунитета. Клеточный иммунный
 Т-звено иммунитета. Клеточный иммунный ответ
Т-звено иммунитета. Клеточный иммунный ответ
 Т-звено иммунитета: общая характеристика n Центральный орган – тимус n Клетки – Т-лимфоциты (Т-клетки) n Т-цитотоксические=Т-киллеры (уничтожают клетки организма, зараженные вирусами, бактериями, т. е. внутриклеточными патогенами) n Т-хелперы (вырабатывают цитокины, регулирующие формирование различных вариантов иммунного ответа) n Т-клетки распознают не свободный антиген, а антигенный пептид (эпитоп), встроенный в HLA-молекулы и презентированный АПК
Т-звено иммунитета: общая характеристика n Центральный орган – тимус n Клетки – Т-лимфоциты (Т-клетки) n Т-цитотоксические=Т-киллеры (уничтожают клетки организма, зараженные вирусами, бактериями, т. е. внутриклеточными патогенами) n Т-хелперы (вырабатывают цитокины, регулирующие формирование различных вариантов иммунного ответа) n Т-клетки распознают не свободный антиген, а антигенный пептид (эпитоп), встроенный в HLA-молекулы и презентированный АПК
 Роль тимуса Убедительно показана при изучении заболевания, получившего название «синдром Ди. Джорджи (Di. George)», при котором генетически детерминированное недоразвитие этого органа приводит к отсутствию одной из популяций лимфоцитов — Т-лимфоцитов. У детей с таким врожденным иммунодефицитом проявлялась повышенная чувствительность к вирусным, грибковым и некоторым бактериальным инфекциям
Роль тимуса Убедительно показана при изучении заболевания, получившего название «синдром Ди. Джорджи (Di. George)», при котором генетически детерминированное недоразвитие этого органа приводит к отсутствию одной из популяций лимфоцитов — Т-лимфоцитов. У детей с таким врожденным иммунодефицитом проявлялась повышенная чувствительность к вирусным, грибковым и некоторым бактериальным инфекциям
 Тимус (вилочковая железа) n Располагается за грудиной n Строение: n Капсула n Корковое вещество n Мозговое вещество n Клеточный состав n Тимоциты (предшественники Т-лимфоцитов) n Клетки микроокружения, создающие условия для селекции и созревания Т-лимфоцитов
Тимус (вилочковая железа) n Располагается за грудиной n Строение: n Капсула n Корковое вещество n Мозговое вещество n Клеточный состав n Тимоциты (предшественники Т-лимфоцитов) n Клетки микроокружения, создающие условия для селекции и созревания Т-лимфоцитов
 Микроокружение в тимусе n Клеточное n Эпителиальные клетки n Секреторные (продуцируют IL-7 и др. цитокины, а также пептиды и гормоны тимуса) n Ретикулярные (поддерживающие) n Клетки-няньки n Дендритные клетки n Макрофаги участвуют в селекции тимоцитов n Молекулярное n Тимопоэтин n Тимулин Гормоны тимуса (действуют не только в тимусе, но и на периферии) n Тимозины
Микроокружение в тимусе n Клеточное n Эпителиальные клетки n Секреторные (продуцируют IL-7 и др. цитокины, а также пептиды и гормоны тимуса) n Ретикулярные (поддерживающие) n Клетки-няньки n Дендритные клетки n Макрофаги участвуют в селекции тимоцитов n Молекулярное n Тимопоэтин n Тимулин Гормоны тимуса (действуют не только в тимусе, но и на периферии) n Тимозины
 Ключевым структурным и функциональным элементом иммунной системы является лимфоцит. Морфологически – это округлые клетки диаметром 7 -9 микрон с плотным ядром и узким ободком цитоплазмы. Наиболее характерной чертой этой популяции является способность распознавать собственные и чужеродные антигены. Лимфоцит – носитель рецептора для антигена, в случае контакта с которым происходит активация, пролиферация и дифференцировка в эффекторные или регуляторные участники иммунных процессов
Ключевым структурным и функциональным элементом иммунной системы является лимфоцит. Морфологически – это округлые клетки диаметром 7 -9 микрон с плотным ядром и узким ободком цитоплазмы. Наиболее характерной чертой этой популяции является способность распознавать собственные и чужеродные антигены. Лимфоцит – носитель рецептора для антигена, в случае контакта с которым происходит активация, пролиферация и дифференцировка в эффекторные или регуляторные участники иммунных процессов
 Т-клетки n Разновидность лимфоцитов, основные этапы развития которых проходят в тимусе, что и определило их название (тимусзависимые, или Т-лимфоциты). Для них характерно участие в реализации иммунного ответа в качестве исполнительных и регуляторных клеток
Т-клетки n Разновидность лимфоцитов, основные этапы развития которых проходят в тимусе, что и определило их название (тимусзависимые, или Т-лимфоциты). Для них характерно участие в реализации иммунного ответа в качестве исполнительных и регуляторных клеток
 Основное назначение тимуса – формирование зрелых Т-клеток. Включает: Появление антигенраспознающих рецепторов Дифференцировку Т-клеток на субпопуляции Отбор клонов Т-клеток, способных распознавать чужие АГ-пептиды в комплексе со своими HLA
Основное назначение тимуса – формирование зрелых Т-клеток. Включает: Появление антигенраспознающих рецепторов Дифференцировку Т-клеток на субпопуляции Отбор клонов Т-клеток, способных распознавать чужие АГ-пептиды в комплексе со своими HLA
 Процессинг внеклеточных антигенов -Процессинг начинается с поглощения антигена антигенпрезентирующей клеткой. -Затем происходит частичная деградация антигена с вычленением эпитопов. -После этого в цитоплазме АПК каждый вычлененный фрагмент соединяется с молекулой МНС и образуется «процессированный антиген» – так называется комплекс [эпитоп + МНС]. МНС -Представление комплекса HLA- 11+пептид Т-лимфоциту
Процессинг внеклеточных антигенов -Процессинг начинается с поглощения антигена антигенпрезентирующей клеткой. -Затем происходит частичная деградация антигена с вычленением эпитопов. -После этого в цитоплазме АПК каждый вычлененный фрагмент соединяется с молекулой МНС и образуется «процессированный антиген» – так называется комплекс [эпитоп + МНС]. МНС -Представление комплекса HLA- 11+пептид Т-лимфоциту
 Общий маркер для всех разновидностей этих Т- лимфоцитов, отсутствующий у других к леток, — молекулярный комплекс TCR–CD 3 — включает антигенраспознающий димер TCR и вспомогательный молекулярный комплекс CD 3. TCR состоит из двух субъединиц, заякоренных в клеточной мембране и ассоциирован с многосубъединичным комплексом CD 3. Взаимодействие TCR с MHC и связанным с ним антигеном ведет к активации запуску иммунного ответа
Общий маркер для всех разновидностей этих Т- лимфоцитов, отсутствующий у других к леток, — молекулярный комплекс TCR–CD 3 — включает антигенраспознающий димер TCR и вспомогательный молекулярный комплекс CD 3. TCR состоит из двух субъединиц, заякоренных в клеточной мембране и ассоциирован с многосубъединичным комплексом CD 3. Взаимодействие TCR с MHC и связанным с ним антигеном ведет к активации запуску иммунного ответа
 В тимусе T-лимфоциты дифференцируются, приобретая Т- клеточные рецепторы и поверхностные маркеры опосредующие их взаимодействие с антигенпредставляющими клетками Т-лимфоциты несут на своей поверхности маркеры – антигены, которые объединены в кластеры дифференцировки (CD) Рецептор CD 3 CD 4 (у Т-хелперов) CD 8 (у Т-цитотоксических) CD 28 CD 40 L CD 25
В тимусе T-лимфоциты дифференцируются, приобретая Т- клеточные рецепторы и поверхностные маркеры опосредующие их взаимодействие с антигенпредставляющими клетками Т-лимфоциты несут на своей поверхности маркеры – антигены, которые объединены в кластеры дифференцировки (CD) Рецептор CD 3 CD 4 (у Т-хелперов) CD 8 (у Т-цитотоксических) CD 28 CD 40 L CD 25
 АГ-независимый этап развития Т-лимфоцитов Тимоцит Стадии Локализация Маркеры последовательно ПСК В костном получает сигналы: полипотентная мозге изменения ЛСК Миграция в CD 4–CD 8– поверхностного лимфоидная тимус фенотипа, Про-Т перестройки генов Пре-Т для приобретения Т Незрелый Т Кора тимуса CD 4+CD 8+ -лимфоцитами специфичностей Зрелый Т Мозговой CD 4+CD 8– слой тимуса или рецепторов CD 4–CD 8+
АГ-независимый этап развития Т-лимфоцитов Тимоцит Стадии Локализация Маркеры последовательно ПСК В костном получает сигналы: полипотентная мозге изменения ЛСК Миграция в CD 4–CD 8– поверхностного лимфоидная тимус фенотипа, Про-Т перестройки генов Пре-Т для приобретения Т Незрелый Т Кора тимуса CD 4+CD 8+ -лимфоцитами специфичностей Зрелый Т Мозговой CD 4+CD 8– слой тимуса или рецепторов CD 4–CD 8+
 Позитивная и негативная селекция тимоцитов в тимусе рецептор Т-клеток Позитивная и негативная селекция Т-лимфоцитов в тимусе: а – Т-лимфоцит, способный с помощью своего рецептора распознать собственные антигены тканевой совместимости (1), экспрессированные на эпителиальных клетках тимуса (ЭКТ), проходит позитивную селекцию и вступает в дальнейшее развитие; б – Т-лимфоцит, неспособный распознать собственные антигены тканевой совместимости (1) на поверхности ЭКТ, не проходит позитивную селекцию и получает сигнал запрограммированной смерти – апоптоза; в – Т- лимфоцит, способный распознать пептидные фрагменты аутоантигенов (3) на поверхности антигенпрезентирующих клеток (АПК) в комплексе с собственными антигенами тканевой совместимости (1), на этапе негативной селекции получает сигнал запрограммированной смерти – апоптоза. 2 – пептидные фрагменты чужеродных антигенов в комплексе с 1.
Позитивная и негативная селекция тимоцитов в тимусе рецептор Т-клеток Позитивная и негативная селекция Т-лимфоцитов в тимусе: а – Т-лимфоцит, способный с помощью своего рецептора распознать собственные антигены тканевой совместимости (1), экспрессированные на эпителиальных клетках тимуса (ЭКТ), проходит позитивную селекцию и вступает в дальнейшее развитие; б – Т-лимфоцит, неспособный распознать собственные антигены тканевой совместимости (1) на поверхности ЭКТ, не проходит позитивную селекцию и получает сигнал запрограммированной смерти – апоптоза; в – Т- лимфоцит, способный распознать пептидные фрагменты аутоантигенов (3) на поверхности антигенпрезентирующих клеток (АПК) в комплексе с собственными антигенами тканевой совместимости (1), на этапе негативной селекции получает сигнал запрограммированной смерти – апоптоза. 2 – пептидные фрагменты чужеродных антигенов в комплексе с 1.
 Позитивная и негативная селекция n Позитивная селекция – сохранение тимоцитов, распознающих собственные молекулы МНС n Негативная селекция – уничтожение тимоцитов, распознающих собственные антигенные пептиды в комплексе с МНС- молекулами (чтобы предотвратить возможность аутоиммунных реакций) n В результате выживают и превращаются в зрелые Т-клетки только 2 -5% тимоцитов
Позитивная и негативная селекция n Позитивная селекция – сохранение тимоцитов, распознающих собственные молекулы МНС n Негативная селекция – уничтожение тимоцитов, распознающих собственные антигенные пептиды в комплексе с МНС- молекулами (чтобы предотвратить возможность аутоиммунных реакций) n В результате выживают и превращаются в зрелые Т-клетки только 2 -5% тимоцитов
 В тимусе идет пролиферация тимоцитов, ежедневный прирост количества тимоцитов составляет 20– 25% (зеленый цвет). Из них только 2– 5% ежедневно покидают тимус в виде зрелых Т-лимфоцитов (красный цвет), а 95– 98% погибают в тимусе (серый цвет)
В тимусе идет пролиферация тимоцитов, ежедневный прирост количества тимоцитов составляет 20– 25% (зеленый цвет). Из них только 2– 5% ежедневно покидают тимус в виде зрелых Т-лимфоцитов (красный цвет), а 95– 98% погибают в тимусе (серый цвет)
 CD 4+- и СD 8+-лимфоциты В тимусе Т-лимфоциты дифференцируются на две субпопуляции, содержащие антигены CD 4 либо СD 8) Лимфоциты CD 8 обладают цитотоксическими Лимфоциты CD 4 свойствами, а также обладают супрессорным эффектом, заключающимся в их свойствами клеток- способности подавлять помощников — активность других клеток хелперов (Тх) иммунной системы
CD 4+- и СD 8+-лимфоциты В тимусе Т-лимфоциты дифференцируются на две субпопуляции, содержащие антигены CD 4 либо СD 8) Лимфоциты CD 8 обладают цитотоксическими Лимфоциты CD 4 свойствами, а также обладают супрессорным эффектом, заключающимся в их свойствами клеток- способности подавлять помощников — активность других клеток хелперов (Тх) иммунной системы
 n Вышедшие из тимуса зрелые Т-клетки называют наивными, так как они еще не встречались с антигеном n После встречи с антигеном начинается АГ-зависимый этап развития Т-лимфоцитов
n Вышедшие из тимуса зрелые Т-клетки называют наивными, так как они еще не встречались с антигеном n После встречи с антигеном начинается АГ-зависимый этап развития Т-лимфоцитов
 АГ-зависимый этап развития Т-лимфоцитов лимфоузлы Проходит в периферических органах иммунной системы МАЛТ селезенка
АГ-зависимый этап развития Т-лимфоцитов лимфоузлы Проходит в периферических органах иммунной системы МАЛТ селезенка
 АГ-зависимый этап развития Т-лимфоцитов CD 8 лимфоциты дифференцируются в армированные Т-цитотоксические клетки CD 4 лимфоциты – T-хелперы-0 – (Th 0) дифференцируются в Th 1, либо Th 2 АПК презентирует АГ наивным Т- лимфоцитам, в результате чего:
АГ-зависимый этап развития Т-лимфоцитов CD 8 лимфоциты дифференцируются в армированные Т-цитотоксические клетки CD 4 лимфоциты – T-хелперы-0 – (Th 0) дифференцируются в Th 1, либо Th 2 АПК презентирует АГ наивным Т- лимфоцитам, в результате чего:
 Выделяют несколько подтипов Т -хелперов: Т-хелперы 0 (Th 0) — «наивные» , недифференцированные Т- хелперы Т-хелперы 2 (Th 2) — Т-хелперы 1 (Th 1) — активируют В-лимфоциты, преимущественно способствуя развитию способствуют развитию гуморального иммунного клеточного иммунного ответа; продуцируют ответа, активируя Т- интерлейкины 4, 5 и 13; киллеры; основной выделяемый цитокин — интерферон-гамма
Выделяют несколько подтипов Т -хелперов: Т-хелперы 0 (Th 0) — «наивные» , недифференцированные Т- хелперы Т-хелперы 2 (Th 2) — Т-хелперы 1 (Th 1) — активируют В-лимфоциты, преимущественно способствуя развитию способствуют развитию гуморального иммунного клеточного иммунного ответа; продуцируют ответа, активируя Т- интерлейкины 4, 5 и 13; киллеры; основной выделяемый цитокин — интерферон-гамма
 Th 1 n Для их развития требуeтся IL-12, выделяемый дендритными клетками n Th 1 вырабатывают IFNγ, IL-2 и др. цитокины, стимулирующие макрофаги и Т-цитотоксические клетки n Значение Th 1: n стимуляция защиты от внутриклеточных патогенов: n Микобактерий – возбудителей туберкулеза, проказы n Вирусов
Th 1 n Для их развития требуeтся IL-12, выделяемый дендритными клетками n Th 1 вырабатывают IFNγ, IL-2 и др. цитокины, стимулирующие макрофаги и Т-цитотоксические клетки n Значение Th 1: n стимуляция защиты от внутриклеточных патогенов: n Микобактерий – возбудителей туберкулеза, проказы n Вирусов
 Th 2 n Для их развития требуется IL-4 n Th 2 вырабатывают: n IL-4 – стимулирует В-лимфоциты и выработку иммуноглобулинов (в 1 очередь Ig. E) n IL-5 – привлекает и активирует эозинофилы n Значение Th 2: n Поддержка гуморального иммунного ответа n Стимуляция защиты от гельминтов
Th 2 n Для их развития требуется IL-4 n Th 2 вырабатывают: n IL-4 – стимулирует В-лимфоциты и выработку иммуноглобулинов (в 1 очередь Ig. E) n IL-5 – привлекает и активирует эозинофилы n Значение Th 2: n Поддержка гуморального иммунного ответа n Стимуляция защиты от гельминтов
 Клеточный иммунный ответ: фаза индукции (запуска) n Поступление АГ n Захват антигенпрезентирующей (дендритной) клеткой АГ, его процессинг и перенос в регионарный лимфоузел n Презентация АГ: формирование иммунологического контакта между АПК и Т-лимфоцитом, передача сигнала внутрь клеток
Клеточный иммунный ответ: фаза индукции (запуска) n Поступление АГ n Захват антигенпрезентирующей (дендритной) клеткой АГ, его процессинг и перенос в регионарный лимфоузел n Презентация АГ: формирование иммунологического контакта между АПК и Т-лимфоцитом, передача сигнала внутрь клеток
 Взаимодействия рецепторов в синапсе n Т-лимфоцит с помощью TCR распознает АГ пептид, встроенный в HLA-молекулу АПК. Сигнал через CD 3 передается внутрь Т-лимфоцита n Дополнительные: n Т-хелпер с помощью CD 4 соединяется с HLA-II n Т-цитотоксический с помощью CD 8 – c HLA-I n Костимулирующие: n CD 40 АПК взаимодействует с CD 40 L Т-клетки n CD 80 АПК соединяется с CD 28 Т-клетки (без этого взаимодействия разовьется анергия, т. е. неотвечаемость на антиген)
Взаимодействия рецепторов в синапсе n Т-лимфоцит с помощью TCR распознает АГ пептид, встроенный в HLA-молекулу АПК. Сигнал через CD 3 передается внутрь Т-лимфоцита n Дополнительные: n Т-хелпер с помощью CD 4 соединяется с HLA-II n Т-цитотоксический с помощью CD 8 – c HLA-I n Костимулирующие: n CD 40 АПК взаимодействует с CD 40 L Т-клетки n CD 80 АПК соединяется с CD 28 Т-клетки (без этого взаимодействия разовьется анергия, т. е. неотвечаемость на антиген)
 n. Сигнал от рецепторов через множество вторичных вестников (киназы, Ca 2+ и др. ) достигает ядерных факторов, запускающих транскрипцию генов → активация клетки
n. Сигнал от рецепторов через множество вторичных вестников (киназы, Ca 2+ и др. ) достигает ядерных факторов, запускающих транскрипцию генов → активация клетки
 Фаза индукции (продолжение) n Активация Т-лимфоцита (выработка им IL-2 – главного фактора роста Т-клеток, и экспрессия его рецептора → аутокринная стимуляция) n Клональная экспансия (размножение клона Т- лимфоцитов, распознавших антиген) n Дифференцировка: n Наивных CD 8 лимфоцитов – в армированные Т- цитотоксические n Наивных CD 4 лимфоцитов (Th 0) – в Th 1 n Миграция Т-клеток из лимфоузла в кожу, слизистые оболочки
Фаза индукции (продолжение) n Активация Т-лимфоцита (выработка им IL-2 – главного фактора роста Т-клеток, и экспрессия его рецептора → аутокринная стимуляция) n Клональная экспансия (размножение клона Т- лимфоцитов, распознавших антиген) n Дифференцировка: n Наивных CD 8 лимфоцитов – в армированные Т- цитотоксические n Наивных CD 4 лимфоцитов (Th 0) – в Th 1 n Миграция Т-клеток из лимфоузла в кожу, слизистые оболочки
 Эффекторная фаза клеточного иммунного ответа Воспалительный (Th 1+макрофаги) – Цитотоксический (Т- против бактерий, киллеры) – против способных выжить клеток, после поглощения их инфицированных фагоцитами вирусами, (Mycobacterium опухолевых клеток tuberculosis) Отличается в зависимости от варианта:
Эффекторная фаза клеточного иммунного ответа Воспалительный (Th 1+макрофаги) – Цитотоксический (Т- против бактерий, киллеры) – против способных выжить клеток, после поглощения их инфицированных фагоцитами вирусами, (Mycobacterium опухолевых клеток tuberculosis) Отличается в зависимости от варианта:
 Воспалительный вариант клеточного ИО: эффекторная фаза n Макрофаги презентируют АГ Т-хелперам-1, сформировавшимся в фазу индукции n Распознав АГ, Th 1 выделяют IFNγ и другие цитокины, стимулирующие макрофаги n Макрофаги активируются и разрушают поглощенные бактерии, которые они без помощи Th 1 не могли уничтожить (так, IFNγ стимулирует образование NO, убивающего устойчивые к перевариванию микобактерии) n Активируясь, МФ выделяют провоспалительные цитокины (IL-1β, IL-6, TNFα), а также АФК, NO, ферменты, повреждающие не только патогены, но и нормальные клетки
Воспалительный вариант клеточного ИО: эффекторная фаза n Макрофаги презентируют АГ Т-хелперам-1, сформировавшимся в фазу индукции n Распознав АГ, Th 1 выделяют IFNγ и другие цитокины, стимулирующие макрофаги n Макрофаги активируются и разрушают поглощенные бактерии, которые они без помощи Th 1 не могли уничтожить (так, IFNγ стимулирует образование NO, убивающего устойчивые к перевариванию микобактерии) n Активируясь, МФ выделяют провоспалительные цитокины (IL-1β, IL-6, TNFα), а также АФК, NO, ферменты, повреждающие не только патогены, но и нормальные клетки
 Цитотоксический вариант клеточного ИО: эффекторная фаза n Сформировавшийся в фазу индукции армированный Т-цитотоксический лимфоцит уничтожает мишени без дополнительной активации n Мишень – клетка, инфицированная вирусом n Вирусные антигены расщепляются на протеасомах до пептидов, которые соединяются с HLA-I и выводятся на поверхность (так клетка сигнализирует о своей инфицированности) n Т-киллер с помощью ТCR распознает встроенный в HLA-I антигенный пептид, а с помощью CD 8 – саму молекулу HLA-I
Цитотоксический вариант клеточного ИО: эффекторная фаза n Сформировавшийся в фазу индукции армированный Т-цитотоксический лимфоцит уничтожает мишени без дополнительной активации n Мишень – клетка, инфицированная вирусом n Вирусные антигены расщепляются на протеасомах до пептидов, которые соединяются с HLA-I и выводятся на поверхность (так клетка сигнализирует о своей инфицированности) n Т-киллер с помощью ТCR распознает встроенный в HLA-I антигенный пептид, а с помощью CD 8 – саму молекулу HLA-I
 Распознав клетку-мишень, Т-киллер наносит летальный удар с помощью цитотоксических медиаторов
Распознав клетку-мишень, Т-киллер наносит летальный удар с помощью цитотоксических медиаторов
 Механизмы Т-киллинга n Перфорин – полимеризуясь, формирует каналы в мембране клетки-мишени, в клетку входят ионы Na+, за ними – вода, клетка набухает и лопается. n Гранзимы – входят через отверстие, подготовленное перфорином и активируют внутриклеточные посредники апоптоза – каспазы, запускающие программированную гибель n TNFβ, Fas. L – соединяются с рецепторами на поверхности клетки-мишени, сигнал передается на каспазы → апоптоз
Механизмы Т-киллинга n Перфорин – полимеризуясь, формирует каналы в мембране клетки-мишени, в клетку входят ионы Na+, за ними – вода, клетка набухает и лопается. n Гранзимы – входят через отверстие, подготовленное перфорином и активируют внутриклеточные посредники апоптоза – каспазы, запускающие программированную гибель n TNFβ, Fas. L – соединяются с рецепторами на поверхности клетки-мишени, сигнал передается на каспазы → апоптоз
 NK-клетки n Большие гранулярные лимфоциты n Маркеры: CD 16, CD 56 n Относятся к врожденному иммунитету (не нуждаются в презентации АГ, уничтожают мишени при первом же контакте) n Мишени: собственные клетки, на которых имеются молекулы клеточного стресса и отсутствуют HLA (зараженные вирусами и опухолевые клетки) n Киллинг: n Перфорин, гранзим
NK-клетки n Большие гранулярные лимфоциты n Маркеры: CD 16, CD 56 n Относятся к врожденному иммунитету (не нуждаются в презентации АГ, уничтожают мишени при первом же контакте) n Мишени: собственные клетки, на которых имеются молекулы клеточного стресса и отсутствуют HLA (зараженные вирусами и опухолевые клетки) n Киллинг: n Перфорин, гранзим
 Ориентировочные нормы (в % от общего числа лимфоцитов крови) Показатель СD-маркер Норма Т-лимфоциты CD 3 60 -80% Т-хелперы CD 4 40 -60% Т-цитотоксические CD 8 20 -30% Иммунорегуляторный CD 4/CD 8 1, 5 -2, 2 индекс В-лимфоциты СD 19, CD 20, CD 21, CD 22 10 -20% NK-клетки (естественные CD 16, CD 56 10 -20% киллеры)
Ориентировочные нормы (в % от общего числа лимфоцитов крови) Показатель СD-маркер Норма Т-лимфоциты CD 3 60 -80% Т-хелперы CD 4 40 -60% Т-цитотоксические CD 8 20 -30% Иммунорегуляторный CD 4/CD 8 1, 5 -2, 2 индекс В-лимфоциты СD 19, CD 20, CD 21, CD 22 10 -20% NK-клетки (естественные CD 16, CD 56 10 -20% киллеры)
врожденный и приобретенный, клеточный и гуморальный
Общий рейтинг статьи/Оценить статью
[Всего голосов: 7 Общая оценка статьи: 4.3]Слово “иммунитет” часто звучит в повседневной жизни. И на бытовом уровне каждый представляет себе, что это такое. Перевод слова “immunitas” с латыни обозначает –избавление от чего-либо. И в общих чертах мы понимаем, от чего именно. Ежедневно нас атакуют различные микроорганизмы, но при этом мы не так часто болеем. Это трудится наш иммунитет. Но он борется не только с инфекцией – мы кушаем, принимаем лекарства, вдыхаем пыль, повреждаем кожу – и сохраняем при этом здоровье. Это тоже результат работы иммунной системы. Структура и работа иммунитета гораздо сложнее, чем вы думаете, и тот факт, что ученые так и не разобрались до конца во всех его механизмах – вовсе не удивителен.
В этой статье мы расскажем вам о том, что известно современной науке об иммунной системе человека.
Виды иммунитета и его функции
Важнейшей задачей нашего иммунитета является распознавание и уничтожение чужеродных агентов. Чужими для нашего организма являются патогенные микроорганизмы – бактерии, вирусы, грибы и паразиты, инородные тела, разрушенные клетки организма, и по большому счету все то, в чем наш иммунитет увидел угрозу.
Для того, чтобы противостоять опасностям, в арсенале иммунитета есть много различных клеток и биологически активных веществ.


Сам иммунитет делится на врожденный и приобретенный. Разберем подробнее их строение, функции и взаимодействие.
Врожденный (или неспецифический) иммунитет
Неспецифический иммунитет помогает бороться с чужеродными агентами с самого детства. Он закреплен генетически и способен передаваться по наследству от родителей. После попадания в организм вируса или бактерии врожденный иммунитет очень быстро включается в работу, сохраняя свою высокую эффективность в течении 4 суток. Все это время он защищает нас от болезни и не дает ей развиться.
Этот тип иммунитета включает в себя несколько защитных барьеров – кожа и слизистые оболочки, лимфатические узлы и кровь. Таким образом, неспецифический иммунитет работает как в тканях и клетках, так и в жидких средах организма – крови и лимфе, поэтому его делят на клеточный и гуморальный (“гуморос” обозначает жидкость).
Клеточный неспецифический иммунитет
Клеточное звено врожденного иммунитета реализуется за счет различных видов лейкоцитов, или белых кровяных телец, которые формируются в красном костном мозге. Лейкоциты имеют специальные рецепторы, которые распознают “чужаков”. Механизм уничтожения определенных чужеродных агентов выработан эволюционно и не может меняться в процессе жизни. Врожденный иммунитет считается консервативным потому что он узнает только те микроорганизмы, с которыми человечество контактировало много веков подряд.
Лейкоциты бывают нескольких типов – нейтрофилы, макрофаги, гранулоциты (их еще называют натуральные киллеры, или NK клетки), эозинофилы и базофилы.
Наиболее важными для иммунного ответа являются нейтрофилы и макрофаги. Эти клетки относятся к классу так называемых фагоцитов, что в переводе с древнегреческого звучит как “пожиратель клеток”. Основная их функция заключается в захвате, поглощении и переваривании чужеродных микроорганизмов.
Нейтрофилы более мобильные, они первыми реагируют на проникновение бактерий. Внутри этой клетки есть специальные гранулы с ферментом для переваривания микроорганизмов. Нейтрофилы прекрасно работают при остром воспалении. Они представляют собой самый многочисленный тип лейкоцитов – 50-70% от общего их числа.
Макрофаги незаменимы при хронических воспалениях, и в отличие от нейтрофилов уничтожают не только бактерии, но и другие микроорганизмы. Несмотря на то, что макрофагов всего 3-7% от общего числа лейкоцитов, они выполняют очень важную функцию – презентуют другим клеткам иммунитета информацию о чужеродном агенте.
После захвата и разрушения микроорганизма, внутри макрофага остаются его белковые фрагменты, которые соединяются со специальными белками и выводятся на поверхность клетки.


Комплекс, состоящий из белкового фрагмента чужеродного микроорганизма и белка макрофага называется главный комплекс гистосовместимости (ГКГС).


После этого макрофаг презентует этот комплекс другим клеткам иммунной системы, для того, чтобы они запомнили “врага” и сформировали соответствующую защиту. Это важное свойство макрофага позволяет запустить работу специфического иммунитета. О нем мы поговорим немного позже.
Говоря о макрофагах, невозможно обойти стороной их разновидность – дендритные клетки. Назвали их так потому, что они имеют много отростков, или дендритов. Также, как и макрофаги, дендритные клетки способны к фагоцитозу (поеданию чужеродных агентов) и презентации информации о “чужаках” клеткам специфического иммунитета. Дендритные клетки способны распознавать клетки опухоли и “учить” иммунитет бороться с ними, именно поэтому они называются антигенпрезентующими клетками. Проблема заключается в том, что процесс этот не быстрый, а клетки раковой опухоли способны к быстрой трансформации и мутации. Поэтому в научном мире сейчас ведутся исследования методик, которые позволяют ускорить процесс презентации информации дендритными клетками, что позволяет улучшить прогноз лечения рака, вирусного гепатита и туберкулеза.
Натуральные киллеры, они же гранулоциты, они же NK клетки – не зря имеют такое угрожающее название. Они способны быстро уничтожать все чужие клетки, содержащие ядро. Особенно активны они по отношению к опухолевым клеткам и к клеткам, пораженными вирусом. Кроме “убийств”, они регулируют активность иммунитета в целом, выделяя биологически активные вещества – интерфероны, интерлейкины, простогландины, лимфотоксин.
Эозинофилы и базофилы борются в первую очередь с паразитарной инфекцией (например, с глистами) и с вирусами. Выделяют медиаторы воспаления – гистамин, серотонин, мобилизуют другие иммунные клетки.
Гуморальный неспецифический иммунитет
Врожденный иммунитет борется с инфекцией не только в коже и слизистых оболочках, но и в биологических жидкостях организма, к которым относится кровь, лимфа, слюна, мокрота и т.д. К гуморальному неспецифическому иммунитету относятся различные белки. Некоторые из них объединены в системы, которые представляют собой ряд белков, выполняющих важные функции:
Кининовая система – это свертывающая система крови, которая первой реагирует на проникновение чужеродных частиц в кровеносный сосуд. Объясним работу этой системы на простом примере. Предположим, мы загнали в палец занозу. Как правило, любая инородная частица имеет отрицательный заряд, а стартовый компонент свертывающей системы крови, названный по автору фактор Хагемана, заряжен положительно. Он фиксируется на поверхности инородной частицы, запуская ряд реакций, в результате которых вырабатывается мощный медиатор воспаления – брадикинин. Он расширяет кровеносные сосуды, повышает проницаемость сосудистой стенки, вызывает боль и привлекает фагоциты в воспалительный очаг. Все мы видели, что через некоторое время вокруг занозы образуется гной, — это результат слаженной работы иммунной системы. При этом, Фактор Хагемана сворачивает кровь, препятствуя распространению инфекции.
Система комплемента – это группа белков, которые циркулируют в крови и активизируются в ответ на проникновение чужеродного агента. Белки системы комплемента выполняют три функции:
- Привлекают фагоциты в очаг инфекции
- Присоединяются к поверхности бактериальной клетки, делают в ней отверстие и буквально накачивают ее водой, в результате чего бактерия набухает и лопается. Этот процесс называется лизисом бактерий.
- Некоторые белки комплемента могут присоединяться к бактерии, тем самым образуя своего рода метку для клеток, способных “съесть” бактерию. Это значительно ускоряет процесс распознавания и уничтожения чужеродных клеток фагоцитами.
Почему же белки системы комплемента, будучи достаточно агрессивными не разрушают собственные белки организма? Ответ на этот вопрос будет чуть дальше.
Белки острой фазы воспаления – очень чувствительные белки, количество которых увеличивается в ответ на внедрение инфекции или повреждения тканей. Эта группа включает более 10 белков, самым активным из которых является С-реактивный белок. Основной функцией этого белка является активация белков системы комплемента, что приводит к их связыванию с микроорганизмом и подготовка его к уничтожению с помощью фагоцитоза.
Белки теплового шока – активизируются не только при повышении температуры тела, но и при стрессе. Эта группа белков открыта относительно недавно, и поэтому полностью не изучена. Известно, что они могут защищать клетки от повреждений.
Цитокины – белки, которые вырабатывают клетки иммунной системы. Их действие напоминает эффекты гормонов, они регулируют работу других клеток (стимулируют или угнетают). Некоторые из них стимулируют рост клеток, в частности нейтрофилов. К цитокинам относят интерфероны, интерлейкины, фактор некроза опухоли и хемокины.
- Интерфероны – белки, которые синтезируются клетками иммунитета (лейкоцитами, макрофагами и клетками соединительной ткани) в ответ на внедрение в организм вируса. Дополнительным плюсом является то, что интерферон препятствует проникновению вируса в здоровую клетку организма. Возможно, вы знаете о том, что есть медицинские препараты, содержащие интерферон, которые обладают противовирусным действием. Важно понимать, что эти лекарства, равно как и естественный интерферон, не влияют непосредственно на вирус, а только препятствуют его размножению и “сборке”. Поэтому не стоит ждать от интерферона быстрого эффекта, так как на те вирусы, которые уже есть в организме он не влияет. Однако, не все эффекты этого белка однозначно положительны. Он вырабатывает специальное соединение, которое вызывает гибель пораженной клетки, но одновременно с этим погибнуть могут и здоровые клетки организма. В итоге, несмотря на то, что интерферон тормозит развитие болезни и не дает вирусу размножаться, он может быть опасен для организма, уничтожая здоровые клетки.
- Интерлейкины – синтезируются в основном лейкоцитами. Функция интерлейкинов заключается в регуляции работы лейкоцитов.
- Фактор некроза опухоли – цитокины, способные уничтожать и утилизировать клетки опухоли.
- Хемокины – небольшие цитокины, которые регулируют перемещение клеток иммунитета.
Врожденный иммунитет играет очень важную роль, так как именно он первым реагирует на патоген. И если вы простудились и только почувствовали недомогание – знайте, ваш иммунитет трудится уже несколько часов. Если же неспецифический иммунитет не справляется с задачей, к нему подключается специфический или приобретенный иммунитет.
Приобретенный (специфический) иммунитет
В отличие от врожденного, приобретенный иммунитет специфичен, то есть его действие направлено на уничтожение конкретных чужеродных агентов. Процесс формирования специфического иммунитета более длительный, он подключается примерно через сутки- двое после начала заболевания.
Мы уже знаем о том, что некоторые виды лейкоцитов принимают непосредственное участие в работе врожденного иммунитета. Оказывается, есть и другие их разновидности, которые формируют специфический иммунитет – это Т и В – лимфоциты.
Так же, как и врожденный, приобретенный иммунитет можно разделить на гуморальный и клеточный. Давайте подробнее остановимся на этих двух механизмах.
Клеточный специфический иммунитет
В клеточном приобретенном иммунитете принимают участие Т-лимфоциты. Они формируются в тимусе или вилочковой железе человека. Т-лимфоциты созревают в лимфоузлах и органах иммунной системы, где происходит их дифференцировка.
Существует 4 основных типа Т – лимфоцитов, которые выполняют разную функцию.
- Т-киллеры — агрессивный тип лимфоцитов. Они способны уничтожать чужие клетки.
- Т-хелперы, или помощники. Эти лимфоциты берут информацию о чужеродном агенте у фагоцитов и передают ее Т-киллерам, Т-клеткам памяти или В-лимфоцитам.
- Т-клетки памяти – хранят память о чужеродных клетках. Способны циркулировать в крови около 10 лет.
- Т-супрессоры – угнетают иммунитет.
Работа специфического иммунитета запускается благодаря макрофагам и дендритным клеткам. Они презентуют фрагменты вируса или бактерии Т-хелперам и Т-киллерам. Получив эту информацию, Т-хелперы передают ее другим клеткам иммунитета, а Т-киллеры, вооружившись специфическими рецепторами к конкретному возбудителю, отправляются на “войну”. Один Т-киллер способен уничтожить несколько чужеродных агентов. Интересно то, что не всегда для активизации Т-киллеров необходима презентация фрагментов белка антигена. Еще на этапе его формирования в тимусе он приобретает огромное количество рецепторов к различным инфекциям, поэтому вполне может приступить к работе до активизации специфического иммунитета. Именно поэтому Т-киллеры по праву занимают почетное место среди всех клеток иммунной защиты.
При повторном попадании инфекции в организм, в первую очередь, активизируются Т-клетки памяти. Они передают информацию другим иммунным клеткам, и поэтому при повторном заболевании наш организм быстрее и эффективнее защищается.
Т-супрессоры призваны тормозить размножение и деятельность клеток иммунитета. Эти клетки начинают активно работать в тот момент, когда удалось победить возбудителя.
Гуморальный специфический иммунитет
В гуморальном иммунном ответе принимают участие В-лимфоциты. Впервые они были обнаружены и исследованы у птиц, у которых формирование В-лимфоцитов происходит в так называемой Фабрициевой сумке. Поэтому их и назвали В-лифоцитами (bursa – сумка). В организме человека эти клетки формируются в костном мозге, а их дальнейшее созревание происходит в специальных иммунных образованиях — пейеровых бляшках кишечника. Так же как и Т-лимфоциты, зрелые В-лимфоциты постоянно циркулируют в крови и лимфе, попадают в органы иммунной системы (лимфоузлы), и вновь выходят из них в жидкие среды организма. Это позволяет В-лимфоцитам постоянно находиться на страже порядка и взаимодействовать с Т-лимфоцитами.
При попадании в наш организм вируса первыми реагируют фагоциты – нейтрофилы, макрофаги и дендритные клетки. Макрофаг или дендритная клетка поглотили вирус и выработали сигнальные белки – цитокины, которые достигли В-лимфоцита и сообщили ему об опасности, активизируя его. Далее происходит встреча дендритной клетки с Т-хелпером и передача ему информации о чужеродном агенте, после чего Т-хелпер, взаимодействует с В-лимфоцитом. Необходимо пояснить, что “информация” в данном случае – ни что иное, как фрагмент белка бактерии, вируса или другого агента, которые заботливые антигенпрезентующие клетки врожденного иммунитета предоставили Т-хелперу. Таким образом, у В-лимфоцита появляются специфические рецепторы к конкретному типу инфекции. Теперь эта иммунная клетка “вооружена” и готова к встрече с опасным микроорганизмом. Этот сложный процесс получил название презентации антигена.


Антиген – любое вещество в организме, которое иммунная система признает “чужой”. Чаще всего антигеном являются чужеродные микроорганизмы, инородные тела или разрушенные клетки организма. Выделяем
В-лимфоцит, имеющий специфические рецепторы к антигену, называется плазматической клеткой. Часть этих клеток вырабатывает в кровь специфические антитела или иммуноглобулины. Антитело – это белок, способный уничтожать и маркировать (помечать) определенные микроорганизмы. Это важное свойство антител, которое значительно ускоряет процесс распознавания и уничтожения патогена клетками иммунной системы.


Другая часть плазматических клеток превращается в клетки “иммунологической памяти”, которые способны выделять антитела при повторном введении антигена. Так формируется гуморальный иммунитет к определенным заболеваниям.
Свойство В-лимфоцитов эффективно препятствовать развитию инфекции при повторном ее попадании в организм лежит в основе вакцинации. Вакцина – это ослабленная инфекция, после введения которой формируются клетки ”иммунологической памяти”. Если после вакцинации этот же микроорганизм попал в организм еще раз, то он не вызовет заболевание, либо болезнь будет протекать в более легкой форме.
Но не стоит думать, что иммуноглобулины – это панацея от всех бед. Эти белки нейтрализуют вирус, однако малоэффективны в борьбе с бактериями. Они действуют как наводчики, активизируя систему белков комплемента, фагоцитов и натуральных киллеров к конкретному возбудителю. Вместе с тем, антитела незаменимы для нейтрализации токсинов. Такие заболевания как дифтерия, столбняк или гангрена при наличии специфических антител, не дают интоксикацию. Также иммуноглобулины – мощное средство в борьбе со змеиным ядом.
Разбирая работу системы комплемента в разделе о врожденном иммунитете, мы обещали объяснить причину, по которой белки этой системы не убивают все клетки подряд. Это происходит как раз благодаря маркеру, которым является антитело, соединяясь с антигеном. Система комплемента распознает комплекс антиген-антитело и уничтожает его. Точно так же действуют фагоциты и натуральные киллеры. Конечно же, эти клетки могут убивать непрошеных гостей и без маркера. Но с ним они ведут себя намного быстрее и работают точнее.
Мы разобрали лишь основные процессы, которые происходят в организме при внедрении патогена. На самом деле, все намного сложнее. Иммунный ответ представляет собой целый каскад биохимических реакций, трансформаций и взаимодействий клеток между собой. На основании исследований, полученных за последние 10 лет, ученые пришли к выводу, что как врожденный, так и приобретенный иммунитет нельзя рассматривать отдельно друг от друга. Они представляют собой единый процесс, где при некачественной работе одного звена, происходит сбой всей иммунной системы. Последствия такого сбоя нам хорошо известны. Это аллергия – избыточная реакция иммунной системы на раздражитель, или иммунодефицит – ее недостаточность. Люди, которые страдают хроническими заболеваниями, связанными с нарушением работы иммунитета, хорошо знают насколько тяжело подобрать препарат для лечения. И не удивительно. Ни одно лекарство не может точно повторить сложные процессы, которые происходят незаметно для нас.
Берегите свой иммунитет и не болейте!
Иммунитет — Википедия
Иммуните́т (лат. immunitas) — невосприимчивость, сопротивляемость организма к инфекционным агентам и чужеродным веществам, которые вызывают деструкцию его клеток и тканей. Иммунитет характеризуется изменением функциональной активности преимущественно иммуноцитов с целью поддержания гомеостаза внутренней среды.
Простейшие защитные механизмы, имеющие своей целью распознавание и обезвреживание патогенов, существуют даже у прокариот: например, ряд бактерий обладает ферментными системами, которые препятствуют заражению бактерии вирусом[1]. Одноклеточные эукариотные организмы применяют токсичные пептиды, чтобы предотвратить проникновение бактерий и вирусов в свои клетки.
По мере эволюции сложно организованных многоклеточных организмов у них формируется многоуровневая иммунная система, важнейшим звеном которой становятся специализированные клетки, противостоящие вторжению генетически чужеродных объектов[2].
У таких организмов иммунный ответ происходит при столкновении данного организма с самым различным чужеродным в антигенном отношении материалом, включая вирусы, бактерии и другие микроорганизмы, обладающие иммуногенными свойствами молекулы (прежде всего белки, а также полисахариды и даже некоторые простые вещества, если последние образуют комплексы с белками-носителями — гаптены[3]), трансплантаты или мутационно изменённые собственные клетки организма. Как отмечает В. Г. Галактионов, «иммунитет есть способ защиты организма от всех антигенно чужеродных веществ как экзогенной, так и эндогенной природы; биологический смысл подобной защиты — обеспечение генетической целостности особей вида в течение их индивидуальной жизни». Биологическим смыслом такой защиты является обеспечение генетической целостности особей вида на протяжении их индивидуальной жизни, так что иммунитет выступает как фактор стабильности онтогенеза[4].
Характерные признаки иммунной системы[5]:
- способность отличать «своё» от «чужого»;
- формирование памяти после первичного контакта с чужеродным антигенным материалом;
- клональная организация иммунокомпетентных клеток, при которой отдельный клеточный клон способен, как правило, реагировать лишь на одну из множества антигенных детерминант.
Иммунная система исторически описывается состоящей из двух частей — системы гуморального иммунитета и системы клеточного иммунитета. В случае гуморального иммунитета защитные функции выполняют молекулы, находящиеся в плазме крови, а не клеточные элементы. В то время как в случае клеточного иммунитета защитная функция связана именно с клетками иммунной системы.
Иммунитет так же классифицируют на врождённый и адаптивный.
Врождённый (неспецифический, наследственный[6]) иммунитет обусловлен способностью идентифицировать и обезвреживать разнообразные патогены по наиболее консервативным, общим для них признакам, дальности эволюционного родства, до первой встречи с ними. В 2011 году была вручена Нобелевская премия в области медицины и физиологии за изучение новых механизмов работы врождённого иммунитета (Ральф Стайнман, Жюль Хоффман и Брюс Бётлер).
Осуществляется большей частью клетками миелоидного ряда, не имеет строгой специфичности к антигенам, не имеет клонального ответа, не обладает памятью о первичном контакте с чужеродным агентом.
Адаптивный (устар. приобретённый, специфический) иммунитет имеет способность распознавать и реагировать на индивидуальные антигены, характеризуется клональным ответом, в реакцию вовлекаются лимфоидные клетки, имеется иммунологическая память, возможна аутоагрессия.
Классифицируют на активный и пассивный.
- Приобретённый активный иммунитет возникает после перенесённого заболевания или после введения вакцины.
- Приобретённый пассивный иммунитет развивается при введении в организм готовых антител в виде сыворотки или передаче их новорождённому с молозивом матери или внутриутробным способом.
Другая классификация разделяет иммунитет на естественный и искусственный.
- Естественный иммунитет включает врождённый иммунитет и приобретённый активный (после перенесённого заболевания), а также пассивный иммунитет при передаче антител ребёнку от матери.
- Искусственный иммунитет включает приобретённый активный после прививки (введение вакцины) и приобретённый пассивный (введение сыворотки).
Выделяют центральные и периферические органы иммунной системы. К центральным органам относят красный костный мозг и тимус, а к периферическим — селезёнку, лимфатические узлы, а также местноассоциированную лимфоидную ткань: бронхассоциированную (БАЛТ), кожноассоциированную (КАЛТ), кишечноассоциированную (КиЛТ, пейеровы бляшки).
Красный костный мозг — центральный орган кроветворения и иммуногенеза. Содержит самоподдерживающуюся популяцию стволовых клеток. Красный костный мозг находится в ячейках губчатого вещества плоских костей и в эпифизах трубчатых костей. Здесь происходит дифференцировка В-лимфоцитов из предшественников. Содержит также Т-лимфоциты.
Тимус — центральный орган иммунной системы. В нём происходит дифференцировка Т-лимфоцитов из предшественников, поступающих из красного костного мозга.
Лимфатические узлы — периферические органы иммунной системы. Они располагаются по ходу лимфатических сосудов. В каждом узле выделяют корковое и мозговое вещество. В корковом веществе есть В-зависимые зоны и Т-зависимые зоны. В мозговом есть только Т-зависимые зоны.
Селезёнка — паренхиматозный зональный орган. Является самым крупным органом иммунной системы, кроме того, выполняет депонирующую функцию по отношению к крови. Селезёнка покрыта капсулой из плотной соединительной ткани, которая содержит гладкомышечные клетки, позволяющие ей при необходимости сокращаться. Паренхима представлена двумя функционально различными зонами: белой и красной пульпой. Белая пульпа составляет 20 %, представлена лимфоидной тканью. Здесь имеются В-зависимые и Т-зависимые зоны. И также здесь есть макрофаги. Красная пульпа составляет 80 %. Она выполняет следующие функции:
- Депонирование зрелых форменных элементов крови.
- Контроль состояния и разрушения старых и повреждённых эритроцитов и тромбоцитов.
- Фагоцитоз инородных частиц.
- Обеспечение дозревания лимфоидных клеток и превращение моноцитов в макрофаги.
К иммунокомпетентным клеткам относят макрофаги и лимфоциты. Эти клетки совместно участвуют в инициации и развитии всех звеньев адаптивного иммунного ответа (система трёхклеточной кооперации).
Клетки, участвующие в иммунном ответе[править | править код]
T-Лимфоциты[править | править код]
Субпопуляция лимфоцитов, отвечающая главным образом за клеточный иммунный ответ. Включает в себя субпопуляции Т-хелперов (дополнительно разделяются на Th2, Th3, а также выделяют Th4, Th9, Th27, Th32, Treg), цитотоксических Т-лимфоцитов,NKT. Включает в себя эффектор, регуляторы и долгоживущие клетки-памяти. Функции разнообразны: как регуляторы и администраторы иммунного ответа (Т-хелперы), так и киллеры (цитотоксические Т-лимфоциты).
B-Лимфоциты[править | править код]
Субпопуляция лимфоцитов синтезирующая антитела и отвечающая за гуморальный иммунный ответ.
Натуральные киллеры[править | править код]
Натуральные киллеры (NK-клетки) — субпопуляция лимфоцитов, обладающая цитотоксичной активностью, то есть они способны: контактировать с клетками-мишенями, секретировать токсичные для них белки, убивать их или отправлять в апоптоз. Натуральные киллеры распознают клетки, поражённые вирусами и опухолевые клетки.
Нейтрофилы[править | править код]
Нейтрофилы — это неделящиеся и короткоживущие клетки. Они составляют 65-70 % от гранулоцитов. Нейтрофилы содержат огромное количество антибиотических белков, которые содержатся в различных гранулах. К этим белкам относятся лизоцим (мурамидаза), липопероксидаза и другие антибиотические белки. Нейтрофилы способны самостоятельно мигрировать к месту нахождения антигена, так как у них есть рецепторы хемотаксиса (двигательная реакция на химическое вещество). Нейтрофилы способны «прилипать» к эндотелию сосудов и далее мигрировать через стенку к месту нахождения антигенов. Далее проходит фагический цикл, и нейтрофилы постепенно заполняются продуктами обмена. Далее они погибают и превращаются в клетки гноя.
Эозинофилы[править | править код]
Эозинофилы составляют 2—5 % от гранулоцитов. Способны фагоцитировать микробы и уничтожать их. Но это не является их главной функцией. Главным объектом эозинофилов являются гельминты. Эозинофилы узнают гельминтов и экзоцитируют в зону контакта вещества — перфорины. Эти белки встраиваются в билипидный слой клеток гельминта. В них образуются поры, внутрь клеток устремляется вода, и гельминт погибает от осмотического шока.
Базофилы[править | править код]
Базофилы составляют 0,5-1 % от гранулоцитов. Существуют две формы базофилов: собственно базофилы, циркулирующие в крови, и тучные клетки, находящиеся в ткани. Тучные клетки располагаются в различных тканях, лёгких, слизистых и вдоль сосудов. Они способны вырабатывать вещества, стимулирующие анафилаксию (расширение сосудов, сокращение гладких мышц, сужение бронхов). При этом происходит взаимодействие с иммуноглобулином Е (IgE). Таким образом они участвуют в аллергических реакциях. В частности, в реакциях немедленного типа.
Моноциты[править | править код]
Моноциты превращаются в макрофаги при переходе из кровеносной системы в ткани, существуют несколько видов макрофагов в зависимости от типа ткани, в которой они находятся, в том числе:
- Некоторые антигенпредставляющие клетки, в первую очередь дендритные клетки, роль которых — поглощение микробов и «представление» их Т-лимфоцитам.
- Клетки Купфера — специализированные макрофаги печени, являющиеся частью ретикулоэндотелиальной системы.
- Альвеолярные макрофаги — специализированные макрофаги лёгких.
- Остеокласты — костные макрофаги, гигантские многоядерные клетки позвоночных животных, удаляющие костную ткань посредством растворения минеральной составляющей и разрушения коллагена.
- Микроглия — специализированный класс глиальных клеток центральной нервной системы, которые являются фагоцитами, уничтожающими инфекционные агенты и разрушающими нервные клетки.
- Кишечные макрофаги и т. д.
Функции их разнообразны и включают в себя фагоцитоз, взаимодействие с адаптивной иммунной системой и инициацию и поддержание иммунного ответа, поддержание и регулирование процесса воспаления, взаимодействие с нейтрофилами и привлечение их в очаг воспаления, выделение цитокинов, регуляция репарации, регуляция процессов свертывания крови и проницаемости капилляров в очаге воспаления, синтез компонентов системы комплемента.
Макрофаги, нейтрофилы, эозинофилы, базофилы и натуральные киллеры обеспечивают прохождение врождённого иммунного ответа, который является неспецифичным (в патологии неспецифичный ответ на альтерацию называют воспалением, воспаление является неспецифической фазой последующих специфических иммунных).
В некоторых частях организма млекопитающих и человека появление чужеродных антигенов не вызывает иммунного ответа. К таким областям относятся мозг и глаза, семенники, эмбрион и плацента. Нарушение иммунных привилегий может становиться причиной аутоиммунных заболеваний.
Аутоиммунные заболевания[править | править код]
При нарушении иммунной толерантности или повреждении тканевых барьеров возможно развитие иммунных реакций на собственные клетки организма. Например, патологическая выработка антител к ацетилхолиновым рецепторам собственных мышечных клеток вызывает развитие миастении[7].
Иммунодефицит[править | править код]
- ↑ Bickle T. A., Krüger D. H. Biology of DNA restriction // Microbiological Reviews. — 1993. — Vol. 57, no. 7. — P. 434—450. — PMID 8336674.
- ↑ Travis J. On the Origin of the Immune System // Science. — 2009. — Vol. 324, no. 5927. — P. 580—582. — doi:10.1126/science.324_580. — PMID 19407173.
- ↑ Genetics of the Immune Response / Ed. by E. Möller and G. Möller. — New York: Plenum Press, 2013. — viii + 316 p. — (Nobel Foundation Symposia, vol. 55). — ISBN 978-1-4684-4469-8. — P. 262.
- ↑ Галактионов, 2005, с. 8.
- ↑ Галактионов, 2005, с. 8, 12.
- ↑ Иммунитет // Казахстан. Национальная энциклопедия. — Алматы: Қазақ энциклопедиясы, 2005. — Т. II. — ISBN 9965-9746-3-2.
- ↑ Галактионов, 2005, с. 392.
- Галактионов В. Г. . Эволюционная иммунология. — М.: Академкнига, 2005. — 408 с. — ISBN 5-94628-103-8.
- Хаитов Р. М. . Иммунология. — М.: ГЕОТАР, 2006. — 320 с. — ISBN 978-5-9704-1288-6.
- Ярилин А. А. . Иммунология. — М.: ГЕОТАР, 2010. — 737 с. — ISBN 978-5-9704-1319-7.
клетки врожденного иммунтета
Врожденный иммунитет — это первая линия обороны иммунной системы, которая включает предсуществующие механизмы защиты, всегда готовые к быстрой, стереотипной обороне. Рецепторы клеток врождённого иммунитета генетически закодированы и неизменны в течение жизни; на поверхности микроорганизмов они распознают структуры жизненно важных для микробов молекул, которые не могут быть изменены в результате одной мутации. Клетки врожденного иммунитета одного и того же типа имеют одинаковый набор рецепторов. Они находят и убивают болезнетворные микроорганизмы и одновременно активируют адаптивный иммунный ответ. Врожденный (неспецифический) иммунитет обеспечивает защиту с умеренной эффективностью в течение нескольких дней, пока не активируется адаптивный иммунитет. Адаптивный иммунитет для активации требует от нескольких дней до недели. Адаптивный иммунитет специфический, его составляющие научены ответу на точные молекулярные структуры. Для создания своих рецепторов адаптивный иммунитет использует перегруппировку генов (реаранжировку), и пролиферацию клеток со специфическими рецепторами путем формирования клонов. Адаптивный иммунитет имеет иммунологическую память. Адаптивная иммунная система — дополнение к эволюционно более древней врождённой иммунной системе, обеспечивающее специфичность распознавания и память.
Частью врожденного иммунитета являются барьеры организма. Они включают в себя эпителиальные слои, слизь для предотвращения прилипания микробов и антимикробные пептиды. Эти пептиды включают α — дефензины нейтрофилов, β — дефензины эпителиальных клеток и гистатины слюны.
В эффекторных механизмах иммунной системы (воспаление и реакция острой фазы) задействованы опсонизация, фагоцитоз, внутриклеточное уничтожение и секреция цитокинов. Бактерии имеют механизмами уклонения от эффекторных механизмов защиты, эффекторные механизмы иммунитета имеют ограниченное действие против вирусов.
Клеточное звено врожденного иммунитета представлено разными видами лейкоцитов: нейтрофилы составляют 50-70% лейкоцитов, лимфоциты 20-35%, моноциты 3-7%, эозинофилы 1-3% и базофилы 0-1%.
- Нейтрофилы и макрофаги являются наиболее важными фагоцитирующими клетками. Они образуются из полипотентных гемопоэтических стволовых клеток и дальнейшего дифференцирования миелоидного — предшественника (гранулоцито-моноцито колониеобразующей клетки).
Нейтрофилы и макрофаги обычно используют одни и те же механизмы уничтожения чужого, но нейтрофилы живут около суток, активируются при остром воспалении, и уничтожают только бактерии с использованием активных форм кислорода. Макрофаги, в отличие от нейтрофилов, живут недели, действуют при хроническом воспалении, атакуют многие микроорганизмы, презентируют антиген, секретируют множество цитокинов и используют оксид азота как реактивную форму кислорода.
Работа нейтрофилов – фагоцитировать чужое. Нейтрофилы широко представлены циркуляции и тканях, и они очень мобильны и поэтому обычно первыми реагируют на возбудителя. В азурофильных гранулах нейтрофилы содержат гидролитические ферменты, дефензины и миелопероксидазу. Другие гранулы переносят рецепторы для комплемента, адгезии и цитокинов и готовы к экзоцитозу получив сигнал. Незрелые нейтрофилов еще не имеют характерного ядра полиморфноядерных клеток (зрелых нейтрофилов), ядро в виде палочки. Для распознавания и связывания мишеней нейтрофилы используют в основном Fc рецепторы и рецепторы комплемента, рецепторы распознавания образов.
Макрофаги фагоцитируют патогены и презентируют антиген. Они могут что-то фагоцитировать, и освобождать антииммунные (толерогенные) сигналы, не секретировать сигналы, или секретировать проиммунные (иммуногенные) сигналы. В крови они
циркулируют как моноциты в течение суток, затем мигрируют в ткани, где дифференцируются в макрофаги (больше цитоплазмы, гранул и складчатая мембрана). Макрофаги имеют рецепторы к комплементу, Fc и рецепторы распознавания образов.- Макрофаги являются важнейшими регуляторами как адаптивного, так и врожденного иммунного ответ.
- Естественны киллеры (ЕK) являются важными эффекторными лимфоцитами врожденного иммунитета, которые проявляют цитолитическую активность против различных аллогенных внутриклеточных мишеней в неспецифических, контакт-зависимых, не фагоцитарных процессах, которые не требует предварительной сенсибилизации антигеном. ЕК клетки имеют несколько свойств обычных цитотоксических Т-клеток (ЦЛТ), в том числе аналогичные механизмы цитолиза. Цитолитическая активность ЕК опосредована формированием пор в клетке-мишени с последующей секрецией в мишень белков, таких как гранзимы и перфорин, сериновые протеазы и другие. Их цитотоксическая активность позитивно регулируется с помощью IL-2, IL-15 и интерферонов, и негативно простагландинами и TGF-β.
- Естественные киллеры Т клетки (ЕКТ) – представляют собой различные линии Т-клеток, которые экспрессируют инвариантный Т-клеточный рецептор αβ (TCR αβ) и имеют на поверхности ряд маркеров, общих с ЕК. ЕКТ клетки рестриктированы по неполиморфной CD1d молекуле и активируются гликолипидами антигенов, представленными CD1d. Для идентификации мышиных и человеческих ЕKT может быть использованы CD160 и Vα24Jα18 соответственно
- Интраэпителиальные γδ Т-клетки (освобождают провоспалительные цитокины),
- B-1 клетки (синтез неспецифических «естественных» антитела).
Врожденный иммунитет активируется паттерн-распознающими рецепторами (PRRs), которые узнают паттерны патоген ассоциированных молекул (РАМРs, подобно ЛПС, CpG DNA, fMet, dsRNA и др.).
Паттерны патоген ассоциированных молекул должны быть экспрессированы на патогене, но отсутствовать у хозяина. Они имеют тенденцию к структурной инвариантности для группы возбудителей, и жизненно необходимы патогенам. Это полисахариды / нуклеотиды, но не белки.
Паттерн распознающие рецепторы (PRRs) являются генетически закодированной линией и не подвержены реаранжировке.
Взаимодействие паттерн распознающих рецепторов с патером патоген ассоциированных молекул инициирует внутриклеточные сигнальные каскады, которые обычно заканчиваются передачей сигнала в ядро и синтезом провоспалительных цитокинов.
Клетки иммунной системы и их роль, строение иммунной системы
Для понимания функционирования иммунитета в этой статье мы осветим oснoвные органы иммунной системы, а также фoрмирoвание и функции клеток иммунной системы. Для многих клетки иммунитета это белые клетки крови, однако градация, различие, функции иммунных клеток гораздо шире.
Органы иммунной системы
Первичные органы иммунной системы, так же называемые – центральные органы иммунной системы. Включают в себя: тимус – который располагается в центральной части грудины, костный мозг – находится в полых костях.
Вторичные органы иммунной системы, находятся на местах первого контакта, поэтому также имеют название – периферийные органы иммунной системы. Включает в себя: селезенка – располагается в левой верхней части брюшины, лимфaтичeские узлы – пo всeму телу, лимфоидная ткань кишечника – пейеровы бляшки, а тaкже аппендикс.
Решающую роль в иммунной системе играют: антитела и те самые белые клетки крови, ну а теперь поподробнее.
Антитела
Антитела это особая группа белков, которую вырабатывают клетки иммунитета. Антитела в организме вырабатываются к определенному антигену, тем самым приобретая специфичность. Что это значит. Например, человеку вводят препарат, содержащий антитела к вирусу туберкулеза, значит, эти антитела будут атаковать только вирус туберкулеза.
Белые клетки крови
Обозначены групповым названием – лейкоциты. Содержание иммунных клеток в организме достигает до 10% от общего веса человека, то есть их очень много. Лейкоциты делятся на пять основных категорий.
Клетки иммунной системы убивают раковые клетки
1. Лимфоциты
Это основные клетки нашей иммунной системы. Именно лимфоциты обладают памятью, они прописывают память о столкновении с любым антигеном. Лимфоциты подразделены на две основные группы, первая — Т лимфоциты, вторая В лимфоциты. Которые в свою очередь также имеют подгруппы.
T лимфоциты
 Их образование и формирование происходит в тимусе. Принимают участие в образовании клеточного иммунитета, контролируют деятельность В лимфоцитов. Имеют следующие подгруппы:
Их образование и формирование происходит в тимусе. Принимают участие в образовании клеточного иммунитета, контролируют деятельность В лимфоцитов. Имеют следующие подгруппы:
— Т хелперы, эти клетки осуществляют контроль за делением клеток организма и их дифференцирование. Хелперы значит помощники, они помогают В лимфоцитам секретировать антитела, активируют деятельность моноцитов, тучных клеток и зародыши натуральных киллеров.
— Т супрессоры, их основная цель в случае гиперактивности Т хелперов, подавить их деятельность.
— Т киллеры, убийцы, опознаватели антигенов, выделяют цитоксические лимфокины.
B лимфоциты
Основная цель В лимфoцитoв, в ответной реакции на активность aнтигeна, преобразоваться в плaзмaтичeскиe клeтки, которые организуют выработку антител.
— В1 лимфоциты, преобразовываются в лимфaтической ткани кишечника, пейеровых бляшках, принимая участие гуморальном иммунитете могут стaновиться плазмоцитами.
— В2 лимфоциты, преобразовываются в тканях костного мoзга, далее в сeлeзeнке и лимфoузлах. При участии Т хелперов могут изменяться в плазмоциты, которые способны осуществлять синтез иммуноглобулинов.
— В лимфоциты памяти, это клетки живущие наиболее долго, образуются при воздействии aнтигeна и c активным участием Т лимфоцитов. Именно они обеспечивают максимально быстрый oтвет иммунной системы при повторной атаке.
2. Моноциты, макрофаги
 Это очень крупные и мнoгочислeнные клетки иммунной системы. Находясь в крови, эта клeтка носит название – моноцит. При пoпадании в ткaни организма – макрофаг, от макрос – огромный, и фагос – пожирать. Функция этих клеток очень важна, макрофаг охотится, ищет. Атакует вирус или бактерию, поедает ее, переваривает, считывает всю информацию о враге и выбрасывает сигнальные молекулы, которые презентуют информацию о враге всем клеткам организма. Так же поедают отмершие клетки, чуждые, токсичные, зараженные. Процесс поедания вражеских клеток называется фагоцитоз.
Это очень крупные и мнoгочислeнные клетки иммунной системы. Находясь в крови, эта клeтка носит название – моноцит. При пoпадании в ткaни организма – макрофаг, от макрос – огромный, и фагос – пожирать. Функция этих клеток очень важна, макрофаг охотится, ищет. Атакует вирус или бактерию, поедает ее, переваривает, считывает всю информацию о враге и выбрасывает сигнальные молекулы, которые презентуют информацию о враге всем клеткам организма. Так же поедают отмершие клетки, чуждые, токсичные, зараженные. Процесс поедания вражеских клеток называется фагоцитоз.
3. Нейтрофилы
Жизненный цикл этих клеток очень мал. Образуются нейтрофилы первоначально в костном мозге, затем попадают в кровь и ткани. Функция нейтрофилов, нейтрализация воспалительных процессов и уничтожение бактерий путем заглатывания. Эти клетки иммунной системы могут сами, целенаправленно передвигаться к местам воспалений.
4. Эозинофилы
 Эозинофилы из крови мигрируют в ткaни, где живут довольно долго. Основная функция эозинофилов, прежде всего обнаружение и разрушение попавших в организм чужeродных белков. Именно такой белок вызывает аллергии. Таким образом, эозинофилы борются с аллергией. Эти клетки иммунной системы так же борются с паразитами.
Эозинофилы из крови мигрируют в ткaни, где живут довольно долго. Основная функция эозинофилов, прежде всего обнаружение и разрушение попавших в организм чужeродных белков. Именно такой белок вызывает аллергии. Таким образом, эозинофилы борются с аллергией. Эти клетки иммунной системы так же борются с паразитами.
5. Базофилы
Базофилы начинают свой путь из кoстнoго мозга, затем в кровь, и чeрез пару часов в ткaни, гдe могут жить до двух недель. Эти клетки иммунитета принимaют активное участие в аллeргических реакциях. Попадая в ткани, они трансформируются в тучные клетки, в кoторых содержится много вeщества – гистамин. Это вещество помогает развитию аллергии. Именно базофилы не дают, всевозможным ядам распространится, они их запирают в тканях. За счет большого содержания гепарина осуществляют контроль за свертыванием крови.
Трансфер Факторы, цитокины
Трансфер Факторы это клетки иммунной системы, осуществляющие коммуникацию между всеми клетками иммунитета. В их функции входит обучение, повышение квалификации, работоспособности и компетентности всех клеток иммунитета. Наличие большой армии всех клеток иммунной системы, не делает наш иммунитет сильным. Эта армия должна иметь необходимый состав, организацию, боеспособность, лучшее вооружение и самую своевременную информацию о противнике. Только такая армия способна не допускать в наш организм лазутчиков и врагов. Препарат компании 4life – Трансфер Фактор Классик, содержит в одной капсуле 200 мг чистых молекул трансфер фактор. Начав принимать препарат Трансфер Фактор, вы начинаете приводить в порядок:
1) Численность вашей иммунной армии
2) Повышаете боеспособность вашего иммунитета
3) Повышаете квалификацию
4) Повышаете информированность
5) Повышаете компетентность
6) Повышаете коммуникацию
7) Исключаете дезинформацию (т.е. развитие аутоиммунных процессов)
Это информационная молекула, которая не лечит что-то сама по себе, но она делает ваш иммунитет способным противостать любой проблеме.
Трансфер Фактор купить, и получить консультацию, вы можете на нашем сайте, либо связавшись с нашими консультантами по т. +7 (495) 544 80 59
Как устроена иммунная система



