Биологическое значение железа — Самый важный металл
В живых организмах железо является важным микроэлементом, катализирующим процессы обмена кислородом (дыхания). В организме взрослого человека содержится около 3,5 грамма железа (около 0,02 %), из которых 78 % являются главным действующим элементом гемоглобина крови, остальное входит в состав ферментов других клеток, катализируя процессы дыхания в клетках. Недостаток железа проявляется как болезнь организма (хлороз у растений и анемия у животных).
Обычно железо входит в ферменты в виде комплекса, называемого гемом. В частности, этот комплекс присутствует в гемоглобине — важнейшем белке, обеспечивающем транспорт кислорода с кровью ко всем органам человека и животных. И именно он окрашивает кровь в характерный красный цвет.
Комплексы железа, отличные от гема, встречаются, например, в ферменте метан-моноксигеназе, окисляющем метан в метанол, в важном ферменте рибонуклеотид-редуктазе, который участвует в синтезе ДНК.
Неорганические соединения железа встречаются в некоторых бактериях, иногда используется ими для связывания азота воздуха.
В организм животных и человека железо поступает с пищей (наиболее богаты им печень, мясо, яйца, бобовые, хлеб, крупы, свёкла). Интересно, что некогда шпинатошибочно был внесён в этот список (из-за опечатки в результатах анализа — был потерян «лишний» ноль после запятой).
Суточная потребность человека в железе следующая: дети — от 4 до 18 мг, взрослые мужчины — 10 мг, взрослые женщины — 18 мг, беременные женщины во второй половине беременности — 33 мг. У женщин потребность несколько выше, чем у мужчин. Как правило, железа, поступающего с пищей, вполне достаточно, но в некоторых специальных случаях (анемия, а также при донорстве крови) необходимо применять железосодержащие препараты и пищевые добавки (гематоген,ферроплекс). Суточная потребность в железе мала и её легко удовлетворить. В то время, как некоторые исследователи считают, что кормление грудью приводит кдефициту железа, есть множество исследований, показывающих, что это не так и дети, которых кормят грудью, усваивают железо намного лучше. В организме легко восстанавливается равновесие между поступлением и выведением железа, и временный дефицит его легко восполняется за счет имеющихся запасов. Потребность в железе значительно возрастает при анемии, вызванной, например, такими паразитарными инвазиями, как малярия и анкилостомоз, которые очень широко распространены в тропических странах.
В организме легко восстанавливается равновесие между поступлением и выведением железа, и временный дефицит его легко восполняется за счет имеющихся запасов. Потребность в железе значительно возрастает при анемии, вызванной, например, такими паразитарными инвазиями, как малярия и анкилостомоз, которые очень широко распространены в тропических странах.
Содержание железа в воде больше 1—2 мг/л значительно ухудшает её органолептические свойства, придавая ей неприятный вяжущий вкус, и делает воду малопригодной для использования, вызывает у человека аллергические реакции, может стать причиной болезни крови и печени (гемохроматоз). ПДК железа в воде 0,3 мг/л.
Избыточная доза железа (200 мг и выше) может оказывать токсическое действие. Передозировка железа угнетает антиоксидантную систему организма, поэтому употреблять препараты железа здоровым людям не рекомендуется.
Таблица суточной нормы потребления железа
| Пол | Возраст | Суточная норма железа, мг/сутки |
|---|---|---|
| Младенцы | до 6 месяцев | 0,27 |
| Младенцы | 7 — 12 месяцев | 11 |
| Дети | 1 — 3 года | 7 |
| Дети | 4 — 8 лет | 10 |
| Юноши | 9 — 13 лет | 8 |
| Юноши | 14 — 18 лет | 11 |
| Мужчины | 19 лет и старше | 8 |
| Девушки | 9 — 13 лет | 8 |
| Девушки | 14 — 18 лет | 15 |
| Женщины | 19 — 50 лет | 18 |
| Женщины | 50 лет и старше | 8 |
Железо в живых организмах — презентация онлайн
Учитель химии и биологииКаширина Любовь Ивановна
2.
 Человек не может обойтись без железа! Гипотеза:
Человек не может обойтись без железа! Гипотеза:Если в организме человека избыток
или недостаток железа, то у него
развивается болезнь.
3. Цель: установить взаимосвязь между содержанием железа и здоровьем человека.
4. Задачи исследования
Выяснить, какую роль играет железо вживых организмах;
Уметь находить в различных источниках, и
анализировать информацию, необходимую
для изучения данной темы;
Научиться
проводить самостоятельное
исследование
и
обрабатывать
его
результаты.
5. Ход исследования
1.2.
3.
4.
5.
6.
7.
Проанализировали необходимую литературу; сайты
Интернет; CD – диски.
Совершили экскурсию в лабораторию ЦРБ и аптеку.
Получили информацию, побеседовав с медицинскими
работниками.
Провели эксперимент по обнаружению железа в продуктах
питания.
Детально изучили инструкции по применению препаратов
железа.

Проанализировали полученные результаты.
Сделали выводы по гипотезе, оформили результаты.
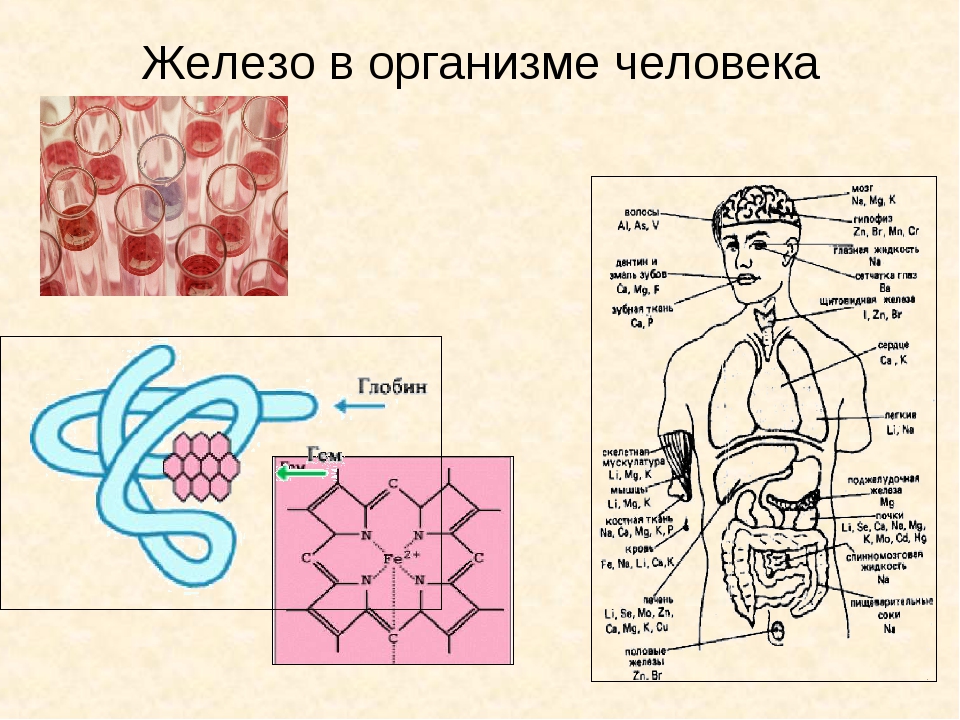
6. Историческая справка
Масса железа у взрослого мужчины составляет около 4,5г, уженщины 3-4г. Основная масса (около75%) сосредоточена в
гемоглобине. Наиболее богаты железом печень (500-600мг.),
костный мозг (до 300мг), селезенка (60-100). Вся масса крови
содержит около 3г. железа, мышечный гемоглобин (миоглобин) 300-600мг.,железо дыхательных ферментов — 1г.
Гемоглобин — красный пигмент крови человека, его функция–
перенос кислорода от органов дыхания к тканям и углекислый
газ от тканей к дыхательным органам. При нормальном
содержании гемоглобина в 100г.крови содержится 53,4 мг. железа.
Гемоглобин до 6 лет>110 г/л,
старше 6 лет >120 г/л.
7. Результаты исследования Ученые выяснили, что значение железа для организма трудно переоценить.
Биологическая роль железа определяется:Многогранностью его функций;
Незаменимостью его в сложных биохимических
процессах;
Активным участием в клеточном дыхании.

8. Экскурсия в лабораторию ЦРБ
Здесь детально изучили информацию о составекрови больного и здорового человека .
Узнали от медицинских работников основные
причины дефицита железа
в организме
человека.
Познакомились с тем, к чему приведет
понижение гемоглобина в эритроцитах, как
бороться с болезнью.
9. Результаты исследования
Основные причины дефицита железа :Разнообразные кровопотери.
Недостаточное поступление и усвоение железа из
пищи.
Повышенные затраты железа при интенсивном
росте, беременности и занятиями физической
культурой.
Инфекционно-воспалительные заболевания.
10. Результаты исследования
Недостаток железа в организме приводит кразвитию анемии (малокровии), при которой
снижается уровень эритроцитов в единице объема
крови , падает и содержание гемоглобина в них.
Кроме
того,
нарушается
и
функция
пищеварительных
нервной
системы,
мышечного аппарата.
 При анемии наблюдается
При анемии наблюдаетсяголовная боль, быстрая утомляемость, вялость,
апатия ко всему.
11. Результаты исследования
В организм железо поступает с пищей.Суточная потребность в железе
различная разными возрастными
категориями :
— дети от 1 до 3 лет-15 мг.,
— мужчины от 19 до 22 лет-10мг.,
— женщины от 19 до 22- 18мг.
Железодефицитное состояние может
развиваться при длительном
употреблении пищи с недостаточным
содержанием железа.
12. Эксперимент (сравнение)
Наличие железа в продуктахпитания
Мы не можем в школьных условиях
провести эксперимент по определению
количества железа в продуктах питания,
поэтому мы провели качественные
реакции на обнаружение ионов железа.
Эксперимент (сравнение)
1.Для
этого
возьмем
такие
продукты
как:
хлеб,
крупа
гречневая,
горох,
яблоко,
картофель, морковь и другие.
Протерли их и залили водой на 4
часа, сделали вытяжки.

2.В пробирки с вытяжкой добавили
по каплям раствор гидроксида
натрия и роданида калия — KSCN до
появления
явных
признаков
химической реакции.
3.Записали наблюдения и сделали
вывод.
14. Содержание железа в продуктах питания
ПродуктыСодержание железа
Хлеб ржаной
+
Крупа гречневая
+
Рис
+
Горох
+
Мясо (говядина)
+
Печень (говяжья)
+
Молоко коровье
+
Картофель
+
Шоколад
+
Яблоки
+
Халва
+
15. Результаты исследования
Лучше всего железо усваивается из мяса,значительно хуже из зерновых злаков. Организм
усваивает 10-20 % железа от суточной потребности.
Железо не выводится с мочой, оно выделяется с
желчью и калом, а также при кровотечениях.
превышает 10 лет.
16. Экскурсия в аптеку
Здесь детально изучили информацию наэтикетках лекарственных веществ,
содержащих железо, и познакомились с
инструкциями их применения .

Сделали вывод, что препараты необходимо
применять строго по рекомендации врача.
Передозировка лекарств может привести к
необратимым последствиям.
Необходимо соблюдать условия хранения
лекарств.
17. Аптека (изучение инструкций)
НазваниеСостав
Показание
Способ
применения
Актиферрин
1капсула содержит
сульфат железа 113мг.
Железодефици
тная анемия
По 1-2 капсуле
после еды
Венофер
Железо(III) гидроксид
сахарозный комплекс
Железодефици
т
Для инъекций
внутривенно
Мальтофер
1 жевательная
таблетка содержит
100мг.железа
Железодефици
т
2-3 таблетки после
еды
Фенюльс
1капсула содержит
сульфат железа150мг
Профилактика
и лечение
железодефици
тной анемии
1 -2 капсулы
Витрум
ВитаминА,С,Д, железо
фумарат
Профилактика,
для будущих
матерей
По 1 таблетке в день
после завтрака
18.
 Результаты исследования В тоже время железо является токсичным
Результаты исследования В тоже время железо является токсичнымвеществом. Избыток железа может привести к
отравлению. При приеме внутрь дозы железа 200-250
мг/кг у человека появляется рвота, боли в животе,
ощущение жара , снижение артериального давления,
резкое снижение свертываемости крови, поражение
печени.
Вдыхание пыли, содержащей соединения железа,
приведет к заболеванию легких, сердечно-сосудистой
дистании, изменению состава крови, возникновению
стоматита, гастрита.
19. Рекомендации
При назначении препаратов железа внутрь следуетучитывать атомно-функциональное состояние желудочнокишечного тракта, особенно его верхних отделов: желудка,
кишки,
являющихся
наиболее
активными участками всасывания железа.
Сульфат железа (II) используется при лечении малокровия.
Он входит в состав лекарства «Ферроплекс», «Ферродок»,
«Витрум» и др. Хлорид железа (III) применяют как
дезинфицирующее и кровоостанавливающее средство.

20. Критерии эффективности лечения препаратами железа
12
3
4
5
6
• Повышение цветного показателя крови
• Повышение числа эритроцитов показателя гематокрита
• Нормализация величины концентрации сывороточного
железа
• Снижение общей и латентной железо-связывающей
способности сыворотки крови
• Повышение насыщенности трансферрина железа
• Пополнение тканевых резервов железа, определяемых
при помощи десфераловой пробы
21. Сравнение с гипотезой
В ходе исследования данная гипотезаполностью подтвердилась. При недостатке или
избытке железа в организме могут наступить
необратимые реакции.
Вывод:
Для нормального роста и выполнения
биологических функций человеку необходим
целый ряд неорганических элементов, одним
из которых является железо.
22. Информационные ресурсы
1. Большая Медицинская Энциклопедия,под редакцией Б.В. Петровского, М., 1998.
2.
 Верблюдович П.А., Утешев А.Б. «Железо в животном организме»,
Верблюдович П.А., Утешев А.Б. «Железо в животном организме»,А-Ата, 2007.
3. Кассирский И.А. «Клиническая гематология», М., 1970.
4. Ленинджер А. «Основы биохимии», М., 1985
5. Петров В.Н. «Физиология и патология обмена железа», Л., 2002.
6.WWW. school-cillection.ru
7.WWW. elementu. ru
8.WWW. wikipedia. ru
A Colorimetric Method for Measuring Iron Content in Plants
Железо (Fe) является важным микроэлементов во всех живых организмах. В растениях это важнейших микроэлементов1 из-за его участия в основных процессов, таких как биосинтеза хлорофилла, дыхание и фотосинтез. Высокое накопление ионов свободного железа вредно для растительных клеток за счет реакции, ведущие к освобождению свободных радикалов, вызывая оксидативного стресса. Для поддержания гомеостаза железа в растительной клетке, ионы хранятся в вакуоли и поглощенных внутри ferritins, белок клеток, непосредственно участвующих в Железный гомеостаза В то же время железо дефицитной анемии затрагивает значительную долю населения, привело растущую потребность растений рекомендовавшая Fe. Благодаря уникальным свойствам растений ферритина обогащение пищи с ферритина железом предлагает перспективные стратегии для борьбы с этой проблемой недоедания3.
В то же время железо дефицитной анемии затрагивает значительную долю населения, привело растущую потребность растений рекомендовавшая Fe. Благодаря уникальным свойствам растений ферритина обогащение пищи с ферритина железом предлагает перспективные стратегии для борьбы с этой проблемой недоедания3.
Ионы железа, главным образом в двух окисления, а именно черных (двухвалентной Fe2 + или железа (II)) и железа (Fe трехвалентного3 + или железа (III)) формы. Несколько других форм железа, например кластеров железа 4, также находятся в клетках. FE хранится в виде оксида железа в клетки и естественно форм hematites (Fe2O3) и ferryhidrites ((Fe)3 +2O3•0.5 H2O) при физиологических условиях5. Гидроксиды, сформированные в этих реакциях, особенно железа форме, имеют очень низкую растворимость. Удержание железа поэтому зависит от рН раствора и в значительной степени в твердом состоянии выше рН 5-6.
Учитывая плохая растворимость и высокая реакционная способность Fe ее передачи среди растительных тканей и органов должен быть связан с подходящим хелатирующий молекул. Кроме того необходимо контролировать его редокс государств между черной и железа формы1 . В листьях около 80% железа находится в фотосинтезирующих клеток, из-за ее существенную роль в транспортная система электронов, в биосинтезе цитохромов, хлорофилл и других молекул гема и в формировании Fe-S
Железо может измеряться в тканях растений на несколько методов, включая пламени атомной абсорбционной спектроскопии9 (ФААС) или колориметрический анализов10, бывший, будучи гораздо более точным, чем последний. ФААС это очень точная техника, которая позволяет одному определить химический состав выборки на основе электромагнитного излучения отдельных элементов. ФААС преобразует ионов металлов в атомной государствам, пламя Отопление образца, привело к Ион возбуждения и выбросов определенной длины волны, когда данный Ион возвращается в состояние земли. Выбросы из различных ионов разделенных монохроматора и обнаружен датчик поглощения11. ФААС таким образом служит для непосредственно количественного определения концентрации железа. Другие методы для визуализации железа в биологических тканях доступны, однако. Индуктивно связанная плазма масс-спектрометрия (ИСП-МС)12 является очень точный метод измерения железа и других микроэлементов, но отсутствие оборудования, как для ФААС и ИСП-МС, является общей проблемой. С другой стороны измерения железа тиоцианат колориметрии13 недостает точности и не удается обнаружить небольшие вариации между выборками. Прусский синий окрашивание,14,,151617 это косвенный метод, основанный на реакции железа Ферроцианид калия (K4Fe(CN)6) с катионов Fe, производство сильный синий цвет и используется для обнаружения качественной железа в гистологических срезах тканей животных и растений.
ФААС преобразует ионов металлов в атомной государствам, пламя Отопление образца, привело к Ион возбуждения и выбросов определенной длины волны, когда данный Ион возвращается в состояние земли. Выбросы из различных ионов разделенных монохроматора и обнаружен датчик поглощения11. ФААС таким образом служит для непосредственно количественного определения концентрации железа. Другие методы для визуализации железа в биологических тканях доступны, однако. Индуктивно связанная плазма масс-спектрометрия (ИСП-МС)12 является очень точный метод измерения железа и других микроэлементов, но отсутствие оборудования, как для ФААС и ИСП-МС, является общей проблемой. С другой стороны измерения железа тиоцианат колориметрии13 недостает точности и не удается обнаружить небольшие вариации между выборками. Прусский синий окрашивание,14,,151617 это косвенный метод, основанный на реакции железа Ферроцианид калия (K4Fe(CN)6) с катионов Fe, производство сильный синий цвет и используется для обнаружения качественной железа в гистологических срезах тканей животных и растений.
Металлические (нулевой Валент) железо является редким в литосфере. Доминирующей не complexed ионной форме железа в окружающей среде основном диктуется количество кислорода в окрестностях, с будучи относительно более обильные в анаэробной среде черных и железа чугуна, преобладающая в аэробных сайтов. Эта последняя форма также является доминирующей в крайне-кислых средах, хотя возбудители черных железа окисления часто отличаются в анаэробных и кислой окрестности18. Когда железа солюбилизирован в 4% HCl (рН 0) в аэробных условиях, большая часть разреженных железа существует как железа (Fe)3 +19,20.
Реакции между ионами Fe и K4Fe(CN)6 являются следующие:
FE3 +: FeCl K4Fe(CN)6 +3 = KFe(III)Fe(II)(CN)6¯ + 3KCl
FE2 +: 4 FeCl2 + 2 K4Fe(CN)6 =4(Fe(CN)6) Fe2 + 8 KCl
В настоящем исследовании мы спросили ли Прусский голубой окраски может быть полезен для измерения уровня железа в растворе.
Первоначально мы проверили корреляции между концентрацией Fe в водном растворе и прусского синего окрашивания. Концентрация в водных растворах Fe (как FeCl2, FeCl3 или 1:1 смесь двух) был измерен атомной спектроскопии и поглощения (OD) после добавления лазурь. Рисунок 1 показывает кривые линейной регрессии для измерений, полученных каждым методом. Мы пришли к выводу, что Прусский синий метод может использоваться для количественного анализа концентрации железа в растворе.
Рисунок 1: линейной регрессии между Fe концентрация измеряется ФААС и поглощения света (OD, 715 Нм) получены методом Прусский синий. Синие квадраты и линии представляют собой Fe2 + решение, красные квадраты и линии представляют собой решение3 + Fe и черные квадраты и линии представляют собой смесь 1:1 между Fe2 + и Fe3 +. Были получены следующие регрессии: [Fe2 +] = 3 + 123 x ОД, r = 0. 996, R2 = 0.989; [Fe3 +] = 1 + 292 x ОД, r = 0,999, R2 = 0,997; и [Fe2 +/ 3 +] = 11 + 146 x ОД, r = 0.983, R2 = 0.956. Fe2 + доноров был FeCl2 и Fe3 + доноров был FeCl3. Пожалуйста, нажмите здесь, чтобы посмотреть большую версию этой фигуры.
996, R2 = 0.989; [Fe3 +] = 1 + 292 x ОД, r = 0,999, R2 = 0,997; и [Fe2 +/ 3 +] = 11 + 146 x ОД, r = 0.983, R2 = 0.956. Fe2 + доноров был FeCl2 и Fe3 + доноров был FeCl3. Пожалуйста, нажмите здесь, чтобы посмотреть большую версию этой фигуры.
Адаптировать колориметрические Прусский синий метод для анализа количественных железа растительных тканей, содержание железа табачных листьев пепел был измерен пламени атомной абсорбционной спектроскопии и Прусский синий окрашивания. Там была хорошая корреляция между результаты из двух методов.
Subscription Required. Please recommend JoVE to your librarian.
Макроэлементы | справочник Пестициды.ru
Макроэлементы принимают непосредственное участие в построении органических и неорганических соединений растения, составляя основную массу его сухого вещества. Большей частью они представлены в клетках ионами.
Макроэлементы и их соединения являются действующими веществами различных минеральных удобрений.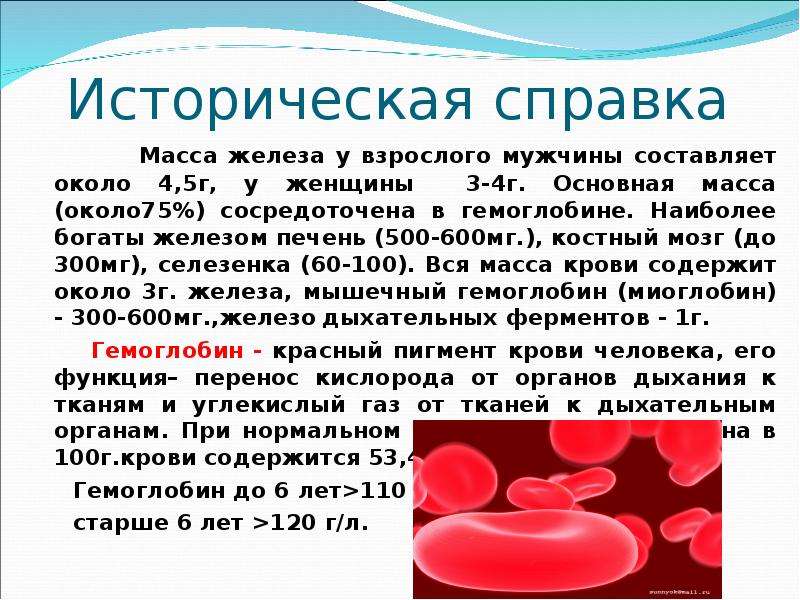 В зависимости от вида и формы, они применяются в качестве основного, припосевного удобрения и подкормки. К макроэлементам относятся: углерод, водород, кислород, азот, фосфор, калий, кальций, магний, сера и некоторые другие, однако основными элементами питания растений являются азот, фосфор и калий.
В зависимости от вида и формы, они применяются в качестве основного, припосевного удобрения и подкормки. К макроэлементам относятся: углерод, водород, кислород, азот, фосфор, калий, кальций, магний, сера и некоторые другие, однако основными элементами питания растений являются азот, фосфор и калий.
В теле взрослого человека содержится порядка 4 граммов железа, 100 г натрия, 140 г калия, 700 г фосфора и 1 кг кальция. Несмотря на такие разные цифры, вывод очевиден: вещества, объединенные под названием «макроэлементы», жизненно необходимы нам для существования.[8] Большую потребность в них испытывают и другие организмы: прокариоты, растения, животные.
Сторонники эволюционного учения утверждают, что необходимость в макроэлементах определяется условиями, в которых зародилась жизнь на Земле. Когда суша состояла из твердых пород, атмосфера была насыщенна углекислотой, азотом, метаном и водяными парами, а вместо дождя на землю выпадали растворы кислот, именно макроэлементы были единственной матрицей, на основе которых могли появиться первые органические вещества и примитивные формы жизни. Поэтому даже сейчас, миллиарды лет спустя, все живое на нашей планете продолжает испытывать необходимость в обновлении внутренних ресурсов магния, серы, азота и других важных элементов, образующих физическую структуру биологических объектов.
Поэтому даже сейчас, миллиарды лет спустя, все живое на нашей планете продолжает испытывать необходимость в обновлении внутренних ресурсов магния, серы, азота и других важных элементов, образующих физическую структуру биологических объектов.
Физические и химические свойства
Макроэлементы различны как по химическим, так и по физическим свойствам. Среди них выделяются металлы (калий, кальций, магний и прочие) и неметаллы (фосфор, сера, азот и прочие).
Некоторые физические и химические свойства макроэлементов, согласно данным:[2] | |||||||
Макроэлемент | Атомный номер | Атомная масса | Группа | Cвойства | Т. кип, °C | Т. плавл, °C | Физическое состояние при нормальны условиях |
Азот (N) | 7 | 14,0 | V | неметалл | 195,8 | 210,00 | бесцветный газ |
Фосфор (P) (белый фосфор) | 15 | 30,97 | V | неметалл | 44,1 | 257 | твердое вещество |
Калий (K) | 19 | 39,1 | I | металл | 771 | 63,5 | металл серебристо-белого цвета |
Кальций (Ca) | 20 | 40,8 | II | металл | 1495 | 842 | твердый белый металл |
Магний (Mg) | 12 | 24,31 | II | металл | 1095 | 650 | металл серебристо-белого цвета |
Сера (S) | 16 | 3,07 | VI | неметалл | 444, 6 | 112,8 | хрупкие кристаллы желтого цвета |
Железо (Fe) | 26 | 55,85 | VIII | металл | 1539 | 2870 | металл серебристого цвета |
Содержание макроэлементов в природе
Макроэлементы содержатся в природе повсеместно: в почве, горных породах, растениях, живых организмах. Некоторые из них, такие, как азот, кислород и углерод, являются составными элементами земной атмосферы.
Некоторые из них, такие, как азот, кислород и углерод, являются составными элементами земной атмосферы.
Симптомы недостатка некоторых элементов питания у сельскохозяйственных культур, согласно данным:[6] | ||
Элемент | Общие симптомы | Чувствительные культуры |
Азот | Изменение зеленой окраски листьев на бледно-зеленую, желтоватую и бурую, Уменьшается размер листьев, Листья узкие и расположены под острым углом к стеблю, Число плодов (семян, зерен) резко уменьшается | Картофель, Капуста белокочанная и цветная, Томаты, Репчатый лук, Огурцы, Свекла, Земляника, Черная смородина, Яблоня |
Фосфор | Скручивание краев листовой пластинки, Образование фиолетовой окраски | Картофель, Капуста, Томаты, Свекла, Лук, Земляника, Малина, Красная смородина, Яблоня |
Калий | Краевой ожог листьев, Вялость листьев, Свисание листьев, Полегание растений, Нарушение цветения, Нарушение плодоношения | Картофель, Томаты, Свекла, Морковь, Лук, Огурцы, Земляника, Малина, Черная смородина, Яблоня |
Кальций | Побеление верхушечной почки, Побеление молодых листьев, Кончики листьев загнуты вниз, Края листьев закручиваются вверх | Картофель, Томаты, Капуста белокочанная и цветная, Яблоня |
Магний | Хлороз листьев | Картофель, Капуста белокочанная и цветная, Томаты, Огурцы, Лук, Свекла, Малина, Черная смородина, Вишня, Яблоня |
Сера | Изменение интенсивности зеленой окраски листьев, Стебли – деревянистые, Замедление роста, Низкое содержание белков | Томаты, Огурцы, Подсолнечник, Бобовые, Горчица, Капуста |
Железо | Окраска листьев меняется до белой, Хлороз листьев
| Плодовые, Люпин, Картофель, Кукуруза, Капуста, Томаты |
- Азот в связанном состоянии присутствует в водах рек, океанов, литосфере, атмосфере. Большая часть азота в атмосфере содержится в свободном состоянии. Без азота невозможно формирование белковых молекул.[2]
- Фосфор легко окисляется и в этой связи в чистом виде в природе не обнаруживается. Однако в соединениях встречается практически повсеместно. Является важной составляющей белков растительного и животного происхождения.[2]
- Калий присутствует в почве в виде солей. В растениях откладывается в основном в стеблях.[2]
- Магний распространен повсеместно. В массивных горных породах содержится в виде алюминатов. В почве есть сульфаты, карбонаты и хлориды, но преобладают силикаты. В виде иона содержится в морской воде.[1]
- Кальций – один из самых распространенных в природе элементов. Его отложения можно встретить в виде мела, известняка, мрамора. В растительных организмах обнаруживается в виде фосфатов, сульфатов, карбонатов.[4]
- Сера в природе очень широко распространена: как в свободном состоянии, так и в виде различных соединений. Обнаруживается и в горных породах, и в живых организмах.[1]
- Железо – один из самых распространенных металлов на Земле, однако в свободном состоянии встречается только в метеоритах. В минералах земного происхождения железо присутствует в сульфидах, оксидах, силикатах и многих других соединениях.[2]
Роль в растении
Биохимические функции
Высокий урожай любой сельскохозяйственной культуры возможен только при условии полноценного и достаточного питания. Кроме света, тепла и воды, растениям необходимы питательные вещества. В состав растительных организмов входит более 70 химических элементов, из них 16 абсолютно необходимых – это органогены (углерод, водород, азот, кислород), зольные микроэлементы (фосфор, калий, кальций, магний, сера), а также железо и марганец.
Каждый элемент выполняет в растениях свои функции, и заменить один элемент другим совершенно невозможно.
в растения в основном поступают кислород, углерод и водород. На их долю приходится 93,5 % сухой массы, в том числе, на углерод – 45 %, на кислород – 42 %, на водород – 6,5 %.[7]- Углерод поглощается из воздуха листьями растений и немного корнями из почвы в виде двуокиси углерода (CO2). Является основой состава всех органических соединений: жиров, белков, углеводов и прочих.
- Водород потребляется в составе воды, крайне необходим для синтеза органических веществ.
- Кислород поглощается листьями из воздуха, корнями из почвы, а также выделяется из состава других соединений. Необходим как для дыхания, так и для синтеза органических соединений.[7]
- Азот – важнейший элемент для развития растений, а именно, для образования белковых веществ. Его содержание в белках варьирует от 15 до 19 %. Он входит в состав хлорофилла, а значит, участвует в фотосинтезе. Азот обнаруживается в ферментах – катализаторах различных процессов в организмах.[7]
- Фосфор присутствует в составе ядер клеток, ферментов, фитина, витаминов и прочих не менее важных соединений. Участвует в процессах преобразования углеводов и азотосодержащих веществ. В растениях он содержится как в органической, так и в минеральной форме. Минеральные соединения – соли ортофосфорной кислоты – применяются при синтезе углеводов. Растения используют и органические фосфорные соединения (гексофосфаты, фосфатиды, нуклеопротеиды, сахарофосфаты, фитин).[7]
- Калий играет важную роль в белковом и углеводном обмене, усиливает эффект от использования азота из аммиачных форм. Питание калием – мощный фактор развития отдельных органов растений. Этот элемент благоприятствует накоплению сахара в клеточном соке, что повышает устойчивость растений к неблагоприятным природным факторам в зимний период, способствует развитию сосудистых пучков и утолщает клетки.[7]
- Сера входит в состав аминокислот – цистеина и метионина, играет важную роль как в белковом обмене, так и в окислительно-восстановительных процессах. Положительно влияет на образование хлорофилла, способствует образованию клубеньков на корневой части бобовых растений, а также клубеньковых бактерий, усваивающих азот из атмосферы.[7]
- Кальций – участник углеводного и белкового обмена, оказывает положительное влияние на рост корней. Остро необходим для нормального питания растений. Известкование кислых почв кальцием обеспечивает повышение плодородия почвы.[7]
- Магний участвует в фотосинтезе, его содержание в хлорофилле достигает 10 % от его общего содержания в зеленых частях растений. Потребность в магнии у растений неодинакова.[7]
- Железо в состав хлорофилла не входит, однако участвует в окислительно-восстановительных процессах, крайне важных для образования хлорофилла. Играет большую роль в дыхании, поскольку является составной частью дыхательных ферментов. Оно необходимо как зеленым растениям, так и бесхлорофильным организмам.[7]
Недостаток (дефицит) макроэлементов в растениях
О дефиците того или иного макроэлемента в почве, а следовательно, и в растении отчетливо свидетельствуют внешние признаки. Чувствительность каждого вида растений к недостатку макроэлементов строго индивидуальна, однако имеются и некоторые схожие признаки. Например, при недостатке азота, фосфора, калия и магния страдают старые листья нижних ярусов, при нехватке кальция, серы и железа – молодые органы, свежие листья и точка роста.
Особенно отчетливо недостаток питания проявляется у высокоурожайных культур.
Избыток макроэлементов в растениях
На состояние растений влияет не только недостаток, но и избыток макроэлементов. Он проявляется, прежде всего, в старых органах, и задерживает рост растений. Часто признаки недостатка и избытка одних и тех же элементов бывают несколько схожи.[6]
Симптомы избытка макроэлементов в растениях, согласно данным:[6] | |
Элемент | Симптомы |
Азот | Подавляется рост растений в молодом возрасте Во взрослом – бурное развитие вегетативной массы Снижается урожайность, вкусовые качества и лежкость плодов и овощей Затягивается рост и созревание Снижается устойчивость к грибным заболеваниям Повышается концентрация нитратов Хлороз развивается на краях листьев и распространяется между жилками Коричневый некроз Концы листьев свертываются Листья опадают |
Фосфор | Листья желтеют На концах и краях более старые листья становятся желтоватыми или коричневыми Появляются яркие некротические пятна Раннее опадение листьев |
Калий | Неравномерность созревания Полегание Снижение сопротивляемости грибковым заболеваниям Снижение устойчивости к неблагоприятным климатическим условиям Ткань не некротическая Слабый рост Удлинение междоузлий На листьях пятна Листья вянут и опадают |
Кальций | Межжилковый хлороз с беловатыми некротическими пятнами Пятна окрашены либо имеют наполненные водой концентрические кольца Рост листовых розеток Отмирание побегов Опадание листьев |
Магний | Листья темнеют Листья немного уменьшаются Сморщивание молодых листьев Концы листьев втянуты и отмирают |
Сера | Снижается урожай Общее огрубение растений |
Железо | Ткань не некротическая Хлороз развивается между жилками молодых листьев Жилки зеленые, позднее весь лист – желтый и беловатый |
Содержание макроэлементов в различных соединениях
Азотные удобрения
Рекомендуются к применению на достаточно увлажненных дерново-подзолистых, серых лесных почвах, а также на выщелоченных черноземах. Они способны обеспечить до половины от общей прибавки урожая, получаемой от полной минеральной подкормки (NPK).
Однокомпонентные азотные удобрения делят на несколько групп:
- Нитратные удобрения. Это соли азотной кислоты и селитры. Азот содержится в них в нитратной форме.
- Аммонийные и аммиачные удобрения: выпускают твердые и жидкие. Содержат азот в аммонийной и, соответственно, аммиачной форме.
- Аммонийно-нитратные удобрения. Это азот в аммонийной и нитратной форме. Пример – аммиачная селитра.
- Амидные удобрения. Азот в амидной форме. К ним относятся мочевина и карбамид.
- КАС. Это карбамид-амиачная селитра, водный раствор мочевины и аммиачной селитры.
Источник получения промышленных азотных удобрений – синтетический аммиак, образованный из молекулярного азота и воздуха.[5]
Фосфорные удобрения
Рекомендуется к применению на почвах легкого гранулометрического состава, а также на всех прочих почвах с низким содержанием подвижного фосфора.
Фосфорные удобрения делят на несколько групп:
- Содержащие фосфор в водорастворимой форме – суперфосфаты простой и двойной. Фосфор удобрений данной группы легко доступен растениям.
- Содержащие фосфор, не растворимый в воде, но растворимый в слабых кислотах (в 2%-ной лимонной) и щелочном растворе цитрата аммония. К ним относятся томасшлак, преципитат, термофосфаты и другие. Фосфор доступен растениям.
- Содержащие фосфор, не растворимый в воде и плохо растворимый в слабых кислотах. Полностью фосфор данных соединений может растворяться только в сильных кислотах. Это костяная и фосфоритная мука. Считаются наиболее труднодоступными источниками фосфора для растений.
Основные источники получения фосфорных удобрений – природные фосфорсодержащие руды (апатиты и фосфориты). Кроме того, для получения этого вида удобрений используют богатые фосфором отходы металлургической промышленности (мартеновские шлаки, томасшлак).[5]
Калийные удобрения
Применение этого вида удобрений рекомендовано на почвах с легким гранулометрическим составом, а также на торфянистых почвах с низким содержанием калия. На прочих почвах с высоким валовым запасом калия потребность в данных удобрениях возникает только при возделывании калиелюбивых культур. К ним относятся корнеплоды, клубнеплоды, силосные, овощные культуры, подсолнечник и прочие. Характерно, что эффективность калийных удобрений тем сильнее, чем выше обеспеченность растений прочими основными элементами питания.
Калийные удобрения подразделяют на:
- Местные калийсодержащие материалы. Это непромышленные калийсодержащие материалы: сырые калийные соли, кварц-глауконитовые пески, отходы алюминиевой и цементной продукции, растительная зола Однако использование этих источников неудобно. В районах с залежами калийсодержащих материалов их действие ослаблено, а дальняя транспортировка нерентабельна.
- Промышленные калийные удобрения. Получают в результате обработки калийных солей промышленными способами. К ним относятся хлористый калий, хлоркалий-электролит, калимагнезия, калимаг и другие.
Источник производства калийных удобрений – природные месторождения калийных солей.[5]
Магниевые удобрения
По составу подразделяют на:
- Простые – содержат только один питательный элемент. Это магнезит и дунит.
- Сложные – содержат два и более питательных элемента. К ним относятся азотно-магниевые (аммошенит или доломит-аммиачная селитра), фосфорно-магниевые (фосфат магниевый плавленый), калийно-магниевые (калимагнезия, полигалит карналлит), бормагниевые (борат магния), известково-магниевые (доломит), содержащие азот, фосфор и магний (магний-аммонийфосфат).
Источники производства магнийсодержащих удобрений – природные соединения. Некоторые используются непосредственно как источники магния, другие перерабатываются.[4]
Симптомы недостатка и избытка фосфораСимптомы недостатка и избытка фосфора
Симптомы недостатка и избытка фосфора у пшеницы:
1 – избыток; 2 – недостаток
Использованы изображения:[11][12]
Серосодержащие удобрения
Элементарная сера применяется незначительно, поскольку доступной растениям она становится только после перевода в сульфатную форму с помощью микроорганизмов. Процесс это достаточно долговременный. Для обогащения почв серой в основном используют простой суперфосфат, фосфогипс, гипс. Последний обычно применяется для мелиорации солонцов.[4]
Железосодержащие удобрения
Рекомендуются к употреблению на карбонатных почвах и на почвах с высоким содержанием усвояемых фосфатов.
Соединения железа в почву не вносят, поскольку железо способно очень быстро переходить в неусвояемые растениями формы. Исключение составляют хелаты – органические соединения железа. Для обогащения железом растения опрыскивают железным купоросом, слабыми растворами хлорного и лимоннокислого железа.[4]
Известковые удобрения
Известкование почв – это один из методов химической мелиорации. Считается самым выгодным способом повышения урожайности на кислых почвах. Действующее вещество известковых удобрений – это кальций (Ca) в форме карбоната кальция (CaCO3) или оксида кальция СаО.
Известковые удобрения делятся на:
- Твердые известковые породы, которым необходимы размол и обжиг. Это известняки, известняки доломитизированные, доломиты.
- Мягкие известковые породы, не требующие размола, – известковые туфы, озерная известь (гажа).
- Отходы промышленности с высоким содержанием извести – сланцевая зола, дефекационная грязь (дефекат).[4]
органический источник макроэлементов
Навоз на соломенной подстилке –
органический источник макроэлементов
Использовано изображение:[9]
Содержание макроэлементов в органических удобрениях
Органические удобрения содержат значительное количество макроэлементов и являются важным средством для воспроизводства плодородия почв и роста продуктивности земледелия. Содержание макроэлементов в органических удобрениях колеблется от долей процента до нескольких процентов и зависит от многих природных факторов.
включает в состав весь спектр необходимых для жизни растения микроэлементов: азота – 0,45 – 0, 83 %, фосфора – 0,19 – 0,28 %, калия 0,50 – 0,67%, кальция 0,18 – 0,40 %, магния 0,09 – 0,18 %, серы 0,06 – 0,15% от всего объема вещества, включая воду и органику. содержит несколько больше макроэлементов: азота – 0,5 – 0,86%, фосфора – 0,26 – 0,47 %, калия – 0,59 – 0,60%.Торф, в зависимости от вида, содержит от 0,1 до 3,3% различных макроэлементов.
Птичий помет, особенно куриный, является важным источником макроэлементов. Их содержание в нем для различных элементов колеблется от 0,2 до 2,4 %.
, в зависимости от вида подстилки, содержит азота от 1,6 до 2,22%, фосфора от 1,4 – 2,0%, калия от 0,62 – 0,78 %. содержит в процентном соотношении несколько меньше макроэлементов. Однако это наиболее быстродействующее удобрение из числа органических. Содержание макроэлементов и других питательных веществ в ней различно. В среднем количество азота колеблется от 0,26-0,39 %, фосфора – 0,06 – 0, 12%, а калия – 0,36 – 0,58 %.Содержание макроэлементов в органических удобрениях, %, согласно данным:[4] | ||||||
Вид удобрения | Макроэлементы | |||||
Азот (общий) N | Фосфор, по P2O5 | Калий, по K2O | Кальций, по CaO | Магний, по MgO | Сера, по SO3 | |
Свежий навоз на соломенной подстилке | ||||||
Крупного рогатого скота | 0,45 | 0,28 | 0,50 | 0,40 | 0,11 | 0,06 |
Конский | 0,58 | 0,28 | 0,63 | 0,21 | 0,14 | 0,07 |
Овечий | 0,83 | 0,23 | 0,67 | 0,33 | 0,18 | 0,15 |
Свиной | 0,45 | 0,19 | 0,60 | 0,18 | 0,09 | 0,08 |
Торф | ||||||
Верховой | 0,8 – 1,2 | 0,06 – 0,12 | < 0.1 | н.д. | н.д. | н.д. |
Переходный | 1,0 – 2,3 | 0,1 – 0,2 | 0,1 | н.д. | н.д. | н.д. |
Низинный | 2,3 – 3,3 | 0,12 – 0,5 | < 0.15 | н.д. | н.д. | н.д. |
Птичий помет | ||||||
Куриный | 1,6 | 1,5 | 0,8 | 2,4 | 0,7 | 0,4 |
Гусиный | 0,7 | 0,9 | 0,6 | 1,1 | 0,2 | 0,3 |
Утиный | 0,5 | 0,5 | 0,9 | 0,8 | 0,2 | 0,3 |
Навозная жижа | ||||||
При молочно-товарных фермах | 0,26 | 0,38 | 0,12 | н.д. | н.д. | н.д. |
При свиноводческих | 0,31 | 0,36 | 0,06 | н.д. | н.д. | н.д. |
При конюшнях | 0,39 | 0,58 | 0,08 | н.д. | н.д. | н.д. |
Способы и сроки внесения минеральных удобрений
Способы и сроки внесения минеральных удобрений зависят от физико-химических свойств различных видов удобрений, а также от почвенных условий и особенностей биологии выращиваемой культуры. Способы внесения удобрений различны:
Основное внесениеорганических удобрений
Основное внесение
органических удобрений
Использовано изображение:[10]
- Допосевное или основное внесение. Включает в себя внесение наибольшей части (70 – 80 %) общей дозы минеральных удобрений. Удобрения заделывают под вспашку в глубокие увлажненные почвенные слои. Такое внесение призвано обеспечить растения питанием на протяжении практически всего периода вегетации.[7]
- Припосевное или припосадочное внесение. В данном случае удобрения вносят одновременно с посевом или посадкой. Глубина заделки – 2 – 3 см ниже уровня заделки семян или комбинированной сеялкой, в которой семена и удобрения смешаны. Удобрения вносятся рядковым или гнездовым способом. Эти способы рассчитаны на обеспечение растений питанием в самом начале их развития. Припосевное удобрение вносится в малых дозах и призвано обеспечивать растение питанием только первые 2 – 3 недели жизни.[7]
- Послепосевное внесение служит для корневой и внекорневой подкормки возделываемых культур в отдельные периоды их развития.[7]
Аммиачная селитра, карбамид, жидкие азотные удобрения, сульфат аммония, калийные и другие удобрения, содержащие питательные вещества в формах, легко доступных растениям, в районах с достаточным увлажнением вносят под яровые культуры в полной норме. Обычно это мероприятие проводят весной при предпосевной обработке почвы.
под озимые зерновые культуры рекомендуется вносить в полной дозе осенью, под вспашку.Азотные удобрения добавляются под озимые культуры. Первую половину вносят осенью при бороновании почвы, а вторую – ранней весной при подкормке озимых.
, содержащие питательные вещества в малорастворимой форме, рекомендуется вносить под вспашку для озимых культур и под зяблевую вспашку для яровых культур.В лесостепных и степных районах с меньшим количеством осадков все минеральные удобрения, в частности, фосфорные и калийные, рекомендуется вносить осенью и под озимые, и под яровые культуры. В этом случае обеспечивается заделка удобрений в более глубокий почвенный слой, менее подверженный иссушению.
Минеральные удобрения вносят и в подкормку пропашных культур во время вегетации. Этот способ применяется в орошаемом земледелии, в частности, под хлопчатник.[7]
Эффект от применения минеральных удобрений
Минеральные удобрения повышают урожай сельскохозяйственных культур. Установлено, что каждый четвертый житель Земли питается продуктами, полученными при применении удобрений.
За счет применения удобрений урожай на дерново-подзолистых почвах повышается на 55 %, на серых лесных – на 28 %, а на черноземах – на 25 %.
Значение минеральных удобрений состоит также в том, что при их применении не только повышается урожайность, но и улучшается качество возделываемых культур.
ведет к повышению белка в зерне от 1 до 3 %. увеличивают крахмалистость клубней картофеля, сахаристость корней корнеплодов, выход волокна у льна-долгунца.Эффективность применения минеральных удобрений в Центральном районе России на дерново-подзолистых суглиныстых почвах, согласно данным:[7] | ||||
Культура | Средняя норма удобрения кг/га | Средняя прибавка урожая ц/га | ||
N | P2O5 | K2O |
| |
Озимая пшеница | 60 | 60 | 40 | 10,2 |
Озимая рожь | 60 | 60 | 40 | 8,2 |
Яровой ячмень | 60 | 60 | 40 | 11,2 |
Овес | 35 | 40 | 40 | 5,3 |
Картофель | 90 | 60 | 60 | 54 |
Лен-долгунец | 30 | 55 | 75 | 5,7 |
Капуста | 90 | 80 | 150 | 215 |
Многолетние травы | 70 | 55 | 55 | 14 |
Естественные сенокосы и пастбища | 90 | 50 | 50 | 30 |
Огромное влияние оказывают минеральные удобрения и на плодородие почвы. Они улучшают агрохимические, физические и биологические свойства почв.
Известкование кислых почв устраняет вредное влияние кислотности, создает благоприятные условия для растений, повышает урожайность. Кроме того, известкование кислых почв снижает подвижность радиоактивных элементов, тяжелых металлов и пестицидов в почве, чем препятствует их поступлению в конечный растительный продукт.[3]
Статья составлена с использованием следующих материалов:
Литературные источники:
1.Власюк П.А. Биологические элементы в жизнедеятельности растений. Издательство «Наукова Думка», Киев, 1969
2.Глинка Н.Л. Общая химия. Учебник для ВУЗов. Изд: Л: Химия, 1985 г, с 731
3.Калинский А.А., Вильдфлуш И.Р., Ионас В.А. и др. – Агрохимия в вопросах и ответах – Мн.: Урожай,1991. – 240 с.: ил.
4.Минеев В.Г. Агрохимия: Учебник.– 2-е издание, переработанное и дополненное.– М.: Издательство МГУ, Издательство «КолосС», 2004.– 720 с., [16] л. ил.: ил. – (Классический университетский учебник).
5.Муравин Э.А. Агрохимия. – М. КолосС, 2003.– 384 с.: ил. – (Учебники и учебные пособия для студентов средних учебных заведений).
6.Петров Б.А., Селиверстов Н.Ф. Минеральное питание растений. Справочное пособие для студентов и огородников. Екатеринбург, 1998. 79 с.
7.Соколовский А. А.; Унанянц Т.П. Краткий справочник по минеральным удобрениям. М., «Химия», 1977. – 376 с.
8.Энциклопедия для детей. Том 17. Химия. / Глав. ред. В.А. Володин. – М.: Аванта +, 2000. – 640 с., ил.
Изображения (переработаны):
9.10.11.12. Свернуть Список всех источниковЖелезо биологическая роль — Справочник химика 21
Биологическая роль кислорода в значительной мере определяется его способностью прочно связывать электроны. В состав пищи разнообразных организмов входят вещества, в молекулах которых электроны находятся на более высоком энергетическом уровне, чем в кислороде. Поэтому переход электронов от пищевых веществ (углеводы, жиры и иногда у некоторых бактерий различные неорганические вещества — сероводород, метан, даже железо) к кислороду может доставить организму энергию, необходимую [c.187]Железо играет исключительно важную биологическую роль, так как входит в состав гемоглобина и некоторых ферментов. Гемоглобин, связывая кислород, переносит его из легких к мышцам, где они передаются миоглобину, после чего, связывая СО2, переносит его в легкие. Нехватка железа в организме приводит к таким заболеваниям, как анемия и малокровие. [c.262]
Применение и биологическая роль железа и его соединений [c.311]
Биологическая роль андрогенов в мужском организме в основном связана с дифференцировкой и функционированием репродуктивной системы, причем в отличие от эстрогенов андрогенные гормоны уже в эмбриональном периоде оказывают существенное влияние на дифференцировку мужских половых желез, а также других тканей, определяя характер секреции гонадотропных гормонов у взрослых. Во взрослом организме андрогены регулируют развитие мужских вторичных половых признаков, сперматогенез в семенниках и т.д. Следует отметить, что андрогены оказывают значительное анаболическое действие, выражающееся в стимуляции синтеза белка во всех тканях, но в большей степени в мышцах. Для реализации анаболического эффекта андрогенов необходимым условием является присутствие соматотропина. Имеются данные, сввдетельствую-щие об участии андрогенов в регуляции биосинтеза макромолекул в женских репродуктивных органах, в частности синтеза мРИК в матке. [c.283]
В ЖИВЫХ ОРГАНИЗМАХ. Биологическая роль сурьмы до сих пор не выяснена. Известно, что и сама сурьма, и ее соединения токсичны. Отравления возможны при производстве сурьмы и ее сплавов, поэтому технике безопасности, механизации производства, вентиляции уделяют здесь особое внимание. Однако, с другой стороны, сурьма обнаружена в растениях —0,0б мг на килограмм сухого веса, в организмах животных и человека. Этот элемент избира тельно концентрируется в печени, селезенке, щитовидной железе. Интересно, что в плазме крови в основном накапливается сурьма в степени окисления +5, а в эритроцитах — +3. [c.60]
В патогенезе асбестоза определенное место занимает образо-вание так называемых асбестовых телец, представляющих собой частицу А. в капсуле из богатого железом белкового гелеподобного субстрата вероятнее всего, их биологическая роль заключается в изолировании агрессивной поверхности А. [c.383]
Представлялось необходимым дать оценку качества полученной пресной воды в отношении содержания в ней микроэлементов иода и фтора, биологическая роль которых чрезвычайно важна. Биологическое значение иода, постоянной составной части организма, обусловлено в основном органически связанным иодом, входящим в состав гормона щитовидной железы — тироксина. [c.399]
Аналог царского вещества, 10-окси-2-транс-деценовая кислота (160), содержится в больших количествах в маточном молочке (так называемом королевском желе ), вырабатываемом мандибулярными железами рабочих пчел. Биологическая роль этого вещества неясна, но оно, несомненно, как-то участвует в развитии личинок, обычной пищей которых наряду с пыльцой является маточное молочко. [c.121]
Биологическая роль нуклеопротеидов тесно связана с процессами роста и морфогенеза. Особенно важной функцией нуклеопротеидов является, повидимому, синтез белка. Быстро растущие органы и ткани (эмбриональные ткани, опухоли), а также органы, в которых интенсивно происходят синтетические процессы (кроветворные органы, поджелудочная железа,. половые и другие железы), содержат особенно много нуклеопротеидов. Очень богаты нуклео-протеидами бактерии и другие микроорганизмы, а вирусы почти полностью построены из этих соединений. [c.42]
Более тщательные исследования позволили, однако, установить весьма важное биологическое значение и этих элементов, по крайней мере многих их них. Хотя суточная потребность человеческого организма в микроэлементах нередко выражается всего лишь в тысячных и миллионных долях миллиграмма, тем не менее при полном исключении их из пищи возникает ряд заболеваний и расстройств обмена веществ. Не говоря уже о железе и йоде, значение которых для нормальной жизнедеятельности организма человека и животных было показано сравнительно давно, несомненно, что важную биологическую роль играют и такие элементы, как, например, Си, 2п и Со. Эти металлы входят, в частности, в состав простетических групп некоторых ферментов (карбоангидраза, например, содержит 2п, тирозиназа — Си), а иногда и витаминов (витамин В12 содержит Со). [c.391]
Биологическая роль порфиринов значительно шире их участия в построении систем гемоглобина и хлорофилла. Установлено, что без них живые организмы не могли бы приспособиться при переходе от ранней восстановительной к современной окислительной атмосфере. Есть основания полагать, что абиогенный синтез порфирина и далее гема и хлорофилла осуществлялся конденсацией янтарной кислоты (возникшей из уксусной кислоты) и глицина в а-амино-Р-кетоадипиновую кислоту, которая после декарбоксилирования превращалась в б-аминолевулиновую кислоту две ее молекулы, взаимно конденсируясь, образовали пиррольное ядро. Серия последующих процессов окисления и конденсации привела к тетра-пиррольной порфириновой системе. Далее синтез гема и хлорофилла осуществлялся почти тождественной, совпадающей последовательностью реакций, разветвившихся на стадии образования комплексов железа и магния [c.546]
Для поддержания жизни, как показано в настоящее время, существенное значение имеют около 20 элементов, хотя живая ткань часто содержит в следовых количествах все элементы, находящиеся в окружающей среде. Основные элементы живых систем — это водород, углерод, азот и кислород (2—60 ат. %). Установлено, что из всех элементов, присутствующих в следовых количествах (0,02—0,1 ат. %), фосфор, сера, хлор, натрий, калий, магний и кальций необходимы для поддержания процессов жизнедеятельности. Некоторые из элементов, присутствующих в сверхмалых количествах (менее 0,001 ат. %), также относятся к числу необходимых. Это марганец, железо и медь. Весьма вероятно, что ванадий, кобальт, молибден, бор и кремний также имеют общее биологическое значение, однако показать, что тот или иной элемент, присутствующий в сверхмалых количествах, биологически необходим, часто весьма трудно. В отдельных случаях биологическая роль элемента для растений и животных может быть установлена по тем последствиям, которые вызывает его отсутствие в почве. Так, отсутствие меди в почве некоторых районов Австралии вызвало нарушения в нервной системе овец и привело к заболеванию их анемией и к выпадению шерсти. Утверждалось также, что недостаток в почве бора приводит к аномалиям в развитии свеклы и сельдерея и к ухудшению качества [c.7]
НО также и потому, что в гемопротеинах имеется необычайно тонкое равновесие между состояниями с максимальной и минимальной спиновой мультиплетностью. Можно предположить, что изменение спинового состояния железа определяется стереохимическими факторами. Изменение спинового состояния при переносе электрона между уровнями eg и t2g сопровождается изменением ионного радиуса катиона железа и изменением длин связей металл — лиганд. Как показано на примере простых неорганических комплексов [58], ионный радиус Fe(II) или Ре(И1) увеличивается примерно на 20% при переходе от низкоспинового состояния к высокоспиновому (табл. 3). Стереохимическое значение данного спинового состояния железопорфиринового комплекса, следовательно, заключается в том, что расположение катиона железа относительно плоскости координируемых атомов азота пиррольных колец порфирина зависит от длин связей железо — порфирин, изменяющихся по мере того, как меняется ионный радиус металла и взаимодействие металл-лиганд. Кроме того, поскольку связывание кислорода сопровождается изменением спинового состояния [105] и положение атома железа относительно плоскости порфирина должно коррелировать во времени и пространстве со связыванием молекулы кислорода, предполагается [103, 104], что изменение стереохимии железо-порфирина вызывает конформационные изменения, ответственные за кооперативное связывание кислорода. В этом и заключается биологическая роль электронной конфигурации атома железа в физиологической функции гемоглобина. [c.40]
БИОЛОГИЧЕСКАЯ РОЛЬ МНОГОЯДЕРНЫХ КОМПЛЕКСОВ ЖЕЛЕЗА(1П) [c.352]
Биологическая роль марганца в жизни растений и животных весьма значительна. Для животных организмов присутствие марганца необходимо. Он усиливает рост молодых организмов, влияет на кроветворение (в сочетании с железом, медью и кобальтом). [c.14]
Основная биологическая роль щитовидной железы заключается в связывании иода в гормон тироксин, регулирующий обмен жиров, углеводов и белков в организме. Поступающий в тело животного неорганический иод аккумулируется преимущественно в щитовидной железе, где его концентрация в тысячи раз больше, чем в других органах. В ряде работ, основные из которых выполнены Майковым, радиоактивный иод был применен для изучения деятельности щитовидной железы, происходящих в ней химических процессов и дальнейшей судьбы иода в организме. Были также изучены патологические нарушения функции щитовидной железы и терапевтическое действие ряда лекарственных веществ. В ранних работах применяли преимущественно более легко получаемый короткоживущий J который позже был заменен изотопом с полупериодом 8,14 дней, получаемым в достаточных количествах при помощи урановых реакторов. Исследования на живых организмах могут вестись без затруднения, так как жесткое 8-излучение обоих изотопов легко проходит сквозь ткани и регистрируется счетчиком, расположенным вблизи соответствующего участка шеи человека или опытного животного. [c.508]
Биологическая роль макроэлементов. Кальций в организме человека составляет около 40 % общего количества всех минеральных веществ. Он входит в состав костей и зубов, придавая им прочность, депонируется в мембранах ретикулума скелетных мышц, участвует в запуске сокращения мышц, передаче нервных импульсов, регуляции проницаемости мембран клеток, в процессах свертывания крови, активирует многие обменные процессы, в том числе распад АТФ, способствует усвоению организмом железа и витамина В,2- Недостаточное поступление кальция в ткани организма приводит к выходу его из костей, что вызывает снижение их прочности (остеопороз), а также нарушение функции нервной системы, кровообращения, в том числе и мышечной деятельности. [c.70]
Биологическая роль микроэлементов. Железо играет очень важную роль в процессах аэробного энергообразования в организме. Оно входит в состав белков гемоглобина, миоглобина, которые осуществляют транспорт Oj и Og в организме, а также в состав цитохромов — компонентов дыхательной цепи, на которой протекают процессы биологического окисления и образования АТФ. Недостаточность железа в организме приводит к нарушению образования гемоглобина и снижению его концентрации в крови. Это может привести к развитию железодефицитной анемии, снижению кислородной емкости крови и резкому снижению физической работоспособности. [c.71]
Какова биологическая роль гормонов щитовидной железы [c.150]
Биологическая роль с -элементов семейства железа. [c.280]
По сравнению с железом и кобальтом никель играет менее важную биологическую роль, что, вероятно, связано с уменьшением химической активности элементов в триаде железа при переходе от Fe к Ni. [c.200]
Биологическая роль крахмала состоит в том, что он является запасным питательным веществом в растениях и когда возникает потребность в энергии и источнике углерода, крахмал высвобождается из запасных гранул и гидролизуется ферментами — амилазами. Они расщепляют связи 1 ->4 в амилозе и амилопектине в различных участках, что приводит к образованию смеси глюкозы и мальтозы. В результате действия амилаз происходит полное расщепление амилозы, но амилопектин расщепляется лишь частично, и для разрыва связей 1—>6 необходимо действие специальных ферментов -мальтаз, которые разрывают связи в крахмале в точках ветвления амилопектина. Благодаря комбинированному действию амилаз и мальтаз крахмал полностью гидролизуется до a-D-глюкoзы, которая затем активно включается в различные метаболические реакции. В противоположность целлюлозе, крахмал хорошо усваивается в организме животных и человека, так как расщепляющие его ферменты содержатся в слюне и поджелудочной железе. [c.69]
Биологическая роль. Рибофлавин входит в состав флавиновых коферментов, в частности ФМН и ФАД , являющихся в свою очередь простетическими группами ферментов ряда других сложных белков —флавопротеинов. Некоторые флавопротеины в дополнение к ФМН или ФАД содержат еще прочно связанные неорганические ионы, в частности железо или молибден, наделенные способностью катализировать транспорт электронов. Различают 2 типа химических реакций, катализируемых этими ферментами. К первому относятся реакции, в которых фермент осуществляет прямое окисление с участием кислорода, т.е. дегидрирование (отщепление электронов и протонов) исходного субстрата или промежуточного метаболита. К ферментам этой группы относятся оксидазы Ь- и О-аминокислот, глициноксидаза, альдегидоксидаза, ксантиноксидаза и др. Вторая группа реакций, катализируемых флавопротеинами, характеризуется переносом электронов и протонов не от исходного субстрата, а от восстановленных пиридиновых коферментов. Ферменты этой группы играют главную роль в биологическом окислении. В каталитическом цикле изоаллоксазиновый остаток ФАД или ФМН подвергается обратимому восстановлению с присоединением электронов и атомов водорода к и ФМН и ФАД прочно связываются с белковым компонентом, иногда даже ковалентно, как, например, в молекуле сукцинатдегидрогеназы. [c.224]
Ведущую роль в регуляции синтеза эстрогенов и прогестерона играют гонадотропные гормоны гипофиза (фоллитропин и лютропин), которые опосредованно, через рецепторы клеток яичника и систему аденилатциклаза—цАМФ и, вероятнее всего, путем синтеза специфического белка, контролируют синтез гормонов. Основная биологическая роль эстрогенов и прогестерона, синтез которых начинается после наступления половой зрелости, заключается в обеспечении репродуктивной функции организма женщины. В этот период они вызывают развитие вторичных половых признаков и создают оптимальные условия, обеспечивающие возможность оплодотворения яйцеклетки после овуляции. Прогестерон выполняет в организме ряд специфических функций подготавливает слизистую оболочку матки к успешной имплантации яйцеклетки в случае ее оплодотворения, а при наступлении беременности основная роль—сохранение беременности оказывает тормозящее влияние на овуляцию и стимулирует развитие ткани молочной железы. Эстрогены оказывают анаболическое действие на организм, стимулируя синтез белка. [c.281]
Еще сравнительно недавно протеиназы традиционно связывали только с процессами переваривания. В настоящее время появляется все больше данных о более широкой биологической роли протеолитических ферментов органов и тканей в регуляции ряда вне- и внутриклеточных процессов. Некоторые протеиназы выполняют защитную функцию (свертывание крови, система комплемента, лизис клеток), другие генерируют гормоны, токсины, вазоактивные агенты (ангиотензин, кинины). Ряд протеиназ регулирует образование пищеварительных ферментов, взаимодействие между клетками и клеточными поверхностями, процессы фертилизации (хитин-синтетаза) и дифференциации. Регуляция в большинстве случаев предусматривает превращение неактивного предшественника в активный белок путем отщепления ограниченного числа пептидов. Этот процесс, впервые описанный К. Линдерстрем-Лангом еще в 50-е годы, в последнее время называют ограниченным протеолизом. Значение его очень важно для понимания сущности биологического синтеза в клетках неактивных пре-и пробелков. Кроме того, этот процесс нашел широкое практическое применение в лабораториях и промышленности. В регуляции действия протеолитических ферментов участвуют также ингибиторы протеиназ белковой природы, открытые не только в поджелудочной железе, но и в плазме крови, курином яйце и т.д. [c.423]
Биологическая роль гемоглобина заключается в осуществлении процесса дыхания — переносе кислорода в животном организме от легких к тканям. Гемоглобин, в котором гем является активным центром, образует с кислородом нестойкое молекулярное соединение— оксигемоглобин, легко диссоциирующий с выделением кислорода. Важно отметить, что железо гема связывает кислород только в присутствии глобина в течение всего процесса железо остается двухвалентным [c.548]
Результаты детальных исследований структуры ряда многоядерных комплексов, которые мы обсуждали в предыдущей главе, можно сопоставить с биологической ролью многоядерных систем, образуемых Fe(III) (гл. 20). Фосвитин является основным пищевым компонентом яичного желтка, причем подавление поглощения железа этим белком связано с его устойчивостью, к действию протеолити-ческих ферментов [106] и с его способностью связывать около 50 молей железа на 1 моль белка с образованием многоядерных структур [97]. Диетологические исследования показали, что входящие в состав пищи инозитгексафосфорная кислота (фитовая кислота) и фосфаты сильно подавляют усвоение железа [1 ], вероятно, путем образования нерастворимого Ре(1П) в виде его фосфатов. Связывание железа фосфитином — прежде всего при участии фосфатных групп серинфосфатных боковых цепей — не приводит к осаждению железа, но все же переводит железо в форму, не доступную для поглощения, вследствие его связывания в макромолекулярный комплекс. Однако данные об относительной роли различных компонентов пищи, являющихся потенциальными хелатирующими агентами в отношении железа, весьма немногочисленны. [c.369]
Простетической группой гемоглобина и других подобных белков является гем, представляющий собой комплекс порфирина с железом. Интенсивное и тщательное изучение гемоглобина было обусловлено, с одной стороны, его биологической ролью в качестве переносчика кислорода, с другой — тем, что он очень легко может быть получен в кристаллическом виде и имеет интенсивную окраску, дающую возможность проводить колориметрические определения. Очень важное значение имеет и то обстоятельство, что изменения в нативном состоянии гемоглобина могут быть легко уловлены по изменению его окраски и спектра поглощения. В нашу задачу не входит рассмотрение структуры гема и различных порфиринов дальнейшее изложение будет посвящено поэтому только тем вопросам, которые касаются структуры и свойств белка, входящего в состав гемоглобина. [c.242]
Биологическая роль прогестерона выяснена достаточно полно. В яичнике женщины после созревания и разрыва фолликула образуется ткань, которая из-за наличия в ней большого количества желтого пигмента каротина получила название желтого тела ( корпус лутеум ). Основные функции желтого тела заключаются в подготовке и сохранении беременности. Как было установлено еще в начале нашего столетия, удаление желтого тела приводит к прерыванию беременности, откуда родилось предположение, что оно является эндокринной железой и вырабатывает гормоны. Действительно, изменения, вызываемые беременностью, можно восстановить введением экстрактов желтого тела. Все это позволило исследователям выделить из желтого тела гормон прогестерон (1934 г.), хотя задача оказалась исключительно сложной в силу лабильности этого вещества. Сейчас прогестерон получают как путем изолирования из яичников животных, так и на основе химических-и микробиологических методов из других стероидных соединений (холестерина, диосгенина и т. п.). [c.85]
Определив функцию сидерохромов как переносчиков железа, целесообразно рассмотреть в свете их признанной биологической роли химическую структуру и свойства наиболее типичных соединений— фенолята железа(П1) [железо(III)энтеробактин (1а)] и гидроксамата железа(III) [феррихром (Va)]. [c.214]
Ципк, введенный в организм, распределяется в нем и накапливается в печени и поджелудочной железе. Выводятся соли цинка главным образом через желудочно-кишечный тракт, в меньшей степени — мочой. Цинк поступает в организм с пищей. Является широко распространенным элементом как в неживой природе, так и в растительных и животных организмах. В жизни растений и животных играет определенную биологическую роль. Содержание цинка в органах человека, по данным А. О. Вой-нара, приведено в табл. 13. [c.348]
Все основные биохимические процессы, связанные с Ж1)зне-де.чтельностью любого организма, происходят в клетке. Ткани, выреза1 кые из организма, продолжают некоторое время дышать поглощать кислород и выделять углекислоту. Отсюда н возникло понятие о клеточном и тканевом дыхании. Биологическая роль дыхания заключается в извлечеыпн энергии за счет окисления и распада органических веществ, которая используется клетками для выполнения тех или иных видов физиологической работы (непрерывное обновление организма, рост и движение клеток и тканей, работа сердца, сокращение мышц, секреция желез и т. д.). Следовательно, химизм аэробного клеточного дыхания обусловлен биологическими окислительно-восстановительными процессами, протекающими в живых клетках организма. [c.354]
В начале XX в. считалось, что для нормального существования живых организмов необходимо регулярное снабжение их так называемыми органогенами, к которым относили атомы углерода, водорода, кислорода, азота и зольные элементы фосфор, калий, кальций, магний, натрий, сера, железо и йод. Остальные химические элементы, в тех случаях когда они обнаруживались в золе, считали случайными, засоряющими организм, бес-1юлезными для него, и попадающими с водою или продуктами питания. Однако с течением времени в связи с разработкой и применением новых методов анализа, позволяющих обнаружить и количественно определить ничтожно малые количества элементов, накоплялось все больше данных о наличии и важной биологической роли в организмах различных минеральных веществ. Оказалось, что круг биогенных элементов не ограничивается теми, которые встречаются в организмах в значительных количествах. Многие элементы, обнаруживаемые в минимальных количествах, как было выяснено, играют существенную роль, входя в состав таких важных для жизнедеятельности организмов веществ, как ферменты, гормоны и др. Вместе с этим было показано, что недостаток тех или иных минеральных веществ в пище вызывает глубокие расстройства в жизнедеятельности животных, в развитии растений. [c.202]
Сидерамины очень прочно связывают трехвалентное железо, которое после восстановления легко реализуется. Их биологическая роль в первую очередь связана с транспортом железа из внешнего раствора в клетку, а также включением его в молекулу тетрапиррола и Ре-белки негеминовой природы. [c.232]
Занятие 6. В. Лечебные свойства минералов: медь, железо, алюминий, натрий, калий, магний, кобальт.
- Опубликовано: 21.02.2020 07:30
Медь любят все – и животные и растения. При недостатке меди в почве растения заболевают, листья быстро увядают, появляются плесневые грибы. Введение медный удобрений (медный купорос) излечивает растения. Много меди в какао, миндале, пшеничных отрубях, горохе. Наиболее богаты медью грибы шампиньоны, чайный куст. Медь содержится в организме животных. Морские животные конденсируют медь из морской воды. У устриц высокое содержание меди, в их крови меди в двести раз больше, чем у человека. У человека «депо» меди – печень. В больших дозах медь является ядом. От паров меди заболевают литейщики, прокатчики, работники сельского хозяйства. Больше всего меди содержится в сердце, печени, мозге и почках, однако в небольших количествах, она есть во всем организме. Организм использует медь в процессе обмена веществ. Медь входит в состав многих ферментов и поэтому необходима для поддержания в здоровом состоянии сердца, костей, нервов, мозга и эритроцитов. Медь помогает извлекать энергию из белков, углеводов и жиров и производить простагландины – вещества, похожие на гормоны. Простагландины же, в свою очередь, регулируют артериальное давление, ритм сердцебиения и способствуют быстрейшему заживлению ран. Медь является частью ферментов, которые охраняют клетки от окисления. Поэтому медь помогает организму бороться с раком, сердечными заболеваниями и старением. Она необходима и для укрепления костей. Нехватка меди в организме может привести к сердечным заболеваниям, повышенному давлению, деформации костей, депрессии, утомлению, слабости, анемии, диарее, сколиозу, затрудненному дыханию, заражению инфекциями и заболеваниям крови и, кроме того, нанести вред кровеносным сосудам и коже. Медь содержать отдельные крупы, зерновой хлеб, орехи, субпродукты, листовые овощи, домашняя птица, горох и бобы. В обычной медицине медь практически не применяется, хотя было отмечено, что рабочие медных производств не заболевали холерой.
Железо. Больше всего железа в болотистых водах. Их даже используют при анемиях. Например, приписывают «Полюстрово». Без окислов железа невозможна жизнь растений, любого живого организма, но в растениях железо не накапливается. Больше других содержит железо мхи, сине-зеленые водоросли. Железо ежедневно выводится из организма, поэтому и должно поступать с пище ежедневно. При анемии, особенно у беременных, — возьмите антоновское яблоко и воткните в него сильно заржавевшие гвозди. Оставьте на сутки, после чего гвозди выньте, а яблоко съешьте. Съедать по 2 яблока в течение 2 недель. Официальная медицина также использует железо в качестве лекарственного средства. Препараты железа назначаются внутрь при снижении гемоглобина в крови – это соли железа (сульфат, лактат, карбонат, хлорид, восстановленное железо) и гематоген. Гематоген эффективно действует на детей со склонностью к кровотечениям, к простудам, а также для профилактики анемии – он подходит и взрослым, и детям.
Алюминий – вовсе не простой элемент. Металл, распространенность в земной коре высокая – 8%. Алюмосиликаты (соединение кремния и алюминия) – полевые шпаты – называют краеугольными камнями земной коры. Особенно богаты алюминием тропические почвы и месторождения глины. Некоторые растения – концентраторы – накапливают более 10 % алюминия. Богаты алюминием плауны, лишайники, чаи, молочай, багульник, рододендрон. В живом организме алюминий содержится во всех клетках, всех тканях и органах, и больше всего в мозге. Квасцы – белый порошок растворяют в воде и используют для примочек, полоскания, глазных капель. Еще одна форма выпуска – кровоостанавливающий карандаш, который применяют при мелких порезах и ссадинах после бритья. Квасцы жженые используют для присыпок при потливости ног.
Натрий – это типичный металл, но в малых количествах он необходим все живым организмам. Натрий – очень активный элемент и в химических реакциях, и живом организме. Он активно вступает в различные соединения, в организме проникает внутрь клетки, обеспечивая водно-солевой обмен. Его нарушения относятся к числу из самых тяжелых. Большинство народов поклонялись соли как символу самой жизни, вечности и постоянства, благополучия и мира. Поваренную соль добывают разными способами: подземным – каменную соль, открытым – озерную соль, выпариванием на солнце из морской воды – бассейновую соль. Во всех случаях соль непременно содержит примеси. Для человека полезна соль, содержащая микроэлементы. Наиболее полезная соль – морская, благодаря тому, что у нее наиболее естественное сочетание химических элементов, близких по составу к биологическим жидкостям человека. В числе прочего, она обладает антитоксическими свойствами. Обычно человек получает достаточное количество соли с пищей, но при больших потерях натрия с потом (у рабочих горячих цехов) наблюдаются колики, судороги, нарушение кровообращения, слабость, снижение давления, может быть обморок. Для питья рабочим дается соленая вода. В медицине применяется хлористый натрий в виде раствора для внутривенного введения и гипертонический раствор для очищения ран.
Калий необходим для питания растений, при его недостатке рост приостанавливается, растения поражаются грибками, не происходит образования семян и рано опадают листья. В молодых листьях накапливается калий, а затем он заменяется на кальций. В большом количестве калий содержится в зеленых листьях салата, шпината, бананах, апельсинах, петрушке, цветной капусте, сливе. В организме человека калий является необходимым элементом, находится во всех клетках и участвует во всех видах обмена. В медицине применяют препараты калия – в виде солей и других соединений. Чаще других используется панангин.
Магний. В земной коре 1,8% магния, он образует 191 минерал. Особенно много магния в морской воде; если его количество в воде увеличивается, вода становится жесткой. В растительном мире магний играет важную роль – входит в состав хлорофилла. Без магния не может быть ни зеленых растений, ни питающихся ими животных. Особенно много магния содержат зеленые водоросли. В организме человека магний входит в состав всех клеток и тканой, поступает в организм с водой, солью, растительной пищей (листья). Магний относится к группе костных элементов. Он контролирует работу митохондрий – главных энергетических станций организма. Он, как невидимый кочегар, пережигает все ненужное и следит за работой электростанции, но стоит ему отлучиться – и работа всего организма сорвана. При стрессе повышается потребность в энергии и магнии. У детей-искусственников возникает дефицит магния в крови, могут быть судороги. Несмотря на то что его в коровьем молоке в 4 раза больше, чем в женском, усвоение идет труднее. Обеднение крови магнием у детей отмечено и при рахите. В медицине применяются сульфаты магния или английская соль в качестве слабительного и в виде инъекций при гипертонической болезни, судорогах. Изучается как средство для лечения предраковых заболеваний кожи и предупреждения развития злокачественных новообразований.
Кобальт не распространен в природе широко, им богаты почвы влажных тропиков. Кобальт обнаружен во всех растениях, особенно его много в красном перце, щавеле, редьке, зеленом луке, свекле. Он найден в организме морских и наземных животных и человека. Обнаружен в печени, крови, поджелудочной железе, почках, мозге и других органов. Кобальт входит в состав витамина В12 и необходим каждому организму, это важный биоэлемент. Кобальт содержится в витамине В12 и используется для лечения тяжелых анемий, невралгий, остеоартрозов и остеопорозов.
ЗУБ МОЛЛЮСКА ПОМОГ УЧЕНЫМ СОЗДАТЬ МАТЕРИАЛ ДЛЯ 3D-ПЕЧАТИ
Немецкие и американские материаловеды выяснили, что делает зубные ткани моллюсков прочными и твердыми. Они обнаружили в ткани стилуса моллюска Cryptochiton stelleri минерал сантабарбарит, который ранее не встречался в живых организмах, и даже сумели частично воспроизвести структуру этой ткани в новом материал для 3D-печати. Результаты исследования опубликованы в журнале Proceedings of the National Academy of Sciences.
Создавая композитные материалы, ученые и инженеры пытаются усидеть на двух стульях — сделать материал одновременно прочным и легким. Такие композиты состоят из мягкой (чаще всего полимерной) матрицы и более твердых включений. Механические свойства зависят от многих параметров: состава матрицы и включений, размера включений и даже их ориентации относительно волокон матрицы. Композитные материалы часто встречаются в живых организмах — в этом случае матрицей служит мягкий биополимер, а включения состоят из более жестких полимерных волокон или частиц минерала. Например, древесина состоит из волокон целлюлозы в матрице лигнина, а благодаря упорядоченному расположению волокон целлюлозы превосходит многие созданные человеком материалы по соотношению прочности и легкости. Работая над новыми композитными материалами, ученые нередко «подсматривают» идеи у природы.
Дерк Джостер (Derk Joester) из Северо-Западного Университета и его коллеги из Германии и США разобрались, как устроены зубные ткани панцирных моллюсков Cryptochiton stelleri. Для добычи и измельчения пищи моллюски используют радулу (или терку), которая им заменяет одновременно и губы и челюсти и язык. Радула состоит из рядов мелких зубчиков на поверхности радулярной мембраны — своеобразного жесткого языка.
Больше всего ученых интересовал стилус (stylus) — небольшое L-образное тело, которое прикрепляет твердую коронку зубчика к более мягкой и гибкой радулярной мембране. Стилус испытывает большие нагрузки и обладает прочностью, в то же время его основание, которое соединяется с радулярной мембраной, должно быть более гибким и пластичным. Поэтому долгое время ученые не могли прийти к единому мнению, как устроена эта ткань и есть ли в ней минеральные включения.
Джостер и его коллеги выяснили, что стилус состоит из хитиновых волокон толщиной около пяти нанометров и включений железосодержащих минералов. Одним из минералов оказался аморфный фосфат железа FePO₄ (АФЖ), уже хорошо знакомый ученым — его довольно много и в зубных коронках у Cryptochiton stelleri. Однако кроме АФЖ, в тканях стилуса нашли другой минерал с более низким содержанием железа. Установить его формулу оказалось непросто — образцы тканей были небольшими и имели сложную форму, а соли железа содержались там не в кристаллическом, а в аморфном состоянии. С помощью метода Мёссбауэровской спектроскопии с синхротронным источником излучения Джостер и его коллеги изучили ближнее окружение ионов железа в второй минеральной фазе и выяснили, что железо связано с гидроксильными группами (ОН).
Полностью охарактеризовать второй минерал помогло исследование ближней тонкой структуры рентгеновского поглощения (XANES). Оказалось, что в стилусе содержится довольно близкий родственник АФЖ— щелочной фосфат железа (Fe3(PO4)2(OH)3 · 5H2O или сантабарбарит. Любопытно, что этот минерал ранее не обнаруживали в живых организмах. Это легкий минерал с низким массовым содержанием железа и высокой удельной прочностью. Научившись строить свои зубные ткани из сантабарбарита, моллюски, вероятно, смогли не только уменьшить вес радулы, но и обходиться меньшим количеством железа.
В ткани стилуса сантабарбарит находятся в виде наночастиц размером от трех до одиннадцати нанометров, а его содержание для разных частей стилуса оказалось разным. Больше всего сантабарбарита (до 50 массовых процентов) в верхней части стилуса, которая граничит с коронкой зуба, а меньше всего (10 массовых процентов) — в нижней части, которая соединяется с радулярной мембраной. Вместе с долей сантабарбарита меняются и механические свойства стилуса — богатый минералами более твердый и прочный (твердость 1,8 гигапаскаля, модуль упругости 30 гигапаскалей), а основание более мягкое (твердость 0,2 гигапаскаля, модуль упругости 7 гигапаскалей).
Механические свойства биологических и рукотворных (отмечены звездочками) композитных материалов
Stegbauer, et al. / Proceedings of the National Academy of Sciences, 2021
Джостер и его коллеги попробовали воссоздать структуру ткани стилуса для 3D-печати, чтобы в дальнейшем использовать такие композитные материалы для зубных имплантов. В качестве матрицы использовали ацетат хитозана, добавив туда растворы ацетата железа и гидрофосфата аммония. Согласно их плану, частицы фосфата железа должны были образоваться из ацетата железа уже в процессе печати. Получился материал с частицами аморфного фосфата железа размером около 40 нанометров (примерно в десять раз больше, чем средний размер частиц в ткани стилуса).
Частиц сантабарбарита авторы в материале не обнаружили. Джостеру и коллегам удалось добиться почти таких же значений модуля упругости, как у ткани стилуса (до 30 гигапаскалей), а вот в твердости их материал пока что уступает. Более того, механическая твердость почти не увеличивалась с ростом содержания фосфата железа — авторы пробовали составы с его количеством от 10 до 75 массовых процентов. Возможная причина — слишком большой размер включений фосфата железа и недостаточно равномерное их распределение в материале.
Впрочем, новые композиты уже оказались прочнее многих современных материалов для зубных имплантов, и авторы предполагают, что в дальнейшем их можно будет сделать еще прочнее. В первую очередь они будут искать способы уменьшить размер частиц фосфата железа.
Два года назад ученые из США сумели воссоздать биополимер, который входит в состав зубной ткани кальмара. У них получился материал, который не только обладает высокой эластичностью прочностью, но и способен самозаживляться.
Наталия Самойлова, источник: https://nplus1.ru/
Обзор железа и его значения для здоровья человека
J Res Med Sci. 2014 фев; 19 (2): 164–174.
Назанин Аббаспур
Департамент наук о системах окружающей среды, Институт наземных экосистем, Швейцарский федеральный технологический институт, Цюрих, Швейцария
Ричард Харрелл
1 Департамент здравоохранения и технологий, Лаборатория питания человека, Институт пищевых продуктов , Питание и здоровье, Швейцарский федеральный технологический институт, Цюрих, Швейцария
Ройя Келишади
2 Исследовательский центр детского роста и развития, Исфаханский университет медицинских наук, Исфахан, Иран
Департамент науки о системах окружающей среды, Институт наземных исследований Экосистема, Швейцарский федеральный технологический институт, Цюрих, Швейцария
1 Департамент медицинских наук и технологий, Лаборатория питания человека, Институт питания, питания и здоровья Швейцарского федерального технологического института, Цюрих, Швейцария
2 Исследования роста и развития детей Ce nter, Исфаханский университет медицинских наук, Исфахан, Иран
Адрес для корреспонденции: Prof.Роя Келишади, Исследовательский центр детского роста и развития Исфаханский университет медицинских наук, Исфахан, Иран. Эл. Почта: ri.ca.ium.dem@idahsilekПоступила в редакцию 8 июня 2013 г .; Пересмотрено 3 ноября 2013 г .; Принято 27 ноября 2013 г.
Авторские права: © Journal of Research in Medical SciencesЭто статья в открытом доступе, распространяемая в соответствии с условиями Creative Commons Attribution-Noncommercial-Share Alike 3.0 Unported, что разрешает неограниченное использование, распространение и воспроизведение в на любом носителе при условии правильного цитирования оригинальной работы.
Эта статья цитируется в других статьях в PMC.Abstract
Хорошо известно, что недостаток или чрезмерное воздействие различных элементов оказывает заметное влияние на здоровье человека. Действие элемента определяется несколькими характеристиками, включая абсорбцию, метаболизм и степень взаимодействия с физиологическими процессами. Железо является важным элементом почти для всех живых организмов, поскольку оно участвует в широком спектре метаболических процессов, включая транспорт кислорода, синтез дезоксирибонуклеиновой кислоты (ДНК) и транспорт электронов.Однако, поскольку железо может образовывать свободные радикалы, его концентрацию в тканях организма необходимо строго регулировать, поскольку в чрезмерных количествах оно может привести к повреждению тканей. Нарушения метаболизма железа являются одними из наиболее распространенных заболеваний человека и охватывают широкий спектр заболеваний с различными клиническими проявлениями, от анемии до перегрузки железом и, возможно, до нейродегенеративных заболеваний. В этом обзоре мы обсуждаем последние достижения в исследованиях метаболизма и биодоступности железа, а также наше текущее понимание потребности человека в железе, а также последствий и причин дефицита железа.Наконец, мы обсуждаем стратегии профилактики дефицита железа.
Ключевые слова: Анемия, потребность человека в железе, биодоступность железа, дефицит железа, метаболизм железа
ВВЕДЕНИЕ
С древних времен человек осознавал особую роль железа в здоровье и болезнях. [1] Железо вначале использовалось в медицине египтянами, индуистами, греками и римлянами. [2, 3] В 17 — веках железо использовалось для лечения хлороза (зеленой болезни), состояния, часто возникающего из-за дефицита железа.[4] Однако только в 1932 году важность железа была окончательно установлена убедительным доказательством того, что неорганическое железо необходимо для синтеза гемоглобина. [5] В течение многих лет пищевой интерес к железу был сосредоточен на его роли в образовании гемоглобина и транспорте кислорода. [6] В настоящее время, хотя низкое потребление железа и / или его биодоступность являются причиной большинства анемий в промышленно развитых странах, они составляют лишь около половины анемии в развивающихся странах [7], где инфекционные и воспалительные заболевания (особенно малярия), кровопотеря от паразитарных инфекций. , и дефицит других питательных веществ (витамина А, рибофлавина, фолиевой кислоты и витамина B12) также являются важными причинами.[8]
Биохимия и физиология
В отличие от цинка, железо является распространенным элементом на Земле [2,9] и является биологически важным компонентом каждого живого организма. [10,11] Однако, несмотря на его геологическое изобилие, железо часто является фактором, ограничивающим рост в окружающей среде. [9] Этот кажущийся парадокс связан с тем фактом, что при контакте с кислородом железо образует оксиды, которые очень нерастворимы и, следовательно, не доступны для усвоения организмами [2]. В ответ на это возникли различные клеточные механизмы захвата железа из окружающей среды в биологически полезных формах.Примерами являются сидерофоры, секретируемые микробами для захвата железа в высокоспецифический комплекс [12], или механизмы восстановления железа из нерастворимого трехвалентного железа (Fe +3 ) до растворимой двухвалентной формы (Fe +2 ), как в дрожжах. [13] Многие механизмы, обнаруженные у низших организмов, имеют аналогичные аналоги у высших организмов, включая человека. В организме человека железо в основном существует в сложных формах, связанных с белком (гемопротеином), в виде гемовых соединений (гемоглобин или миоглобин), гемовых ферментов или негемовых соединений (ферменты флавин-железо, переносчики и ферритин).[3] Организму требуется железо для синтеза белков, переносящих кислород, в частности гемоглобина и миоглобина, а также для образования гемовых ферментов и других железосодержащих ферментов, участвующих в переносе электронов и окислении-восстановлении. [14,3] Почти Две трети железа в организме содержится в гемоглобине, присутствующем в циркулирующих эритроцитах, 25% содержится в легко мобилизуемых запасах железа, а оставшиеся 15% связаны с миоглобином в мышечной ткани и с различными ферментами, участвующими в окислительном процессе. метаболизм и многие другие функции клеток.[15]
Железо перерабатывается и, таким образом, сохраняется в организме. показана схематическая диаграмма цикла железа в организме. Железо доставляется в ткани с помощью циркулирующего трансферрина, переносчика, который захватывает железо, высвобождаемое в плазму, в основном из кишечных энтероцитов или ретикулоэндотелиальных макрофагов. Связывание нагруженного железом трансферрина с рецептором трансферрина на клеточной поверхности (TfR) 1 приводит к эндоцитозу и поглощению металлического груза. Интернализованное железо транспортируется в митохондрии для синтеза гема или кластеров железо-сера, которые являются неотъемлемой частью нескольких металлопротеинов, а избыток железа накапливается и детоксифицируется в цитозольном ферритине.
Железо связывается и транспортируется в организме через трансферрин и сохраняется в молекулах ферритина. После всасывания железа не существует физиологического механизма выведения избыточного железа из организма, кроме кровопотери, то есть беременности, менструации или другого кровотечения обычно низкий, но может колебаться от 5% до 35% в зависимости от обстоятельств и типа железа. [3]
Поглощение железа происходит энтероцитами переносчиком двухвалентного металла 1, членом группы переносчиков растворенных веществ мембранных транспортных белков.Это происходит преимущественно в двенадцатиперстной кишке и верхних отделах тощей кишки [16]. Затем он переносится через слизистую двенадцатиперстной кишки в кровь, где транспортируется трансферрином к клеткам или костному мозгу для эритропоэза [продуцирования красных кровяных телец (эритроцитов)]. [14,17,18] Существует механизм обратной связи, который усиливается. всасывание железа у людей с дефицитом железа. Напротив, люди с перегрузкой железом снижают абсорбцию железа через гепсидин. В настоящее время общепринято, что абсорбция железа контролируется ферропортином, который позволяет или не позволяет железу из клетки слизистой оболочки попадать в плазму.
Физическое состояние железа, поступающего в двенадцатиперстную кишку, сильно влияет на его всасывание. При физиологическом pH двухвалентное железо (Fe +2 ) быстро окисляется до нерастворимой трехвалентной формы (Fe +3 ). Желудочная кислота понижает pH в проксимальном отделе двенадцатиперстной кишки, уменьшая Fe +3 в просвете кишечника за счет редуктазы железа, тем самым обеспечивая последующий транспорт Fe +2 через апикальную мембрану энтероцитов. Это увеличивает растворимость и поглощение трехвалентного железа.Когда продукция желудочного сока нарушена (например, ингибиторами кислотного насоса, такими как лекарство, прилосек), абсорбция железа существенно снижается.
Диетический гем также может транспортироваться через апикальную мембрану по еще неизвестному механизму и впоследствии метаболизироваться в энтероцитах гемоксигеназой 1 (HO-1) с высвобождением (Fe +2 ) [19]. Этот процесс более эффективен, чем абсорбция неорганического железа, и не зависит от рН двенадцатиперстной кишки. Таким образом, на него не влияют такие ингибиторы, как фитат и полифенолы.Следовательно, красное мясо с высоким содержанием гемоглобина является отличным источником железа. Непосредственно интернализованный Fe +2 обрабатывается энтероцитами и в конечном итоге (или нет) экспортируется через базолатеральную мембрану в кровоток через транспортер ферропортин Fe +2 . Ферропортин-опосредованный отток Fe +2 связан с его повторным окислением с Fe +2 , катализируемым мембраносвязанным ферроксидазным гефестином, который физически взаимодействует с ферропортином [20] и, возможно, также его гомологом в плазме церулоплазмином.Экспортируемое железо улавливается трансферрином, который поддерживает Fe +3 в окислительно-восстановительном инертном состоянии и доставляет его в ткани. Общее содержание железа в трансферрине (≈3 мг) соответствует менее 0,1% железа в организме, но оно очень динамично и подвергается более чем 10-кратному ежедневному обороту для поддержания эритропоэза. Пул трансферрина железа пополняется в основном за счет железа, рециркулируемого из неэффективных эритроцитов, и, в меньшей степени, за счет вновь абсорбированного пищевого железа. Стареющие эритроциты очищаются ретикулоэндотелиальными макрофагами, которые метаболизируют гемоглобин и гем и высвобождают железо в кровоток.По аналогии с кишечными энтероцитами, макрофаги экспортируют Fe +2 из своей плазматической мембраны через ферропортин в процессе, сопряженном с повторным окислением Fe +2 до Fe +3 церулоплазмином с последующей загрузкой Fe +3. на трансферрин. [21]
Theil et al ., [21] недавно сообщили, что существует также независимый механизм абсорбции растительных ферритинов, в основном присутствующих в бобовых. Однако актуальность переносчика ферритина неясна, поскольку большая часть ферритина, по-видимому, разлагается во время обработки и переваривания пищи, тем самым высвобождая неорганическое железо из оболочки ферритина для поглощения по нормальному механизму.[22] Поскольку одна молекула ферритина содержит 1000 или более атомов железа и на нее также не должны влиять ингибиторы абсорбции железа, такой механизм может стать важным источником железа в развивающихся странах, где обычно потребляются бобовые.
Регуляция гомеостаза железа
Поскольку железо требуется для ряда разнообразных клеточных функций, для поддержания гомеостаза железа требуется постоянный баланс между поглощением, транспортом, хранением и использованием железа. [11] Поскольку в организме отсутствует определенный механизм активного выведения железа, баланс железа в основном регулируется в точке абсорбции.[23,24]
Гепсидин — это циркулирующий пептидный гормон, секретируемый печенью, который играет центральную роль в регуляции гомеостаза железа. Это главный регулятор системного гомеостаза железа, координирующий использование и хранение железа с приобретением железа. [25] Этот гормон в первую очередь вырабатывается гепатоцитами и является негативным регулятором поступления железа в плазму []. Гепсидин действует путем связывания с ферропортином, переносчиком железа, присутствующим на клетках двенадцатиперстной кишки, макрофагах и клетках плаценты.Связывание гепсидина вызывает интернализацию и деградацию ферропортина. [26] Потеря ферропортина с поверхности клетки предотвращает попадание железа в плазму []. Снижение поступления железа в плазму приводит к низкому насыщению трансферрина и меньшему количеству железа доставляется в развивающийся эритробласт. И наоборот, снижение экспрессии гепсидина приводит к увеличению ферропортина на клеточной поверхности и увеличению абсорбции железа [27] []. У всех видов концентрация железа в биологических жидкостях строго регулируется, чтобы обеспечить необходимое количество железа и избежать токсичности, поскольку избыток железа может привести к образованию активных форм кислорода.[28] Гомеостаз железа у млекопитающих регулируется на уровне кишечной абсорбции, поскольку для железа не существует экскреторного пути.
Гепсидин-опосредованная регуляция гомеостаза железа. (а) Повышенная экспрессия гепсидина печенью является результатом воспалительных стимулов. Высокий уровень гепсидина в кровотоке приводит к интернализации и деградации ферропортина, экспортера железа. Потеря ферропортина на клеточной поверхности приводит к загрузке железа макрофагами, низким уровням железа в плазме и снижению эритропоэза из-за снижения количества железа, связанного с трансферрином.Снижение эритропоэза приводит к анемии хронического заболевания. (b) Нормальные уровни гепсидина в ответ на потребность в железе регулируют уровень импорта железа в плазму, нормальное насыщение трансферрина и нормальные уровни эритропоэза. (c) Гемохроматоз или перегрузка железом возникает из-за недостаточного уровня гепсидина, вызывая повышенный импорт железа в плазму, высокое насыщение трансферрина и избыточное отложение железа в печени. Источник: De Domenico, и др. . [27]
Уровни гепсидина в плазме регулируются различными стимулами, включая цитокины, железо в плазме, анемию и гипоксию.Нарушение регуляции экспрессии гепсидина приводит к нарушениям железа. Избыточная экспрессия гепсидина приводит к анемии хронического заболевания, в то время как низкая продукция гепсидина приводит к наследственному гемохроматозу (HFE) с последующим накоплением железа в жизненно важных органах []. Большинство наследственных заболеваний, связанных с железом, возникают в результате недостаточного производства гепсидина по сравнению со степенью накопления железа в тканях. Было показано, что нарушение экспрессии гепсидина является результатом мутаций в любом из 4 различных генов: TfR2, HFE, гемохроматоз типа 2 (HFE2) и антимикробный пептид гепсидина (HAMP).Мутации в HAMP, гене, кодирующем гепсидин, приводят к болезни, связанной с перегрузкой железом, поскольку отсутствие гепсидина обеспечивает постоянное высокое всасывание железа. Роль других генов (TFR2, HFE и HFE2) в регуляции продукции гепсидина не ясна [27].
Хранение
Концентрация ферритина вместе с концентрацией гемосидерина отражает запасы железа в организме. Они хранят железо в нерастворимой форме и присутствуют в основном в печени, селезенке и костном мозге. [2] Большая часть железа связана с широко распространенным и высококонсервативным железосвязывающим белком ферритином.[18] Гемосидерин представляет собой комплекс хранения железа, который с меньшей готовностью выделяет железо для нужд организма. В условиях устойчивого состояния сывороточные концентрации ферритина хорошо коррелируют с общими запасами железа в организме. [29] Таким образом, сывороточный ферритин является наиболее удобным лабораторным тестом для оценки запасов железа.
Экскреция
Помимо потерь железа из-за менструации, другого кровотечения или беременности, железо очень консервативно и нелегко выводится из организма. [30] Существует некоторая обязательная потеря железа из организма в результате физиологического отшелушивания клеток с эпителиальных поверхностей [30], включая кожу, мочеполовые и желудочно-кишечные тракты.[3] Однако, по оценкам, эти потери очень ограничены (≈1 мг / день). [31] Потери железа из-за кровотечения могут быть значительными, а чрезмерная менструальная кровопотеря является наиболее частой причиной дефицита железа у женщин.
БИОЛОГИЧЕСКАЯ ДОСТУПНОСТЬ
Пищевое железо встречается в двух формах: гемовая и негемовая. [23] Основными источниками гемового железа являются гемоглобин и миоглобин из мяса, птицы и рыбы, тогда как негемовое железо получают из злаков, бобовых, бобовых, фруктов и овощей.[32] Гемовое железо обладает высокой биодоступностью (15–35%), и диетические факторы мало влияют на его абсорбцию, тогда как абсорбция негемового железа намного ниже (2–20%) и сильно зависит от присутствия других пищевых компонентов. [23] Напротив, количество негемового железа в рационе во много раз превышает количество гемового железа в большинстве приемов пищи. Таким образом, несмотря на свою более низкую биодоступность, негемовое железо обычно вносит больший вклад в питание железом, чем гемовое железо. [33] Основными ингибиторами абсорбции железа являются фитиновая кислота, полифенолы, кальций и пептиды из частично переваренных белков.[23] Усилители — это аскорбиновая кислота и мышечная ткань, которые могут восстанавливать трехвалентное железо до двухвалентного железа и связывать его в растворимые комплексы, доступные для абсорбции. [23]
Факторы, повышающие абсорбцию железа
На абсорбцию железа влияет ряд диетических факторов. Аскорбат и цитрат частично увеличивают усвоение железа, действуя как слабые хелатирующие агенты, способствующие растворению металла в двенадцатиперстной кишке []. [34] Железо легко переносится из этих соединений в клетки слизистой оболочки. Исследователи продемонстрировали дозозависимый усиливающий эффект нативной или добавленной аскорбиновой кислоты на абсорбцию железа.[34] Усиливающий эффект в значительной степени связан с его способностью восстанавливать трехвалентное железо до двухвалентного железа, но также из-за его способности хелатировать железо. [35] Аскорбиновая кислота преодолеет отрицательное влияние на абсорбцию железа всех ингибиторов, включая фитат, [36] полифенолы, [37], кальций и белки, содержащиеся в молочных продуктах [38], и увеличит абсорбцию как нативного, так и обогащенного железа. Во фруктах и овощах усиливающий эффект аскорбиновой кислоты часто нивелируется ингибирующим действием полифенолов.[39] Аскорбиновая кислота является единственным усилителем всасывания в вегетарианских диетах, а всасывание железа из вегетарианских и веганских блюд можно оптимизировать путем включения овощей, содержащих аскорбиновую кислоту. [40] Варка, промышленная переработка и хранение разлагают аскорбиновую кислоту и устраняют ее усиливающий эффект на усвоение железа. [41]
Таблица 1
Факторы, которые могут влиять на всасывание железа
Было показано усиливающее действие мяса, рыбы или птицы на всасывание железа из вегетарианских блюд [42], и 30 г мышечной ткани считается эквивалентом 25 мг аскорбиновой кислоты. .[33] Бьорн-Расмуссен и Халлберг [43] сообщили, что добавление курицы, говядины или рыбы к кукурузной муке увеличивало всасывание негемового железа в 2-3 раза без влияния того же количества белка, что и яичного альбумина. Как и в случае с аскорбиновой кислотой, было несколько сложнее продемонстрировать усиливающий эффект мяса при многократном приёме пищи и в полных исследованиях диеты. Редди и др. ., [44] сообщили только о незначительном улучшении всасывания железа (35%) в самостоятельно выбранных диетах в течение 5 дней, когда ежедневное потребление мышечной ткани было увеличено до 300 г / день, хотя в аналогичных 5-дневных рационах. В ходе дневного исследования 60 г свинины, добавленные к вегетарианской диете, увеличили всасывание железа на 50%.[45]
Факторы, ингибирующие абсорбцию железа
В растительной диете фитат (мио-инозитол гексакисфосфат) является основным ингибитором абсорбции железа. [23] Было показано, что отрицательное влияние фитата на абсорбцию железа зависит от дозы и начинается с очень низких концентраций 2-10 мг / прием пищи. [37,46] Молярное отношение фитата к железу может быть использовано для оценки влияния на абсорбцию. . Соотношение должно составлять 1: 1 или предпочтительно 0,4: 1 для значительного улучшения всасывания железа в простых злаковых или бобовых блюдах, которые не содержат каких-либо усилителей усвоения железа, или 6: 1 в комбинированных блюдах с некоторыми овощами, содержащими аскорбин. кислота и мясо как усилители.[47]
Полифенолы содержатся в различных количествах в растительной пище и напитках, таких как овощи, фрукты, некоторые злаки и бобовые, чай, кофе и вино. Ингибирующее действие полифенолов на абсорбцию железа было показано с черным чаем и, в меньшей степени, с травяными чаями. [48,49] В зерновых и бобовых культурах полифенолы усиливают ингибирующий эффект фитата, как было показано в исследовании, сравнивающем сорго с высоким и низким содержанием полифенолов. [23]
Было показано, что кальций отрицательно влияет на абсорбцию негемового и гемового железа, что отличает его от других ингибиторов, влияющих только на абсорбцию негемового железа.[50] Дозозависимые ингибирующие эффекты были показаны при дозах 75-300 мг, когда кальций добавлялся в булочки, и при дозах 165 мг кальция из молочных продуктов. [51] Предполагается, что исследования однократного приема пищи показывают отрицательное влияние кальция на абсорбцию железа, тогда как исследования многократного приема пищи с большим разнообразием продуктов и различными концентрациями других ингибиторов и усилителей показывают, что кальций лишь ограниченно влияет на абсорбцию железа. [52]
Было показано, что животные белки, такие как молочные белки, яичные белки и альбумин, ингибируют абсорбцию железа.[53] Было показано, что две основные белковые фракции коровьего молока, казеин и сыворотка, а также яичный белок ингибируют абсорбцию железа у человека. [54] Белки сои также снижают всасывание железа. [55]
Конкуренция с железом
Исследования конкуренции показывают, что несколько других тяжелых металлов могут участвовать в пути всасывания железа в кишечнике. К ним относятся свинец, марганец, кобальт и цинк. Поскольку дефицит железа часто сочетается с интоксикацией свинцом, это взаимодействие может вызвать особенно серьезные медицинские осложнения у детей.[56]
Свинец является особенно опасным элементом для метаболизма железа. [57] Свинец поглощается механизмом поглощения железа (DTM1) и вторично блокирует железо за счет конкурентного торможения. Кроме того, свинец препятствует ряду важных железозависимых метаболических этапов, таких как биосинтез гема. Это многогранное влияние имеет особенно тяжелые последствия для детей, поскольку свинец не только вызывает анемию, но и может ухудшить когнитивное развитие. Свинец в естественных условиях присутствует в больших количествах в грунтовых водах и почве в некоторых регионах и может тайно нанести вред здоровью детей.По этой причине большинство педиатров в США обычно проверяют содержание свинца в раннем возрасте с помощью простого анализа крови.
ТРЕБОВАНИЯ К ЧЕЛОВЕКУ
В раннем детстве потребности в железе удовлетворяются за счет небольшого количества железа, содержащегося в грудном молоке. [58] Потребность в железе заметно возрастает через 4-6 месяцев после рождения и составляет около 0,7-0,9 мг / день в течение оставшейся части первого года [58]. В возрасте от 1 до 6 лет содержание железа в организме снова увеличивается вдвое. [58] Потребность в железе также очень высока у подростков, особенно в период скачка роста.У девочек обычно происходит скачок роста до менархе, но к этому времени рост не заканчивается. У мальчиков наблюдается заметное увеличение массы и концентрации гемоглобина в период полового созревания. На этой стадии потребности в железе повышаются до уровня, превышающего средние потребности в железе у менструирующих женщин [58] [см.].
Таблица 2
Потребность в железе 97,5% людей с точки зрения абсорбированного железа a , по возрастным группам и полу (Всемирная организация здравоохранения, 1989 г.) ее тело.Точный баланс между потреблением и потерей пищи поддерживает этот баланс. Около 1 мг железа теряется каждый день из-за отшелушивания клеток кожи и слизистых оболочек, включая слизистую оболочку желудочно-кишечного тракта. [59] Менструация увеличивает среднесуточную потерю железа примерно до 2 мг в день у взрослых женщин в пременопаузе. [60] Увеличение массы тела во время скачков роста в неонатальном и детском возрасте временно увеличивает потребность в железе. [61]
Потребление железа с пищей необходимо для восполнения потери железа с калом и мочой, а также через кожу.Эти базальные потери составляют примерно 0,9 мг железа для взрослого мужчины и 0,8 мг для взрослой женщины. [62] У женщин репродуктивного возраста необходимо учитывать потерю железа с менструальной кровью [].
ГРУППЫ ПОВЫШЕННОГО РИСКА
Наибольшая вероятность дефицита железа обнаруживается в тех частях населения, которые не имеют надлежащего доступа к пище, богатой усвояемым железом, во время стадий высокой потребности в железе. Эти группы соответствуют детям, подросткам и женщинам репродуктивного возраста, особенно во время беременности.[63,58]
У младенцев и подростков повышенная потребность в железе является результатом быстрого роста. Для женщин репродуктивного возраста основная причина — чрезмерная кровопотеря во время менструации. Во время беременности потребность в железе значительно возрастает из-за быстрого роста плаценты и плода, а также увеличения глобулярной массы. [63] Напротив, взрослые мужчины и женщины в постменопаузе имеют низкий риск дефицита железа, и количество железа в нормальном рационе обычно достаточно для удовлетворения их физиологических потребностей.[63]
ПОСЛЕДСТВИЯ И ПРИЧИНЫ ДЕФИЦИТА ЖЕЛЕЗА
Последствия дефицита железа
Дефицит железа определяется как состояние, при котором отсутствуют мобилизуемые запасы железа и при котором появляются признаки нарушения поступления железа в ткани, включая эритрон. , отмечены. [64] Дефицит железа может сопровождаться анемией или без нее. Некоторые функциональные изменения могут произойти в отсутствие анемии, но наиболее функциональные нарушения, по-видимому, возникают при развитии анемии. [2] Даже легкие и средние формы железодефицитной анемии могут быть связаны с функциональными нарушениями, влияющими на когнитивное развитие [65], механизмы иммунитета [66] и работоспособность.[67] Дефицит железа во время беременности связан с множеством неблагоприятных исходов как для матери, так и для ребенка, включая повышенный риск сепсиса, материнской смертности, перинатальной смертности и низкой массы тела при рождении. [68] Дефицит железа и анемия также снижают способность к обучению и связаны с повышенным уровнем заболеваемости. [68]
Причины дефицита железа
Дефицит железа возникает в результате истощения запасов железа и возникает, когда абсорбция железа не может идти в ногу с метаболическими потребностями в железе для поддержания роста и восполнения потери железа, что в первую очередь связано с кровопотерей .[2] Основные причины дефицита железа включают низкое потребление биодоступного железа, повышенную потребность в железе в результате быстрого роста, беременности, менструации и избыточную кровопотерю, вызванную патологическими инфекциями, такими как анкилостомы и власоглавы, вызывающие потерю крови из желудочно-кишечного тракта [2] 69,70,71,72] и нарушение всасывания железа. [73] Частота дефицита железа увеличивается у девочек-подростков, потому что менструальные потери железа накладываются на потребность в быстром росте [74]. Другими факторами риска дефицита железа у молодых женщин являются высокий паритет, использование внутриматочной спирали и вегетарианская диета.[75]
Дефицит железа в питании возникает, когда физиологические потребности не могут быть удовлетворены за счет абсорбции железа из рациона. [72] Биодоступность пищевого железа низка в группах населения, потребляющих однообразные растительные диеты с небольшим количеством мяса. [72] Во многих развивающихся странах растительные продукты для отлучения от груди редко обогащаются железом, а частота анемии превышает 50% у детей младше 4 лет. [64]
Когда запасы железа истощаются и железа недостаточно для эритропоэза, синтез гемоглобина в предшественниках эритроцитов нарушается и появляются гематологические признаки железодефицитной анемии.
ОЦЕНКА СТАТУСА ЖЕЛЕЗА
Дефицит железа и, в конечном итоге, анемия развиваются поэтапно и могут быть оценены путем измерения различных биохимических показателей. Хотя некоторые ферменты железа чувствительны к дефициту железа [63], их активность не использовалась в качестве успешного рутинного измерения статуса железа [2].
Лабораторные измерения необходимы для правильной диагностики дефицита железа. Они наиболее информативны, когда несколько показателей уровня железа исследуются и оцениваются в контексте питания и истории болезни.
Пул железа в плазме или сыворотке — это фракция всего железа в организме, которая циркулирует в основном связанном с трансферрином. Три способа оценки уровня железа в плазме или сыворотке включают: 1) измерение общего содержания железа в единице объема в мкг / дл; 2) измерение общего количества сайтов связывания для атомов железа на трансферрине, известного как общая железосвязывающая способность в мкг / дл 2 ; и 3) оценка процента двух сайтов связывания на всех занятых молекулах трансферрина, называемого процентным насыщением трансферрина.[76] Однако заметные биологические вариации этих значений могут возникать в результате суточных колебаний, наличия инфекции или воспалительных состояний и недавнего потребления железа с пищей. [76]
Протопорфирин цинка отражает нехватку железа на последних стадиях синтеза гемоглобина, так что цинк вставляется в молекулу протопорфирина вместо железа. Протопорфирин цинка может быть обнаружен в эритроцитах с помощью флуориметрии и является мерой тяжести дефицита железа. [76]
Сывороточный ферритин является хорошим индикатором запасов железа в организме в большинстве случаев.Когда концентрация сывороточного ферритина ≥15 мкг / л, присутствуют запасы железа; более высокие концентрации отражают размер склада железа; при низкой концентрации (<12 мкг / л для детей младше 5 лет и <15 мкг / л для детей старше 5 лет) запасы железа истощаются. [76] Однако ферритин является белком-реагентом острой фазы, и его сывороточные концентрации могут быть повышены независимо от изменения запасов железа, инфекции или воспаления. [76,2] Это означает, что может быть трудно интерпретировать концентрацию ферритина там, где инфекция болезни распространены.
Еще одним индикатором статуса железа является концентрация TfR в сыворотке крови. Поскольку TfR в основном происходит из развивающихся эритроцитов, он отражает интенсивность эритропоэза и потребность в железе. Когда запасы железа истощаются, концентрация повышается при железодефицитной анемии, что указывает на серьезную недостаточность железа. Это при условии, что нет других причин аномального эритропоэза. [76] Клинические исследования показывают, что сывороточный TfR менее подвержен воспалению, чем сывороточный ферритин. [77] Основным преимуществом TfR как индикатора является возможность оценки величины функционального дефицита железа после истощения запасов железа.[78]
Отношение TfR к ферритину (TfR / ферритин) было разработано для оценки изменений как в накопленном, так и в функциональном железе и считается более полезным, чем TfR или ферритин отдельно. [79] TfR / ферритин использовался для оценки запасов железа в организме как у детей, так и у взрослых. [80] Однако высокая стоимость и отсутствие стандартизации анализа TfR до сих пор ограничивали применимость метода [81].
Низкая концентрация гемоглобина является показателем анемии, конечной стадии дефицита железа.[76,2]
АНЕМИЯ И ЕЕ ПРИЧИНЫ
Анемия описывает состояние, при котором количество эритроцитов в крови низкое или в клетках крови содержится меньше нормального гемоглобина. Человека, страдающего анемией, называют анемичным. Цель эритроцитов — доставлять кислород из легких в другие части тела. Молекула гемоглобина является функциональной единицей эритроцитов и представляет собой сложную белковую структуру, которая находится внутри эритроцитов. Несмотря на то, что эритроциты производятся в костном мозге, в их производство вовлечены многие другие факторы.Например, железо — очень важный компонент молекулы гемоглобина; эритропоэтин, молекула, секретируемая почками, способствует образованию эритроцитов в костном мозге.
Наличие правильного количества эритроцитов и профилактика анемии требует взаимодействия между почками, костным мозгом и питательными веществами в организме. Если почки или костный мозг не функционируют, или организм плохо питается, то нормальное количество и функции эритроцитов может быть трудно поддерживать.
Анемия на самом деле является признаком болезненного процесса, а не самой болезни.Обычно его классифицируют как хронический или острый. Хроническая анемия возникает в течение длительного периода времени. Острая анемия возникает быстро. Определение того, присутствует ли анемия в течение длительного времени или это что-то новое, помогает врачам найти причину. Это также помогает предсказать, насколько серьезными могут быть симптомы анемии. При хронической анемии симптомы обычно начинаются медленно и постепенно прогрессируют; тогда как при острой анемии симптомы могут быть резкими и более тревожными.
Эритроциты живут около 100 дней, поэтому организм постоянно пытается их заменить.У взрослых производство эритроцитов происходит в костном мозге. Врачи пытаются определить, вызвано ли низкое количество эритроцитов повышенной кровопотерей эритроцитов или их снижением в костном мозге. Знание того, изменилось ли количество лейкоцитов и / или тромбоцитов, также помогает определить причину анемии.
По оценкам Всемирной организации здравоохранения (ВОЗ), два миллиарда человек во всем мире страдают анемией и примерно 50% всех анемий объясняются дефицитом железа. [64] Это происходит на всех этапах жизненного цикла, но чаще встречается у беременных женщин и маленьких детей.[82] Анемия является результатом множества причин, которые можно изолировать, но чаще всего они сосуществуют. Некоторые из этих причин включают следующие:
Железодефицитная анемия
Наиболее важной и частой причиной анемии является дефицит железа. [82] Если потребление железа ограничено или неадекватно из-за плохого питания, в результате может возникнуть анемия. Это называется железодефицитной анемией. Железодефицитная анемия также может возникать при наличии язвы желудка или других источников медленного хронического кровотечения (рак толстой кишки, рак матки, полипы кишечника, геморрой и т. Д.).[83]
Анемия хронического заболевания
Любое длительное заболевание может привести к анемии. Этот тип анемии является вторым по распространенности после анемии, вызванной дефицитом железа, и развивается у пациентов с острым или хроническим системным заболеванием или воспалением. [84] Это состояние было названо «анемией воспаления» из-за повышенного содержания гепсидина, который блокирует как рециркуляцию железа из макрофагов, так и абсорбцию железа. [85]
Анемия из-за активного кровотечения
Потеря крови из-за обильного менструального кровотечения или ран может вызвать анемию.[82] Язвы желудочно-кишечного тракта или раковые заболевания, такие как рак толстой кишки, могут медленно терять кровь и также могут вызывать анемию. [86,87]
Анемия, связанная с заболеванием почек
Почки выделяют гормон эритропоэтин, который помогает костному мозгу сделать эритроциты. У людей с хроническим (длительным) заболеванием почек выработка этого гормона снижена, а это, в свою очередь, снижает выработку эритроцитов, вызывая анемию. [88] Хотя дефицит эритропоэтина является основной причиной анемии при хронической почечной недостаточности, это не единственная причина.Следовательно, необходимо минимальное обследование, чтобы исключить дефицит железа и другие аномалии клеточной линии. [89]
Анемия, связанная с беременностью
Увеличение объема плазмы во время беременности приводит к разбавлению эритроцитов и может проявляться как анемия. [90] Железодефицитная анемия составляет 75% всех анемий во время беременности. [90]
Анемия, связанная с плохим питанием
Витамины и минералы необходимы для образования эритроцитов. Помимо железа, для правильного производства гемоглобина необходимы витамин B12, виамин A, фолиевая кислота, рибофлавин и медь.[82] Дефицит любого из этих питательных микроэлементов может вызвать анемию из-за недостаточного производства эритроцитов. Плохое питание — важная причина низкого уровня витаминов и, как следствие, анемии.
Ожирение и анемия
Ожирение характеризуется хроническим слабым системным воспалением, повышенным уровнем гепсидина, которое, в свою очередь, связано с анемией хронического заболевания. Ausk и Ioannou [91] предположили, что ожирение может быть связано с особенностями анемии хронического заболевания, включая низкую концентрацию гемоглобина, низкое содержание железа и трансферрина в сыворотке, а также повышенный уровень ферритина в сыворотке.Избыточный вес и ожирение были связаны с изменениями сывороточного железа, насыщения трансферрина и ферритина, которые, как ожидается, произойдут в условиях хронического системного воспаления. Воспаление, связанное с ожирением, может повышать концентрацию гепсидина и снижать доступность железа. Aeberli и др. ., [92] сравнили уровень железа, потребление железа с пищей и его биодоступность, а также циркулирующие уровни гепсидина, лептина и интерлейкина-6 (ИЛ-6) у детей с избыточной массой тела и детей с нормальным весом.Они указали, что существует пониженная доступность железа для эритропоэза у детей с избыточным весом и что это, вероятно, связано с опосредованным гепсидином сниженным всасыванием железа и / или повышенным секвестрацией железа, а не с низким содержанием железа с пищей.
Алкоголизм
Алкоголь оказывает многочисленные неблагоприятные эффекты на различные типы клеток крови и их функции. [93] У алкоголиков часто есть дефектные эритроциты, которые преждевременно разрушаются. [93,94] Сам по себе алкоголь также может быть токсичным для костного мозга и может замедлять производство эритроцитов.[93,94] Кроме того, плохое питание и дефицит витаминов и минералов связаны с алкоголизмом. [95] Сочетание этих факторов может привести к анемии у алкоголиков.
Серповидно-клеточная анемия
Серповидно-клеточная анемия — одно из наиболее распространенных наследственных заболеваний. [96] Это заболевание, связанное с кровью, которое влияет на молекулу гемоглобина и приводит к изменению формы всей клетки крови в стрессовых условиях [97]. В таком состоянии проблема с гемоглобином бывает качественной или функциональной.Аномальные молекулы гемоглобина могут вызвать проблемы в целостности структуры эритроцитов, и они могут стать серповидными (серповидные клетки). [97] Существуют разные типы серповидно-клеточной анемии разной степени тяжести. Это особенно распространено у африканцев, ближневосточных и средиземноморских предков. [97]
Талассемия
Это еще одна группа причин анемии, связанных с гемоглобином, которая связана с отсутствием или ошибками в генах, ответственных за выработку гемоглобина. [97] Молекула гемоглобина имеет субъединицы, обычно называемые альфа- и бета-цепями глобина.Отсутствие определенной субъединицы определяет тип альфа- или бета-талассемии. [97,98] Существует много типов талассемии, которые различаются по степени тяжести от легкой (малая талассемия) до тяжелой (большая талассемия). [98] Они также являются наследственными, но вызывают количественные аномалии гемоглобина, то есть вырабатывается недостаточное количество молекул правильного типа. Альфа- и бета-талассемии являются наиболее распространенными наследственными моногенными заболеваниями в мире с наибольшей распространенностью в регионах, где малярия была или все еще является эндемической.[97]
Апластическая анемия
Апластическая анемия — это заболевание, при котором разрушается костный мозг и снижается выработка клеток крови. [99] Это вызывает дефицит всех трех типов клеток крови (панцитопения), включая эритроциты (анемия), лейкоциты (лейкопения) и тромбоциты (тромбоцитопения). [100,101] Многие распространенные лекарства могут иногда вызывать этот тип анемии в качестве побочного эффекта. у некоторых людей. [99]
Гемолитическая анемия
Гемолитическая анемия — это тип анемии, при которой происходит разрыв эритроцитов, известный как гемолиз, который разрушается быстрее, чем костный мозг может их заменить.[102] Гемолитическая анемия может возникнуть по разным причинам и часто классифицируется как приобретенная или наследственная. Распространенными приобретенными причинами гемолитической анемии являются аутоиммунитет, микроангиопатия и инфекции. Нарушения ферментов эритроцитов, мембран и гемоглобина вызывают наследственную гемолитическую анемию. [102]
ПРЕДОТВРАЩЕНИЕ НЕДОСТАТОЧНОСТИ ЖЕЛЕЗА (СТРАТЕГИИ ВМЕШАТЕЛЬСТВА)
Четыре основных стратегии коррекции эффективности микронутриентов в популяциях могут использоваться для коррекции дефицита железа, как по отдельности, так и в комбинации.Это обучение в сочетании с модификацией диеты для улучшения потребления железа и его биодоступности; добавление железа (обеспечение железом, обычно в более высоких дозах, без еды), обогащение пищевых продуктов железом и новый подход к биофортификации. Однако есть некоторые трудности в применении некоторых из этих стратегий при рассмотрении железа.
Диверсификация продуктов питания
Модификации рациона питания для сокращения потребления Индийской стоматологической ассоциации включают увеличение потребления продуктов, богатых железом, особенно мясных продуктов, увеличение потребления фруктов и овощей, богатых аскорбиновой кислотой, для увеличения абсорбции негемового железа и снижение потребления чая и кофе, которые подавляют всасывание негемового железа.[103,58] Другая стратегия — снизить содержание антинутриентов, чтобы сделать железо, поступающее из их пищевых источников, более доступным. Биодоступность железа может быть увеличена такими методами, как проращивание и ферментация, которые способствуют ферментативному гидролизу фитиновой кислоты в цельнозерновых зерновых и бобовых культурах за счет повышения активности эндогенных или экзогенных ферментов фитазы. [104] Даже использование неферментативных методов, таких как термическая обработка, замачивание и измельчение, для снижения содержания фитиновой кислоты в основных продуктах растительного происхождения позволило улучшить биодоступность железа (и цинка).[105,106]
Добавка
Для перорального приема добавок железа предпочтительны соли двухвалентного железа (сульфат двухвалентного железа и глюконат двухвалентного железа) из-за их низкой стоимости и высокой биодоступности. [72] Хотя абсорбция железа выше при приеме добавок железа натощак, тошнота и боль в эпигастрии могут развиться из-за введенных более высоких доз железа (обычно 60 мг Fe / день). Если возникают такие побочные эффекты, следует попытаться снизить дозу между приемами пищи или давать железо во время еды, хотя пища снижает всасывание лекарственного железа примерно на две трети.[107] Добавки железа во время беременности рекомендуется в развивающихся странах, где женщины часто вступают в беременность с низкими запасами железа. [108] Хотя обычно считалось, что польза от приема добавок железа перевешивает предполагаемый риск, есть некоторые свидетельства того, что добавление в дозах, рекомендованных для здоровых детей, несет в себе риск увеличения тяжести инфекционного заболевания на фоне малярии. [109,110]
Обогащение
Обогащение пищевых продуктов железом сложнее, чем обогащение такими питательными веществами, как цинк в муке, йод в соли и витамин А в кулинарном масле.[72] Наиболее биодоступные соединения железа растворимы в воде или разбавленной кислоте, но часто вступают в реакцию с другими пищевыми компонентами, вызывая неприятный запах, изменение цвета или окисление жиров. [103] Таким образом, менее растворимые формы железа, хотя и хуже усваиваются, часто выбираются для обогащения, чтобы избежать нежелательных сенсорных изменений. [72] Обогащение обычно производится с гораздо более низкими дозами железа, чем с добавками. Это ближе к физиологической среде и может быть самым безопасным вмешательством в малярийных областях. [111] Нет никаких опасений по поводу безопасности добавок железа или обогащения железа в немалярийных эндемичных районах.[112]
Соединения железа, рекомендованные [7] для обогащения пищевых продуктов, включают сульфат железа, фумарат железа, пирофосфат железа и порошок электролитического железа. Пшеничная мука является наиболее распространенным пищевым продуктом, обогащенным железом, и обычно она обогащается порошками элементарного железа, которые не рекомендуются ВОЗ. [7,113] Харрелл и Эгли [23] сообщили, что из 78 национальных программ по пшеничной муке только восемь улучшатся. статус железа. В этих программах использовались рекомендуемые соединения железа на рекомендованных уровнях.Другие страны использовали не рекомендуемые соединения или более низкие уровни железа по сравнению с потреблением муки. Коммерческое детское питание, такое как смеси и злаки, также обычно обогащено железом.
Биообогащение
Содержание железа колеблется от 25 до 56 мг / кг в различных сортах пшеницы и 7-23 мг / кг в зернах риса. Однако большая часть этого железа удаляется в процессе измельчения. Поглощение железа зерновыми и бобовыми культурами, многие из которых имеют высокое содержание самородного железа, обычно низкое из-за высокого содержания в них фитата, а иногда и полифенолов.[48] Стратегии биофортификации включают селекцию растений и генную инженерию. Уровни железа в обычных бобах и просе были успешно увеличены путем селекции растений, но использование других основных продуктов питания является более трудным или невозможным (рис) из-за недостаточной естественной генетической изменчивости. Lucca и др. ., [114] увеличили содержание железа в эндосперме риса, чтобы улучшить его всасывание в кишечнике человека с помощью генной инженерии. Они ввели ген ферритина из Phaseolus vulgaris в рисовые зерна, увеличив содержание железа в них вдвое.Для увеличения биодоступности железа они ввели в эндосперм риса термотолерантную фитазу из Aspergillus fumigatus . Они указали, что этот рис с более высоким содержанием железа и богатым фитазой имеет большой потенциал для существенного улучшения питания железом в тех популяциях, где дефицит железа так широко распространен. [114] К сожалению, фитаза не устояла перед приготовлением. Важность различных минералов, таких как цинк [115] и железо, требует большего внимания на индивидуальном уровне и уровне общественного здравоохранения.
Сноски
Источник поддержки: Нет
Конфликт интересов: Не объявлен.
СПИСОК ЛИТЕРАТУРЫ
1. Борода Дж. Л., Доусон HD. Железо. В: О’Делл Б.Л., Сунде Р.А., редакторы. Справочник по незаменимым в питании минеральным элементам. Нью-Йорк: CRC Press; 1997. С. 275–334. [Google Scholar] 2. Вуд Р.Дж., Ронненберг А. Железо. В: Shils ME, Shike M, Ross AC, Caballero B, Cousins RJ, редакторы. Современное питание в здоровье и болезнях. 10-е изд. Балтимор: Липпинкотт Уильямс и Уилкинс; 2005 г.С. 248–70. [Google Scholar] 3. Макдауэлл LR. 2-е изд. Амстердам: Elsevier Science; 2003. Минералы в питании животных и человека; п. 660. [Google Scholar] 4. Гуггенхайм KY. Хлороз: возникновение и исчезновение болезни, связанной с питанием. J Nutr. 1995; 125: 1822–5. [PubMed] [Google Scholar] 5. Ип Р., Даллман PR. Железо. В: Ziegler EE, Filer LJ, редакторы. Присутствуют знания в области питания. 7-е изд. Вашингтон, округ Колумбия: ILSI Press; 1996. С. 278–92. [Google Scholar] 6. Андервуд Э.Дж., Саттл Н.Ф. 3-е изд. Уоллингфорд: международное издательство CABI; 1999 г.Минеральное питание скота; п. 614. [Google Scholar] 7. Аллен Л., де Бенуа Б., Дари О., Харрелл Р., редакторы. Женева: ВОЗ и ФАО; 2006. ВОЗ. Рекомендации по обогащению пищевых продуктов микронутриентами; п. 236. [Google Scholar] 8. Брабин Б.Дж., Премжи З., Верхое ff Ф. Анализ анемии и детской смертности. J Nutr. 2001; 131: 636–45С. [PubMed] [Google Scholar] 9. Quintero-Gutiérrez AG, González-Rosendo G, Sánchez-Muñoz J, Polo-Pozo J, Rodríguez-Jerez JJ. Биодоступность гемового железа в начинке для печенья с использованием поросят в качестве модели животных для человека.Int J Biol Sci. 2008; 4: 58–62. [Бесплатная статья PMC] [PubMed] [Google Scholar] 10. Айзен П., Эннс С., Весслинг-Резник М. Химия и биология метаболизма железа в эукариотах. Int J Biochem Cell Biol. 2001; 33: 940–59. [PubMed] [Google Scholar] 11. Лиу П. Т., Хейскала М., Петерсон П. А., Ян Ю. Роль железа в здоровье и болезнях. Мол Аспекты Мед. 2001; 2: 1–87. [PubMed] [Google Scholar] 12. Guerinot ML. Транспорт микробного железа. Annu Rev Microbiol. 1994; 48: 743–72. [PubMed] [Google Scholar] 13. Асквит К., Каплан Дж.Транспорт железа и меди в дрожжах и его значение для болезней человека. Trends Biochem Sci. 1998. 23: 135–8. [PubMed] [Google Scholar] 15. Вашингтон, округ Колумбия: Национальная академия прессы; 2001. МОМ. Институт медицины. железо. В: Диетические рекомендуемые дозы витамина А, витамина К, мышьяка, бора, хрома, меди, йода, железа, марганца, молибдена, никеля, кремния, ванадия и цинка; С. 290–393. [PubMed] [Google Scholar] 16. Мюир А., Хопфер У. Региональная специфичность поглощения железа щеточно-граничными мембранами тонкого кишечника у нормальных мышей и мышей с дефицитом железа.Am J Physiol. 1985; 248: G376–9. [PubMed] [Google Scholar] 17. Фрейзер Д.М., Андерсон Г.Дж. Импорт железа. I. Абсорбция железа в кишечнике и ее регуляция. Am J Physiol Gastrointest Liver Physiol. 2005; 289: G631–5. [PubMed] [Google Scholar] 18. Наддур С.С., Шрирама К., Мудипалли А. Механизмы транспорта и гомеостаза железа: их роль в здоровье и болезнях. Индийский J Med Res. 2008; 128: 533–44. [PubMed] [Google Scholar] 20. Yeh KY, Yeh M, Mims L, Glass J. Кормление железом индуцирует миграцию и взаимодействие ферропортина 1 и гефестина в двенадцатиперстном эпителии крыс.Am J Physiol Gastrointest Liver Physiol. 2009; 296: 55–65. [Бесплатная статья PMC] [PubMed] [Google Scholar] 21. Тейл Э.С., Чен Х., Миранда С., Янсер Х., Эльзенханс Б., Нуньес М.Т. и др. Абсорбция железа из ферритина не зависит от гемового железа и солей двухвалентного железа у женщин и сегментов кишечника крыс. J Nutr. 2012; 142: 478–83. [Бесплатная статья PMC] [PubMed] [Google Scholar] 22. Hoppler M, Schoenbaechler A, Meile L, Hurrell RF, Walczyk T. Ферритин-железо высвобождается при кипячении и in vitro при пищеварении в желудке .J Nutr. 2008. 138: 878–84. [PubMed] [Google Scholar] 23. Hurrell R, Egli I. Биодоступность железа и диетические контрольные значения. Am J Clin Nutr. 2010; 91: 1461–7S. [PubMed] [Google Scholar] 25. Немет Э., Ганц Т. Регулирование метаболизма железа гепсидином. Annu Rev Nutr. 2006; 26: 323–42. [PubMed] [Google Scholar] 26. Немет Э., Таттл М.С., Пауэлсон Дж., Вон М.Б., Донован А., Уорд Д.М. и др. Гепсидин регулирует отток клеточного железа, связываясь с ферропортином и индуцируя его интернализацию. Наука. 2004; 306: 2090–3.[PubMed] [Google Scholar] 28. Браун В., Киллманн Х. Бактериальные решения проблемы снабжения железом. Trends Biochem Sci. 1999; 24: 104–109. [PubMed] [Google Scholar] 29. Хант-младший. Насколько важна биодоступность железа с пищей? Am J Clin Nutr. 2001; 73: 3–4. [PubMed] [Google Scholar] 30. Хант-младший, Зито, Калифорния, Джонсон, Лос-Анджелес. Выведение железа из организма здоровыми мужчинами и женщинами. Am J Clin Nutr. 2009; 89: 1–7. [PubMed] [Google Scholar] 31. Фэрбенкс В.Ф. Железо в медицине и питании. В: Shils ME, Shike M, Ross AC, Caballero B, Cousins RJ, редакторы.Современное питание в здоровье и болезнях. 10-е изд. Балтимор: Липпинкотт Уильямс и Уилкинс; 1999. С. 193–221. [Google Scholar] 32. потребности человека в витаминах и минералах. Рим: ФАО; 2001. ФАО / ВОЗ. Пищевые подходы к удовлетворению потребностей в витаминах и минералах; С. 7–25. [Google Scholar] 33. Monsen ER, Hallberg L, Layrisse M, Hegsted DM, Cook JD, Mertz W. и др. Оценка доступного пищевого железа. Am J Clin Nutr. 1978; 31: 134–41. [PubMed] [Google Scholar] 34. Конрад ME, Umbreit JN. Краткий обзор: абсорбция железа — путь муцин-мобилферрин-интегрин.Конкурентоспособный путь поглощения металлов. Am J Hematol. 1993; 42: 67–73. [PubMed] [Google Scholar] 35. Конрад М.Э., Шаде С.Г. Хелаты аскорбиновой кислоты в абсорбции железа: роль соляной кислоты и желчи. Гастроэнтерология. 1968; 55: 35–45. [PubMed] [Google Scholar] 36. Холлберг Л., Брюн М., Россандер Л. Поглощение железа у человека: аскорбиновая кислота и дозозависимое ингибирование фитатом. Am J Clin Nutr. 1989; 49: 140–4. [PubMed] [Google Scholar] 37. Зигенберг Д., Бейнс Р.Д., Ботвелл Т.Х., Макфарлейн Б.Дж., Лампарелли Р.Д., Car NG и др.Аскорбиновая кислота предотвращает дозозависимое ингибирующее действие полифенолов и фитатов на абсорбцию негемового железа. Am J Clin Nutr. 1991; 53: 537–41. [PubMed] [Google Scholar] 38. Стекель А., Оливарес М., Писарро Ф., Чадуд П., Лопес И., Амар М. Поглощение обогащающего железа из молочных смесей у младенцев. Am J Clin Nutr. 1986; 43: 917–22. [PubMed] [Google Scholar] 39. Бюллетень D, Бейнс Р.Д., Ботвелл Т.Х., Гиллули М., Макфарлейн Б.Дж., Макфейл А.П. и др. Влияние фруктовых соков и фруктов на усвоение железа из рисовой муки.Br J Nutr. 1987. 57: 331–43. [PubMed] [Google Scholar] 40. Линч SR, Кук JD. Взаимодействие витамина С и железа. Ann N Y Acad Sci. 1980; 355: 32–44. [PubMed] [Google Scholar] 41. Teucher B, Olivares M, Cori H. Усилители поглощения железа: аскорбиновая кислота и другие органические кислоты. Int J Vitam Nutr Res. 2004; 74: 403–19. [PubMed] [Google Scholar] 42. Линч С.Р., Харрелл Р.Ф., Дассенко С.А., Кук Дж.Д. Влияние пищевых белков на биодоступность железа у человека. Adv Exp Med Biol. 1989; 249: 117–32. [PubMed] [Google Scholar] 43.Бьорн-Расмуссен Э., Халльберг Л. Влияние животных белков на усвоение пищевого железа человеком. Нутр Метаб. 1979; 23: 192–202. [PubMed] [Google Scholar] 44. Редди МБ, Харрелл Р.Ф., Кук JD. Разнообразное питание незначительно влияет на всасывание негемового железа у нормальных людей. J Nutr. 2006; 136: 576–81. [PubMed] [Google Scholar] 45. Бах Кристенсен М., Хелс О, Морберг С., Марвинг Дж., Бугель С., Тетенс I. Свинина увеличивает усвоение железа при 5-дневной полностью контролируемой диете по сравнению с вегетарианской диетой с аналогичным содержанием витамина С и фитиновой кислоты.Br J Nutr. 2005. 94: 78–83. [PubMed] [Google Scholar] 46. Харрелл Р.Ф., Джуллерат М.А., Редди М.Б., Линч С.Р., Дассенко С.А., Кук Дж.Д. Соевый белок, фитат и абсорбция железа у человека. Am J Clin Nutr. 1992; 56: 573–8. [PubMed] [Google Scholar] 47. Hurrell RF. Разложение фитиновой кислоты как средство улучшения усвоения железа. Int J Vitam Nutr Res. 2004. 74: 445–52. [PubMed] [Google Scholar] 48. Харрелл Р.Ф., Редди М., Кук Дж. Д.. Подавление абсорбции негемного железа у человека напитками, содержащими полифенолы. Br J Nutr.1999. 81: 289–95. [PubMed] [Google Scholar] 49. Холлберг Л., Россандер Л. Влияние различных напитков на усвоение негемового железа из сложных блюд. Hum Nutr Appl Nutr. 1982; 36: 116–23. [PubMed] [Google Scholar] 50. Hallberg L, Rossander-Hulthen L, Brune M, Gleerup A. Ингибирование усвоения гемового железа у человека кальцием. Br J Nutr. 1993; 69: 533–40. [PubMed] [Google Scholar] 51. Халлберг Л., Россандер-Хюльтен Л. Потребность в железе у менструирующих женщин. Am J Clin Nutr. 1991; 54: 1047–58. [PubMed] [Google Scholar] 52.Линч SR. Влияние кальция на усвоение железа. Nutr Res Rev.2000; 13: 141–58. [PubMed] [Google Scholar] 53. Повар JD, Monsen ER. Поглощение пищевого железа у людей. III. Сравнение влияния животных белков на всасывание негемового железа. Am J Clin Nutr. 1976; 29: 859–67. [PubMed] [Google Scholar] 54. Харрелл РФ, Линч С.Р., Тринидад Т.П., Дассенко С.А., Кук Дж.Д. Абсорбция железа у людей: бычий сывороточный альбумин по сравнению с говяжьими мышцами и яичным белком. Am J Clin Nutr. 1988; 47: 102–7. [PubMed] [Google Scholar] 55.Линч С.Р., Дассенко С.А., Кук Дж.Д., Джульерат М.А., Харрелл РФ. Ингибирующий эффект фрагмента, связанного с соевым белком, на абсорбцию железа у людей. Am J Clin Nutr. 1994; 60: 567–72. [PubMed] [Google Scholar] 56. Piomelli S, Seaman C, Kapoor S. Вызванные свинцом аномалии метаболизма порфирина, связь с дефицитом железа. Ann N Y Acad Sci. 1987; 514: 278–88. [PubMed] [Google Scholar] 58. 2-е изд. Бангкок: 2004 г. ФАО / ВОЗ. Консультации экспертов по потребностям человека в витаминах и минералах, потребностях в витаминах и минералах в питании человека: отчет совместного экспертного заключения ФАО / ВОЗ; п.341. [Google Scholar] 59. Cook JD, Skikne BS, Lynch SR, Reusser ME. Оценки достаточности железа у населения США. Кровь. 1986; 68: 726–31. [PubMed] [Google Scholar] 60. Ботвелл TH, Чарльтон RW. Общий подход к проблемам железодефицита и перегрузки железом у населения в целом. Semin Hematol. 1982; 19: 54–67. [PubMed] [Google Scholar] 61. Гибсон Р.С., Макдональд А.С., Смит-Вандеркой П.Д. Параметры сывороточного ферритина и пищевого железа в выборке канадских детей дошкольного возраста. J Can Dietetic Assoc.1988; 49: 23–8. [Google Scholar] 62. ДеМайер Э.М., Даллман П., Герни Дж. М., Холлберг Л., Суд С. К., Срикантия С. Г., редакторы. Женева: Всемирная организация здравоохранения; 1989. ВОЗ. Профилактика и контроль железодефицитной анемии с помощью первичной медико-санитарной помощи: руководство для администраторов здравоохранения и руководителей программ; п. 58. [Google Scholar] 63. Даллман П. Айрон. В: Браун М.Л., редактор. Настоящие знания в области питания. 6-е изд. Вашингтон, округ Колумбия: Фонд питания; 1990. С. 241–50. [Google Scholar] 64. Женева: Швейцария: Всемирная организация здравоохранения; 2001 г.ВОЗ / ЮНИСЕФ / УООН. Оценка, профилактика и контроль железодефицитной анемии; п. 114. [Google Scholar] 65. Борода Дж. Л., Коннор Дж. Р. Статус железа и нейронное функционирование. Annu Rev Nutr. 2003. 23: 41–58. [PubMed] [Google Scholar] 66. Failla ML. Микроэлементы и защита хозяина: последние достижения и сохраняющиеся проблемы. J Nutr. 2003; 133: S1443–7. [PubMed] [Google Scholar] 67. Витери Ф.Е., Торунь Б. Анемия и физическая работоспособность. В: Гарби Л., редактор. Клиники гематологии. Vol. 3. Лондон: У. Б. Сондерс; 1974. стр.609–26. [Google Scholar] 68. CDC. Табель успеваемости по грудному вскармливанию, США: показатели результатов (публикация из Центров по контролю и профилактике заболеваний, Национальное обследование иммунизации. 2010 г. [последний доступ 11 мая 2010 г.]. Http://www.cdc.gov/breastfeeding/data/index .htm .69. Купер Е.С., Банди Д.А. Трихоцефалопатия. Ballieres Clin Trop Med Commun Dis. 1987; 2: 629–43. [Google Scholar] 70. Всемирная организация здравоохранения, Женева; 1995. ВОЗ. Отчет неофициальной консультации ВОЗ. на анкилостомоз и анемию у девочек и женщин; с.46. [Google Scholar] 71. Crompton DW, Nesheim MC. Влияние кишечных гельминтозов на питание в течение жизненного цикла человека. Annu Rev Nutr. 2002; 22: 35–99. [PubMed] [Google Scholar] 72. Ларок Р., Касапиа М., Готуццо Е., Дьоркос Т.В. Взаимосвязь между интенсивностью заражения гельминтами, передающимися через почву, и анемией во время беременности. Am J Trop Med Hyg. 2005. 73: 783–9. [PubMed] [Google Scholar] 73. Циммерманн МБ, Харрелл РФ. Недостаток пищевого железа. Ланцет. 2007; 370: 115–20. [Google Scholar] 74. Харви LJ, Armah CN, Dainty JR, Foxall RJ, John Lewis D, Langford NJ и др.Влияние менструальной кровопотери и диеты на дефицит железа у женщин в Великобритании. Br J Nutr. 2005. 94: 557–64. [PubMed] [Google Scholar] 75. Борода JL. Потребность в железе у девочек-подростков. Симпозиум: Повышение уровня железа у подростков до деторождения. J Nutr. 2000; 130: S440–2. [PubMed] [Google Scholar] 77. Бегин Ю. Растворимый рецептор трансферрина для оценки эритропоэза и статуса железа. Clinica Chimica Acta. 2003. 329: 9–22. [PubMed] [Google Scholar] 79. Повар JD, Flowers CH, Skikne BS. Количественная оценка bodyiron.Кровь. 2003. 101: 3359–64. [PubMed] [Google Scholar] 80. Кук JD, Boy E, Flowers C, Daroca Mdel C. Влияние высокогорной жизни на железо тела. Кровь. 2005; 106: 1441–6. [PubMed] [Google Scholar] 81. Ян З., Дьюи К.Г., Лоннердал Б., Хернелл О., Чапарро С., Аду-Афарвуа С. и др. Сравнение концентрации ферритина в плазме с соотношением рецептора трансферрина в плазме к ферритину для оценки запасов железа в организме: результаты 4 интервенционных испытаний. Am J Clin Nutr. 2008; 87: 1892–8. [PubMed] [Google Scholar] 82.Де Бенуа Б., Маклин Э., Эгли И., Когсуэлл М. — редакторы. Женева: Пресса ВОЗ, Всемирная организация здравоохранения; 2008. ВОЗ / CDC. Данные библиотечной каталогизации в публикации. Распространенность анемии в мире, 1993–2005 гг .: глобальная база данных ВОЗ по анемии; п. 40. [Google Scholar] 83. Джонсон-Уимбли Т.Д., Грэм Д.Ю. Диагностика и лечение железодефицитной анемии в 21 веке. Ther Adv Гастроэнтерол. 2011; 4: 177–84. [Бесплатная статья PMC] [PubMed] [Google Scholar] 84. Зарычанский Р., Хьюстон Д.С. Анемия хронического заболевания: вредное заболевание или адаптивная, полезная реакция? Can Med Assoc J.2008. 179: 333–7. [Бесплатная статья PMC] [PubMed] [Google Scholar] 85. Weiss G, Goodnough LT. Анемия хронического заболевания. N Engl J Med. 2005; 352: 1011–23. [PubMed] [Google Scholar] 86. 2-е изд. Женева: 2004 г. ВОЗ / CDC. Отчет о совместной технической консультации Всемирной организации здравоохранения / Центров по контролю и профилактике заболеваний по оценке статуса железа на уровне населения; п. 108. [Google Scholar] 87. Knight K, Wade S, Balducci L. Распространенность и исходы анемии при раке: систематический обзор литературы.Am J Med. 2004; 116: 11–26С. [PubMed] [Google Scholar] 88. О’Мара NB. Больные анемией с хроническими заболеваниями почек. Спектр диабета. 2008; 21: 12–9. [Google Scholar] 89. Нурко С. Анемия при хронической болезни почек: причины, диагностика, лечение. Cleve Clin J Med. 2006. 73: 289–97. [PubMed] [Google Scholar] 90. Горовиц К.М., Ингардия С.Дж., Боргида А.Ф. 2013, Анемия при беременности. Clin Lab Med. 2013; 33: 281–91. [PubMed] [Google Scholar] 91. Ауск К.Дж., Иоанну Г.Н. Связано ли ожирение с анемией хронического заболевания? Популяционное исследование.Ожирение. 2008. 16: 2356–61. [PubMed] [Google Scholar] 92. Aeberli I, Hurrell RF, Zimmermann MB. Дети с избыточным весом имеют более высокие концентрации циркулирующего гепсидина и более низкий статус железа, но их потребление железа с пищей и биодоступность сопоставимы с детьми с нормальным весом. Int J Obes. 2009; 33: 1111–7. [PubMed] [Google Scholar] 94. Lewis G, Wise MP, Poynton C, Godkin A. Случай стойкой анемии и злоупотребления алкоголем. Нат Клин Практ Гастроэнтерол Гепатол. 2007; 4: 521–6. [PubMed] [Google Scholar] 95. Lindenbaum J, Роман MJ.Пищевая анемия при алкоголизме. Am J Clin Nutr. 1980; 33: 2727–35. [PubMed] [Google Scholar] 96. Cox SE, L’Esperance V, Makani J, Soka D, Prentice AM, Hill CM и др. Серповидно-клеточная анемия: доступность железа и ночная оксиметрия. J Clin Sleep Med. 2012; 8: 541–5. [Бесплатная статья PMC] [PubMed] [Google Scholar] 98. Манси Х.Л., младший, Кэмпбелл Дж. Альфа- и бета-талассемия. Я семейный врач. 2009; 80: 339–44. [PubMed] [Google Scholar] 99. Сегель ГБ, Лихтман М.А. Апластическая анемия: приобретенная и наследственная. В: Каушанский К., Вильямс В.Дж., редакторы.Гематология Вильямса. 8-е изд. Нью-Йорк: McGraw-Hill Medical; 2010. С. 569–90. [Google Scholar] 100. Янг Н.С., Каладо Р.Т., Шейнберг П. Современные концепции патофизиологии и лечения апластической анемии. Кровь. 2006; 108: 2509–19. [Бесплатная статья PMC] [PubMed] [Google Scholar] 101. Шейнберг П., Чен Дж. Апластическая анемия: что мы узнали на моделях на животных и в клинике. Semin Hematol. 2013; 50: 156–64. [PubMed] [Google Scholar] 102. Dhaliwal G, Cornett PA, Tierney LM., Jr Гемолитическая анемия.Я семейный врач. 2004; 69: 2599–606. [PubMed] [Google Scholar] 103. Hurrell RF. Как обеспечить адекватное усвоение железа из продуктов, обогащенных железом. Nutr Rev. 2002; 60: S7–15. [PubMed] [Google Scholar] 104. Повар JD. Диагностика и лечение железодефицитной анемии. Лучшая практика Res Clin Haematol. 2005; 18: 319–32. [PubMed] [Google Scholar] 105. Schlemmer U, Frølich W, Prieto RM, Grases F. Фитат в пищевых продуктах и значение для человека: источники пищи, потребление, обработка, биодоступность, защитная роль и анализ.Mol Nutr Food Res. 2009; 53: S330–75. [PubMed] [Google Scholar] 106. Лян Дж., Хан Б.З., Ноут М.Дж., Хамер Р.Дж. Влияние замачивания, прорастания и ферментации на общую фитиновую кислоту и растворимый цинк in vitro в коричневом рисе. Food Chem. 2008; 110: 821–8. [PubMed] [Google Scholar] 107. Кавалли-Сфорца Т., Бергер Дж., Смитасири С., Витери Ф. Еженедельное употребление добавок железа и фолиевой кислоты для женщин репродуктивного возраста: обзор воздействия, извлеченные уроки, планы расширения и вклад в достижение целей развития тысячелетия.Nutr Rev.2005; 63: S152–8. [PubMed] [Google Scholar] 109. Oppenheimer SJ. Железо и его отношение к иммунитету и инфекционным заболеваниям. J Nutr. 2001; 131: S616–33. [PubMed] [Google Scholar] 110. Sazawal S, Black RE, Ramsan M, Chwaya HM, Stoltzfus RJ, Dutta A и др. Влияние рутинных профилактических добавок с железом и фолиевой кислотой на госпитализацию и смертность детей дошкольного возраста в условиях высокой передачи малярии: рандомизированное плацебо-контролируемое исследование на уровне общины. Ланцет. 2006; 367: 133–43.[PubMed] [Google Scholar] 112. Hurrell RF. Обогащение железом: его эффективность и безопасность в отношении инфекций. Еда Nutr Bull. 2007. 28: 585–94. [PubMed] [Google Scholar] 114. Лукка П., Харрелл Р., Потрикус И. Борьба с железодефицитной анемией с помощью риса, богатого железом. J Am Coll Nutr. 2002; 21: 184С – 90. [PubMed] [Google Scholar] 115. Рухани Н., Харрелл Р., Келишади Р., Шулин Р. Цинк и его значение для здоровья человека: интегративный обзор. J Res Med Sci. 2013; 18: 144–57. [Бесплатная статья PMC] [PubMed] [Google Scholar]Обзор железа и его значения для здоровья человека
J Res Med Sci.2014 фев; 19 (2): 164–174.
Назанин Аббаспур
Департамент наук о системах окружающей среды, Институт наземных экосистем, Швейцарский федеральный технологический институт, Цюрих, Швейцария
Ричард Харрелл
1 Департамент здравоохранения и технологий, Лаборатория питания человека, Институт пищевых продуктов , Питание и здоровье, Швейцарский федеральный технологический институт, Цюрих, Швейцария
Ройя Келишади
2 Исследовательский центр детского роста и развития, Исфаханский университет медицинских наук, Исфахан, Иран
Департамент науки о системах окружающей среды, Институт наземных исследований Экосистема, Швейцарский федеральный технологический институт, Цюрих, Швейцария
1 Департамент медицинских наук и технологий, Лаборатория питания человека, Институт питания, питания и здоровья Швейцарского федерального технологического института, Цюрих, Швейцария
2 Исследования роста и развития детей Ce nter, Исфаханский университет медицинских наук, Исфахан, Иран
Адрес для корреспонденции: Prof.Роя Келишади, Исследовательский центр детского роста и развития Исфаханский университет медицинских наук, Исфахан, Иран. Эл. Почта: ri.ca.ium.dem@idahsilekПоступила в редакцию 8 июня 2013 г .; Пересмотрено 3 ноября 2013 г .; Принято 27 ноября 2013 г.
Авторские права: © Journal of Research in Medical SciencesЭто статья в открытом доступе, распространяемая в соответствии с условиями Creative Commons Attribution-Noncommercial-Share Alike 3.0 Unported, что разрешает неограниченное использование, распространение и воспроизведение в на любом носителе при условии правильного цитирования оригинальной работы.
Эта статья цитируется в других статьях в PMC.Abstract
Хорошо известно, что недостаток или чрезмерное воздействие различных элементов оказывает заметное влияние на здоровье человека. Действие элемента определяется несколькими характеристиками, включая абсорбцию, метаболизм и степень взаимодействия с физиологическими процессами. Железо является важным элементом почти для всех живых организмов, поскольку оно участвует в широком спектре метаболических процессов, включая транспорт кислорода, синтез дезоксирибонуклеиновой кислоты (ДНК) и транспорт электронов.Однако, поскольку железо может образовывать свободные радикалы, его концентрацию в тканях организма необходимо строго регулировать, поскольку в чрезмерных количествах оно может привести к повреждению тканей. Нарушения метаболизма железа являются одними из наиболее распространенных заболеваний человека и охватывают широкий спектр заболеваний с различными клиническими проявлениями, от анемии до перегрузки железом и, возможно, до нейродегенеративных заболеваний. В этом обзоре мы обсуждаем последние достижения в исследованиях метаболизма и биодоступности железа, а также наше текущее понимание потребности человека в железе, а также последствий и причин дефицита железа.Наконец, мы обсуждаем стратегии профилактики дефицита железа.
Ключевые слова: Анемия, потребность человека в железе, биодоступность железа, дефицит железа, метаболизм железа
ВВЕДЕНИЕ
С древних времен человек осознавал особую роль железа в здоровье и болезнях. [1] Железо вначале использовалось в медицине египтянами, индуистами, греками и римлянами. [2, 3] В 17 — веках железо использовалось для лечения хлороза (зеленой болезни), состояния, часто возникающего из-за дефицита железа.[4] Однако только в 1932 году важность железа была окончательно установлена убедительным доказательством того, что неорганическое железо необходимо для синтеза гемоглобина. [5] В течение многих лет пищевой интерес к железу был сосредоточен на его роли в образовании гемоглобина и транспорте кислорода. [6] В настоящее время, хотя низкое потребление железа и / или его биодоступность являются причиной большинства анемий в промышленно развитых странах, они составляют лишь около половины анемии в развивающихся странах [7], где инфекционные и воспалительные заболевания (особенно малярия), кровопотеря от паразитарных инфекций. , и дефицит других питательных веществ (витамина А, рибофлавина, фолиевой кислоты и витамина B12) также являются важными причинами.[8]
Биохимия и физиология
В отличие от цинка, железо является распространенным элементом на Земле [2,9] и является биологически важным компонентом каждого живого организма. [10,11] Однако, несмотря на его геологическое изобилие, железо часто является фактором, ограничивающим рост в окружающей среде. [9] Этот кажущийся парадокс связан с тем фактом, что при контакте с кислородом железо образует оксиды, которые очень нерастворимы и, следовательно, не доступны для усвоения организмами [2]. В ответ на это возникли различные клеточные механизмы захвата железа из окружающей среды в биологически полезных формах.Примерами являются сидерофоры, секретируемые микробами для захвата железа в высокоспецифический комплекс [12], или механизмы восстановления железа из нерастворимого трехвалентного железа (Fe +3 ) до растворимой двухвалентной формы (Fe +2 ), как в дрожжах. [13] Многие механизмы, обнаруженные у низших организмов, имеют аналогичные аналоги у высших организмов, включая человека. В организме человека железо в основном существует в сложных формах, связанных с белком (гемопротеином), в виде гемовых соединений (гемоглобин или миоглобин), гемовых ферментов или негемовых соединений (ферменты флавин-железо, переносчики и ферритин).[3] Организму требуется железо для синтеза белков, переносящих кислород, в частности гемоглобина и миоглобина, а также для образования гемовых ферментов и других железосодержащих ферментов, участвующих в переносе электронов и окислении-восстановлении. [14,3] Почти Две трети железа в организме содержится в гемоглобине, присутствующем в циркулирующих эритроцитах, 25% содержится в легко мобилизуемых запасах железа, а оставшиеся 15% связаны с миоглобином в мышечной ткани и с различными ферментами, участвующими в окислительном процессе. метаболизм и многие другие функции клеток.[15]
Железо перерабатывается и, таким образом, сохраняется в организме. показана схематическая диаграмма цикла железа в организме. Железо доставляется в ткани с помощью циркулирующего трансферрина, переносчика, который захватывает железо, высвобождаемое в плазму, в основном из кишечных энтероцитов или ретикулоэндотелиальных макрофагов. Связывание нагруженного железом трансферрина с рецептором трансферрина на клеточной поверхности (TfR) 1 приводит к эндоцитозу и поглощению металлического груза. Интернализованное железо транспортируется в митохондрии для синтеза гема или кластеров железо-сера, которые являются неотъемлемой частью нескольких металлопротеинов, а избыток железа накапливается и детоксифицируется в цитозольном ферритине.
Железо связывается и транспортируется в организме через трансферрин и сохраняется в молекулах ферритина. После всасывания железа не существует физиологического механизма выведения избыточного железа из организма, кроме кровопотери, то есть беременности, менструации или другого кровотечения обычно низкий, но может колебаться от 5% до 35% в зависимости от обстоятельств и типа железа. [3]
Поглощение железа происходит энтероцитами переносчиком двухвалентного металла 1, членом группы переносчиков растворенных веществ мембранных транспортных белков.Это происходит преимущественно в двенадцатиперстной кишке и верхних отделах тощей кишки [16]. Затем он переносится через слизистую двенадцатиперстной кишки в кровь, где транспортируется трансферрином к клеткам или костному мозгу для эритропоэза [продуцирования красных кровяных телец (эритроцитов)]. [14,17,18] Существует механизм обратной связи, который усиливается. всасывание железа у людей с дефицитом железа. Напротив, люди с перегрузкой железом снижают абсорбцию железа через гепсидин. В настоящее время общепринято, что абсорбция железа контролируется ферропортином, который позволяет или не позволяет железу из клетки слизистой оболочки попадать в плазму.
Физическое состояние железа, поступающего в двенадцатиперстную кишку, сильно влияет на его всасывание. При физиологическом pH двухвалентное железо (Fe +2 ) быстро окисляется до нерастворимой трехвалентной формы (Fe +3 ). Желудочная кислота понижает pH в проксимальном отделе двенадцатиперстной кишки, уменьшая Fe +3 в просвете кишечника за счет редуктазы железа, тем самым обеспечивая последующий транспорт Fe +2 через апикальную мембрану энтероцитов. Это увеличивает растворимость и поглощение трехвалентного железа.Когда продукция желудочного сока нарушена (например, ингибиторами кислотного насоса, такими как лекарство, прилосек), абсорбция железа существенно снижается.
Диетический гем также может транспортироваться через апикальную мембрану по еще неизвестному механизму и впоследствии метаболизироваться в энтероцитах гемоксигеназой 1 (HO-1) с высвобождением (Fe +2 ) [19]. Этот процесс более эффективен, чем абсорбция неорганического железа, и не зависит от рН двенадцатиперстной кишки. Таким образом, на него не влияют такие ингибиторы, как фитат и полифенолы.Следовательно, красное мясо с высоким содержанием гемоглобина является отличным источником железа. Непосредственно интернализованный Fe +2 обрабатывается энтероцитами и в конечном итоге (или нет) экспортируется через базолатеральную мембрану в кровоток через транспортер ферропортин Fe +2 . Ферропортин-опосредованный отток Fe +2 связан с его повторным окислением с Fe +2 , катализируемым мембраносвязанным ферроксидазным гефестином, который физически взаимодействует с ферропортином [20] и, возможно, также его гомологом в плазме церулоплазмином.Экспортируемое железо улавливается трансферрином, который поддерживает Fe +3 в окислительно-восстановительном инертном состоянии и доставляет его в ткани. Общее содержание железа в трансферрине (≈3 мг) соответствует менее 0,1% железа в организме, но оно очень динамично и подвергается более чем 10-кратному ежедневному обороту для поддержания эритропоэза. Пул трансферрина железа пополняется в основном за счет железа, рециркулируемого из неэффективных эритроцитов, и, в меньшей степени, за счет вновь абсорбированного пищевого железа. Стареющие эритроциты очищаются ретикулоэндотелиальными макрофагами, которые метаболизируют гемоглобин и гем и высвобождают железо в кровоток.По аналогии с кишечными энтероцитами, макрофаги экспортируют Fe +2 из своей плазматической мембраны через ферропортин в процессе, сопряженном с повторным окислением Fe +2 до Fe +3 церулоплазмином с последующей загрузкой Fe +3. на трансферрин. [21]
Theil et al ., [21] недавно сообщили, что существует также независимый механизм абсорбции растительных ферритинов, в основном присутствующих в бобовых. Однако актуальность переносчика ферритина неясна, поскольку большая часть ферритина, по-видимому, разлагается во время обработки и переваривания пищи, тем самым высвобождая неорганическое железо из оболочки ферритина для поглощения по нормальному механизму.[22] Поскольку одна молекула ферритина содержит 1000 или более атомов железа и на нее также не должны влиять ингибиторы абсорбции железа, такой механизм может стать важным источником железа в развивающихся странах, где обычно потребляются бобовые.
Регуляция гомеостаза железа
Поскольку железо требуется для ряда разнообразных клеточных функций, для поддержания гомеостаза железа требуется постоянный баланс между поглощением, транспортом, хранением и использованием железа. [11] Поскольку в организме отсутствует определенный механизм активного выведения железа, баланс железа в основном регулируется в точке абсорбции.[23,24]
Гепсидин — это циркулирующий пептидный гормон, секретируемый печенью, который играет центральную роль в регуляции гомеостаза железа. Это главный регулятор системного гомеостаза железа, координирующий использование и хранение железа с приобретением железа. [25] Этот гормон в первую очередь вырабатывается гепатоцитами и является негативным регулятором поступления железа в плазму []. Гепсидин действует путем связывания с ферропортином, переносчиком железа, присутствующим на клетках двенадцатиперстной кишки, макрофагах и клетках плаценты.Связывание гепсидина вызывает интернализацию и деградацию ферропортина. [26] Потеря ферропортина с поверхности клетки предотвращает попадание железа в плазму []. Снижение поступления железа в плазму приводит к низкому насыщению трансферрина и меньшему количеству железа доставляется в развивающийся эритробласт. И наоборот, снижение экспрессии гепсидина приводит к увеличению ферропортина на клеточной поверхности и увеличению абсорбции железа [27] []. У всех видов концентрация железа в биологических жидкостях строго регулируется, чтобы обеспечить необходимое количество железа и избежать токсичности, поскольку избыток железа может привести к образованию активных форм кислорода.[28] Гомеостаз железа у млекопитающих регулируется на уровне кишечной абсорбции, поскольку для железа не существует экскреторного пути.
Гепсидин-опосредованная регуляция гомеостаза железа. (а) Повышенная экспрессия гепсидина печенью является результатом воспалительных стимулов. Высокий уровень гепсидина в кровотоке приводит к интернализации и деградации ферропортина, экспортера железа. Потеря ферропортина на клеточной поверхности приводит к загрузке железа макрофагами, низким уровням железа в плазме и снижению эритропоэза из-за снижения количества железа, связанного с трансферрином.Снижение эритропоэза приводит к анемии хронического заболевания. (b) Нормальные уровни гепсидина в ответ на потребность в железе регулируют уровень импорта железа в плазму, нормальное насыщение трансферрина и нормальные уровни эритропоэза. (c) Гемохроматоз или перегрузка железом возникает из-за недостаточного уровня гепсидина, вызывая повышенный импорт железа в плазму, высокое насыщение трансферрина и избыточное отложение железа в печени. Источник: De Domenico, и др. . [27]
Уровни гепсидина в плазме регулируются различными стимулами, включая цитокины, железо в плазме, анемию и гипоксию.Нарушение регуляции экспрессии гепсидина приводит к нарушениям железа. Избыточная экспрессия гепсидина приводит к анемии хронического заболевания, в то время как низкая продукция гепсидина приводит к наследственному гемохроматозу (HFE) с последующим накоплением железа в жизненно важных органах []. Большинство наследственных заболеваний, связанных с железом, возникают в результате недостаточного производства гепсидина по сравнению со степенью накопления железа в тканях. Было показано, что нарушение экспрессии гепсидина является результатом мутаций в любом из 4 различных генов: TfR2, HFE, гемохроматоз типа 2 (HFE2) и антимикробный пептид гепсидина (HAMP).Мутации в HAMP, гене, кодирующем гепсидин, приводят к болезни, связанной с перегрузкой железом, поскольку отсутствие гепсидина обеспечивает постоянное высокое всасывание железа. Роль других генов (TFR2, HFE и HFE2) в регуляции продукции гепсидина не ясна [27].
Хранение
Концентрация ферритина вместе с концентрацией гемосидерина отражает запасы железа в организме. Они хранят железо в нерастворимой форме и присутствуют в основном в печени, селезенке и костном мозге. [2] Большая часть железа связана с широко распространенным и высококонсервативным железосвязывающим белком ферритином.[18] Гемосидерин представляет собой комплекс хранения железа, который с меньшей готовностью выделяет железо для нужд организма. В условиях устойчивого состояния сывороточные концентрации ферритина хорошо коррелируют с общими запасами железа в организме. [29] Таким образом, сывороточный ферритин является наиболее удобным лабораторным тестом для оценки запасов железа.
Экскреция
Помимо потерь железа из-за менструации, другого кровотечения или беременности, железо очень консервативно и нелегко выводится из организма. [30] Существует некоторая обязательная потеря железа из организма в результате физиологического отшелушивания клеток с эпителиальных поверхностей [30], включая кожу, мочеполовые и желудочно-кишечные тракты.[3] Однако, по оценкам, эти потери очень ограничены (≈1 мг / день). [31] Потери железа из-за кровотечения могут быть значительными, а чрезмерная менструальная кровопотеря является наиболее частой причиной дефицита железа у женщин.
БИОЛОГИЧЕСКАЯ ДОСТУПНОСТЬ
Пищевое железо встречается в двух формах: гемовая и негемовая. [23] Основными источниками гемового железа являются гемоглобин и миоглобин из мяса, птицы и рыбы, тогда как негемовое железо получают из злаков, бобовых, бобовых, фруктов и овощей.[32] Гемовое железо обладает высокой биодоступностью (15–35%), и диетические факторы мало влияют на его абсорбцию, тогда как абсорбция негемового железа намного ниже (2–20%) и сильно зависит от присутствия других пищевых компонентов. [23] Напротив, количество негемового железа в рационе во много раз превышает количество гемового железа в большинстве приемов пищи. Таким образом, несмотря на свою более низкую биодоступность, негемовое железо обычно вносит больший вклад в питание железом, чем гемовое железо. [33] Основными ингибиторами абсорбции железа являются фитиновая кислота, полифенолы, кальций и пептиды из частично переваренных белков.[23] Усилители — это аскорбиновая кислота и мышечная ткань, которые могут восстанавливать трехвалентное железо до двухвалентного железа и связывать его в растворимые комплексы, доступные для абсорбции. [23]
Факторы, повышающие абсорбцию железа
На абсорбцию железа влияет ряд диетических факторов. Аскорбат и цитрат частично увеличивают усвоение железа, действуя как слабые хелатирующие агенты, способствующие растворению металла в двенадцатиперстной кишке []. [34] Железо легко переносится из этих соединений в клетки слизистой оболочки. Исследователи продемонстрировали дозозависимый усиливающий эффект нативной или добавленной аскорбиновой кислоты на абсорбцию железа.[34] Усиливающий эффект в значительной степени связан с его способностью восстанавливать трехвалентное железо до двухвалентного железа, но также из-за его способности хелатировать железо. [35] Аскорбиновая кислота преодолеет отрицательное влияние на абсорбцию железа всех ингибиторов, включая фитат, [36] полифенолы, [37], кальций и белки, содержащиеся в молочных продуктах [38], и увеличит абсорбцию как нативного, так и обогащенного железа. Во фруктах и овощах усиливающий эффект аскорбиновой кислоты часто нивелируется ингибирующим действием полифенолов.[39] Аскорбиновая кислота является единственным усилителем всасывания в вегетарианских диетах, а всасывание железа из вегетарианских и веганских блюд можно оптимизировать путем включения овощей, содержащих аскорбиновую кислоту. [40] Варка, промышленная переработка и хранение разлагают аскорбиновую кислоту и устраняют ее усиливающий эффект на усвоение железа. [41]
Таблица 1
Факторы, которые могут влиять на всасывание железа
Было показано усиливающее действие мяса, рыбы или птицы на всасывание железа из вегетарианских блюд [42], и 30 г мышечной ткани считается эквивалентом 25 мг аскорбиновой кислоты. .[33] Бьорн-Расмуссен и Халлберг [43] сообщили, что добавление курицы, говядины или рыбы к кукурузной муке увеличивало всасывание негемового железа в 2-3 раза без влияния того же количества белка, что и яичного альбумина. Как и в случае с аскорбиновой кислотой, было несколько сложнее продемонстрировать усиливающий эффект мяса при многократном приёме пищи и в полных исследованиях диеты. Редди и др. ., [44] сообщили только о незначительном улучшении всасывания железа (35%) в самостоятельно выбранных диетах в течение 5 дней, когда ежедневное потребление мышечной ткани было увеличено до 300 г / день, хотя в аналогичных 5-дневных рационах. В ходе дневного исследования 60 г свинины, добавленные к вегетарианской диете, увеличили всасывание железа на 50%.[45]
Факторы, ингибирующие абсорбцию железа
В растительной диете фитат (мио-инозитол гексакисфосфат) является основным ингибитором абсорбции железа. [23] Было показано, что отрицательное влияние фитата на абсорбцию железа зависит от дозы и начинается с очень низких концентраций 2-10 мг / прием пищи. [37,46] Молярное отношение фитата к железу может быть использовано для оценки влияния на абсорбцию. . Соотношение должно составлять 1: 1 или предпочтительно 0,4: 1 для значительного улучшения всасывания железа в простых злаковых или бобовых блюдах, которые не содержат каких-либо усилителей усвоения железа, или 6: 1 в комбинированных блюдах с некоторыми овощами, содержащими аскорбин. кислота и мясо как усилители.[47]
Полифенолы содержатся в различных количествах в растительной пище и напитках, таких как овощи, фрукты, некоторые злаки и бобовые, чай, кофе и вино. Ингибирующее действие полифенолов на абсорбцию железа было показано с черным чаем и, в меньшей степени, с травяными чаями. [48,49] В зерновых и бобовых культурах полифенолы усиливают ингибирующий эффект фитата, как было показано в исследовании, сравнивающем сорго с высоким и низким содержанием полифенолов. [23]
Было показано, что кальций отрицательно влияет на абсорбцию негемового и гемового железа, что отличает его от других ингибиторов, влияющих только на абсорбцию негемового железа.[50] Дозозависимые ингибирующие эффекты были показаны при дозах 75-300 мг, когда кальций добавлялся в булочки, и при дозах 165 мг кальция из молочных продуктов. [51] Предполагается, что исследования однократного приема пищи показывают отрицательное влияние кальция на абсорбцию железа, тогда как исследования многократного приема пищи с большим разнообразием продуктов и различными концентрациями других ингибиторов и усилителей показывают, что кальций лишь ограниченно влияет на абсорбцию железа. [52]
Было показано, что животные белки, такие как молочные белки, яичные белки и альбумин, ингибируют абсорбцию железа.[53] Было показано, что две основные белковые фракции коровьего молока, казеин и сыворотка, а также яичный белок ингибируют абсорбцию железа у человека. [54] Белки сои также снижают всасывание железа. [55]
Конкуренция с железом
Исследования конкуренции показывают, что несколько других тяжелых металлов могут участвовать в пути всасывания железа в кишечнике. К ним относятся свинец, марганец, кобальт и цинк. Поскольку дефицит железа часто сочетается с интоксикацией свинцом, это взаимодействие может вызвать особенно серьезные медицинские осложнения у детей.[56]
Свинец является особенно опасным элементом для метаболизма железа. [57] Свинец поглощается механизмом поглощения железа (DTM1) и вторично блокирует железо за счет конкурентного торможения. Кроме того, свинец препятствует ряду важных железозависимых метаболических этапов, таких как биосинтез гема. Это многогранное влияние имеет особенно тяжелые последствия для детей, поскольку свинец не только вызывает анемию, но и может ухудшить когнитивное развитие. Свинец в естественных условиях присутствует в больших количествах в грунтовых водах и почве в некоторых регионах и может тайно нанести вред здоровью детей.По этой причине большинство педиатров в США обычно проверяют содержание свинца в раннем возрасте с помощью простого анализа крови.
ТРЕБОВАНИЯ К ЧЕЛОВЕКУ
В раннем детстве потребности в железе удовлетворяются за счет небольшого количества железа, содержащегося в грудном молоке. [58] Потребность в железе заметно возрастает через 4-6 месяцев после рождения и составляет около 0,7-0,9 мг / день в течение оставшейся части первого года [58]. В возрасте от 1 до 6 лет содержание железа в организме снова увеличивается вдвое. [58] Потребность в железе также очень высока у подростков, особенно в период скачка роста.У девочек обычно происходит скачок роста до менархе, но к этому времени рост не заканчивается. У мальчиков наблюдается заметное увеличение массы и концентрации гемоглобина в период полового созревания. На этой стадии потребности в железе повышаются до уровня, превышающего средние потребности в железе у менструирующих женщин [58] [см.].
Таблица 2
Потребность в железе 97,5% людей с точки зрения абсорбированного железа a , по возрастным группам и полу (Всемирная организация здравоохранения, 1989 г.) ее тело.Точный баланс между потреблением и потерей пищи поддерживает этот баланс. Около 1 мг железа теряется каждый день из-за отшелушивания клеток кожи и слизистых оболочек, включая слизистую оболочку желудочно-кишечного тракта. [59] Менструация увеличивает среднесуточную потерю железа примерно до 2 мг в день у взрослых женщин в пременопаузе. [60] Увеличение массы тела во время скачков роста в неонатальном и детском возрасте временно увеличивает потребность в железе. [61]
Потребление железа с пищей необходимо для восполнения потери железа с калом и мочой, а также через кожу.Эти базальные потери составляют примерно 0,9 мг железа для взрослого мужчины и 0,8 мг для взрослой женщины. [62] У женщин репродуктивного возраста необходимо учитывать потерю железа с менструальной кровью [].
ГРУППЫ ПОВЫШЕННОГО РИСКА
Наибольшая вероятность дефицита железа обнаруживается в тех частях населения, которые не имеют надлежащего доступа к пище, богатой усвояемым железом, во время стадий высокой потребности в железе. Эти группы соответствуют детям, подросткам и женщинам репродуктивного возраста, особенно во время беременности.[63,58]
У младенцев и подростков повышенная потребность в железе является результатом быстрого роста. Для женщин репродуктивного возраста основная причина — чрезмерная кровопотеря во время менструации. Во время беременности потребность в железе значительно возрастает из-за быстрого роста плаценты и плода, а также увеличения глобулярной массы. [63] Напротив, взрослые мужчины и женщины в постменопаузе имеют низкий риск дефицита железа, и количество железа в нормальном рационе обычно достаточно для удовлетворения их физиологических потребностей.[63]
ПОСЛЕДСТВИЯ И ПРИЧИНЫ ДЕФИЦИТА ЖЕЛЕЗА
Последствия дефицита железа
Дефицит железа определяется как состояние, при котором отсутствуют мобилизуемые запасы железа и при котором появляются признаки нарушения поступления железа в ткани, включая эритрон. , отмечены. [64] Дефицит железа может сопровождаться анемией или без нее. Некоторые функциональные изменения могут произойти в отсутствие анемии, но наиболее функциональные нарушения, по-видимому, возникают при развитии анемии. [2] Даже легкие и средние формы железодефицитной анемии могут быть связаны с функциональными нарушениями, влияющими на когнитивное развитие [65], механизмы иммунитета [66] и работоспособность.[67] Дефицит железа во время беременности связан с множеством неблагоприятных исходов как для матери, так и для ребенка, включая повышенный риск сепсиса, материнской смертности, перинатальной смертности и низкой массы тела при рождении. [68] Дефицит железа и анемия также снижают способность к обучению и связаны с повышенным уровнем заболеваемости. [68]
Причины дефицита железа
Дефицит железа возникает в результате истощения запасов железа и возникает, когда абсорбция железа не может идти в ногу с метаболическими потребностями в железе для поддержания роста и восполнения потери железа, что в первую очередь связано с кровопотерей .[2] Основные причины дефицита железа включают низкое потребление биодоступного железа, повышенную потребность в железе в результате быстрого роста, беременности, менструации и избыточную кровопотерю, вызванную патологическими инфекциями, такими как анкилостомы и власоглавы, вызывающие потерю крови из желудочно-кишечного тракта [2] 69,70,71,72] и нарушение всасывания железа. [73] Частота дефицита железа увеличивается у девочек-подростков, потому что менструальные потери железа накладываются на потребность в быстром росте [74]. Другими факторами риска дефицита железа у молодых женщин являются высокий паритет, использование внутриматочной спирали и вегетарианская диета.[75]
Дефицит железа в питании возникает, когда физиологические потребности не могут быть удовлетворены за счет абсорбции железа из рациона. [72] Биодоступность пищевого железа низка в группах населения, потребляющих однообразные растительные диеты с небольшим количеством мяса. [72] Во многих развивающихся странах растительные продукты для отлучения от груди редко обогащаются железом, а частота анемии превышает 50% у детей младше 4 лет. [64]
Когда запасы железа истощаются и железа недостаточно для эритропоэза, синтез гемоглобина в предшественниках эритроцитов нарушается и появляются гематологические признаки железодефицитной анемии.
ОЦЕНКА СТАТУСА ЖЕЛЕЗА
Дефицит железа и, в конечном итоге, анемия развиваются поэтапно и могут быть оценены путем измерения различных биохимических показателей. Хотя некоторые ферменты железа чувствительны к дефициту железа [63], их активность не использовалась в качестве успешного рутинного измерения статуса железа [2].
Лабораторные измерения необходимы для правильной диагностики дефицита железа. Они наиболее информативны, когда несколько показателей уровня железа исследуются и оцениваются в контексте питания и истории болезни.
Пул железа в плазме или сыворотке — это фракция всего железа в организме, которая циркулирует в основном связанном с трансферрином. Три способа оценки уровня железа в плазме или сыворотке включают: 1) измерение общего содержания железа в единице объема в мкг / дл; 2) измерение общего количества сайтов связывания для атомов железа на трансферрине, известного как общая железосвязывающая способность в мкг / дл 2 ; и 3) оценка процента двух сайтов связывания на всех занятых молекулах трансферрина, называемого процентным насыщением трансферрина.[76] Однако заметные биологические вариации этих значений могут возникать в результате суточных колебаний, наличия инфекции или воспалительных состояний и недавнего потребления железа с пищей. [76]
Протопорфирин цинка отражает нехватку железа на последних стадиях синтеза гемоглобина, так что цинк вставляется в молекулу протопорфирина вместо железа. Протопорфирин цинка может быть обнаружен в эритроцитах с помощью флуориметрии и является мерой тяжести дефицита железа. [76]
Сывороточный ферритин является хорошим индикатором запасов железа в организме в большинстве случаев.Когда концентрация сывороточного ферритина ≥15 мкг / л, присутствуют запасы железа; более высокие концентрации отражают размер склада железа; при низкой концентрации (<12 мкг / л для детей младше 5 лет и <15 мкг / л для детей старше 5 лет) запасы железа истощаются. [76] Однако ферритин является белком-реагентом острой фазы, и его сывороточные концентрации могут быть повышены независимо от изменения запасов железа, инфекции или воспаления. [76,2] Это означает, что может быть трудно интерпретировать концентрацию ферритина там, где инфекция болезни распространены.
Еще одним индикатором статуса железа является концентрация TfR в сыворотке крови. Поскольку TfR в основном происходит из развивающихся эритроцитов, он отражает интенсивность эритропоэза и потребность в железе. Когда запасы железа истощаются, концентрация повышается при железодефицитной анемии, что указывает на серьезную недостаточность железа. Это при условии, что нет других причин аномального эритропоэза. [76] Клинические исследования показывают, что сывороточный TfR менее подвержен воспалению, чем сывороточный ферритин. [77] Основным преимуществом TfR как индикатора является возможность оценки величины функционального дефицита железа после истощения запасов железа.[78]
Отношение TfR к ферритину (TfR / ферритин) было разработано для оценки изменений как в накопленном, так и в функциональном железе и считается более полезным, чем TfR или ферритин отдельно. [79] TfR / ферритин использовался для оценки запасов железа в организме как у детей, так и у взрослых. [80] Однако высокая стоимость и отсутствие стандартизации анализа TfR до сих пор ограничивали применимость метода [81].
Низкая концентрация гемоглобина является показателем анемии, конечной стадии дефицита железа.[76,2]
АНЕМИЯ И ЕЕ ПРИЧИНЫ
Анемия описывает состояние, при котором количество эритроцитов в крови низкое или в клетках крови содержится меньше нормального гемоглобина. Человека, страдающего анемией, называют анемичным. Цель эритроцитов — доставлять кислород из легких в другие части тела. Молекула гемоглобина является функциональной единицей эритроцитов и представляет собой сложную белковую структуру, которая находится внутри эритроцитов. Несмотря на то, что эритроциты производятся в костном мозге, в их производство вовлечены многие другие факторы.Например, железо — очень важный компонент молекулы гемоглобина; эритропоэтин, молекула, секретируемая почками, способствует образованию эритроцитов в костном мозге.
Наличие правильного количества эритроцитов и профилактика анемии требует взаимодействия между почками, костным мозгом и питательными веществами в организме. Если почки или костный мозг не функционируют, или организм плохо питается, то нормальное количество и функции эритроцитов может быть трудно поддерживать.
Анемия на самом деле является признаком болезненного процесса, а не самой болезни.Обычно его классифицируют как хронический или острый. Хроническая анемия возникает в течение длительного периода времени. Острая анемия возникает быстро. Определение того, присутствует ли анемия в течение длительного времени или это что-то новое, помогает врачам найти причину. Это также помогает предсказать, насколько серьезными могут быть симптомы анемии. При хронической анемии симптомы обычно начинаются медленно и постепенно прогрессируют; тогда как при острой анемии симптомы могут быть резкими и более тревожными.
Эритроциты живут около 100 дней, поэтому организм постоянно пытается их заменить.У взрослых производство эритроцитов происходит в костном мозге. Врачи пытаются определить, вызвано ли низкое количество эритроцитов повышенной кровопотерей эритроцитов или их снижением в костном мозге. Знание того, изменилось ли количество лейкоцитов и / или тромбоцитов, также помогает определить причину анемии.
По оценкам Всемирной организации здравоохранения (ВОЗ), два миллиарда человек во всем мире страдают анемией и примерно 50% всех анемий объясняются дефицитом железа. [64] Это происходит на всех этапах жизненного цикла, но чаще встречается у беременных женщин и маленьких детей.[82] Анемия является результатом множества причин, которые можно изолировать, но чаще всего они сосуществуют. Некоторые из этих причин включают следующие:
Железодефицитная анемия
Наиболее важной и частой причиной анемии является дефицит железа. [82] Если потребление железа ограничено или неадекватно из-за плохого питания, в результате может возникнуть анемия. Это называется железодефицитной анемией. Железодефицитная анемия также может возникать при наличии язвы желудка или других источников медленного хронического кровотечения (рак толстой кишки, рак матки, полипы кишечника, геморрой и т. Д.).[83]
Анемия хронического заболевания
Любое длительное заболевание может привести к анемии. Этот тип анемии является вторым по распространенности после анемии, вызванной дефицитом железа, и развивается у пациентов с острым или хроническим системным заболеванием или воспалением. [84] Это состояние было названо «анемией воспаления» из-за повышенного содержания гепсидина, который блокирует как рециркуляцию железа из макрофагов, так и абсорбцию железа. [85]
Анемия из-за активного кровотечения
Потеря крови из-за обильного менструального кровотечения или ран может вызвать анемию.[82] Язвы желудочно-кишечного тракта или раковые заболевания, такие как рак толстой кишки, могут медленно терять кровь и также могут вызывать анемию. [86,87]
Анемия, связанная с заболеванием почек
Почки выделяют гормон эритропоэтин, который помогает костному мозгу сделать эритроциты. У людей с хроническим (длительным) заболеванием почек выработка этого гормона снижена, а это, в свою очередь, снижает выработку эритроцитов, вызывая анемию. [88] Хотя дефицит эритропоэтина является основной причиной анемии при хронической почечной недостаточности, это не единственная причина.Следовательно, необходимо минимальное обследование, чтобы исключить дефицит железа и другие аномалии клеточной линии. [89]
Анемия, связанная с беременностью
Увеличение объема плазмы во время беременности приводит к разбавлению эритроцитов и может проявляться как анемия. [90] Железодефицитная анемия составляет 75% всех анемий во время беременности. [90]
Анемия, связанная с плохим питанием
Витамины и минералы необходимы для образования эритроцитов. Помимо железа, для правильного производства гемоглобина необходимы витамин B12, виамин A, фолиевая кислота, рибофлавин и медь.[82] Дефицит любого из этих питательных микроэлементов может вызвать анемию из-за недостаточного производства эритроцитов. Плохое питание — важная причина низкого уровня витаминов и, как следствие, анемии.
Ожирение и анемия
Ожирение характеризуется хроническим слабым системным воспалением, повышенным уровнем гепсидина, которое, в свою очередь, связано с анемией хронического заболевания. Ausk и Ioannou [91] предположили, что ожирение может быть связано с особенностями анемии хронического заболевания, включая низкую концентрацию гемоглобина, низкое содержание железа и трансферрина в сыворотке, а также повышенный уровень ферритина в сыворотке.Избыточный вес и ожирение были связаны с изменениями сывороточного железа, насыщения трансферрина и ферритина, которые, как ожидается, произойдут в условиях хронического системного воспаления. Воспаление, связанное с ожирением, может повышать концентрацию гепсидина и снижать доступность железа. Aeberli и др. ., [92] сравнили уровень железа, потребление железа с пищей и его биодоступность, а также циркулирующие уровни гепсидина, лептина и интерлейкина-6 (ИЛ-6) у детей с избыточной массой тела и детей с нормальным весом.Они указали, что существует пониженная доступность железа для эритропоэза у детей с избыточным весом и что это, вероятно, связано с опосредованным гепсидином сниженным всасыванием железа и / или повышенным секвестрацией железа, а не с низким содержанием железа с пищей.
Алкоголизм
Алкоголь оказывает многочисленные неблагоприятные эффекты на различные типы клеток крови и их функции. [93] У алкоголиков часто есть дефектные эритроциты, которые преждевременно разрушаются. [93,94] Сам по себе алкоголь также может быть токсичным для костного мозга и может замедлять производство эритроцитов.[93,94] Кроме того, плохое питание и дефицит витаминов и минералов связаны с алкоголизмом. [95] Сочетание этих факторов может привести к анемии у алкоголиков.
Серповидно-клеточная анемия
Серповидно-клеточная анемия — одно из наиболее распространенных наследственных заболеваний. [96] Это заболевание, связанное с кровью, которое влияет на молекулу гемоглобина и приводит к изменению формы всей клетки крови в стрессовых условиях [97]. В таком состоянии проблема с гемоглобином бывает качественной или функциональной.Аномальные молекулы гемоглобина могут вызвать проблемы в целостности структуры эритроцитов, и они могут стать серповидными (серповидные клетки). [97] Существуют разные типы серповидно-клеточной анемии разной степени тяжести. Это особенно распространено у африканцев, ближневосточных и средиземноморских предков. [97]
Талассемия
Это еще одна группа причин анемии, связанных с гемоглобином, которая связана с отсутствием или ошибками в генах, ответственных за выработку гемоглобина. [97] Молекула гемоглобина имеет субъединицы, обычно называемые альфа- и бета-цепями глобина.Отсутствие определенной субъединицы определяет тип альфа- или бета-талассемии. [97,98] Существует много типов талассемии, которые различаются по степени тяжести от легкой (малая талассемия) до тяжелой (большая талассемия). [98] Они также являются наследственными, но вызывают количественные аномалии гемоглобина, то есть вырабатывается недостаточное количество молекул правильного типа. Альфа- и бета-талассемии являются наиболее распространенными наследственными моногенными заболеваниями в мире с наибольшей распространенностью в регионах, где малярия была или все еще является эндемической.[97]
Апластическая анемия
Апластическая анемия — это заболевание, при котором разрушается костный мозг и снижается выработка клеток крови. [99] Это вызывает дефицит всех трех типов клеток крови (панцитопения), включая эритроциты (анемия), лейкоциты (лейкопения) и тромбоциты (тромбоцитопения). [100,101] Многие распространенные лекарства могут иногда вызывать этот тип анемии в качестве побочного эффекта. у некоторых людей. [99]
Гемолитическая анемия
Гемолитическая анемия — это тип анемии, при которой происходит разрыв эритроцитов, известный как гемолиз, который разрушается быстрее, чем костный мозг может их заменить.[102] Гемолитическая анемия может возникнуть по разным причинам и часто классифицируется как приобретенная или наследственная. Распространенными приобретенными причинами гемолитической анемии являются аутоиммунитет, микроангиопатия и инфекции. Нарушения ферментов эритроцитов, мембран и гемоглобина вызывают наследственную гемолитическую анемию. [102]
ПРЕДОТВРАЩЕНИЕ НЕДОСТАТОЧНОСТИ ЖЕЛЕЗА (СТРАТЕГИИ ВМЕШАТЕЛЬСТВА)
Четыре основных стратегии коррекции эффективности микронутриентов в популяциях могут использоваться для коррекции дефицита железа, как по отдельности, так и в комбинации.Это обучение в сочетании с модификацией диеты для улучшения потребления железа и его биодоступности; добавление железа (обеспечение железом, обычно в более высоких дозах, без еды), обогащение пищевых продуктов железом и новый подход к биофортификации. Однако есть некоторые трудности в применении некоторых из этих стратегий при рассмотрении железа.
Диверсификация продуктов питания
Модификации рациона питания для сокращения потребления Индийской стоматологической ассоциации включают увеличение потребления продуктов, богатых железом, особенно мясных продуктов, увеличение потребления фруктов и овощей, богатых аскорбиновой кислотой, для увеличения абсорбции негемового железа и снижение потребления чая и кофе, которые подавляют всасывание негемового железа.[103,58] Другая стратегия — снизить содержание антинутриентов, чтобы сделать железо, поступающее из их пищевых источников, более доступным. Биодоступность железа может быть увеличена такими методами, как проращивание и ферментация, которые способствуют ферментативному гидролизу фитиновой кислоты в цельнозерновых зерновых и бобовых культурах за счет повышения активности эндогенных или экзогенных ферментов фитазы. [104] Даже использование неферментативных методов, таких как термическая обработка, замачивание и измельчение, для снижения содержания фитиновой кислоты в основных продуктах растительного происхождения позволило улучшить биодоступность железа (и цинка).[105,106]
Добавка
Для перорального приема добавок железа предпочтительны соли двухвалентного железа (сульфат двухвалентного железа и глюконат двухвалентного железа) из-за их низкой стоимости и высокой биодоступности. [72] Хотя абсорбция железа выше при приеме добавок железа натощак, тошнота и боль в эпигастрии могут развиться из-за введенных более высоких доз железа (обычно 60 мг Fe / день). Если возникают такие побочные эффекты, следует попытаться снизить дозу между приемами пищи или давать железо во время еды, хотя пища снижает всасывание лекарственного железа примерно на две трети.[107] Добавки железа во время беременности рекомендуется в развивающихся странах, где женщины часто вступают в беременность с низкими запасами железа. [108] Хотя обычно считалось, что польза от приема добавок железа перевешивает предполагаемый риск, есть некоторые свидетельства того, что добавление в дозах, рекомендованных для здоровых детей, несет в себе риск увеличения тяжести инфекционного заболевания на фоне малярии. [109,110]
Обогащение
Обогащение пищевых продуктов железом сложнее, чем обогащение такими питательными веществами, как цинк в муке, йод в соли и витамин А в кулинарном масле.[72] Наиболее биодоступные соединения железа растворимы в воде или разбавленной кислоте, но часто вступают в реакцию с другими пищевыми компонентами, вызывая неприятный запах, изменение цвета или окисление жиров. [103] Таким образом, менее растворимые формы железа, хотя и хуже усваиваются, часто выбираются для обогащения, чтобы избежать нежелательных сенсорных изменений. [72] Обогащение обычно производится с гораздо более низкими дозами железа, чем с добавками. Это ближе к физиологической среде и может быть самым безопасным вмешательством в малярийных областях. [111] Нет никаких опасений по поводу безопасности добавок железа или обогащения железа в немалярийных эндемичных районах.[112]
Соединения железа, рекомендованные [7] для обогащения пищевых продуктов, включают сульфат железа, фумарат железа, пирофосфат железа и порошок электролитического железа. Пшеничная мука является наиболее распространенным пищевым продуктом, обогащенным железом, и обычно она обогащается порошками элементарного железа, которые не рекомендуются ВОЗ. [7,113] Харрелл и Эгли [23] сообщили, что из 78 национальных программ по пшеничной муке только восемь улучшатся. статус железа. В этих программах использовались рекомендуемые соединения железа на рекомендованных уровнях.Другие страны использовали не рекомендуемые соединения или более низкие уровни железа по сравнению с потреблением муки. Коммерческое детское питание, такое как смеси и злаки, также обычно обогащено железом.
Биообогащение
Содержание железа колеблется от 25 до 56 мг / кг в различных сортах пшеницы и 7-23 мг / кг в зернах риса. Однако большая часть этого железа удаляется в процессе измельчения. Поглощение железа зерновыми и бобовыми культурами, многие из которых имеют высокое содержание самородного железа, обычно низкое из-за высокого содержания в них фитата, а иногда и полифенолов.[48] Стратегии биофортификации включают селекцию растений и генную инженерию. Уровни железа в обычных бобах и просе были успешно увеличены путем селекции растений, но использование других основных продуктов питания является более трудным или невозможным (рис) из-за недостаточной естественной генетической изменчивости. Lucca и др. ., [114] увеличили содержание железа в эндосперме риса, чтобы улучшить его всасывание в кишечнике человека с помощью генной инженерии. Они ввели ген ферритина из Phaseolus vulgaris в рисовые зерна, увеличив содержание железа в них вдвое.Для увеличения биодоступности железа они ввели в эндосперм риса термотолерантную фитазу из Aspergillus fumigatus . Они указали, что этот рис с более высоким содержанием железа и богатым фитазой имеет большой потенциал для существенного улучшения питания железом в тех популяциях, где дефицит железа так широко распространен. [114] К сожалению, фитаза не устояла перед приготовлением. Важность различных минералов, таких как цинк [115] и железо, требует большего внимания на индивидуальном уровне и уровне общественного здравоохранения.
Сноски
Источник поддержки: Нет
Конфликт интересов: Не объявлен.
СПИСОК ЛИТЕРАТУРЫ
1. Борода Дж. Л., Доусон HD. Железо. В: О’Делл Б.Л., Сунде Р.А., редакторы. Справочник по незаменимым в питании минеральным элементам. Нью-Йорк: CRC Press; 1997. С. 275–334. [Google Scholar] 2. Вуд Р.Дж., Ронненберг А. Железо. В: Shils ME, Shike M, Ross AC, Caballero B, Cousins RJ, редакторы. Современное питание в здоровье и болезнях. 10-е изд. Балтимор: Липпинкотт Уильямс и Уилкинс; 2005 г.С. 248–70. [Google Scholar] 3. Макдауэлл LR. 2-е изд. Амстердам: Elsevier Science; 2003. Минералы в питании животных и человека; п. 660. [Google Scholar] 4. Гуггенхайм KY. Хлороз: возникновение и исчезновение болезни, связанной с питанием. J Nutr. 1995; 125: 1822–5. [PubMed] [Google Scholar] 5. Ип Р., Даллман PR. Железо. В: Ziegler EE, Filer LJ, редакторы. Присутствуют знания в области питания. 7-е изд. Вашингтон, округ Колумбия: ILSI Press; 1996. С. 278–92. [Google Scholar] 6. Андервуд Э.Дж., Саттл Н.Ф. 3-е изд. Уоллингфорд: международное издательство CABI; 1999 г.Минеральное питание скота; п. 614. [Google Scholar] 7. Аллен Л., де Бенуа Б., Дари О., Харрелл Р., редакторы. Женева: ВОЗ и ФАО; 2006. ВОЗ. Рекомендации по обогащению пищевых продуктов микронутриентами; п. 236. [Google Scholar] 8. Брабин Б.Дж., Премжи З., Верхое ff Ф. Анализ анемии и детской смертности. J Nutr. 2001; 131: 636–45С. [PubMed] [Google Scholar] 9. Quintero-Gutiérrez AG, González-Rosendo G, Sánchez-Muñoz J, Polo-Pozo J, Rodríguez-Jerez JJ. Биодоступность гемового железа в начинке для печенья с использованием поросят в качестве модели животных для человека.Int J Biol Sci. 2008; 4: 58–62. [Бесплатная статья PMC] [PubMed] [Google Scholar] 10. Айзен П., Эннс С., Весслинг-Резник М. Химия и биология метаболизма железа в эукариотах. Int J Biochem Cell Biol. 2001; 33: 940–59. [PubMed] [Google Scholar] 11. Лиу П. Т., Хейскала М., Петерсон П. А., Ян Ю. Роль железа в здоровье и болезнях. Мол Аспекты Мед. 2001; 2: 1–87. [PubMed] [Google Scholar] 12. Guerinot ML. Транспорт микробного железа. Annu Rev Microbiol. 1994; 48: 743–72. [PubMed] [Google Scholar] 13. Асквит К., Каплан Дж.Транспорт железа и меди в дрожжах и его значение для болезней человека. Trends Biochem Sci. 1998. 23: 135–8. [PubMed] [Google Scholar] 15. Вашингтон, округ Колумбия: Национальная академия прессы; 2001. МОМ. Институт медицины. железо. В: Диетические рекомендуемые дозы витамина А, витамина К, мышьяка, бора, хрома, меди, йода, железа, марганца, молибдена, никеля, кремния, ванадия и цинка; С. 290–393. [PubMed] [Google Scholar] 16. Мюир А., Хопфер У. Региональная специфичность поглощения железа щеточно-граничными мембранами тонкого кишечника у нормальных мышей и мышей с дефицитом железа.Am J Physiol. 1985; 248: G376–9. [PubMed] [Google Scholar] 17. Фрейзер Д.М., Андерсон Г.Дж. Импорт железа. I. Абсорбция железа в кишечнике и ее регуляция. Am J Physiol Gastrointest Liver Physiol. 2005; 289: G631–5. [PubMed] [Google Scholar] 18. Наддур С.С., Шрирама К., Мудипалли А. Механизмы транспорта и гомеостаза железа: их роль в здоровье и болезнях. Индийский J Med Res. 2008; 128: 533–44. [PubMed] [Google Scholar] 20. Yeh KY, Yeh M, Mims L, Glass J. Кормление железом индуцирует миграцию и взаимодействие ферропортина 1 и гефестина в двенадцатиперстном эпителии крыс.Am J Physiol Gastrointest Liver Physiol. 2009; 296: 55–65. [Бесплатная статья PMC] [PubMed] [Google Scholar] 21. Тейл Э.С., Чен Х., Миранда С., Янсер Х., Эльзенханс Б., Нуньес М.Т. и др. Абсорбция железа из ферритина не зависит от гемового железа и солей двухвалентного железа у женщин и сегментов кишечника крыс. J Nutr. 2012; 142: 478–83. [Бесплатная статья PMC] [PubMed] [Google Scholar] 22. Hoppler M, Schoenbaechler A, Meile L, Hurrell RF, Walczyk T. Ферритин-железо высвобождается при кипячении и in vitro при пищеварении в желудке .J Nutr. 2008. 138: 878–84. [PubMed] [Google Scholar] 23. Hurrell R, Egli I. Биодоступность железа и диетические контрольные значения. Am J Clin Nutr. 2010; 91: 1461–7S. [PubMed] [Google Scholar] 25. Немет Э., Ганц Т. Регулирование метаболизма железа гепсидином. Annu Rev Nutr. 2006; 26: 323–42. [PubMed] [Google Scholar] 26. Немет Э., Таттл М.С., Пауэлсон Дж., Вон М.Б., Донован А., Уорд Д.М. и др. Гепсидин регулирует отток клеточного железа, связываясь с ферропортином и индуцируя его интернализацию. Наука. 2004; 306: 2090–3.[PubMed] [Google Scholar] 28. Браун В., Киллманн Х. Бактериальные решения проблемы снабжения железом. Trends Biochem Sci. 1999; 24: 104–109. [PubMed] [Google Scholar] 29. Хант-младший. Насколько важна биодоступность железа с пищей? Am J Clin Nutr. 2001; 73: 3–4. [PubMed] [Google Scholar] 30. Хант-младший, Зито, Калифорния, Джонсон, Лос-Анджелес. Выведение железа из организма здоровыми мужчинами и женщинами. Am J Clin Nutr. 2009; 89: 1–7. [PubMed] [Google Scholar] 31. Фэрбенкс В.Ф. Железо в медицине и питании. В: Shils ME, Shike M, Ross AC, Caballero B, Cousins RJ, редакторы.Современное питание в здоровье и болезнях. 10-е изд. Балтимор: Липпинкотт Уильямс и Уилкинс; 1999. С. 193–221. [Google Scholar] 32. потребности человека в витаминах и минералах. Рим: ФАО; 2001. ФАО / ВОЗ. Пищевые подходы к удовлетворению потребностей в витаминах и минералах; С. 7–25. [Google Scholar] 33. Monsen ER, Hallberg L, Layrisse M, Hegsted DM, Cook JD, Mertz W. и др. Оценка доступного пищевого железа. Am J Clin Nutr. 1978; 31: 134–41. [PubMed] [Google Scholar] 34. Конрад ME, Umbreit JN. Краткий обзор: абсорбция железа — путь муцин-мобилферрин-интегрин.Конкурентоспособный путь поглощения металлов. Am J Hematol. 1993; 42: 67–73. [PubMed] [Google Scholar] 35. Конрад М.Э., Шаде С.Г. Хелаты аскорбиновой кислоты в абсорбции железа: роль соляной кислоты и желчи. Гастроэнтерология. 1968; 55: 35–45. [PubMed] [Google Scholar] 36. Холлберг Л., Брюн М., Россандер Л. Поглощение железа у человека: аскорбиновая кислота и дозозависимое ингибирование фитатом. Am J Clin Nutr. 1989; 49: 140–4. [PubMed] [Google Scholar] 37. Зигенберг Д., Бейнс Р.Д., Ботвелл Т.Х., Макфарлейн Б.Дж., Лампарелли Р.Д., Car NG и др.Аскорбиновая кислота предотвращает дозозависимое ингибирующее действие полифенолов и фитатов на абсорбцию негемового железа. Am J Clin Nutr. 1991; 53: 537–41. [PubMed] [Google Scholar] 38. Стекель А., Оливарес М., Писарро Ф., Чадуд П., Лопес И., Амар М. Поглощение обогащающего железа из молочных смесей у младенцев. Am J Clin Nutr. 1986; 43: 917–22. [PubMed] [Google Scholar] 39. Бюллетень D, Бейнс Р.Д., Ботвелл Т.Х., Гиллули М., Макфарлейн Б.Дж., Макфейл А.П. и др. Влияние фруктовых соков и фруктов на усвоение железа из рисовой муки.Br J Nutr. 1987. 57: 331–43. [PubMed] [Google Scholar] 40. Линч SR, Кук JD. Взаимодействие витамина С и железа. Ann N Y Acad Sci. 1980; 355: 32–44. [PubMed] [Google Scholar] 41. Teucher B, Olivares M, Cori H. Усилители поглощения железа: аскорбиновая кислота и другие органические кислоты. Int J Vitam Nutr Res. 2004; 74: 403–19. [PubMed] [Google Scholar] 42. Линч С.Р., Харрелл Р.Ф., Дассенко С.А., Кук Дж.Д. Влияние пищевых белков на биодоступность железа у человека. Adv Exp Med Biol. 1989; 249: 117–32. [PubMed] [Google Scholar] 43.Бьорн-Расмуссен Э., Халльберг Л. Влияние животных белков на усвоение пищевого железа человеком. Нутр Метаб. 1979; 23: 192–202. [PubMed] [Google Scholar] 44. Редди МБ, Харрелл Р.Ф., Кук JD. Разнообразное питание незначительно влияет на всасывание негемового железа у нормальных людей. J Nutr. 2006; 136: 576–81. [PubMed] [Google Scholar] 45. Бах Кристенсен М., Хелс О, Морберг С., Марвинг Дж., Бугель С., Тетенс I. Свинина увеличивает усвоение железа при 5-дневной полностью контролируемой диете по сравнению с вегетарианской диетой с аналогичным содержанием витамина С и фитиновой кислоты.Br J Nutr. 2005. 94: 78–83. [PubMed] [Google Scholar] 46. Харрелл Р.Ф., Джуллерат М.А., Редди М.Б., Линч С.Р., Дассенко С.А., Кук Дж.Д. Соевый белок, фитат и абсорбция железа у человека. Am J Clin Nutr. 1992; 56: 573–8. [PubMed] [Google Scholar] 47. Hurrell RF. Разложение фитиновой кислоты как средство улучшения усвоения железа. Int J Vitam Nutr Res. 2004. 74: 445–52. [PubMed] [Google Scholar] 48. Харрелл Р.Ф., Редди М., Кук Дж. Д.. Подавление абсорбции негемного железа у человека напитками, содержащими полифенолы. Br J Nutr.1999. 81: 289–95. [PubMed] [Google Scholar] 49. Холлберг Л., Россандер Л. Влияние различных напитков на усвоение негемового железа из сложных блюд. Hum Nutr Appl Nutr. 1982; 36: 116–23. [PubMed] [Google Scholar] 50. Hallberg L, Rossander-Hulthen L, Brune M, Gleerup A. Ингибирование усвоения гемового железа у человека кальцием. Br J Nutr. 1993; 69: 533–40. [PubMed] [Google Scholar] 51. Халлберг Л., Россандер-Хюльтен Л. Потребность в железе у менструирующих женщин. Am J Clin Nutr. 1991; 54: 1047–58. [PubMed] [Google Scholar] 52.Линч SR. Влияние кальция на усвоение железа. Nutr Res Rev.2000; 13: 141–58. [PubMed] [Google Scholar] 53. Повар JD, Monsen ER. Поглощение пищевого железа у людей. III. Сравнение влияния животных белков на всасывание негемового железа. Am J Clin Nutr. 1976; 29: 859–67. [PubMed] [Google Scholar] 54. Харрелл РФ, Линч С.Р., Тринидад Т.П., Дассенко С.А., Кук Дж.Д. Абсорбция железа у людей: бычий сывороточный альбумин по сравнению с говяжьими мышцами и яичным белком. Am J Clin Nutr. 1988; 47: 102–7. [PubMed] [Google Scholar] 55.Линч С.Р., Дассенко С.А., Кук Дж.Д., Джульерат М.А., Харрелл РФ. Ингибирующий эффект фрагмента, связанного с соевым белком, на абсорбцию железа у людей. Am J Clin Nutr. 1994; 60: 567–72. [PubMed] [Google Scholar] 56. Piomelli S, Seaman C, Kapoor S. Вызванные свинцом аномалии метаболизма порфирина, связь с дефицитом железа. Ann N Y Acad Sci. 1987; 514: 278–88. [PubMed] [Google Scholar] 58. 2-е изд. Бангкок: 2004 г. ФАО / ВОЗ. Консультации экспертов по потребностям человека в витаминах и минералах, потребностях в витаминах и минералах в питании человека: отчет совместного экспертного заключения ФАО / ВОЗ; п.341. [Google Scholar] 59. Cook JD, Skikne BS, Lynch SR, Reusser ME. Оценки достаточности железа у населения США. Кровь. 1986; 68: 726–31. [PubMed] [Google Scholar] 60. Ботвелл TH, Чарльтон RW. Общий подход к проблемам железодефицита и перегрузки железом у населения в целом. Semin Hematol. 1982; 19: 54–67. [PubMed] [Google Scholar] 61. Гибсон Р.С., Макдональд А.С., Смит-Вандеркой П.Д. Параметры сывороточного ферритина и пищевого железа в выборке канадских детей дошкольного возраста. J Can Dietetic Assoc.1988; 49: 23–8. [Google Scholar] 62. ДеМайер Э.М., Даллман П., Герни Дж. М., Холлберг Л., Суд С. К., Срикантия С. Г., редакторы. Женева: Всемирная организация здравоохранения; 1989. ВОЗ. Профилактика и контроль железодефицитной анемии с помощью первичной медико-санитарной помощи: руководство для администраторов здравоохранения и руководителей программ; п. 58. [Google Scholar] 63. Даллман П. Айрон. В: Браун М.Л., редактор. Настоящие знания в области питания. 6-е изд. Вашингтон, округ Колумбия: Фонд питания; 1990. С. 241–50. [Google Scholar] 64. Женева: Швейцария: Всемирная организация здравоохранения; 2001 г.ВОЗ / ЮНИСЕФ / УООН. Оценка, профилактика и контроль железодефицитной анемии; п. 114. [Google Scholar] 65. Борода Дж. Л., Коннор Дж. Р. Статус железа и нейронное функционирование. Annu Rev Nutr. 2003. 23: 41–58. [PubMed] [Google Scholar] 66. Failla ML. Микроэлементы и защита хозяина: последние достижения и сохраняющиеся проблемы. J Nutr. 2003; 133: S1443–7. [PubMed] [Google Scholar] 67. Витери Ф.Е., Торунь Б. Анемия и физическая работоспособность. В: Гарби Л., редактор. Клиники гематологии. Vol. 3. Лондон: У. Б. Сондерс; 1974. стр.609–26. [Google Scholar] 68. CDC. Табель успеваемости по грудному вскармливанию, США: показатели результатов (публикация из Центров по контролю и профилактике заболеваний, Национальное обследование иммунизации. 2010 г. [последний доступ 11 мая 2010 г.]. Http://www.cdc.gov/breastfeeding/data/index .htm .69. Купер Е.С., Банди Д.А. Трихоцефалопатия. Ballieres Clin Trop Med Commun Dis. 1987; 2: 629–43. [Google Scholar] 70. Всемирная организация здравоохранения, Женева; 1995. ВОЗ. Отчет неофициальной консультации ВОЗ. на анкилостомоз и анемию у девочек и женщин; с.46. [Google Scholar] 71. Crompton DW, Nesheim MC. Влияние кишечных гельминтозов на питание в течение жизненного цикла человека. Annu Rev Nutr. 2002; 22: 35–99. [PubMed] [Google Scholar] 72. Ларок Р., Касапиа М., Готуццо Е., Дьоркос Т.В. Взаимосвязь между интенсивностью заражения гельминтами, передающимися через почву, и анемией во время беременности. Am J Trop Med Hyg. 2005. 73: 783–9. [PubMed] [Google Scholar] 73. Циммерманн МБ, Харрелл РФ. Недостаток пищевого железа. Ланцет. 2007; 370: 115–20. [Google Scholar] 74. Харви LJ, Armah CN, Dainty JR, Foxall RJ, John Lewis D, Langford NJ и др.Влияние менструальной кровопотери и диеты на дефицит железа у женщин в Великобритании. Br J Nutr. 2005. 94: 557–64. [PubMed] [Google Scholar] 75. Борода JL. Потребность в железе у девочек-подростков. Симпозиум: Повышение уровня железа у подростков до деторождения. J Nutr. 2000; 130: S440–2. [PubMed] [Google Scholar] 77. Бегин Ю. Растворимый рецептор трансферрина для оценки эритропоэза и статуса железа. Clinica Chimica Acta. 2003. 329: 9–22. [PubMed] [Google Scholar] 79. Повар JD, Flowers CH, Skikne BS. Количественная оценка bodyiron.Кровь. 2003. 101: 3359–64. [PubMed] [Google Scholar] 80. Кук JD, Boy E, Flowers C, Daroca Mdel C. Влияние высокогорной жизни на железо тела. Кровь. 2005; 106: 1441–6. [PubMed] [Google Scholar] 81. Ян З., Дьюи К.Г., Лоннердал Б., Хернелл О., Чапарро С., Аду-Афарвуа С. и др. Сравнение концентрации ферритина в плазме с соотношением рецептора трансферрина в плазме к ферритину для оценки запасов железа в организме: результаты 4 интервенционных испытаний. Am J Clin Nutr. 2008; 87: 1892–8. [PubMed] [Google Scholar] 82.Де Бенуа Б., Маклин Э., Эгли И., Когсуэлл М. — редакторы. Женева: Пресса ВОЗ, Всемирная организация здравоохранения; 2008. ВОЗ / CDC. Данные библиотечной каталогизации в публикации. Распространенность анемии в мире, 1993–2005 гг .: глобальная база данных ВОЗ по анемии; п. 40. [Google Scholar] 83. Джонсон-Уимбли Т.Д., Грэм Д.Ю. Диагностика и лечение железодефицитной анемии в 21 веке. Ther Adv Гастроэнтерол. 2011; 4: 177–84. [Бесплатная статья PMC] [PubMed] [Google Scholar] 84. Зарычанский Р., Хьюстон Д.С. Анемия хронического заболевания: вредное заболевание или адаптивная, полезная реакция? Can Med Assoc J.2008. 179: 333–7. [Бесплатная статья PMC] [PubMed] [Google Scholar] 85. Weiss G, Goodnough LT. Анемия хронического заболевания. N Engl J Med. 2005; 352: 1011–23. [PubMed] [Google Scholar] 86. 2-е изд. Женева: 2004 г. ВОЗ / CDC. Отчет о совместной технической консультации Всемирной организации здравоохранения / Центров по контролю и профилактике заболеваний по оценке статуса железа на уровне населения; п. 108. [Google Scholar] 87. Knight K, Wade S, Balducci L. Распространенность и исходы анемии при раке: систематический обзор литературы.Am J Med. 2004; 116: 11–26С. [PubMed] [Google Scholar] 88. О’Мара NB. Больные анемией с хроническими заболеваниями почек. Спектр диабета. 2008; 21: 12–9. [Google Scholar] 89. Нурко С. Анемия при хронической болезни почек: причины, диагностика, лечение. Cleve Clin J Med. 2006. 73: 289–97. [PubMed] [Google Scholar] 90. Горовиц К.М., Ингардия С.Дж., Боргида А.Ф. 2013, Анемия при беременности. Clin Lab Med. 2013; 33: 281–91. [PubMed] [Google Scholar] 91. Ауск К.Дж., Иоанну Г.Н. Связано ли ожирение с анемией хронического заболевания? Популяционное исследование.Ожирение. 2008. 16: 2356–61. [PubMed] [Google Scholar] 92. Aeberli I, Hurrell RF, Zimmermann MB. Дети с избыточным весом имеют более высокие концентрации циркулирующего гепсидина и более низкий статус железа, но их потребление железа с пищей и биодоступность сопоставимы с детьми с нормальным весом. Int J Obes. 2009; 33: 1111–7. [PubMed] [Google Scholar] 94. Lewis G, Wise MP, Poynton C, Godkin A. Случай стойкой анемии и злоупотребления алкоголем. Нат Клин Практ Гастроэнтерол Гепатол. 2007; 4: 521–6. [PubMed] [Google Scholar] 95. Lindenbaum J, Роман MJ.Пищевая анемия при алкоголизме. Am J Clin Nutr. 1980; 33: 2727–35. [PubMed] [Google Scholar] 96. Cox SE, L’Esperance V, Makani J, Soka D, Prentice AM, Hill CM и др. Серповидно-клеточная анемия: доступность железа и ночная оксиметрия. J Clin Sleep Med. 2012; 8: 541–5. [Бесплатная статья PMC] [PubMed] [Google Scholar] 98. Манси Х.Л., младший, Кэмпбелл Дж. Альфа- и бета-талассемия. Я семейный врач. 2009; 80: 339–44. [PubMed] [Google Scholar] 99. Сегель ГБ, Лихтман М.А. Апластическая анемия: приобретенная и наследственная. В: Каушанский К., Вильямс В.Дж., редакторы.Гематология Вильямса. 8-е изд. Нью-Йорк: McGraw-Hill Medical; 2010. С. 569–90. [Google Scholar] 100. Янг Н.С., Каладо Р.Т., Шейнберг П. Современные концепции патофизиологии и лечения апластической анемии. Кровь. 2006; 108: 2509–19. [Бесплатная статья PMC] [PubMed] [Google Scholar] 101. Шейнберг П., Чен Дж. Апластическая анемия: что мы узнали на моделях на животных и в клинике. Semin Hematol. 2013; 50: 156–64. [PubMed] [Google Scholar] 102. Dhaliwal G, Cornett PA, Tierney LM., Jr Гемолитическая анемия.Я семейный врач. 2004; 69: 2599–606. [PubMed] [Google Scholar] 103. Hurrell RF. Как обеспечить адекватное усвоение железа из продуктов, обогащенных железом. Nutr Rev. 2002; 60: S7–15. [PubMed] [Google Scholar] 104. Повар JD. Диагностика и лечение железодефицитной анемии. Лучшая практика Res Clin Haematol. 2005; 18: 319–32. [PubMed] [Google Scholar] 105. Schlemmer U, Frølich W, Prieto RM, Grases F. Фитат в пищевых продуктах и значение для человека: источники пищи, потребление, обработка, биодоступность, защитная роль и анализ.Mol Nutr Food Res. 2009; 53: S330–75. [PubMed] [Google Scholar] 106. Лян Дж., Хан Б.З., Ноут М.Дж., Хамер Р.Дж. Влияние замачивания, прорастания и ферментации на общую фитиновую кислоту и растворимый цинк in vitro в коричневом рисе. Food Chem. 2008; 110: 821–8. [PubMed] [Google Scholar] 107. Кавалли-Сфорца Т., Бергер Дж., Смитасири С., Витери Ф. Еженедельное употребление добавок железа и фолиевой кислоты для женщин репродуктивного возраста: обзор воздействия, извлеченные уроки, планы расширения и вклад в достижение целей развития тысячелетия.Nutr Rev.2005; 63: S152–8. [PubMed] [Google Scholar] 109. Oppenheimer SJ. Железо и его отношение к иммунитету и инфекционным заболеваниям. J Nutr. 2001; 131: S616–33. [PubMed] [Google Scholar] 110. Sazawal S, Black RE, Ramsan M, Chwaya HM, Stoltzfus RJ, Dutta A и др. Влияние рутинных профилактических добавок с железом и фолиевой кислотой на госпитализацию и смертность детей дошкольного возраста в условиях высокой передачи малярии: рандомизированное плацебо-контролируемое исследование на уровне общины. Ланцет. 2006; 367: 133–43.[PubMed] [Google Scholar] 112. Hurrell RF. Обогащение железом: его эффективность и безопасность в отношении инфекций. Еда Nutr Bull. 2007. 28: 585–94. [PubMed] [Google Scholar] 114. Лукка П., Харрелл Р., Потрикус И. Борьба с железодефицитной анемией с помощью риса, богатого железом. J Am Coll Nutr. 2002; 21: 184С – 90. [PubMed] [Google Scholar] 115. Рухани Н., Харрелл Р., Келишади Р., Шулин Р. Цинк и его значение для здоровья человека: интегративный обзор. J Res Med Sci. 2013; 18: 144–57. [Бесплатная статья PMC] [PubMed] [Google Scholar]Роль железа в метаболизме энергии у животных
Железо необходимо для широкого спектра метаболических процессов в живых организмах из-за своего химического переходного свойства: оно имеет состояния как двухвалентного (Fe2 +), так и трехвалентного (Fe3 +), которые могут отдавать и принимать электроны соответственно.Железо присутствует в различных формах гема и железо-серы (Fe-S) …
Железо необходимо для широкого спектра метаболических процессов в живых организмах из-за своего химического переходного свойства: оно имеет состояния как двухвалентного (Fe2 +), так и трехвалентного (Fe3 +), которые могут отдавать и принимать электроны соответственно. Железо присутствует в различных формах гема и кластерного белка, связывающего железо-серу (Fe-S), который играет важную роль в различных ферментативных реакциях, таких как аэробное дыхание, функция цикла TCA и синтез ДНК, а также транспорт кислорода и место хранения.
2,7 миллиарда лет назад появление фотосинтезирующих организмов сделало возможным последующую эволюцию систем, которые используют глюкозу и производят АТФ путем окислительного фосфорилирования с использованием ранее существовавшего гликолитического пути. Следовательно, эту эволюцию следует рассматривать как поворотное событие. Однако нарушение транспорта электронов приводит к образованию активных форм кислорода (АФК), поэтому живые организмы разработали антиоксидантные механизмы против АФК с помощью эффективных поглотителей, таких как витамины С и Е, или ферментативной реакции каталазы, супероксиддисмутазы, глутатионпероксидазы и т. Д.Хотя железо жестко контролируется, избыток свободного железа (Fe2 +) ухудшает окислительный стресс, производя наиболее токсичный гидроксильный радикал по реакции Фентона.
В этой теме исследования мы ищем статьи, в которых рассматриваются следующие аспекты роли железа в энергетическом метаболизме животных:
• клеточный и митохондриальный метаболизм железа
• окислительный стресс
• наследственные нарушения метаболизма железа
• перекрестный диалог между железом метаболизм и метаболические заболевания, такие как диабет и липидоз
Ключевые слова : электронная транспортная система, железо, митохондрии, окислительный стресс, окислительное фосфорилирование
Важное примечание : Все материалы по данной теме исследования должны находиться в рамках того раздела и журнала, в который они были отправлены, как это определено в их заявлениях о миссии.Frontiers оставляет за собой право направить рукопись за пределами области охвата в более подходящий раздел или журнал на любом этапе рецензирования.
Гемоглобин и функции железа | Обучение пациентов
Железо — важный элемент для производства крови. Около 70 процентов железа в вашем организме содержится в красных кровяных тельцах вашей крови, называемых гемоглобином, и в мышечных клетках, называемых миоглобином. Гемоглобин необходим для переноса кислорода в крови от легких к тканям.Миоглобин в мышечных клетках принимает, хранит, транспортирует и выделяет кислород.
Около 6 процентов железа в организме является компонентом определенных белков, необходимых для дыхания и энергетического обмена, а также как компонент ферментов, участвующих в синтезе коллагена и некоторых нейротрансмиттеров. Железо также необходимо для правильной работы иммунной системы.
Около 25 процентов железа в организме хранится в виде ферритина, содержится в клетках и циркулирует в крови. Средний взрослый мужчина имеет около 1000 мг запасенного железа (достаточно примерно на три года), тогда как женщины в среднем имеют только около 300 мг (достаточно примерно на шесть месяцев).Когда потребление железа хронически низкое, запасы железа могут истощаться, что снижает уровень гемоглобина.
Когда запасы железа истощены, это состояние называется истощением запасов железа. Дальнейшее снижение может быть названо железодефицитным эритропоэзом, и дальнейшее снижение вызывает железодефицитную анемию.
Кровопотеря — наиболее частая причина дефицита железа. У мужчин и женщин в постменопаузе дефицит железа почти всегда является результатом желудочно-кишечной кровопотери. У менструирующих женщин потеря крови из мочеполовой системы часто является причиной повышенной потребности в железе.Оральные контрацептивы, как правило, уменьшают менструальную кровопотерю, в то время как внутриматочные средства имеют тенденцию увеличивать менструальное кровотечение. Другие причины мочеполовых кровотечений и кровотечений из дыхательных путей также увеличивают потребность в железе.
Для доноров крови каждая сдача крови приводит к потере от 200 до 250 мг железа. В периоды роста в младенчестве, детстве и подростковом возрасте потребности в железе могут превышать поступление железа из рациона и запасов. Потеря железа из-за роста тканей во время беременности и из-за кровотечений во время родов и в послеродовом периоде составляет в среднем 740 мг.Грудное вскармливание увеличивает потребность в железе примерно на 0,5–1 мг в день.
Требования к железу
Ваш «уровень железа» проверяется перед каждой сдачей крови, чтобы определить, безопасно ли для вас сдавать кровь. Железо не вырабатывается в организме и должно усваиваться из того, что вы едите. Минимальная суточная потребность взрослого человека в железе составляет 1,8 мг. Только от 10 до 30 процентов потребляемого вами железа усваивается и используется организмом.
Суточная потребность в железе может быть достигнута путем приема добавок железа.Сульфат железа 325 мг перорально один раз в день и с пищей с высоким содержанием железа. Также рекомендуются продукты с высоким содержанием витамина С, потому что витамин С помогает организму усваивать железо. Приготовление пищи в чугунных кастрюлях может добавить к пище до 80 процентов больше железа. Перед приемом добавок железа проконсультируйтесь с вашим лечащим врачом.
Читать далееНекоторые продукты, богатые железом, включают:
Мясо и птица
- Постная говядина
- Телятина
- Свинина
- Баранина
- Курица
- Турция
- Печень (кроме печени рыбы)
Морепродукты
Овощи
- Зелень всякая
- Тофу
- Брокколи
- Душистый горошек
- Брюссельская капуста
- Кале
- Ростки фасоли
- Помидоры
- Лимская фасоль
- Картофель
- Зеленая фасоль
- Кукуруза
- Свекла
- Капуста
Железо — Физиопедия
Железо является важным элементом почти для всех живых организмов, поскольку оно участвует в широком спектре метаболических процессов, включая транспорт кислорода, синтез дезоксирибонуклеиновой кислоты (ДНК) и транспорт электронов.Однако, поскольку железо может образовывать свободные радикалы, его концентрацию в тканях организма необходимо строго регулировать, поскольку в чрезмерных количествах оно может привести к повреждению тканей.
Железо отвечает за производство гемоглобина, белка, который позволяет эритроцитам (изображение на R эритроцит) переносить кислород в каждую часть вашего тела. Это также компонент миоглобина, который похож на гемоглобин, но содержится в мышечных клетках. Низкий уровень железа в организме снижает выработку красных кровяных телец, что сказывается на здоровье.
Нарушения обмена железа являются одними из наиболее распространенных заболеваний человека и включают широкий спектр заболеваний с различными клиническими проявлениями, включая:
Железо — важный элемент для производства крови.
- В живом организме железо в свободном доступе нет. Основная часть металла заключена в ферритине, гемосидерине, миоглобине и в гемоглобине красных кровяных телец. Связывающие железо белки, трансферрин и лактоферрин, которые содержат лишь незначительную долю железа в организме, обычно только частично насыщены Fe и имеют исключительно высокую константу ассоциации, составляющую около 10 36 для металла. [3]
- Около 70 процентов железа в вашем организме содержится в красных кровяных тельцах, гемоглобине и в мышечных клетках, называемых миоглобином. Гемоглобин необходим для переноса кислорода в крови от легких к тканям. Миоглобин в мышечных клетках принимает, хранит, транспортирует и выделяет кислород.
- Около 6 процентов железа в организме является компонентом определенных белков, необходимых для дыхания и энергетического обмена, а также как компонент ферментов, участвующих в синтезе коллагена и некоторых нейротрансмиттеров.Железо также необходимо для правильной работы иммунной системы.
- Около 25 процентов железа в организме хранится в виде ферритина, содержится в клетках и циркулирует в крови. Средний взрослый мужчина имеет около 1000 мг запасенного железа (достаточно примерно на три года), тогда как женщины в среднем имеют только около 300 мг (достаточно примерно на шесть месяцев). Когда потребление железа хронически низкое, запасы железа могут истощаться, что снижает уровень гемоглобина.
Когда запасы железа истощены, это состояние называется истощением железа.Дальнейшее снижение может быть названо железодефицитным эритропоэзом, и дальнейшее снижение вызывает железодефицитную анемию. [4]
Железо — это питательное вещество, которое помогает крови перемещать кислород от легких к остальным частям тела, а также помогает мышцам накапливать и использовать кислород.
Низкий уровень железа может повлиять на:
- Уровни энергии
- Концентрация
- Память
- Успеваемость на работе / в школе
- Когнитивное развитие
- Потенциал обучения и заработка [5]
По оценкам Всемирной организации здравоохранения (ВОЗ), два миллиарда человек во всем мире страдают анемией, и примерно 50% всех анемий объясняется дефицитом железа.Это происходит на всех этапах жизненного цикла, но чаще встречается у беременных женщин и маленьких детей. Анемия является результатом множества причин, которые можно изолировать, но чаще всего они сосуществуют.
Неорганическое железо необходимо для синтеза гемоглобина и транспорта кислорода. Низкое потребление железа и / или его биодоступность являются причиной
- Большинство анемий в промышленно развитых странах;
- В развивающихся странах на их долю приходится лишь около половины случаев анемии; инфекционные и воспалительные заболевания (особенно малярия), кровопотеря от паразитарных инфекций и дефицит других питательных веществ (витамина A, рибофлавина, фолиевой кислоты и витамина B12) составляют остальные 50% анемий [2] .
Пищевое железо встречается в двух формах: гемовой и негемовой.
- Основными источниками гемового железа являются гемоглобин и миоглобин из мяса, птицы и рыбы. Гемовое железо обладает высокой биодоступностью (15-35%), и диетические факторы мало влияют на его абсорбцию, тогда как абсорбция негемового железа намного ниже (2-20%) и сильно зависит от присутствия других пищевых компонентов.
- Негемовое железо получают из зерновых, бобовых, бобовых, фруктов и овощей.Количество негемового железа в рационе во много раз превышает количество гемового железа в большинстве приемов пищи, поэтому, несмотря на его более низкую биодоступность, негемовое железо обычно вносит больший вклад в питание железом, чем гемовое железо.
Биодоступность
- Основными ингибиторами абсорбции железа являются фитиновая кислота (природный антиоксидант, который в основном содержится в зернах, орехах и семенах) [6] , полифенолы, кальций и пептиды из частично переваренных белков.
- Усилители — мышечная ткань и аскорбиновая кислота. [2] то есть витамин С.Для увеличения усвоения железа есть следующие варианты: поливать пищу лимонным соком; салаты, содержащие источники с высоким содержанием витамина С, такие как красный перец или помидоры; киви, клубника, папайя или стакан свежевыжатого апельсинового сока; смешивание молодого шпината в салатах — зеленые листовые овощи содержат железо и витамин С.
Обратите внимание на то, что абсорбция негемного железа значительно варьируется и, как было показано, выше у людей, которые имеют повышенную потребность в железе. Это говорит о том, что организм адаптируется к низкому уровню железа, увеличивая его абсорбцию [7] .
Исследования конкуренции показывают, что некоторые другие тяжелые металлы могут участвовать в пути всасывания железа в кишечнике. например, свинец, марганец, кобальт и цинк. Поскольку дефицит железа часто сочетается с интоксикацией свинцом, это взаимодействие может вызывать особенно серьезные медицинские осложнения у детей [2] .
Некоторые продукты, богатые железом, включают:
- Печень и другие субпродукты
- Моллюски — такие как устрицы, моллюски, мидии
- Стейк и другое красное мясо
- Цыпленок, индейка, утка и другая домашняя птица
- Тофу
- Темные листовые овощи (шпинат, капуста)
- Бобовые, такие как нут, чечевица, соя, фасоль
- Орехи и семена, особенно тыквенные
- Киноа [5]
Диетические потребности в железе зависят от возраста и пола.Рекомендуемая суточная доза (средняя дневная доза, достаточная для удовлетворения потребностей большинства людей) для мужчин варьируется от восьми до 11 миллиграммов в день для детей в возрасте от 1 до 18 лет и восьми миллиграммов для всех остальных возрастов.
У женщин более высокие требования. Для детей от 14 до 50 лет рекомендуемая суточная доза составляет от 15 миллиграммов (от 14 до 18 лет) до 18 миллиграммов в день. Потребности выше во время беременности, увеличиваясь до 27 миллиграммов в день. Однако во время лактации их немного меньше, от девяти до десяти миллиграммов в день.
Потребность в железе для вегетарианцев оценивается в 1,8 раза больше, чем для невегетарианцев (на основе ограниченного исследования) [7] .
В ответ на системную бактериальную инфекцию иммунная система инициирует процесс, известный как удержание железа (приводящий к гипоферемии). Если бактерии хотят выжить, они должны получать железо из окружающей среды.
- Во время бактериальной инфекции патоген и хозяин конкурируют за железо (Fe). Воспалительная реакция, связанная с инфекцией, перемещает Fe из кровотока в запасы, что приводит к гипоферемии и железодефицитному эритропоэзу и, в конечном итоге, способствует анемии, вызванной воспалением.
- Бактерии для приобретения Fe используют как мембраносвязанные рецепторы трансферрина, так и высокоаффинные железосвязывающие белки, называемые сидерофорами.
- Люди используют железосвязывающие белки лактоферрин, трансферрин и ферритин для перемещения Fe из мест инфекции в хранилище. Синтез и действие этих белков регулируются воспалительными цитокинами.
- Люди реагируют на инфекцию гипоферремией, вызванной воспалительными цитокинами. [8]
Дефицит железа очень распространен у людей и животных.Низкие концентрации железа в сыворотке (гипоферремия), вызванные гормоном гепсидином, подавляют реакцию организма на вакцины и инфекции; наоборот, увеличение количества железа может повысить иммунитет [9] .
- Гепсидин — это циркулирующий пептидный гормон, секретируемый печенью, который играет центральную роль в регуляции гомеостаза железа. Это главный регулятор системного гомеостаза железа, координирующий использование и хранение железа с приобретением железа. Этот гормон в основном вырабатывается гепатоцитами и является негативным регулятором поступления железа в плазму. [2]
Уровень железа в мозге и организме резко повышается до 30 лет из-за метаболических потребностей в процессе роста и остается стабильным в зрелом возрасте. Однако в стареющем головном мозге наблюдается регионально-специфическое увеличение общего железа, вероятно, вызванное воспалением, повышением проницаемости гематоэнцефалического барьера (ГЭБ), перераспределением железа в головном мозге и изменениями гомеостаза железа, а также наблюдается самый высокий уровень железа в мозге. базальный ганглий.
Железный дисгомеостаз может вызывать повреждение нейронов в чувствительных к железу областях мозга.Нейродегенерация с накоплением железа в мозге отражает группу нарушений, вызванных перегрузкой железом в базальных ганглиях. Высокие уровни железа и связанные с железом патогенные триггеры также участвуют в спорадических нейродегенеративных заболеваниях, включая болезнь Альцгеймера (БА), болезнь Паркинсона (БП) и множественную системную атрофию (МСА). Железо-индуцированный дисомеостаз в уязвимых областях мозга все еще недостаточно изучен [2]
- ↑ Границы неврологии.1 марта 2019 г .; 13: 180. Доступно по адресу: https://www.frontiersin.org/articles/10.3389/fnins.2019.00180/full (дата обращения 13.3.2021)
- ↑ 2,0 2,1 2,2 2,3 2,4 2,5 Аббаспур Н., Харрелл Р., Келишади Р. Обзор железа и его значения для здоровья человека. Журнал исследований в области медицинских наук: официальный журнал Исфаханского университета медицинских наук. 2014 февраль; 19 (2): 164. Доступно по адресу: https: //www.ncbi.nlm.nih.gov/pmc/articles/PMC3999603/ (дата обращения 4.3.2021)
- ↑ Буллен Дж. Дж., Роджерс Х. Дж., Гриффитс Э. Роль железа в бактериальной инфекции. Актуальные темы микробиологии и иммунологии. 1978: 1-35. Доступно по адресу: https: //link.springer.com/chapter/10.1007%2F978-3-642-66956-9_1 (дата обращения: 5.3.2021)
- ↑ https://www.ucsfhealth.org/education/hemoglobin-and-functions-of-iron
- ↑ 5,0 5,1 Lucky Fish Факты о железе Доступно по ссылке: https://luckyironfish.com/pages/iron-101 (дата обращения: 4.3.2021)
- ↑ Очень хорошее здоровье Фитиновая кислота Доступно по: https: // www.verywellhealth.com/phytic-acid-5088824 (дата обращения: 4.3.2021)
- ↑ 7,0 7,1 Разговор Почему железо является такой важной частью вашего рациона Доступно по ссылке: https://theconversation.com/why-iron-is-such-an-important-part-of-your-diet -69974 (дата обращения: 4.3.2021)
- ↑ Pieracci FM, Barie PS. Железо и риск заражения. Хирургические инфекции. 2005 1 июня; 6 (S1): s41-6. Доступно по адресу: https://pubmed.ncbi.nlm.nih.gov/19284357/ (дата обращения: 5.3.2021)
- ↑ Frost JN, Tan TK, Abbas M, Wideman SK, Bonadonna M, Stoffel NU, Wray K, Kronsteiner B, Smits G, Campagna DR, Duarte TL.Гепсидин-опосредованная гипоферремия нарушает иммунный ответ на вакцинацию и инфекцию. Med. 2020, 19 ноября, доступно по ссылке: https://www.cell.com/med/fulltext/S2666-6340(20)30021-0 (дата обращения: 5.3.2021)
Железо и паразиты
В этом специальном выпуске мы анализируем важность железа во взаимодействии паразита и хозяина. Железо — переходный элемент и четвертый по распространенности элемент в земной коре. Железо жизненно важно для роста почти всех живых организмов, от прокариот до человека.Железо играет важную роль в нескольких клеточных процессах, таких как дыхание, фотосинтез, транспорт кислорода и синтез ДНК. Железо необходимо, но его биодоступность нелегкая; Растворимость трехвалентного железа низкая при физиологическом pH, тогда как двухвалентное железо в аэробной среде очень токсично. Следовательно, железо обычно связано с белками, и концентрация железа в организме и в клетках должна регулироваться у всех организмов.
Некоторые железосодержащие и связывающие железо белки являются внутриклеточными, например гемоглобин, переносящий кислород, ферритин, запасающий железо, и многочисленные ферменты.Другие — внеклеточные, в основном трансферрин (Tf) и лактоферрин (Lf). Tf и Lf способны захватывать до двух атомов Fe 3+ на молекулу, поддерживая железо в растворимой и стабильной степени окисления в жидкостях и избегая образования токсичных свободных радикалов, полученных из Fe 2+ в результате реакции Фентона. Свободные радикалы вредны для большинства макромолекул. Tf и Lf поддерживают слишком низкую концентрацию свободного железа для поддержания роста паразитов. Tf — переносчик железа, который обеспечивает поглощение клеточного железа; в основном он содержится в сыворотке и лимфе.Lf секретируется в слизистые оболочки и вторичными гранулами нейтрофилов для хелатирования Fe 3+ и предотвращения его доступности для паразитов.
Следовательно, во время заражения между хозяином и захватчиком идет постоянная битва за железо, в которой захватчик пытается получить доступ к железу хоста, а хозяин устраивает сложные механизмы удержания железа, чтобы помешать воровству железа. Фактически, все железосодержащие белки у эукариот могут использоваться в качестве источников железа паразитами, ищущими железо; для этого паразиты разработали несколько сложных стратегий получения железа хозяина.Таким образом, захват и поглощение железа хозяина паразитами считается детерминантами вирулентности.
Сообщалось мало информации о поступлении железа у свободноживущих амеб. В исследовательской статье «Разложение железосвязывающего белка цистеиновыми протеазами Naegleria fowleri » M. Martínez-Castillo et al. сообщают о расщеплении человеческого хололактоферрина, гемоглобина и голотрансферрина этим паразитом. N. fowleri вызывает первичный амебный менингоэнцефалит.Во время инвазии микроорганизм взаимодействует с различными тканями, такими как обонятельный нейроэпителий и обонятельные луковицы, содержащие железосвязывающие белки. Результаты показывают, что у этого простейшего есть несколько протеаз, секретируемых цистеином, которые расщепляют железосвязывающие белки. Используя эту стратегию, N. fowleri может получать железо от хозяина в пораженных тканях.
G. Ortíz-Estrada et al. рассмотреть вопрос о возможном способе доступа кишечного паразита человека Entamoeba histolytica к бычьему лактоферрину, белку, присутствующему в молоке, в основном потребляемом младенцами и младенцами, вскармливаемыми смесями.В своей исследовательской статье «Связывание и эндоцитоз бычьего хололактоферрина паразитом Entamoeba histolytica » авторы сравнивают вирулентные трофозоиты, недавно выделенные из абсцессов печени хомяков, с невирулентными трофозоитами, сохраняемыми более 30 лет в культурах in vitro , относительно их взаимодействия. с бычьим железом Lf (B-holo-Lf). Интересно, что хотя оба варианта амеб могут использовать B-holo-Lf в качестве источника железа и эндоцитозировать этот гликопротеин через покрытые клатрином везикулы, приобретение железа, параметры связывания и количество сайтов связывания с белками на амебу различны.Кроме того, вирулентные амебы также эндоцитировали B-holo-Lf посредством холестерин-зависимого механизма; таким образом, эндоцитоз B-холо-Lf более эффективен у вирулентных амеб.
В мини-обзорной статье «Стратегии внутриклеточных патогенов для получения железа из окружающей среды» N. Leon-Sicairos et al. сосредоточиться на том, как внутриклеточные патогены используют несколько подходов для получения питательного железа из внутриклеточной среды, чтобы использовать этот элемент для репликации. Они исследуют текущие знания о процессе, который происходит во время заражения внутриклеточными патогенами, когда железо требуется как клетке-хозяину, так и патогену, который ее населяет.Внутриклеточные микроорганизмы разрушаются тканями хозяина посредством процессов, которые обычно включают фагоцитоз и разрушение лизосом. Однако некоторые внутриклеточные патогены способны избежать разрушения за счет роста внутри макрофагов и других клеток. Кроме того, обсуждаются последствия этих механизмов для приобретения железа во взаимоотношениях хозяин-патоген.
Африканский трипаносомоз вызывается паразитическими простейшими Trypanosoma brucei . Это хроническое и изнурительное заболевание, от которого страдают в основном жители развивающихся стран.В обзоре «Гомеостаз железа и развитие ассоциированной иммунопатогенности Trypanosoma brucei : битва / поиски железа» B. Stijlemans et al. проанализировать различные стратегии, которые приводят к иммунному ответу хозяина, который приводит к депривации железа, заключающейся в модуляции железом миелоидной фагоцитарной системы хозяина, которая влияет на развитие анемии, связанной с трипаносомозом.
Обзорная статья Р.Arroyo et al. фокусируется на реакции железа Trichomonas vaginalis на продукты семейства генов, такие как цистеиновые протеиназы (CP), участвующие в свойствах вирулентности. В частности, исследуется влияние железа на регуляцию экспрессии генов и функцию L-подобных катепсину и аспарагинилэндопептидазоподобных CP как факторов вирулентности. Аспекты, касающиеся геномной организации CPs, адресованы, чтобы предложить возможные объяснения того факта, что только несколько членов этого большого семейства генов экспрессируются на уровнях РНК и белка.Также предлагаются возможные способы контроля этих конкретных протеолитических активностей. Более того, все известные механизмы регуляции железа CPs на транскрипционном, посттранскрипционном и посттрансляционном уровнях наряду с новым пониманием возможных эпигенетических и miRNA процессов у T. vaginalis также суммированы.
Наконец, в обзорной статье М. Рейес-Лопеса и др. «Трансферрин: эндоцитоз и передача клеточных сигналов у паразитических простейших» авторы описывают наличие специфических рецепторов к Tf у простейших паразитов.Передача сигнала, инициированная связыванием лиганда на плазматической мембране паразита, с процессом в клетках млекопитающих сравнивается на основании большого количества информации об эндоцитозе Tf. В транспортировке Tf участвуют несколько сигнальных путей, таких как встраивание мембранных везикул, и сигнальные пути, опосредованные инозитол-1,4,5-трифосфатом и диацилглицерином, MAPK или факторами роста. Включены некоторые компоненты этих путей, также обнаруженные у паразитов, а также идентификация сигнальных белков, полезных при изучении основных факторов паразитарной жизни и в качестве потенциальных мишеней для разработки химиотерапевтических подходов.
Мы надеемся, что исследователи получат удовольствие от чтения этого специального выпуска, посвященного паразитам и одному из важнейших химических элементов — железу. Несомненно, приобретение хозяина железа патогеном является решающим шагом во время развития инфекции и определяет ее исход.
Rossana Arroyo
Theresa Ochoa
Jung-Hsiang Tai
Mireya de la Garza
Авторские права
Авторские права © 2015 Rossana Arroyo et al. Это статья в открытом доступе, распространяемая по лицензии Creative Commons Attribution License, которая разрешает неограниченное использование, распространение и воспроизведение на любом носителе при условии правильного цитирования оригинальной работы.
Железо: биологический элемент?
Изучая железо, извлеченное из кернов, пробуренных в породах, подобных этим в национальном парке Кариджини, Западная Австралия, исследователи из UW-Madison определили, что половина атомов железа возникла в мелководных океанах после того, как они были обработаны микробами 2,5 миллиарда лет назад.
Фото: Кларк Джонсон
Представьте себе железный предмет: двутавровую балку, раму автомобиля, гвоздь. А теперь представьте, что половина железа в этом объекте обязана своим существованием бактериям, жившим два с половиной миллиарда лет назад.
Это результат исследования, опубликованного на этой неделе в Proceedings of the National Academy of Sciences (PNAS). Результаты имеют значение для таких разнообразных областей, как добыча полезных ископаемых и поиск жизни в космосе.
Кларк Джонсон, профессор геолого-геофизических исследований Университета Висконсин-Мэдисон и бывший научный сотрудник Вэйцян Ли исследовали образцы из полосчатого железного пласта в Западной Австралии. Полосчатое железо — это богатая железом порода, обнаруженная в рудных месторождениях по всему миру, от предполагаемого железного рудника в Северном Висконсине до огромных рудников Западной Австралии.
Эти древние отложения глубиной до 150 метров требовали объяснений, — говорит Джонсон.
Кларк Джонсон
Ученые думали, что железо попало в океан из горячей, богатой минералами воды, выпущенной из отверстий в середине океана, которая затем осаждалась на дно океана. Джонсон и Ли, которые в настоящее время работают в Нанкинском университете в Китае, показывают, что половина железа, содержащегося в полосчатом железе, метаболизировалась древними бактериями, живущими вдоль континентальных шельфов.
Считалось, что полосатость представляет собой своего рода сезонные изменения.Исследователи UW-Madison обнаружили долгосрочные колебания в составе, но не изменения за более короткие периоды, такие как десятилетия или столетия.
Исследование началось с точных измерений изотопов железа и неодима с помощью одного из самых быстрых в мире лазеров, размещенного в геолого-геофизическом отделении UW – Madison. (Изотопы, формы атома, которые различаются только по весу, часто используются для «отпечатка пальца» источника различных образцов.)
Вспышки света длиной менее одной триллионной секунды испаряют тонкие срезы образца без нагревания самого образца.«Это все равно, что взять шарик мороженого и быстро вытащить материал, прежде чем он нагреется», — объясняет Джонсон. «Нагревание традиционными лазерами дало ложные результаты».
«Потребовалось три года, чтобы усовершенствовать работу лазера и связанных с ним масс-спектрометрических приборов», — говорит Ли. Ученый из Мэдисона и соавтор Брайан Бирд руководил разработкой лазерных методов.
Пластинчатые железные образования являются основным источником железной руды во всем мире. Эти породы в государственном парке подземных рудников Судана, Миннесота, показывают полосчатость, вызванную слоями различных минералов в образце 2.7 миллиардов лет.
Предыдущие исследования источника полосатого железа были сосредоточены на изотопах железа. «Были споры о том, что изотопы железа говорят нам об источнике», — говорит Ли. «Добавление неодима изменило эту картину и дало нам независимую оценку количества, поступающего из неглубоких континентальных вод, несущих изотопную сигнатуру жизни».
Идея о том, что организм может усваивать железо, сегодня может показаться странной, но 2,5 миллиарда лет назад Земля была совсем другой.При небольшом количестве кислорода в атмосфере многие организмы получали энергию, метаболизируя железо вместо кислорода.
Биологи говорят, что этот процесс «действительно глубоко укоренился в древе жизни, но до сих пор у нас было мало свидетельств из летописи горных пород», — говорит Джонсон. «Эти древние микробы дышали железом, как мы дышим кислородом. Признаюсь, это сложно осмыслить.
По словам Джонсона, текущее исследование важно по нескольким причинам. «Если вы геолог-разведчик, вы хотите знать источник полезных ископаемых, чтобы знать, где их исследовать.”
«Если вы когда-нибудь задумывались, почему мы объединяем обучение и исследования в этом университете, геомикробиология даст вам ответ. Он полностью перевернул науку о Земле ».
Кларк Джонсон
Исследование также проясняет эволюцию нашей планеты — и самой жизни — в «богатую железом» эпоху 2,5 миллиарда лет назад. «Какие остатки богатого железом мира остаются в нашем метаболизме?» — спрашивает Джонсон. «Не случайно, что железо является важной частью жизни, что ранние биологические молекулы могли быть основаны на железе.”
НАСА сделало поиск жизни в космосе основным направлением деятельности и спонсирует Институт астробиологии Университета штата Вашингтон в Мэдисоне, которым руководит Джонсон. Распознавание незнакомых форм жизни — приоритетная задача космического агентства.
Исследование подчеркивает важность микробов в геологии. «Это огромное изменение», — говорит Джонсон. «В моем вводном учебнике геохимии от 1980 года нет упоминания о биологии, и поэтому каждая диаграмма, показывающая, какие минералы стабильны в каких условиях на поверхности Земли, абсолютно неверна.”
Результаты подобных исследований влияют на то, как проводятся занятия, говорит Джонсон. «Если бы я только учил одному и тому же, я бы учил абсолютно неправильным вещам. Если вы когда-нибудь задумывались, почему мы совмещаем обучение и исследования в этом университете, геомикробиология даст вам ответ.