Железо в организме: зачем оно нужно и как его получить
В организме часто бывает дефицит железа. Это связано с низкой биодоступностью железа — при контакте с кислородом железо образует оксиды, которые слабо растворимы и поэтому сложно доступны для поглощения организмом.
Причины дефицита железа
Дефицит железа возникает в результате истощения запасов железа, когда абсорбция железа в течение длительного периода не успевает за метаболическими потребностями в железе, или происходит резкая потеря железа, связанная с кровопотерей.
Основные причины дефицита железа:
- обильные менструальные или маточные кровопотери,
- кровопотери при хирургических вмешательствах,
- приtм антикоагулянтов или антиагрегантов,
- частое донорство,
- вегетарианство и анорексия,
- хронические заболевания с нарушением всасывания железа (различные гастро-энтерологические патологии, хроническая сердечная, почечная недостаточность).

Группа риска — беременные женщины, недоношенные и дети в периоды интенсивного роста, женщины с обильными месячными и вегетарианцы. Очень часто дефицит железа встречается у девочек-подростков, потому что менструальные потери железа накладываются на потребность в быстром росте.
Когда запасов железа в организме недостаточно, синтез гемоглобина нарушается, и появляются симптомы дефицита железа и анемии.
Наиболее частые симптомы дефицита железа или анемии
- усталость и недостаток энергии,
- одышка при обычной нагрузке,
- заметное сердцебиение (учащенное сердцебиение),
- бледная кожа, десны и слизистая рта.
Менее распространенные симптомы
- трудности с концентрацией внимания,
- необычные вкусовые пристрастия (желание грызть лед, есть мел, клей или землю),
- сильная сухость во рту, трещины в уголках рта и сглаженный язык,
- головная боль и ухудшение памяти,
- непереносимость холода (постоянно холодные руки и ноги),
- снижение иммунитета,
- легко возникающие синяки и кровоизлияния на коже,
- сухость кожи, ломкость ногтей и выпадение волос,
- синдром беспокойных ног.

Последствия дефицита железа
Дефицит железа — это снижение уровня железа в организме при сохранении нормальной концентрации гемоглобина, когда уровень его все еще достаточен для производства эритроцитов, но другие органы и ткани страдают от недостатка железа.
Если не восполнить запасы, то развивается более тяжелое заболевание — железодефицитная анемия. Это состояние, когда железа недостаточно для формирования гемоглобина в эритроцитах, снижается его уровень и количество переносимого кислорода, а значит возникает кислородное голодание тканей всего организма.
По статистике Всемирной организации здравоохранения, анемию имеют треть женщин детородного возраста, а также 42% детей до пяти лет.
Чем меньше железа, тем ниже концентрация гемоглобина в эритроците, тем тяжелее анемия и гипоксия. Даже легкие и умеренные формы анемии могут быть связаны с функциональными нарушениями, влияющими на когнитивное развитие, механизмы иммунитета, способность к обучению и работоспособность.
Риски дефицита железа во время беременности
Дефицит железа опасен во время беременности — возрастает потребность самого организма матери и растет плод — железодефицитная анемия быстро усугубляется.
Риски для женщины:
- недоразвитие плаценты,
- самопроизвольный аборт,
- преждевременные роды,
- вероятность развития тяжелых послеродовых кровотечений.
Риски для ребенка:
- внутриутробная задержка развития плода,
- высокий риск внутриутробной смерти,
- рождение с низкой массой тела или недоношенностью,
- задержка нейрокогнитивного развития после рождения (отстают в развитии и способности к обучению).
Железо | Tervisliku toitumise informatsioon
Железо в организме человека встречается только в связанной, растворимой и нетоксичной форме. Свободное железо для человеческого организма опасно, поскольку оно быстро окисляется до труднорастворимых вредных веществ.
Железо необходимо:
- для кроветворения, где оно используется в синтезе гемо- и миоглобина. Железо играет ключевую роль в связывании и транспорте в составе гемоглобина необходимого для жизни кислорода, в т.ч. оно участвует в доставке кислорода из легких в ткани,
- в составе таких биомолекул, которые участвуют в синтезе АТФ (аденозинтрифосфата, играющего роль оперативного переносчика энергии в клетках) и помогают обезвреживать попавшие в организм чужеродные соединения, повышая таким образом его сопротивляемость стрессу и заболеваниям,
- для уменьшения усталости и поддержания нормального цвета кожи.
Железо встречается как в растительной, так и в животной пище. Железо из животной пищи, например из мяса, усваивается организмом на 15–35 %, а из растительной, например из зерновых, – на 2–20 %, причем в последнем случае велика роль витамина С. Длительный дефицит доступного железа – наиболее распространенная причина анемии. Состав продукта оказывает влияние на то, как усваивается входящее в него железо. Степень усвояемости увеличивается, если в повседневном рационе присутствуют мясо и рыба, а также достаточно витамина С. Усвояемость падает, если человек ест такие продукты (например, шпинат или ревень), в которых наличествуют оксалаты, фитиновая кислота и некоторые другие органические кислоты.
Степень усвояемости увеличивается, если в повседневном рационе присутствуют мясо и рыба, а также достаточно витамина С. Усвояемость падает, если человек ест такие продукты (например, шпинат или ревень), в которых наличествуют оксалаты, фитиновая кислота и некоторые другие органические кислоты.
Дефицит железа может возникнуть:
- при большой кровопотере,
- у беременных,
- у недоношенных детей или детей с низкой массой тела,
- у грудных детей и маленьких детей,
- у девочек-подростков,
- у вегетарианцев,
- при заболевании органов пищеварения.
Чрезмерное употребление железа в течение длительного времени, главным образом в виде биоактивных добавок, может быть вредно для организма. Избыток железа приводит к глубокому оксидативному стрессу, который является причиной многих заболеваний. Избыток железа угрожает прежде всего взрослым мужчинам и женщинам в постменопаузе, и им желательно не превышать в течение долгого времени количество употребляемого железа.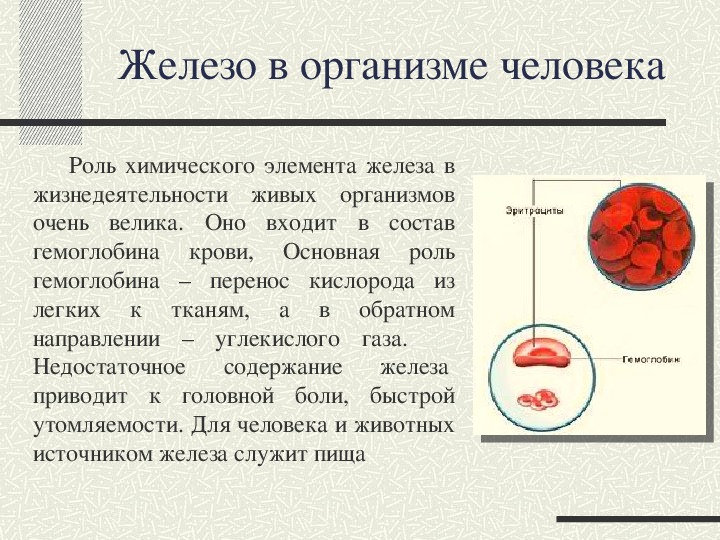
Лучшим источником железа являются продукты животного происхождения, такие как печень, кровяная колбаса, яйца, постная говядина и свинина, но также и семена, изюм, хлеб, цельнозерновые продукты, греча, клубника. Продукты, богатые жирами и сахаром, обычно бедны железом.
У женщин потери железа с менструальной кровью очень различаются. Это значит, что некоторым женщинам требуется больше железа, чем его можно получить из обычной пищи. Если железо усваивается на 15 %, то 90 % потребности в железе у женщин детородного возраста покроют 15 мг железа в день.
Для поддержания баланса железа в организме в начале беременности требуется накопить около 500 мг запасов железа. Некоторым женщинам для покрытия биологической потребности в железе в последние два триместра беременности недостаточно того железа, которое поступает с пищей, и требуются железосодержащие добавки.
Рекомендуемые количества минеральных веществ по возрастным группам см. подробнее в таблице.
Рекомендуемая суточная доза железа составляет 10–15 мг.
 10 мг железа содержат, например, следующие продукты:
10 мг железа содержат, например, следующие продукты:- 50 г тушеной печени,
- 55 г пшеничных отрубей,
- 90 г чечевицы,
- 125 г кровяной колбасы,
- 400 г тушеной говядины.
Если питаться разнообразно, в соответствии с теми количествами продуктов, которые рекомендованы в пирамиде питания, с получением достаточного количества железа проблем не возникает.
О железе просто! Роль железа в организме*)гемоглобин анемия!
Дата публикации: 01.09.2018 14:03
Всем нам известно, что пониженный уровень гемоглобина в крови — это плохо. При недостатке этого белка в организме возникают анемии. Недостаток гемоглобина ведет к снижению выносливости, а это безусловно важнейшая составляющая успеха в циклических видах спорта.
Гемоглобин — это белок отвечающий в организме за доставку в каждую клетку кислорода и «вывоз» углекислого газа. Основную роль в этой транспортировке играет железо. В легких, гемоглобин с помощью железа присоединяет кислород, который меняет в тканях на СО2 и вывозит его назад.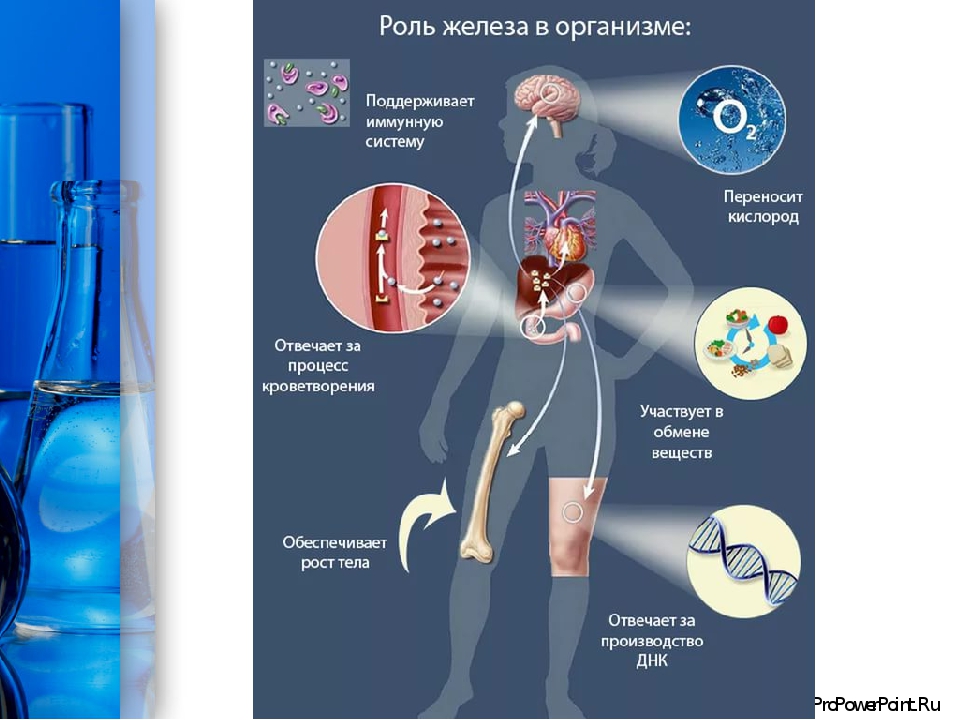
Исследовано, что в 80 случаях из 100 анемии возникающие у человека связаны именно с дефицитом железа. Признаками, говорящими о недостатке железа в организме являются – повышенная утомляемость, нервозность, одышка и даже ухудшение памяти. Но мы пытаемся это объяснять себе другими причинами – возрастом, загруженностью на работе или хроническими заболеваниями.
Особую группу риска составляют женщины, из-за своей физиологии они систематически подвержены риску возникновения дефицита железа. Это обусловлено тем, что каждый менструальный цикл приводит к потере железа в их организме. И в эти периоды организму необходимо восполнять этот дефицит.
Что же делать?
В организме человека железо не синтезируется и его поступление в организм полностью зависит от его количества в употребляемых продуктах. Для поддержания уровня гемоглобина в крови способствует диета с употреблением железосодержащих продуктов (телятина, гречка, рыба, печень, гранаты (только фрукты!))). Но нужно понимать, что эта мера хороша в качестве профилактики, а в условиях повышенных физических нагрузок либо при восстановлении организма после болезни нужны, другие объемы поступления железа в организм.
Для поддержания уровня гемоглобина в крови способствует диета с употреблением железосодержащих продуктов (телятина, гречка, рыба, печень, гранаты (только фрукты!))). Но нужно понимать, что эта мера хороша в качестве профилактики, а в условиях повышенных физических нагрузок либо при восстановлении организма после болезни нужны, другие объемы поступления железа в организм.
Этим поставщиком является клеточный сок пихты входящий в состав продуктов серии Tayga8. Продукция разработана Томскими учеными и за короткое время завоевала положительную репутацию, как среди обычных людей, так и среди тех, кто ведет активный образ жизни.
Влияние железа на здоровье человека
Железо – чрезвычайно важный металл в человеческом организме. Самое большое количество железа (примерно 60 %) содержится в крови человека. Остальная его часть находится в тканях, печени, костном мозге, селезёнке. Железо играет огромную роль в процессе вырабатывания гемоглобина в крови, а также миоглобина и других ферментов.
Продукты, богатые железом, необходимо употреблять детям в период активного роста, беременным женщинам, а также женщинам во время менструаций. Вообще, железо необходимо употреблять при всех заболеваниях, сопровождающихся малокровием.
Нехватка железа в организме человека
Недостаток этого металла в организме человека может привести к неприятным последствиям. При дефиците железа у людей наблюдается быстрая утомляемость, снижение иммунитета. Особенно опасен дефицит железа у детей. Это приводит к задержке физического и умственного развития. Все органы начинают работать хуже. У мужчин недостаток железа может привести к ухудшению работы половых органов, что влечет за собой импотенцию. Беременным женщинам нужно особенно следить за поступлением железа в организм. Его нехватка может сильно навредить потомству (как в умственном, так и в физическом отношении).
Дефицит железа может возникнуть при недостаточном потреблении его с пищей, а также из-за некоторых патологических состояний: различные инфекции, хроническая диарея, после кровопотерь, послеоперационных кровотечений.
Для лучшего усвоения этого металла необходимо употреблять в пищу также марганец, медь, витамин С и кобальт.
Продукты, богатые железом:
1) Такие фрукты, как яблоки, абрикосы, персики, груши, айва;
2) Фасоль, горох, чечевица;
3) Некоторые овощи: репчатый лук, картофель, тыква, свекла;
4) Почки и печень скота;
5) Куриные яйца;
Для того, чтобы защитить организм от дефицита железа детям на 1 кг веса необходимо употреблять 0,6 мг в сутки, взрослым 0,2 мг, беременным женщинам 0,3 мг. Обычно, употребления продуктов, богатых железом, достаточно. Но в отдельных случаях (донорство крови, анемия) следует употреблять препараты или пищевые добавки с железом.
Почему страшен для организма избыток «железа»? — Российская газета
В организме взрослого человека должно быть примерно 4-5 г железа.
Но сегодня все реже встречаются люди, у которых этот элемент содержится в норме. Особенно у горожан все чаще наблюдается повышенная концентрация железа. Хорошо это или плохо?
У нас не заржавеет
Все знают о том, что «низкий уровень железа — это плохо». И только в последнее время заговорили, что и в повышенном содержании этого элемента нет ничего хорошего. Ведь помимо переноса кислорода железо регулирует работу иммунной системы, принимает участие в работе щитовидной железы, способствует выведению токсинов из организма, участвует в процессах регенерации, улучшает состояние кожи, структуру волос и ногтей… Словом, большинство процессов в наших клетках протекает с участием железа. Но при его избытке происходят реакции, похожие на образование ржавчины: молекулы железа окисляются и повреждают живые ткани.
Откуда излишки?
Большая часть железа в нашем теле входит в состав гемоглобина, отвечающего за перенос кислорода в теле. Именно поэтому, когда человеку не хватает кислорода, организм пытается компенсировать это увеличением концентрации гемоглобина. Так происходит у альпинистов в горах. И у жителей городов, где воздух насыщен выхлопными газами. Но альпинисты спускаются с гор. А горожане постоянно испытывают кислородное голодание. Иногда излишки железа в крови — признак болезни печени. А еще есть люди (практически каждый седьмой житель планеты), которые являются носителями особого гена, вызывающего накопление железа. К счастью, ген этот большей частью дремлет, потому гемохроматозом (так называется избыточное содержание железа) страдают немногие. Этот «дефектный» ген еще называют «геном кельтов». Он чаще встречается у жителей Скандинавии. Избыток железа характерен больше для мужчин, из-за физиологических потерь крови женщин эта неприятность затрагивает реже, однако после менопаузы они начинают «догонять» мужчин.
Так происходит у альпинистов в горах. И у жителей городов, где воздух насыщен выхлопными газами. Но альпинисты спускаются с гор. А горожане постоянно испытывают кислородное голодание. Иногда излишки железа в крови — признак болезни печени. А еще есть люди (практически каждый седьмой житель планеты), которые являются носителями особого гена, вызывающего накопление железа. К счастью, ген этот большей частью дремлет, потому гемохроматозом (так называется избыточное содержание железа) страдают немногие. Этот «дефектный» ген еще называют «геном кельтов». Он чаще встречается у жителей Скандинавии. Избыток железа характерен больше для мужчин, из-за физиологических потерь крови женщин эта неприятность затрагивает реже, однако после менопаузы они начинают «догонять» мужчин.
Симптомы
Симптомы избытка железа сходны с признаками гепатита — желтушное окрашивание кожи, склер, а также неба и языка, зуд, увеличение печени.
Кроме того, нарушается сердечный ритм, люди выглядят бледными, худеют. Возможна также пигментация в тех местах, где ее не должно быть по определению, например на ладонях, в области подмышек, в местах старых рубцов. Но для того, чтобы поставить точный диагноз, требуется биохимический анализ крови
Возможна также пигментация в тех местах, где ее не должно быть по определению, например на ладонях, в области подмышек, в местах старых рубцов. Но для того, чтобы поставить точный диагноз, требуется биохимический анализ крови
Больше всего железа накапливается в печени, поджелудочной железе, сердечной мышце, что в конечном итоге становится причиной изменения и самого органа: развивается гепатит, цирроз печени, сахарный диабет, заболевания суставов, нервной системы, сердечные патологии, вплоть до внезапной остановки сердца.
Избыток железа осложняет ход болезней Паркинсона и Альцгеймера, может спровоцировать рак кишечника, печени, легких. Ревматоидный артрит также часто протекает на фоне избытка железа.
Что делать
К людям с сильно повышенным гемоглобином нужен особый подход. Им нельзя назначать даже, казалось бы, безобидную аскорбиновую кислоту, ведь этот витамин имеет свойство усиливать всасывание железа.
Избыток железа устранить даже сложнее, чем недостаток. Пожалуй только старый дедовский способ — кровопускание (флеботомия) — позволяет добиться нужных результатов и даже избежать иногда медикаментозных препаратов при лечении.
Пожалуй только старый дедовский способ — кровопускание (флеботомия) — позволяет добиться нужных результатов и даже избежать иногда медикаментозных препаратов при лечении.
За рубежом, например, людям после 40-50 лет даже рекомендуют донорство — для профилактики ишемической болезни сердца. Так что человек, «переполненный» железом, может смело записываться в ряды доноров крови.
Ну и самый традиционный, но и самый верный способ регуляции уровня железа в крови — правильное питание.
важно знать
Считается, что железо, содержащееся в красном мясе, усваивается лучше, чем железо из растений. Это не всегда так. Например, регулярное употребление сельдерея способно восстановить баланс этого элемента в организме за несколько недель. Железо из растительных продуктов лучше усваивается, когда их сочетают с продуктами животного происхождения.
Лучшему усвоению железа способствуют витамин С и витамины группы В. Так что, например, яблоко в дополнение к мясу полезно съедать при анемии, а вот при повышенном гемоглобине лучше воздержаться. Если же в продуктах питания много кальция и сахара, железо усваивается плохо.Гречка, сваренная на воде (без молока), значительно полезнее при низком гемоглобине.
Если же в продуктах питания много кальция и сахара, железо усваивается плохо.Гречка, сваренная на воде (без молока), значительно полезнее при низком гемоглобине.
Лучше всего готовить пищу в русской печке, но ее может заменить аэрогриль, который готовит по тому же принципу. Блюдо равномерно прогревается со всех сторон, при этом — без лишней воды и масла, что позволяет лучше сохранить полезные свойства продуктов. Все это делает пищу вкусной и полезной, она хорошо усваивается организмом, поставляя максимум необходимых элементов. Не только овощи, но и мясо, приготовленное в аэрогриле, соответствует рекомендациям диетологов и помогает нормализации гемоглобина.
Обмен железа
directions
Железо является одним из самых важных микроэлементов человеческого организма. Оно отвечает за процессы обмена кислородом. Большая часть железа является действующим элементом гемоглобина плазмы крови. Оно поступает в организм вместе с пищей. Как правило, этого уровня достаточно для потребностей человека. Однако в некоторых случаях необходима дополнительная подпитка, например при анемии. У женщин потребность в железе несколько выше, чем у мужчин, в особенности во второй половине беременности. Избыточное содержание железа вызывает токсическое действие. Чтобы устранить все проблемы, возникающие в работе организма, необходимо пройти обследование на содержание железа. Все анализы можно сделать в нашем медицинском центре.
Однако в некоторых случаях необходима дополнительная подпитка, например при анемии. У женщин потребность в железе несколько выше, чем у мужчин, в особенности во второй половине беременности. Избыточное содержание железа вызывает токсическое действие. Чтобы устранить все проблемы, возникающие в работе организма, необходимо пройти обследование на содержание железа. Все анализы можно сделать в нашем медицинском центре.
Врачи-специалисты
Старшая медицинская сестра
Медицинская сестра
Медицинская сестра эндоскопического кабинета
Врач-терапевт
Анализ на коронавирус методом ПЦР. Результат в течение суток
Результат в течение суток
Наши клиники в Санкт-Петербурге
Медицентр Юго-ЗападПр.Маршала Жукова 28к2
Кировский район
- Автово
- Проспект Ветеранов
- Ленинский проспект
Получить подробную информацию и записаться на прием Вы можете по телефону +7 (812) 640-55-25
Железо выполняет очень важную роль в организме человека. Оно выполняет функцию переноса кислорода, принимает участие в окислительных процессах, ферментативных реакциях, обеспечении иммунных функций, метаболизме холестерина. Помимо эритроцитов железо ещё содержится и в клетках мозга.
Оно выполняет функцию переноса кислорода, принимает участие в окислительных процессах, ферментативных реакциях, обеспечении иммунных функций, метаболизме холестерина. Помимо эритроцитов железо ещё содержится и в клетках мозга.
Диагностика нарушения содержания железа в организме.
Содержание железа в организме оценивается посредством проведения анализов мочи, крови и волос. У здорового человека содержание железа в организме равняется 4-5 граммам, в плазме крови — 0,8-1,4 мкг/л, волосах — 10-25 мкг/г и моче — 10-25 мкг/л. У мужчин содержание железа в волосах выше, чем у женщин. Для людей, страдающих заболеваниями селезёнки, печени, хроническим алкоголизмом, содержание железа в волосах выше нормы. При диагностике дефицита железа используют несколько тестов, определяющих сывороточное железо и ферритин, свободный порфирин и общую железосвязывающую способность сыворотки.
Анализ на ферритин характеризует количество запасов железа в организме человека. Во время беременности количество ферритина может уменьшаться.
Во время беременности количество ферритина может уменьшаться.
Железосвязывающая способность сыворотки – это показатель, дающий оценку способности крови к связыванию железа. В организме железо находится в комплексе с белком – трансферрином. Анализ на ЖСС отображает его концентрацию в плазме.
Повышенное содержание железа.
Железо может накапливаться в организме при наличии хронических и некоторых наследственных заболеваний. Чаще всего избавиться от избытка железа намного сложнее, чем устранить его дефицит. Если началось тяжёлое отравление железом, происходит повреждение слизистой оболочки кишечника, появляется тошнота и рвота.
Симптомы избытка железа:
- Отложение железа в органах и тканях.
- Пигментация кожи.
- Тошнота, рвота, боли в желудке, изжога.
- Диарея или запор.
- Головные боли.
- Повышенная утомляемость и слабость.
- Головокружение.
- Снижение уровня сывороточного железа.
- Угнетение иммунитета.
- Уменьшение массы тела и потеря аппетита.
- Печёночная недостаточность.
Причинами избыточного содержания железа могут послужить нарушения в регуляции обмена железом, заболевания селезёнки, печени и чрезмерное поступление вместе с едой.
Пониженное содержание железа.
На данный момент существует множество факторов, которые могут вызвать пониженное содержание железа в крови. Наиболее вероятными причинами низкого содержания железа является недостаточное поступление вместе с продуктами питания, нарушения всасывания в желудке и расстройства метаболизма. Существуют ситуации с абсолютным либо относительным дефицитом железа. К таким случаям относят лактацию, беременность, периоды развития и роста. Ещё одной причиной дефицита железа могут послужить хронические или острые кровопотери.
Недостаточное содержание железа проявляется в виде:
- замедления физического и умственного развития;
- железодефицитной анемии;
- неадекватного поведения у детей;
- слабости, утомляемости, головокружения и головных болей;
- снижения концентрации внимания и памяти;
- ломкости ногтей;
- извращения вкуса;
- угнетения иммунитета и как следствие, частой заболеваемости.
Усвоению железа способствует кальций, а витамин Е и цинк наоборот, снижают способность организма усваивать железо.
Как корректируют содержание железа в организме?
При дефиците железа врач назначает приём железосодержащих препаратов совместно с антиоксидантами (например, витамин С). В случае же хронического избытка железа и отложения его в органах и тканях иногда применяется процедура кровопускания и используются препараты цинка, гепатопротекторы.
Если человек получил острое отравление железом, то ему промывают желудок и назначают специальный препарат для предотвращения тяжёлого поражения печени.
Для новорождённых характерно падение уровня железа в течение нескольких часов после того, как прошли роды.
1269,1322,814,1326,1345,841
Вахтин Дмитрий Сергеевич 12.03.2021 15:43medi-center.ru
Мучился с ангинами и с простудами каждый месяц, пил антибиотики которые давали временный эффект, попал на приём к ЛОРу в Медицентр на Поликарпова Аиде Фаталиевне , которая направила на анализы и поставила правильный диагноз, хронический тонзиллит, миндалины пришлось удалить, живу полгода и радуюсь жизни, за полгода никаких ангин, первый раз за зиму не заболел простудой
Екимова Янина 11.02.2021 19:21medi-center.ru
Хочу поблагодарить ЛОР-врача Саранчина А.С. за чуткое, внимательное отношение к пациентам и професионализм. Огромное спасибо.
Яника Сок 01.02.2021 22:09medi-center.ru
Мне очень понравилось на приеме у доктора. Провела осмотр и УЗИ, это единственный из всех врачей которая увидела на УЗИ спайки!!!Спайки действительно есть!(данные лапароскопии) Во время ультразвукового обследования доктор все объясняла, рассказывала и даже наглядно показывала. Изначально я к ней пришла на ГСГ процедуру доктор провела замечательно, ничего не больно, успокаивала меня (я еще та трусиха)…на основании ГСГ дала свои рекомендации Правильные. Спасибо Вам огромное! Доктор очень вежливая, тактичная и замечательная. Профессионализм Регины Гумеровны на высшем уровне, качеством её работы я осталась полностью довольна. Я и буду советовать доктора к посещению! Прошу премировать доктора!
Здравствуйте! Выражаю благодарность всем сотрудникам медцентра и лично Поддубной Анастасии Михайловне за работу в такое непростое время, хорошие и результативные рекомендации по лечению. Переболел COVID, благодаря вам иду на поправку!
Хочу выразить огромную благодарность ,Агамурату Озармамедовичу Джораеву , в Мурино на Охтинской алее . У ребёнка был вывих локтевого сустава, все сделал очень быстро , вставил на место , нашёл подход к плачущему ребёнку !! Спасибо вашему центру, за отличных врачей !!!
Добрый день! Я хотела бы поблагодарить Клинику МедиЦентр (на алее Поликарпова) и ЛОР-врача Ершову Татьяну Викторовну за их работу. К Татьяне Викторовне на приём первый раз попала в 2016 году. С этого момента, при возникновении проблем с горлом или носом, обращаюсь только к Татьяне Викторовне. Всегда внимательное отношение к описанной симптоматике и тщательный осмотр, направления на уточняющие состояние анализы и, как результат, правильное лечение. Спасибо! С уважением, Мария
Болезни, связанные с водой: aнемия
Анемия
Анемия распространена во всем мире. Ее главная причина — недостаток железа в организме является наиболее распространенной нутриционной недостаточностью в мире. Помимо нехватки железа, важными факторами возникновения анемии является ряд инфекционных заболеваний, связанных с несоблюдением гигиены, санитарии, отсутствием безопасной воды и водоипользованием. К их числу относятся малярия, шистосомоз и анкилостомоз.
Как анемия воздействует на людей
При анемии красные кровяные тельца не переносят достаточно кислорода к тканям организма. Анемия затрагивает все группы населения. Однако ей наиболее подвержены беременные женщины и дети младшего возраста. В более легкой форме болезнь не проявляет себя, протекает бессимптомно. В более тяжелой форме анемия сопровождается усталостью, слабостью, головокружением и сонливостью. К числу ее признаков относится изменение обычного цвета кожи (у людей со светлой кожей), а также губ, языка, ногтевого ложа и кровеносных сосудов в белках глаз.
В отсутствие лечения анемия может принять более тяжелую форму и стать причиной хронического состояния нездоровья, например нарушений в развитии плода во время беременности, задержки когнитивного развития и усиления риска инфекции у детей младшего возраста, а также снижения физических возможностей у всех людей. Риску анемии особо подвержены новорожденные с низкой массой тела, дети младшего возраста и женщины детородного возраста. В организм женщин детородного возраста должно поступать в 2-3 раза больше железа, чем это требуется для мужчин или женщин более старшего возраста.
Причина
Основные причины анемии связаны с питанием и инфекциями. Они обычно сосуществуют в одном организме и усугубляют анемию.
В числе факторов питания, способствующих анемии, наиболее распространенным является нехватка железа. Это вызвано однообразной диетой, богатой, однако, веществами (фитатами), препятствующими всасыванию железа, что не позволяет организму использовать железо из пищевых продуктов. Нехватка железа может также усугубляться неудовлетворительным алиментарным статусом, особенно когда он связан с нехваткой фолиевой кислоты, витамина А или В12, как это часто происходит с населением развивающихся стран.
Что касается инфекции, то малярия является еще одним важным фактором возникновения анемии: ею страдают 300-500 миллионов человек, и в эндемичных районах она может являться главной причиной половины всех серьезных случаев анемии (ВОЗ, 2000 г.). Анемии также способствует заражение анкилостомозом, а в некоторых районах — шистосомозом. Примерно 44 миллиона беременных женщин заражены анкилостомозом, и 20 миллионов человек страдают тяжелой инфекцией шистосомоза. Анемия также может быть вызвана чрезмерными потерями крови, например при гастроэнтерологических инфекциях, связанных с диареей. Наиболее важными причинами анемии, связанными с водой, являются недостаточное питание и инфекции, передающиеся через воду или связанные с водой.
Распространение
Анемия является широко распространенной проблемой во всеми мире, и нехватка железа является самой распространенной нутриционной недостаточностью в мире. Она затрагивает, главным образом, беднейший слои населения, особенно там, где недостаточность питания получила широкое распространение и население подвержено высокому риску инфекции, связанной с водой.
Масштабы проблемы
Девять из десяти лиц с анемией живут в развивающихся странах, около 2 миллиардов человек страдают анемией и еще большее число людей испытывают нехватку железа (ВОЗ, 2000 г.). Анемия, возможно, способствует до 20% случаев смерти матерей.
Меры воздействия
Поскольку анемия является результатом действия многих факторов, выявление этих факторов и причин и типов анемии имеет важное значение. К числу важных мероприятий относятся устранение первопричин, корректировка нехватки железа, лечение исходных болезнетворных процессов (особенной нутриционной недостаточности — нехватки фолиевой кислоты, витамина А и В12).
В борьбе с анемией у детей важное значение имеет содействие грудному вскармливанию и надлежащее дополнительное питание.
Важными мерами профилактики анемии являются повышение уровня гигиены, санитарии и водоснабжения; а также совершенствование управления водными ресурсами в качестве мер борьбы с шистосомозом и малярией там, где они имеют место.
Источники
WHO. Turning the tide of malnutrition: responding to the challenge of the 21st century. Geneva: WHO, 2000 (WHO/NHD.007)
Prepared for World Water Day 2001. Reviewed by staff and experts in the Department of Nutrition for Health and Development (NHD) and the Water, Sanitation and Health Unit (WSH), World Health Organization (WHO), Geneva.
WHO/WSH/WWD/DFS.07
Обзор железа и его значения для здоровья человека
J Res Med Sci. 2014 фев; 19 (2): 164–174.
Назанин Аббаспур
Департамент наук о системах окружающей среды, Институт наземных экосистем, Швейцарский федеральный технологический институт, Цюрих, Швейцария
Ричард Харрелл
1 Департамент здравоохранения и технологий, Лаборатория питания человека, Институт пищевых продуктов , Питание и здоровье, Швейцарский федеральный технологический институт, Цюрих, Швейцария
Роя Келишади
2 Исследовательский центр детского роста и развития, Исфаханский университет медицинских наук, Исфахан, Иран
Департамент науки о системах окружающей среды, Институт наземных исследований Экосистема, Швейцарский федеральный технологический институт, Цюрих, Швейцария
1 Департамент медицинских наук и технологий, Лаборатория питания человека, Институт питания, питания и здоровья Швейцарского федерального технологического института, Цюрих, Швейцария
2 Исследования роста и развития детей Ce nter, Исфаханский университет медицинских наук, Исфахан, Иран
Адрес для корреспонденции: Prof.Роя Келишади, Исследовательский центр детского роста и развития Исфаханский университет медицинских наук, Исфахан, Иран. Электронная почта: ri.ca.ium.dem@idahsilekПоступила в редакцию 8 июня 2013 г .; Пересмотрено 3 ноября 2013 г .; Принято 27 ноября 2013 г.
Авторские права: © Journal of Research in Medical SciencesЭто статья в открытом доступе, распространяемая в соответствии с условиями Creative Commons Attribution-Noncommercial-Share Alike 3.0 Unported, что разрешает неограниченное использование, распространение и воспроизведение в на любом носителе при условии правильного цитирования оригинальной работы.
Эта статья цитируется в других статьях в PMC.Abstract
Хорошо известно, что недостаток или чрезмерное воздействие различных элементов оказывает заметное влияние на здоровье человека. Действие элемента определяется несколькими характеристиками, включая абсорбцию, метаболизм и степень взаимодействия с физиологическими процессами. Железо является важным элементом почти для всех живых организмов, поскольку оно участвует в широком спектре метаболических процессов, включая транспорт кислорода, синтез дезоксирибонуклеиновой кислоты (ДНК) и транспорт электронов.Однако, поскольку железо может образовывать свободные радикалы, его концентрацию в тканях организма необходимо строго регулировать, поскольку в чрезмерных количествах оно может привести к повреждению тканей. Нарушения метаболизма железа являются одними из наиболее распространенных заболеваний человека и охватывают широкий спектр заболеваний с различными клиническими проявлениями, от анемии до перегрузки железом и, возможно, до нейродегенеративных заболеваний. В этом обзоре мы обсуждаем последние достижения в исследованиях метаболизма и биодоступности железа, а также наше текущее понимание потребности человека в железе, а также последствий и причин дефицита железа.Наконец, мы обсуждаем стратегии предотвращения дефицита железа.
Ключевые слова: Анемия, потребность человека в железе, биодоступность железа, дефицит железа, метаболизм железа
ВВЕДЕНИЕ
С древних времен человек осознавал особую роль железа в здоровье и болезнях. [1] Железо вначале использовалось в медицине египтянами, индуистами, греками и римлянами. [2, 3] В 17 — веках железо использовалось для лечения хлороза (зеленой болезни), состояния, часто возникающего из-за дефицита железа.[4] Однако только в 1932 году важность железа была окончательно установлена убедительным доказательством того, что неорганическое железо необходимо для синтеза гемоглобина. [5] В течение многих лет пищевой интерес к железу был сосредоточен на его роли в образовании гемоглобина и транспорте кислорода. [6] В настоящее время, хотя низкое потребление железа и / или его биодоступность являются причиной большинства анемий в промышленно развитых странах, на них приходится лишь около половины анемии в развивающихся странах [7], где инфекционные и воспалительные заболевания (особенно малярия), кровопотеря от паразитарных инфекций. , и дефицит других питательных веществ (витамина А, рибофлавина, фолиевой кислоты и витамина B12) также являются важными причинами.[8]
Биохимия и физиология
В отличие от цинка, железо является распространенным элементом на Земле [2,9] и является биологически важным компонентом каждого живого организма. [10,11] Однако, несмотря на его геологическое изобилие, железо часто является фактором, ограничивающим рост в окружающей среде. [9] Этот кажущийся парадокс связан с тем фактом, что при контакте с кислородом железо образует оксиды, которые очень нерастворимы и, следовательно, не доступны для усвоения организмами [2]. В ответ возникли различные клеточные механизмы захвата железа из окружающей среды в биологически полезных формах.Примерами являются сидерофоры, секретируемые микробами для захвата железа в высокоспецифический комплекс [12], или механизмы восстановления железа из нерастворимого трехвалентного железа (Fe +3 ) до растворимой двухвалентной формы (Fe +2 ), как в дрожжах. [13] Многие механизмы, обнаруженные у низших организмов, имеют аналогичные аналоги у высших организмов, включая человека. В организме человека железо в основном существует в сложных формах, связанных с белком (гемопротеином), в виде гемовых соединений (гемоглобин или миоглобин), гемовых ферментов или негемовых соединений (ферменты флавин-железо, переносчики и ферритин).[3] Организму требуется железо для синтеза белков, переносящих кислород, в частности гемоглобина и миоглобина, а также для образования гемовых ферментов и других железосодержащих ферментов, участвующих в переносе электронов и окислении-восстановлении. [14,3] Почти Две трети железа в организме содержится в гемоглобине, присутствующем в циркулирующих эритроцитах, 25% содержится в легко мобилизуемых запасах железа, а оставшиеся 15% связаны с миоглобином в мышечной ткани и с различными ферментами, участвующими в окислительном процессе. метаболизм и многие другие функции клеток.[15]
Железо перерабатывается и, таким образом, сохраняется в организме. показана схематическая диаграмма цикла железа в организме. Железо доставляется в ткани с помощью циркулирующего трансферрина, переносчика, который захватывает железо, высвобождаемое в плазму, в основном из кишечных энтероцитов или ретикулоэндотелиальных макрофагов. Связывание нагруженного железом трансферрина с рецептором трансферрина на клеточной поверхности (TfR) 1 приводит к эндоцитозу и поглощению металлического груза. Интернализованное железо транспортируется в митохондрии для синтеза гема или кластеров железо-сера, которые являются неотъемлемой частью нескольких металлопротеинов, а избыток железа накапливается и детоксифицируется в цитозольном ферритине.
Железо связывается и транспортируется в организме через трансферрин и сохраняется в молекулах ферритина. После всасывания железа не существует физиологического механизма выведения избыточного железа из организма, кроме кровопотери, то есть беременности, менструации или другого кровотечения обычно низкий, но может колебаться от 5% до 35% в зависимости от обстоятельств и типа железа. [3]
Поглощение железа энтероцитами осуществляется переносчиком двухвалентного металла 1, входящим в группу переносчиков растворенных веществ мембранных транспортных белков.Это происходит преимущественно в двенадцатиперстной кишке и верхних отделах тощей кишки [16]. Затем он переносится через слизистую двенадцатиперстной кишки в кровь, где транспортируется трансферрином к клеткам или костному мозгу для эритропоэза [продуцирования красных кровяных телец (эритроцитов)]. [14,17,18] Существует механизм обратной связи, который усиливается. всасывание железа у людей с дефицитом железа. Напротив, люди с перегрузкой железом снижают абсорбцию железа через гепсидин. В настоящее время общепринято, что абсорбция железа контролируется ферропортином, который позволяет или не позволяет железу из клетки слизистой оболочки попадать в плазму.
Физическое состояние железа, поступающего в двенадцатиперстную кишку, сильно влияет на его всасывание. При физиологическом pH двухвалентное железо (Fe +2 ) быстро окисляется до нерастворимой трехвалентной формы (Fe +3 ). Желудочная кислота снижает pH в проксимальном отделе двенадцатиперстной кишки, снижая содержание Fe +3 в просвете кишечника за счет редуктазы железа, тем самым обеспечивая последующий транспорт Fe +2 через апикальную мембрану энтероцитов. Это увеличивает растворимость и поглощение трехвалентного железа.Когда продукция желудочного сока нарушена (например, ингибиторами кислотного насоса, такими как лекарство, прилосек), абсорбция железа существенно снижается.
Диетический гем также может транспортироваться через апикальную мембрану по еще неизвестному механизму и впоследствии метаболизироваться в энтероцитах гемоксигеназой 1 (HO-1) с высвобождением (Fe +2 ) [19]. Этот процесс более эффективен, чем абсорбция неорганического железа, и не зависит от рН двенадцатиперстной кишки. Таким образом, на него не влияют такие ингибиторы, как фитат и полифенолы.Следовательно, красное мясо с высоким содержанием гемоглобина является отличным источником железа. Непосредственно интернализованный Fe +2 обрабатывается энтероцитами и в конечном итоге (или нет) экспортируется через базолатеральную мембрану в кровоток через транспортер ферропортин Fe +2 . Ферропортин-опосредованный отток Fe +2 связан с его повторным окислением с Fe +2 , катализируемым мембраносвязанным ферроксидазой гефестином, который физически взаимодействует с ферропортином [20] и, возможно, также его плазменным гомологом церулоплазмином.Экспортируемое железо улавливается трансферрином, который поддерживает Fe +3 в окислительно-восстановительном инертном состоянии и доставляет его в ткани. Общее содержание железа в трансферрине (≈3 мг) соответствует менее 0,1% железа в организме, но оно очень динамично и подвергается более чем 10-кратному ежедневному обороту для поддержания эритропоэза. Пул трансферрина железа пополняется в основном за счет железа, рециркулируемого из неэффективных эритроцитов, и, в меньшей степени, за счет вновь абсорбированного пищевого железа. Стареющие эритроциты очищаются ретикулоэндотелиальными макрофагами, которые метаболизируют гемоглобин и гем и высвобождают железо в кровоток.По аналогии с кишечными энтероцитами, макрофаги экспортируют Fe +2 из своей плазматической мембраны через ферропортин в процессе, сопряженном с повторным окислением Fe +2 до Fe +3 церулоплазмином с последующей загрузкой Fe +3. на трансферрин. [21]
Theil et al ., [21] недавно сообщили, что существует также независимый механизм абсорбции растительных ферритинов, в основном присутствующих в бобовых. Однако актуальность переносчика ферритина неясна, поскольку большая часть ферритина, по-видимому, разлагается во время обработки и переваривания пищи, тем самым высвобождая неорганическое железо из оболочки ферритина для поглощения по нормальному механизму.[22] Поскольку одна молекула ферритина содержит 1000 или более атомов железа и на нее также не должны влиять ингибиторы абсорбции железа, такой механизм может стать важным источником железа в развивающихся странах, где обычно потребляются бобовые.
Регуляция гомеостаза железа
Поскольку железо требуется для ряда разнообразных клеточных функций, для поддержания гомеостаза железа требуется постоянный баланс между поглощением, транспортом, хранением и использованием железа. [11] Поскольку в организме отсутствует определенный механизм активного выведения железа, баланс железа в основном регулируется в точке абсорбции.[23,24]
Гепсидин — это циркулирующий пептидный гормон, секретируемый печенью, который играет центральную роль в регуляции гомеостаза железа. Это главный регулятор системного гомеостаза железа, координирующий использование и хранение железа с приобретением железа. [25] Этот гормон в основном вырабатывается гепатоцитами и является негативным регулятором поступления железа в плазму []. Гепсидин действует путем связывания с ферропортином, переносчиком железа, присутствующим на клетках двенадцатиперстной кишки, макрофагах и клетках плаценты.Связывание гепсидина вызывает интернализацию и деградацию ферропортина. [26] Потеря ферропортина с поверхности клетки предотвращает попадание железа в плазму []. Снижение поступления железа в плазму приводит к низкому насыщению трансферрина и меньшему количеству железа доставляется в развивающийся эритробласт. Напротив, снижение экспрессии гепсидина приводит к увеличению ферропортина на клеточной поверхности и увеличению абсорбции железа [27] []. У всех видов концентрация железа в биологических жидкостях строго регулируется, чтобы обеспечить необходимое количество железа и избежать токсичности, поскольку избыток железа может привести к образованию активных форм кислорода.[28] Гомеостаз железа у млекопитающих регулируется на уровне кишечной абсорбции, поскольку для железа не существует экскреторного пути.
Гепсидин-опосредованная регуляция гомеостаза железа. (а) Повышенная экспрессия гепсидина печенью является результатом воспалительных стимулов. Высокий уровень гепсидина в кровотоке приводит к интернализации и деградации ферропортина, экспортера железа. Потеря ферропортина на клеточной поверхности приводит к загрузке железа макрофагами, низким уровням железа в плазме и снижению эритропоэза из-за снижения количества железа, связанного с трансферрином.Снижение эритропоэза приводит к анемии хронического заболевания. (b) Нормальные уровни гепсидина в ответ на потребность в железе регулируют уровень импорта железа в плазму, нормальное насыщение трансферрина и нормальные уровни эритропоэза. (c) Гемохроматоз или перегрузка железом возникает из-за недостаточного уровня гепсидина, вызывая повышенный импорт железа в плазму, высокое насыщение трансферрина и избыточное отложение железа в печени. Источник: Де Доменико, и др. . [27]
Уровни гепсидина в плазме регулируются различными стимулами, включая цитокины, железо в плазме, анемию и гипоксию.Нарушение регуляции экспрессии гепсидина приводит к нарушениям железа. Избыточная экспрессия гепсидина приводит к анемии хронического заболевания, в то время как низкая выработка гепсидина приводит к наследственному гемохроматозу (HFE) с последующим накоплением железа в жизненно важных органах []. Большинство наследственных заболеваний, связанных с железом, возникает в результате недостаточного производства гепсидина по сравнению со степенью накопления железа в тканях. Было показано, что нарушение экспрессии гепсидина является результатом мутаций в любом из 4 различных генов: TfR2, HFE, гемохроматоз типа 2 (HFE2) и антимикробный пептид гепсидина (HAMP).Мутации в HAMP, гене, кодирующем гепсидин, приводят к болезни, связанной с перегрузкой железом, поскольку отсутствие гепсидина обеспечивает постоянное высокое всасывание железа. Роль других генов (TFR2, HFE и HFE2) в регуляции продукции гепсидина не ясна [27].
Хранение
Концентрация ферритина вместе с концентрацией гемосидерина отражает запасы железа в организме. Они хранят железо в нерастворимой форме и присутствуют в основном в печени, селезенке и костном мозге. [2] Большая часть железа связана с широко распространенным и высококонсервативным железосвязывающим белком ферритином.[18] Гемосидерин представляет собой комплекс хранения железа, который с меньшей готовностью выделяет железо для нужд организма. В условиях устойчивого состояния сывороточные концентрации ферритина хорошо коррелируют с общими запасами железа в организме. [29] Таким образом, сывороточный ферритин является наиболее удобным лабораторным тестом для оценки запасов железа.
Выделение
Помимо потерь железа из-за менструации, другого кровотечения или беременности, железо очень консервативно и нелегко выводится из организма. [30] Существует некоторая обязательная потеря железа из организма в результате физиологического отшелушивания клеток с эпителиальных поверхностей [30], включая кожу, мочеполовые и желудочно-кишечные тракты.[3] Однако, по оценкам, эти потери очень ограничены (≈1 мг / день). [31] Потери железа из-за кровотечения могут быть значительными, а чрезмерная менструальная кровопотеря является наиболее частой причиной дефицита железа у женщин.
БИОЛОГИЧЕСКАЯ ДОСТУПНОСТЬ
Пищевое железо встречается в двух формах: гемовая и негемовая. [23] Основными источниками гемового железа являются гемоглобин и миоглобин из мяса, птицы и рыбы, тогда как негемовое железо получают из злаков, бобовых, бобовых, фруктов и овощей.[32] Гемовое железо обладает высокой биодоступностью (15–35%), и диетические факторы мало влияют на его абсорбцию, тогда как абсорбция негемового железа намного ниже (2–20%) и сильно зависит от присутствия других пищевых компонентов. [23] Напротив, количество негемового железа в рационе во много раз превышает количество гемового железа в большинстве приемов пищи. Таким образом, несмотря на более низкую биодоступность, негемовое железо обычно вносит больший вклад в питание железом, чем гемовое железо. [33] Основными ингибиторами абсорбции железа являются фитиновая кислота, полифенолы, кальций и пептиды из частично переваренных белков.[23] Усилители — это аскорбиновая кислота и мышечная ткань, которые могут восстанавливать трехвалентное железо до двухвалентного железа и связывать его в растворимые комплексы, доступные для абсорбции. [23]
Факторы, повышающие абсорбцию железа
На абсорбцию железа влияет ряд диетических факторов. Аскорбат и цитрат частично увеличивают усвоение железа, действуя как слабые хелаторы, помогая растворить металл в двенадцатиперстной кишке []. [34] Железо легко переносится из этих соединений в клетки слизистой оболочки. Исследователи продемонстрировали дозозависимый усиливающий эффект нативной или добавленной аскорбиновой кислоты на абсорбцию железа.[34] Усиливающий эффект в значительной степени связан с его способностью восстанавливать трехвалентное железо до двухвалентного железа, но также из-за его способности хелатировать железо. [35] Аскорбиновая кислота преодолеет негативное влияние на абсорбцию железа всех ингибиторов, включая фитат, [36] полифенолы, [37], кальций и белки, содержащиеся в молочных продуктах [38], и увеличит абсорбцию как нативного, так и обогащенного железа. Во фруктах и овощах усиливающий эффект аскорбиновой кислоты часто нивелируется ингибирующим действием полифенолов.[39] Аскорбиновая кислота является единственным усилителем всасывания в вегетарианских диетах, а всасывание железа из вегетарианских и веганских блюд можно оптимизировать путем включения овощей, содержащих аскорбиновую кислоту. [40] Варка, промышленная обработка и хранение разлагают аскорбиновую кислоту и устраняют ее усиливающий эффект на усвоение железа. [41]
Таблица 1
Факторы, которые могут влиять на всасывание железа
Было показано усиливающее действие мяса, рыбы или птицы на всасывание железа из вегетарианских блюд [42], и 30 г мышечной ткани считается эквивалентом 25 мг аскорбиновой кислоты. .[33] Бьорн-Расмуссен и Халлберг [43] сообщили, что добавление курицы, говядины или рыбы к кукурузной муке увеличивало всасывание негемового железа в 2-3 раза без влияния того же количества белка, что и яичного альбумина. Как и в случае с аскорбиновой кислотой, было несколько сложнее продемонстрировать усиливающий эффект мяса при многократном приёме пищи и в полных исследованиях диеты. Reddy и др. ., [44] сообщили только о незначительном улучшении абсорбции железа (35%) в самостоятельно выбранных диетах в течение 5 дней, когда ежедневное потребление мышечной ткани было увеличено до 300 г / день, хотя в аналогичных 5-дневных рационах. В ходе дневного исследования 60 г свинины, добавленные к вегетарианской диете, увеличили всасывание железа на 50%.[45]
Факторы, ингибирующие абсорбцию железа
В растительной диете фитат (мио-инозитол гексакисфосфат) является основным ингибитором абсорбции железа. [23] Было показано, что отрицательное влияние фитата на абсорбцию железа зависит от дозы и начинается с очень низких концентраций 2-10 мг / прием пищи. [37,46] Молярное отношение фитата к железу может быть использовано для оценки влияния на абсорбцию. . Соотношение должно составлять 1: 1 или предпочтительно 0,4: 1 для значительного улучшения всасывания железа в простых злаковых или бобовых блюдах, не содержащих каких-либо усилителей усвоения железа, или 6: 1 в комбинированных блюдах с некоторыми овощами, содержащими аскорбин кислота и мясо как усилители.[47]
Полифенолы встречаются в различных количествах в растительной пище и напитках, таких как овощи, фрукты, некоторые злаки и бобовые, чай, кофе и вино. Ингибирующее действие полифенолов на абсорбцию железа было показано с черным чаем и, в меньшей степени, с травяными чаями. [48,49] В зерновых и бобовых культурах полифенолы усиливают ингибирующий эффект фитата, как было показано в исследовании, сравнивающем сорго с высоким и низким содержанием полифенолов. [23]
Было показано, что кальций отрицательно влияет на абсорбцию негемового и гемового железа, что отличает его от других ингибиторов, влияющих только на абсорбцию негемового железа.[50] Дозозависимые ингибирующие эффекты были показаны при дозах 75–300 мг, когда кальций добавлялся в булочки, и при дозах 165 мг кальция из молочных продуктов. [51] Предполагается, что исследования однократного приема пищи показывают отрицательное влияние кальция на абсорбцию железа, тогда как исследования многократного приема пищи с большим разнообразием продуктов и различными концентрациями других ингибиторов и усилителей показывают, что кальций лишь ограниченно влияет на абсорбцию железа. [52]
Было показано, что животные белки, такие как молочные белки, яичные белки и альбумин, ингибируют абсорбцию железа.[53] Было показано, что две основные белковые фракции коровьего молока, казеин и сыворотка, а также яичный белок ингибируют абсорбцию железа у человека. [54] Белки сои также снижают всасывание железа. [55]
Конкуренция с железом
Исследования конкуренции показывают, что некоторые другие тяжелые металлы могут участвовать в пути всасывания железа в кишечнике. К ним относятся свинец, марганец, кобальт и цинк. Поскольку дефицит железа часто сочетается с интоксикацией свинцом, это взаимодействие может вызвать особенно серьезные медицинские осложнения у детей.[56]
Свинец является особенно опасным элементом для метаболизма железа. [57] Свинец поглощается механизмом поглощения железа (DTM1) и вторично блокирует железо за счет конкурентного торможения. Кроме того, свинец препятствует ряду важных железозависимых метаболических этапов, таких как биосинтез гема. Это многогранное влияние имеет особенно тяжелые последствия для детей, поскольку свинец не только вызывает анемию, но и может ухудшить когнитивное развитие. Свинец естественным образом присутствует в больших количествах в грунтовых водах и почве в некоторых регионах и может тайно нанести вред здоровью детей.По этой причине большинство педиатров в США обычно проверяют содержание свинца в раннем возрасте с помощью простого анализа крови.
ТРЕБОВАНИЯ К ЧЕЛОВЕКУ
В раннем детстве потребности в железе удовлетворяются за счет небольшого количества железа, содержащегося в грудном молоке. [58] Потребность в железе заметно возрастает через 4-6 месяцев после рождения и составляет около 0,7-0,9 мг / день в течение оставшейся части первого года [58]. В возрасте от 1 до 6 лет содержание железа в организме снова увеличивается вдвое. [58] Потребность в железе также очень высока у подростков, особенно в период скачка роста.У девочек обычно происходит скачок роста до менархе, но к этому времени рост не заканчивается. У мальчиков наблюдается заметное увеличение массы и концентрации гемоглобина в период полового созревания. На этой стадии потребности в железе повышаются до уровня, превышающего средние потребности в железе у менструирующих женщин [58] [см.].
Таблица 2
Потребность в железе 97,5% людей с точки зрения абсорбированного железа a , в разбивке по возрастным группам и полу (Всемирная организация здравоохранения, 1989) ее тело.Точный баланс между потреблением и потерей пищи поддерживает этот баланс. Около 1 мг железа теряется каждый день из-за отшелушивания клеток кожи и слизистых оболочек, включая слизистую оболочку желудочно-кишечного тракта. [59] Менструация увеличивает среднесуточную потерю железа примерно до 2 мг в день у взрослых женщин в пременопаузе. [60] Увеличение массы тела во время скачков роста в неонатальном и детском возрасте временно увеличивает потребность в железе. [61]
Потребление железа с пищей необходимо для восполнения потери железа с калом и мочой, а также через кожу.Эти базальные потери составляют примерно 0,9 мг железа для взрослого мужчины и 0,8 мг для взрослой женщины. [62] У женщин репродуктивного возраста необходимо учитывать потерю железа с менструальной кровью [].
ГРУППЫ ПОВЫШЕННОГО РИСКА
Наибольшая вероятность дефицита железа обнаруживается в тех частях населения, которые не имеют надлежащего доступа к пище, богатой усвояемым железом, во время стадий высокой потребности в железе. Эти группы соответствуют детям, подросткам и женщинам репродуктивного возраста, особенно во время беременности.[63,58]
У младенцев и подростков повышенная потребность в железе является результатом быстрого роста. Для женщин репродуктивного возраста основная причина — чрезмерная кровопотеря во время менструации. Во время беременности потребность в железе значительно возрастает из-за быстрого роста плаценты и плода, а также увеличения глобулярной массы. [63] Напротив, взрослые мужчины и женщины в постменопаузе имеют низкий риск дефицита железа, и количество железа в нормальном рационе обычно достаточно для удовлетворения их физиологических потребностей.[63]
ПОСЛЕДСТВИЯ И ПРИЧИНЫ ДЕФИЦИТА ЖЕЛЕЗА
Последствия дефицита железа
Дефицит железа определяется как состояние, при котором отсутствуют мобилизуемые запасы железа и при котором появляются признаки нарушения поступления железа в ткани, включая эритрон. , отмечены. [64] Дефицит железа может сопровождаться анемией или без нее. Некоторые функциональные изменения могут произойти и в отсутствие анемии, но наиболее функциональные нарушения, по-видимому, возникают при развитии анемии. [2] Даже легкие и умеренные формы железодефицитной анемии могут быть связаны с функциональными нарушениями, влияющими на когнитивное развитие [65], механизмы иммунитета [66] и работоспособность.[67] Дефицит железа во время беременности связан с множеством неблагоприятных исходов как для матери, так и для ребенка, включая повышенный риск сепсиса, материнской смертности, перинатальной смертности и низкой массы тела при рождении. [68] Дефицит железа и анемия также снижают способность к обучению и связаны с повышенным уровнем заболеваемости. [68]
Причины дефицита железа
Дефицит железа возникает в результате истощения запасов железа и возникает, когда абсорбция железа не может идти в ногу с метаболическими потребностями в железе для поддержания роста и восполнения потери железа, что в первую очередь связано с кровопотерей .[2] Основные причины дефицита железа включают низкое потребление биодоступного железа, повышенную потребность в железе в результате быстрого роста, беременности, менструации и избыточную кровопотерю, вызванную патологическими инфекциями, такими как анкилостомы и власоглавы, вызывающие потерю крови из желудочно-кишечного тракта [2] 69,70,71,72] и нарушение всасывания железа. [73] Частота дефицита железа увеличивается у девочек-подростков, потому что менструальные потери железа накладываются на потребность в быстром росте [74]. Другими факторами риска дефицита железа у молодых женщин являются высокий паритет, использование внутриматочной спирали и вегетарианская диета.[75]
Дефицит железа в питании возникает, когда физиологические потребности не могут быть удовлетворены за счет абсорбции железа из рациона. [72] Биодоступность пищевого железа низка в группах населения, потребляющих однообразные растительные диеты с небольшим количеством мяса. [72] Во многих развивающихся странах растительные продукты для отлучения от груди редко обогащены железом, а частота анемии превышает 50% у детей младше 4 лет. [64]
Когда запасы железа истощаются и железа недостаточно для эритропоэза, синтез гемоглобина в предшественниках эритроцитов нарушается и появляются гематологические признаки железодефицитной анемии.
ОЦЕНКА СТАТУСА ЖЕЛЕЗА
Дефицит железа и, в конечном итоге, анемия развиваются поэтапно и могут быть оценены путем измерения различных биохимических показателей. Хотя некоторые ферменты железа чувствительны к дефициту железа [63], их активность не использовалась в качестве успешного рутинного измерения статуса железа [2].
Лабораторные измерения необходимы для правильной диагностики дефицита железа. Они наиболее информативны, когда несколько показателей уровня железа исследуются и оцениваются в контексте питания и истории болезни.
Пул железа в плазме или сыворотке — это фракция всего железа в организме, которая циркулирует в основном связанном с трансферрином. Три способа оценки уровня железа в плазме или сыворотке включают: 1) измерение общего содержания железа в единице объема в мкг / дл; 2) измерение общего количества сайтов связывания для атомов железа на трансферрине, известного как общая железосвязывающая способность в мкг / дл 2 ; и 3) оценка процента двух сайтов связывания на всех занятых молекулах трансферрина, называемого процентным насыщением трансферрина.[76] Однако заметные биологические вариации этих значений могут возникать в результате суточных колебаний, наличия инфекции или воспалительных состояний и недавнего приема железа с пищей. [76]
Протопорфирин цинка отражает нехватку железа на последних стадиях синтеза гемоглобина, так что цинк вставляется в молекулу протопорфирина вместо железа. Протопорфирин цинка может быть обнаружен в эритроцитах с помощью флуориметрии и является мерой тяжести дефицита железа. [76]
Сывороточный ферритин является хорошим индикатором запасов железа в организме в большинстве случаев.Когда концентрация сывороточного ферритина ≥15 мкг / л, присутствуют запасы железа; более высокие концентрации отражают размер хранилища железа; при низкой концентрации (<12 мкг / л для детей младше 5 лет и <15 мкг / л для детей старше 5 лет) запасы железа истощаются. [76] Однако ферритин является белком-реагентом острой фазы, и его сывороточные концентрации могут быть повышены независимо от изменения запасов железа, инфекции или воспаления. [76,2] Это означает, что может быть трудно интерпретировать концентрацию ферритина там, где инфекция болезни распространены.
Еще одним индикатором статуса железа является концентрация TfR в сыворотке крови. Поскольку TfR в основном происходит из развивающихся эритроцитов, он отражает интенсивность эритропоэза и потребность в железе. Когда запасы железа истощаются, концентрация повышается при железодефицитной анемии, что указывает на серьезную недостаточность железа. Это при условии, что нет других причин аномального эритропоэза. [76] Клинические исследования показывают, что сывороточный TfR менее подвержен воспалению, чем сывороточный ферритин. [77] Основным преимуществом TfR как индикатора является возможность оценки величины функционального дефицита железа после истощения запасов железа.[78]
Отношение TfR к ферритину (TfR / ферритин) было разработано для оценки изменений как в накопленном железе, так и в функциональном железе и считается более полезным, чем TfR или ферритин отдельно. [79] TfR / ферритин использовался для оценки запасов железа в организме как у детей, так и у взрослых. [80] Однако высокая стоимость и отсутствие стандартизации анализа TfR до сих пор ограничивали применимость метода [81].
Низкая концентрация гемоглобина является показателем анемии, конечной стадии дефицита железа.[76,2]
АНЕМИЯ И ЕЕ ПРИЧИНЫ
Анемия описывает состояние, при котором количество эритроцитов в крови низкое или в клетках крови содержится меньше нормального гемоглобина. Человека, страдающего анемией, называют анемичным. Цель эритроцитов — доставлять кислород из легких в другие части тела. Молекула гемоглобина является функциональной единицей эритроцитов и представляет собой сложную белковую структуру, которая находится внутри эритроцитов. Несмотря на то, что эритроциты производятся в костном мозге, в их производство вовлечены многие другие факторы.Например, железо — очень важный компонент молекулы гемоглобина; эритропоэтин, молекула, секретируемая почками, способствует образованию эритроцитов в костном мозге.
Наличие правильного количества эритроцитов и профилактика анемии требует взаимодействия между почками, костным мозгом и питательными веществами в организме. Если почки или костный мозг не функционируют, или организм плохо питается, то нормальное количество и функции эритроцитов может быть трудно поддерживать.
Анемия на самом деле является признаком болезненного процесса, а не самой болезни.Обычно его классифицируют как хронический или острый. Хроническая анемия возникает в течение длительного периода времени. Острая анемия возникает быстро. Определение того, присутствует ли анемия в течение длительного времени или это что-то новое, помогает врачам найти причину. Это также помогает предсказать, насколько серьезными могут быть симптомы анемии. При хронической анемии симптомы обычно начинаются медленно и постепенно прогрессируют; тогда как при острой анемии симптомы могут быть резкими и более тревожными.
Эритроциты живут около 100 дней, поэтому организм постоянно пытается их заменить.У взрослых производство эритроцитов происходит в костном мозге. Врачи пытаются определить, вызвано ли низкое количество эритроцитов повышенной кровопотерей эритроцитов или их снижением в костном мозге. Знание того, изменилось ли количество лейкоцитов и / или тромбоцитов, также помогает определить причину анемии.
По оценкам Всемирной организации здравоохранения (ВОЗ), два миллиарда человек во всем мире страдают анемией и примерно 50% всех анемий объясняются дефицитом железа. [64] Это происходит на всех этапах жизненного цикла, но чаще встречается у беременных женщин и маленьких детей.[82] Анемия является результатом множества причин, которые можно изолировать, но чаще всего они сосуществуют. Некоторые из этих причин включают следующие:
Железодефицитная анемия
Наиболее важной и частой причиной анемии является дефицит железа. [82] Если потребление железа ограничено или неадекватно из-за плохого питания, в результате может возникнуть анемия. Это называется железодефицитной анемией. Железодефицитная анемия также может возникать при наличии язвы желудка или других источников медленного хронического кровотечения (рак толстой кишки, рак матки, полипы кишечника, геморрой и т. Д.).[83]
Анемия хронического заболевания
Любое длительное заболевание может привести к анемии. Этот тип анемии является вторым по распространенности после анемии, вызванной дефицитом железа, и развивается у пациентов с острым или хроническим системным заболеванием или воспалением. [84] Это состояние было названо «анемией воспаления» из-за повышенного содержания гепсидина, который блокирует как рециркуляцию железа из макрофагов, так и абсорбцию железа. [85]
Анемия из-за активного кровотечения
Потеря крови из-за обильного менструального кровотечения или ран может вызвать анемию.[82] Язвы желудочно-кишечного тракта или раковые заболевания, такие как рак толстой кишки, могут медленно терять кровь и также могут вызывать анемию. [86,87]
Анемия, связанная с заболеванием почек
Почки выделяют гормон эритропоэтин, который помогает костному мозгу сделать эритроциты. У людей с хроническим (длительным) заболеванием почек выработка этого гормона снижена, а это, в свою очередь, снижает выработку эритроцитов, вызывая анемию. [88] Хотя дефицит эритропоэтина является основной причиной анемии при хронической почечной недостаточности, это не единственная причина.Следовательно, необходимо минимальное обследование, чтобы исключить дефицит железа и другие аномалии клеточной линии. [89]
Анемия, связанная с беременностью
Увеличение объема плазмы во время беременности приводит к разбавлению эритроцитов и может проявляться как анемия. [90] Железодефицитная анемия составляет 75% всех анемий во время беременности. [90]
Анемия, связанная с плохим питанием
Витамины и минералы необходимы для образования эритроцитов. Помимо железа, для правильного производства гемоглобина необходимы витамин B12, виамин А, фолиевая кислота, рибофлавин и медь.[82] Дефицит любого из этих питательных микроэлементов может вызвать анемию из-за недостаточного производства эритроцитов. Плохое питание — важная причина низкого уровня витаминов и, как следствие, анемии.
Ожирение и анемия
Ожирение характеризуется хроническим слабым системным воспалением, повышенным уровнем гепсидина, которое, в свою очередь, связано с анемией хронического заболевания. Ausk и Ioannou [91] предположили, что ожирение может быть связано с особенностями анемии хронического заболевания, включая низкую концентрацию гемоглобина, низкое содержание железа и трансферрина в сыворотке, а также повышенный уровень ферритина в сыворотке.Избыточный вес и ожирение были связаны с изменениями сывороточного железа, насыщения трансферрина и ферритина, которые, как ожидается, произойдут в условиях хронического системного воспаления. Воспаление, связанное с ожирением, может повышать концентрацию гепсидина и снижать доступность железа. Aeberli и др. ., [92] сравнили уровень железа, потребление железа с пищей и его биодоступность, а также циркулирующие уровни гепсидина, лептина и интерлейкина-6 (ИЛ-6) у детей с избыточной массой тела и детей с нормальным весом.Они указали, что существует пониженная доступность железа для эритропоэза у детей с избыточным весом, и что это, вероятно, связано с опосредованным гепсидином сниженным всасыванием железа и / или повышенным секвестрацией железа, а не с низким содержанием железа с пищей.
Алкоголизм
Алкоголь оказывает многочисленные неблагоприятные эффекты на различные типы клеток крови и их функции. [93] У алкоголиков часто есть дефектные эритроциты, которые преждевременно разрушаются. [93,94] Сам по себе алкоголь также может быть токсичным для костного мозга и может замедлять производство эритроцитов.[93,94] Кроме того, с алкоголизмом связаны плохое питание и дефицит витаминов и минералов. [95] Сочетание этих факторов может привести к анемии у алкоголиков.
Серповидно-клеточная анемия
Серповидно-клеточная анемия — одно из наиболее распространенных наследственных заболеваний. [96] Это заболевание, связанное с кровью, которое влияет на молекулу гемоглобина и приводит к изменению формы всей клетки крови в стрессовых условиях [97]. В таком состоянии проблема с гемоглобином бывает качественной или функциональной.Аномальные молекулы гемоглобина могут вызвать проблемы в целостности структуры эритроцитов, и они могут стать серповидными (серповидные клетки). [97] Существуют разные типы серповидно-клеточной анемии разной степени тяжести. Это особенно распространено у африканцев, ближневосточных и средиземноморских предков. [97]
Талассемия
Это еще одна группа причин анемии, связанных с гемоглобином, которая связана с отсутствием или ошибками в генах, ответственных за выработку гемоглобина. [97] Молекула гемоглобина имеет субъединицы, обычно называемые альфа- и бета-цепями глобина.Отсутствие определенной субъединицы определяет тип альфа- или бета-талассемии. [97,98] Существует много типов талассемии, которые различаются по степени тяжести от легкой (малая талассемия) до тяжелой (большая талассемия). [98] Они также являются наследственными, но вызывают количественные аномалии гемоглобина, то есть вырабатывается недостаточное количество молекул правильного типа. Альфа- и бета-талассемии являются наиболее распространенными наследственными моногенными заболеваниями в мире с наибольшей распространенностью в районах, где малярия была или все еще является эндемической.[97]
Апластическая анемия
Апластическая анемия — это заболевание, при котором разрушается костный мозг и снижается выработка клеток крови. [99] Это вызывает дефицит всех трех типов клеток крови (панцитопения), включая эритроциты (анемия), лейкоциты (лейкопения) и тромбоциты (тромбоцитопения). [100,101] Многие распространенные лекарства могут иногда вызывать этот тип анемии в качестве побочного эффекта. у некоторых людей. [99]
Гемолитическая анемия
Гемолитическая анемия — это тип анемии, при которой происходит разрыв эритроцитов, известный как гемолиз, который разрушается быстрее, чем костный мозг может их заменить.[102] Гемолитическая анемия может возникнуть по разным причинам и часто классифицируется как приобретенная или наследственная. Распространенными приобретенными причинами гемолитической анемии являются аутоиммунитет, микроангиопатия и инфекции. Нарушения ферментов эритроцитов, мембран и гемоглобина вызывают наследственную гемолитическую анемию. [102]
ПРЕДОТВРАЩЕНИЕ НЕДОСТАТОЧНОСТИ ЖЕЛЕЗА (СТРАТЕГИИ ВМЕШАТЕЛЬСТВА)
Четыре основных стратегии коррекции эффективности микронутриентов в популяциях могут использоваться для коррекции дефицита железа, как по отдельности, так и в комбинации.Это обучение в сочетании с модификацией диеты для улучшения потребления железа и его биодоступности; добавление железа (обеспечение железом, обычно в более высоких дозах, без еды), обогащение пищевых продуктов железом и новый подход к биофортификации. Однако есть некоторые трудности в применении некоторых из этих стратегий при рассмотрении железа.
Диверсификация продуктов питания
Модификации диеты для сокращения потребления Индийской стоматологической ассоциации включают увеличение потребления продуктов, богатых железом, особенно мясных продуктов, увеличение потребления фруктов и овощей, богатых аскорбиновой кислотой, для увеличения абсорбции негемового железа и снижение потребления чая и кофе, что подавляют всасывание негемового железа.[103,58] Другая стратегия — снизить содержание антинутриентов, чтобы сделать железо, поступающее из их пищевых источников, более доступным. Биодоступность железа может быть увеличена такими методами, как проращивание и ферментация, которые способствуют ферментативному гидролизу фитиновой кислоты в цельнозерновых зерновых и бобовых культурах за счет повышения активности эндогенных или экзогенных ферментов фитазы. [104] Даже использование неферментативных методов, таких как термическая обработка, замачивание и измельчение, для снижения содержания фитиновой кислоты в основных продуктах растительного происхождения было успешным в улучшении биодоступности железа (и цинка).[105,106]
Добавка
Для перорального приема добавок железа предпочтительны соли двухвалентного железа (сульфат двухвалентного железа и глюконат двухвалентного железа) из-за их низкой стоимости и высокой биодоступности. [72] Хотя абсорбция железа выше при приеме добавок железа натощак, тошнота и боль в эпигастрии могут развиться из-за введенных более высоких доз железа (обычно 60 мг Fe / день). Если возникают такие побочные эффекты, следует попытаться снизить дозу между приемами пищи или давать железо во время еды, хотя пища снижает всасывание лекарственного железа примерно на две трети.[107] Добавки железа во время беременности рекомендуется в развивающихся странах, где женщины часто вступают в беременность с низкими запасами железа. [108] Хотя обычно считалось, что польза от приема добавок железа перевешивает предполагаемый риск, есть некоторые свидетельства того, что добавление в дозах, рекомендованных для здоровых детей, несет в себе риск увеличения тяжести инфекционного заболевания на фоне малярии. [109,110]
Обогащение
Обогащение пищевых продуктов железом сложнее, чем обогащение такими питательными веществами, как цинк в муке, йод в соли и витамин А в кулинарном масле.[72] Наиболее биодоступные соединения железа растворимы в воде или разбавленной кислоте, но часто вступают в реакцию с другими пищевыми компонентами, вызывая неприятный запах, изменение цвета или окисление жиров. [103] Таким образом, менее растворимые формы железа, хотя и хуже усваиваются, часто выбираются для обогащения, чтобы избежать нежелательных сенсорных изменений. [72] Обогащение обычно производится с гораздо более низкими дозами железа, чем с добавками. Это ближе к физиологической среде и может быть самым безопасным вмешательством в малярийные районы. [111] Нет никаких опасений по поводу безопасности добавок железа или обогащения железа в немалярийных эндемичных районах.[112]
Соединения железа, рекомендованные [7] для обогащения пищевых продуктов, включают сульфат железа, фумарат железа, пирофосфат железа и порошок электролитического железа. Пшеничная мука является наиболее распространенным пищевым продуктом, обогащенным железом, и она обычно обогащается порошками элементарного железа, которые не рекомендуются ВОЗ. [7,113] Харрелл и Эгли [23] сообщили, что из 78 национальных программ по пшеничной муке только восемь улучшатся. статус железа. В этих программах использовались рекомендуемые соединения железа на рекомендованных уровнях.Другие страны использовали не рекомендуемые соединения или более низкие уровни железа по сравнению с потреблением муки. Коммерческое детское питание, такое как смеси и злаки, также обычно обогащено железом.
Биофортификация
Содержание железа варьируется от 25 до 56 мг / кг в различных сортах пшеницы и от 7 до 23 мг / кг в рисовых зернах. Однако большая часть этого железа удаляется в процессе измельчения. Поглощение железа зерновыми и бобовыми культурами, многие из которых имеют высокое содержание самородного железа, обычно низкое из-за высокого содержания в них фитата, а иногда и полифенолов.[48] Стратегии биофортификации включают селекцию растений и генную инженерию. Уровни железа в обычных бобах и просе были успешно увеличены путем селекции растений, но использование других основных продуктов питания является более трудным или невозможным (рис) из-за недостаточной естественной генетической изменчивости. Lucca и др. ., [114] увеличили содержание железа в эндосперме риса, чтобы улучшить его всасывание в кишечнике человека с помощью генной инженерии. Они ввели ген ферритина из Phaseolus vulgaris в рисовые зерна, увеличив содержание железа в них вдвое.Чтобы увеличить биодоступность железа, они ввели в эндосперм риса термотолерантную фитазу из Aspergillus fumigatus . Они указали, что этот рис с более высоким содержанием железа и богатой фитазой имеет большой потенциал для существенного улучшения питания железом в тех популяциях, где дефицит железа так широко распространен. [114] К сожалению, фитаза не устояла перед приготовлением. Важность различных минералов, таких как цинк [115] и железо, требует большего внимания на индивидуальном уровне и уровне общественного здравоохранения.
Сноски
Источник поддержки: Нет
Конфликт интересов: Не объявлен.
СПИСОК ЛИТЕРАТУРЫ
1. Борода Дж. Л., Доусон HD. Утюг. В: О’Делл Б.Л., Сунде Р.А., редакторы. Справочник по незаменимым в питании минеральным элементам. Нью-Йорк: CRC Press; 1997. С. 275–334. [Google Scholar] 2. Вуд Р.Дж., Ронненберг А. Железо. В: Shils ME, Shike M, Ross AC, Caballero B, Cousins RJ, редакторы. Современное питание в здоровье и болезнях. 10-е изд. Балтимор: Липпинкотт Уильямс и Уилкинс; 2005 г.С. 248–70. [Google Scholar] 3. Макдауэлл LR. 2-е изд. Амстердам: Elsevier Science; 2003. Минералы в питании животных и человека; п. 660. [Google Scholar] 4. Гуггенхайм KY. Хлороз: возникновение и исчезновение болезни, связанной с питанием. J Nutr. 1995; 125: 1822–5. [PubMed] [Google Scholar] 5. Ип Р., Даллман PR. Утюг. В: Ziegler EE, Filer LJ, редакторы. Присутствуют знания в области питания. 7-е изд. Вашингтон, округ Колумбия: ILSI Press; 1996. С. 278–92. [Google Scholar] 6. Андервуд Э.Дж., Саттл Н.Ф. 3-е изд. Уоллингфорд: международное издательство CABI; 1999 г.Минеральное питание скота; п. 614. [Google Scholar] 7. Аллен Л., де Бенуа Б., Дари О., Харрелл Р., редакторы. Женева: ВОЗ и ФАО; 2006. ВОЗ. Рекомендации по обогащению пищевых продуктов микронутриентами; п. 236. [Google Scholar] 8. Брабин Б.Дж., Премжи З., Верхое ff Ф. Анализ анемии и детской смертности. J Nutr. 2001; 131: 636–45С. [PubMed] [Google Scholar] 9. Quintero-Gutiérrez AG, González-Rosendo G, Sánchez-Muñoz J, Polo-Pozo J, Rodríguez-Jerez JJ. Биодоступность гемового железа в начинке для печенья с использованием поросят в качестве модели животных для человека.Int J Biol Sci. 2008; 4: 58–62. [Бесплатная статья PMC] [PubMed] [Google Scholar] 10. Айзен П., Эннс С., Весслинг-Резник М. Химия и биология метаболизма железа в эукариотах. Int J Biochem Cell Biol. 2001; 33: 940–59. [PubMed] [Google Scholar] 11. Лиу П. Т., Хейскала М., Петерсон П. А., Ян Ю. Роль железа в здоровье и болезнях. Мол Аспекты Мед. 2001; 2: 1–87. [PubMed] [Google Scholar] 12. Guerinot ML. Транспорт микробного железа. Annu Rev Microbiol. 1994; 48: 743–72. [PubMed] [Google Scholar] 13. Асквит К., Каплан Дж.Транспорт железа и меди в дрожжах и его значение для болезней человека. Trends Biochem Sci. 1998. 23: 135–8. [PubMed] [Google Scholar] 15. Вашингтон, округ Колумбия: Национальная академия прессы; 2001. МОМ. Институт медицины. утюг. В: Нормы потребления витамина A, витамина K, мышьяка, бора, хрома, меди, йода, железа, марганца, молибдена, никеля, кремния, ванадия и цинка; С. 290–393. [PubMed] [Google Scholar] 16. Muir A, Hopfer U. Региональная специфичность поглощения железа щеточно-граничными мембранами тонкого кишечника у нормальных мышей и мышей с дефицитом железа.Am J Physiol. 1985; 248: G376–9. [PubMed] [Google Scholar] 17. Фрейзер Д.М., Андерсон Г.Дж. Импорт железа. I. Абсорбция железа в кишечнике и ее регуляция. Am J Physiol Gastrointest Liver Physiol. 2005; 289: G631–5. [PubMed] [Google Scholar] 18. Наддур С.С., Шрирама К., Мудипалли А. Механизмы транспорта и гомеостаза железа: их роль в здоровье и болезнях. Индийский J Med Res. 2008; 128: 533–44. [PubMed] [Google Scholar] 20. Yeh KY, Yeh M, Mims L, Glass J. Кормление железом индуцирует миграцию и взаимодействие ферропортина 1 и гефестина в двенадцатиперстном эпителии крыс.Am J Physiol Gastrointest Liver Physiol. 2009. 296: 55–65. [Бесплатная статья PMC] [PubMed] [Google Scholar] 21. Тейл Э.С., Чен Х., Миранда С., Янсер Х., Эльзенханс Б., Нуньес М.Т. и др. Абсорбция железа из ферритина не зависит от гемового железа и солей двухвалентного железа у женщин и сегментов кишечника крыс. J Nutr. 2012; 142: 478–83. [Бесплатная статья PMC] [PubMed] [Google Scholar] 22. Hoppler M, Schoenbaechler A, Meile L, Hurrell RF, Walczyk T. Ферритин-железо высвобождается во время кипячения и in vitro при пищеварении в желудке .J Nutr. 2008. 138: 878–84. [PubMed] [Google Scholar] 23. Hurrell R, Egli I. Биодоступность железа и диетические контрольные значения. Am J Clin Nutr. 2010; 91: 1461–7S. [PubMed] [Google Scholar] 25. Немет Э., Ганц Т. Регулирование метаболизма железа гепсидином. Анну Рев Нутр. 2006; 26: 323–42. [PubMed] [Google Scholar] 26. Немет Э., Таттл М.С., Пауэлсон Дж., Вон М.Б., Донован А., Уорд Д.М. и др. Гепсидин регулирует отток клеточного железа, связываясь с ферропортином и индуцируя его интернализацию. Наука. 2004; 306: 2090–3.[PubMed] [Google Scholar] 28. Браун В., Киллманн Х. Бактериальные решения проблемы снабжения железом. Trends Biochem Sci. 1999; 24: 104–109. [PubMed] [Google Scholar] 29. Хант-младший. Насколько важна биодоступность железа с пищей? Am J Clin Nutr. 2001; 73: 3–4. [PubMed] [Google Scholar] 30. Хант-младший, Зито, Калифорния, Джонсон, Лос-Анджелес. Выведение железа из организма здоровыми мужчинами и женщинами. Am J Clin Nutr. 2009; 89: 1–7. [PubMed] [Google Scholar] 31. Фэрбенкс В.Ф. Железо в медицине и питании. В: Shils ME, Shike M, Ross AC, Caballero B, Cousins RJ, редакторы.Современное питание в здоровье и болезнях. 10-е изд. Балтимор: Липпинкотт Уильямс и Уилкинс; 1999. С. 193–221. [Google Scholar] 32. потребности человека в витаминах и минералах. Рим: ФАО; 2001. ФАО / ВОЗ. Пищевые подходы к удовлетворению потребностей в витаминах и минералах; С. 7–25. [Google Scholar] 33. Monsen ER, Hallberg L, Layrisse M, Hegsted DM, Cook JD, Mertz W. и др. Оценка доступного пищевого железа. Am J Clin Nutr. 1978; 31: 134–41. [PubMed] [Google Scholar] 34. Конрад ME, Umbreit JN. Краткий обзор: абсорбция железа — путь муцин-мобилферрин-интегрин.Конкурентоспособный путь поглощения металлов. Am J Hematol. 1993; 42: 67–73. [PubMed] [Google Scholar] 35. Конрад М.Э., Шаде С.Г. Хелаты аскорбиновой кислоты в абсорбции железа: роль соляной кислоты и желчи. Гастроэнтерология. 1968; 55: 35–45. [PubMed] [Google Scholar] 36. Холлберг Л., Брюн М., Россандер Л. Поглощение железа у человека: аскорбиновая кислота и дозозависимое ингибирование фитатом. Am J Clin Nutr. 1989; 49: 140–4. [PubMed] [Google Scholar] 37. Зигенберг Д., Бейнс Р.Д., Ботвелл Т.Х., Макфарлейн Б.Дж., Лампарелли Р.Д., Car NG и др.Аскорбиновая кислота предотвращает дозозависимое ингибирующее действие полифенолов и фитатов на абсорбцию негемового железа. Am J Clin Nutr. 1991; 53: 537–41. [PubMed] [Google Scholar] 38. Стекель А., Оливарес М., Писарро Ф., Чадуд П., Лопес И., Амар М. Поглощение обогащающего железа из молочных смесей у младенцев. Am J Clin Nutr. 1986; 43: 917–22. [PubMed] [Google Scholar] 39. Бюллетень D, Бейнс Р.Д., Ботвелл Т.Х., Гиллули М., Макфарлейн Б.Дж., Макфейл А.П. и др. Влияние фруктовых соков и фруктов на усвоение железа из рисовой муки.Br J Nutr. 1987; 57: 331–43. [PubMed] [Google Scholar] 40. Линч SR, Кук JD. Взаимодействие витамина С и железа. Ann N Y Acad Sci. 1980; 355: 32–44. [PubMed] [Google Scholar] 41. Teucher B, Olivares M, Cori H. Усилители поглощения железа: аскорбиновая кислота и другие органические кислоты. Int J Vitam Nutr Res. 2004; 74: 403–19. [PubMed] [Google Scholar] 42. Линч С.Р., Харрелл Р.Ф., Дассенко С.А., Кук Дж.Д. Влияние пищевых белков на биодоступность железа у человека. Adv Exp Med Biol. 1989; 249: 117–32. [PubMed] [Google Scholar] 43.Бьорн-Расмуссен Э., Халльберг Л. Влияние животных белков на усвоение пищевого железа человеком. Нутр Метаб. 1979; 23: 192–202. [PubMed] [Google Scholar] 44. Редди МБ, Харрелл Р.Ф., Кук JD. Разнообразное питание незначительно влияет на всасывание негемового железа у нормальных людей. J Nutr. 2006; 136: 576–81. [PubMed] [Google Scholar] 45. Бах Кристенсен М., Хелс О, Морберг С., Марвинг Дж., Бугель С., Тетенс I. Свинина увеличивает усвоение железа при 5-дневной полностью контролируемой диете по сравнению с вегетарианской диетой с аналогичным содержанием витамина С и фитиновой кислоты.Br J Nutr. 2005. 94: 78–83. [PubMed] [Google Scholar] 46. Харрелл Р.Ф., Джуллерат М.А., Редди М.Б., Линч С.Р., Дассенко С.А., Кук Дж.Д. Соевый белок, фитат и абсорбция железа у человека. Am J Clin Nutr. 1992; 56: 573–8. [PubMed] [Google Scholar] 47. Hurrell RF. Разложение фитиновой кислоты как средство улучшения усвоения железа. Int J Vitam Nutr Res. 2004. 74: 445–52. [PubMed] [Google Scholar] 48. Харрелл Р.Ф., Редди М., Кук Дж. Д.. Подавление абсорбции негемного железа у человека напитками, содержащими полифенолы. Br J Nutr.1999. 81: 289–95. [PubMed] [Google Scholar] 49. Холлберг Л., Россандер Л. Влияние различных напитков на усвоение негемового железа из сложных блюд. Hum Nutr Appl Nutr. 1982; 36: 116–23. [PubMed] [Google Scholar] 50. Hallberg L, Rossander-Hulthen L, Brune M, Gleerup A. Ингибирование усвоения гемового железа у человека кальцием. Br J Nutr. 1993; 69: 533–40. [PubMed] [Google Scholar] 51. Hallberg L, Rossander-Hulthen L. Потребность в железе у менструирующих женщин. Am J Clin Nutr. 1991; 54: 1047–58. [PubMed] [Google Scholar] 52.Линч SR. Влияние кальция на усвоение железа. Nutr Res Rev.2000; 13: 141–58. [PubMed] [Google Scholar] 53. Кук JD, Monsen ER. Поглощение пищевого железа у людей. III. Сравнение влияния животных белков на всасывание негемового железа. Am J Clin Nutr. 1976; 29: 859–67. [PubMed] [Google Scholar] 54. Харрелл РФ, Линч С.Р., Тринидад Т.П., Дассенко С.А., Кук Дж.Д. Абсорбция железа у людей: бычий сывороточный альбумин по сравнению с говяжьими мышцами и яичным белком. Am J Clin Nutr. 1988. 47: 102–7. [PubMed] [Google Scholar] 55.Линч С.Р., Дассенко С.А., Кук Дж.Д., Джульерат М.А., Харрелл РФ. Ингибирующий эффект фрагмента, связанного с соевым белком, на абсорбцию железа у людей. Am J Clin Nutr. 1994; 60: 567–72. [PubMed] [Google Scholar] 56. Piomelli S, Seaman C, Kapoor S. Вызванные свинцом аномалии метаболизма порфирина, связь с дефицитом железа. Ann N Y Acad Sci. 1987; 514: 278–88. [PubMed] [Google Scholar] 58. 2-е изд. Бангкок: 2004 г. ФАО / ВОЗ. Консультации экспертов по потребностям человека в витаминах и минералах, потребностях в витаминах и минералах в питании человека: отчет совместного экспертного заключения ФАО / ВОЗ; п.341. [Google Scholar] 59. Cook JD, Skikne BS, Lynch SR, Reusser ME. Оценки достаточности железа у населения США. Кровь. 1986; 68: 726–31. [PubMed] [Google Scholar] 60. Ботвелл TH, Чарльтон RW. Общий подход к проблемам железодефицита и перегрузки железом у населения в целом. Semin Hematol. 1982; 19: 54–67. [PubMed] [Google Scholar] 61. Гибсон Р.С., Макдональд А.С., Смит-Вандеркой П.Д. Параметры сывороточного ферритина и пищевого железа в выборке канадских детей дошкольного возраста. J Can Dietetic Assoc.1988; 49: 23–8. [Google Scholar] 62. ДеМайер Э.М., Даллман П., Герни Дж. М., Холлберг Л., Суд С. К., Срикантия С. Г., редакторы. Женева: Всемирная организация здравоохранения; 1989. ВОЗ. Профилактика и контроль железодефицитной анемии с помощью первичной медико-санитарной помощи: руководство для администраторов здравоохранения и руководителей программ; п. 58. [Google Scholar] 63. Даллман П. Айрон. В: Браун М.Л., редактор. Настоящие знания в области питания. 6-е изд. Вашингтон, округ Колумбия: Фонд питания; 1990. С. 241–50. [Google Scholar] 64. Женева: Швейцария: Всемирная организация здравоохранения; 2001 г.ВОЗ / ЮНИСЕФ / УООН. Оценка, профилактика и контроль железодефицитной анемии; п. 114. [Google Scholar] 65. Борода Дж. Л., Коннор-младший. Статус железа и нейронное функционирование. Анну Рев Нутр. 2003. 23: 41–58. [PubMed] [Google Scholar] 66. Failla ML. Микроэлементы и защита хозяина: последние достижения и сохраняющиеся проблемы. J Nutr. 2003; 133: S1443–7. [PubMed] [Google Scholar] 67. Витери Ф.Е., Торунь Б. Анемия и физическая работоспособность. В: Гарби Л., редактор. Клиники гематологии. Vol. 3. Лондон: У. Б. Сондерс; 1974. стр.609–26. [Google Scholar] 68. CDC. Табель успеваемости по грудному вскармливанию, США: показатели результатов (публикация из Центров по контролю и профилактике заболеваний, Национальное обследование иммунизации. 2010 г. [последний доступ 11 мая 2010 г.]. Http://www.cdc.gov/breastfeeding/data/index .htm .69. Купер Е.С., Банди Д.А. Трихоцефалопатия. Ballieres Clin Trop Med Commun Dis. 1987; 2: 629–43. [Google Scholar] 70. Всемирная организация здравоохранения, Женева; 1995. ВОЗ. Отчет неофициальной консультации ВОЗ. на анкилостомоз и анемию у девочек и женщин; с.46. [Google Scholar] 71. Crompton DW, Nesheim MC. Пищевая ценность кишечных гельминтозов в течение жизненного цикла человека. Анну Рев Нутр. 2002; 22: 35–99. [PubMed] [Google Scholar] 72. Ларок Р., Касапиа М., Готуццо Е., Дьеркос Т.В. Взаимосвязь между интенсивностью заражения гельминтами, передающимися через почву, и анемией во время беременности. Am J Trop Med Hyg. 2005; 73: 783–9. [PubMed] [Google Scholar] 73. Циммерманн МБ, Харрелл РФ. Недостаток пищевого железа. Ланцет. 2007; 370: 115–20. [Google Scholar] 74. Харви LJ, Armah CN, Dainty JR, Foxall RJ, John Lewis D, Langford NJ и др.Влияние менструальной кровопотери и диеты на дефицит железа у женщин в Великобритании. Br J Nutr. 2005. 94: 557–64. [PubMed] [Google Scholar] 75. Борода JL. Потребность в железе у девочек-подростков. Симпозиум: Повышение уровня железа у подростков до деторождения. J Nutr. 2000; 130: S440–2. [PubMed] [Google Scholar] 77. Бегин Ю. Растворимый рецептор трансферрина для оценки эритропоэза и статуса железа. Clinica Chimica Acta. 2003. 329: 9–22. [PubMed] [Google Scholar] 79. Повар JD, Flowers CH, Skikne BS. Количественная оценка bodyiron.Кровь. 2003. 101: 3359–64. [PubMed] [Google Scholar] 80. Кук JD, Boy E, Flowers C, Daroca Mdel C. Влияние высокогорной жизни на железо тела. Кровь. 2005; 106: 1441–6. [PubMed] [Google Scholar] 81. Ян З., Дьюи К.Г., Лоннердал Б., Хернелл О., Чапарро С., Аду-Афарвуа С. и др. Сравнение концентрации ферритина в плазме с соотношением рецептора трансферрина в плазме и ферритина для оценки запасов железа в организме: результаты 4 интервенционных испытаний. Am J Clin Nutr. 2008; 87: 1892–8. [PubMed] [Google Scholar] 82.Де Бенуа Б., Маклин Э., Эгли И., Когсуэлл М. — редакторы. Женева: Пресса ВОЗ, Всемирная организация здравоохранения; 2008. ВОЗ / CDC. Библиотечная каталогизация в публикации. Распространенность анемии в мире, 1993–2005 гг .: глобальная база данных ВОЗ по анемии; п. 40. [Google Scholar] 83. Джонсон-Уимбли Т.Д., Грэм Д.Ю. Диагностика и лечение железодефицитной анемии в 21 веке. Ther Adv Гастроэнтерол. 2011; 4: 177–84. [Бесплатная статья PMC] [PubMed] [Google Scholar] 84. Зарычанский Р., Хьюстон Д.С. Анемия хронического заболевания: вредное заболевание или адаптивная, полезная реакция? Can Med Assoc J.2008. 179: 333–7. [Бесплатная статья PMC] [PubMed] [Google Scholar] 85. Weiss G, Goodnough LT. Анемия хронического заболевания. N Engl J Med. 2005; 352: 1011–23. [PubMed] [Google Scholar] 86. 2-е изд. Женева: 2004 г. ВОЗ / CDC. Отчет о совместной технической консультации Всемирной организации здравоохранения / Центров по контролю и профилактике заболеваний по оценке статуса железа на уровне населения; п. 108. [Google Scholar] 87. Knight K, Wade S, Balducci L. Распространенность и исходы анемии при раке: систематический обзор литературы.Am J Med. 2004; 116: 11–26С. [PubMed] [Google Scholar] 88. О’Мара NB. Больные анемией с хроническими заболеваниями почек. Спектр диабета. 2008; 21: 12–9. [Google Scholar] 89. Нурко С. Анемия при хронической болезни почек: причины, диагностика, лечение. Cleve Clin J Med. 2006. 73: 289–97. [PubMed] [Google Scholar] 90. Горовиц К.М., Ингардия С.Дж., Боргида А.Ф. 2013, Анемия при беременности. Clin Lab Med. 2013; 33: 281–91. [PubMed] [Google Scholar] 91. Ауск К.Дж., Иоанну Г.Н. Связано ли ожирение с анемией хронического заболевания? Популяционное исследование.Ожирение. 2008. 16: 2356–61. [PubMed] [Google Scholar] 92. Aeberli I, Hurrell RF, Zimmermann MB. Дети с избыточным весом имеют более высокие концентрации циркулирующего гепсидина и более низкий статус железа, но их потребление железа с пищей и биодоступность сопоставимы с детьми с нормальным весом. Int J Obes. 2009; 33: 1111–7. [PubMed] [Google Scholar] 94. Lewis G, Wise MP, Poynton C, Godkin A. Случай стойкой анемии и злоупотребления алкоголем. Нат Клин Практ Гастроэнтерол Гепатол. 2007; 4: 521–6. [PubMed] [Google Scholar] 95. Lindenbaum J, Роман MJ.Пищевая анемия при алкоголизме. Am J Clin Nutr. 1980; 33: 2727–35. [PubMed] [Google Scholar] 96. Cox SE, L’Esperance V, Makani J, Soka D, Prentice AM, Hill CM и др. Серповидно-клеточная анемия: доступность железа и ночная оксиметрия. J Clin Sleep Med. 2012; 8: 541–5. [Бесплатная статья PMC] [PubMed] [Google Scholar] 98. Манси Х.Л., младший, Кэмпбелл Дж. Альфа- и бета-талассемия. Я семейный врач. 2009; 80: 339–44. [PubMed] [Google Scholar] 99. Сегель ГБ, Лихтман М.А. Апластическая анемия: приобретенная и наследственная. В: Каушанский К., Вильямс В.Дж., редакторы.Гематология Вильямса. 8-е изд. Нью-Йорк: McGraw-Hill Medical; 2010. С. 569–90. [Google Scholar] 100. Янг Н.С., Каладо Р.Т., Шейнберг П. Современные концепции патофизиологии и лечения апластической анемии. Кровь. 2006; 108: 2509–19. [Бесплатная статья PMC] [PubMed] [Google Scholar] 101. Шейнберг П., Чен Дж. Апластическая анемия: что мы узнали на моделях на животных и в клинике. Semin Hematol. 2013; 50: 156–64. [PubMed] [Google Scholar] 102. Dhaliwal G, Cornett PA, Tierney LM., Jr Гемолитическая анемия.Я семейный врач. 2004. 69: 2599–606. [PubMed] [Google Scholar] 103. Hurrell RF. Как обеспечить адекватное усвоение железа из продуктов, обогащенных железом. Nutr Rev. 2002; 60: S7–15. [PubMed] [Google Scholar] 104. Повар JD. Диагностика и лечение железодефицитной анемии. Лучшая практика Res Clin Haematol. 2005; 18: 319–32. [PubMed] [Google Scholar] 105. Schlemmer U, Frølich W, Prieto RM, Grases F. Фитат в пищевых продуктах и значение для человека: источники пищи, потребление, обработка, биодоступность, защитная роль и анализ.Mol Nutr Food Res. 2009; 53: S330–75. [PubMed] [Google Scholar] 106. Лян Дж., Хан Б.З., Ноут М.Дж., Хамер Р.Дж. Влияние замачивания, прорастания и ферментации на общую фитиновую кислоту и растворимый цинк in vitro в коричневом рисе. Food Chem. 2008; 110: 821–8. [PubMed] [Google Scholar] 107. Кавалли-Сфорца Т., Бергер Дж., Смитасири С., Витери Ф. Еженедельное употребление добавок железа и фолиевой кислоты для женщин репродуктивного возраста: обзор воздействия, извлеченные уроки, планы расширения и вклад в достижение целей развития тысячелетия.Nutr Rev.2005; 63: S152–8. [PubMed] [Google Scholar] 109. Oppenheimer SJ. Железо и его отношение к иммунитету и инфекционным заболеваниям. J Nutr. 2001; 131: S616–33. [PubMed] [Google Scholar] 110. Sazawal S, Black RE, Ramsan M, Chwaya HM, Stoltzfus RJ, Dutta A и др. Влияние обычных профилактических добавок с железом и фолиевой кислотой на госпитализацию и смертность детей дошкольного возраста в условиях высокой передачи малярии: рандомизированное плацебо-контролируемое исследование на уровне общины. Ланцет. 2006; 367: 133–43.[PubMed] [Google Scholar] 112. Hurrell RF. Обогащение железом: его эффективность и безопасность в отношении инфекций. Еда Nutr Bull. 2007. 28: 585–94. [PubMed] [Google Scholar] 114. Лукка П., Харрелл Р., Потрикус И. Борьба с железодефицитной анемией с помощью риса, богатого железом. J Am Coll Nutr. 2002; 21: 184С – 90. [PubMed] [Google Scholar] 115. Рухани Н., Харрелл Р., Келишади Р., Шулин Р. Цинк и его значение для здоровья человека: интегративный обзор. J Res Med Sci. 2013; 18: 144–57. [Бесплатная статья PMC] [PubMed] [Google Scholar]Обзор железа и его значения для здоровья человека
J Res Med Sci.2014 фев; 19 (2): 164–174.
Назанин Аббаспур
Департамент наук о системах окружающей среды, Институт наземных экосистем, Швейцарский федеральный технологический институт, Цюрих, Швейцария
Ричард Харрелл
1 Департамент здравоохранения и технологий, Лаборатория питания человека, Институт пищевых продуктов , Питание и здоровье, Швейцарский федеральный технологический институт, Цюрих, Швейцария
Роя Келишади
2 Исследовательский центр детского роста и развития, Исфаханский университет медицинских наук, Исфахан, Иран
Департамент науки о системах окружающей среды, Институт наземных исследований Экосистема, Швейцарский федеральный технологический институт, Цюрих, Швейцария
1 Департамент медицинских наук и технологий, Лаборатория питания человека, Институт питания, питания и здоровья Швейцарского федерального технологического института, Цюрих, Швейцария
2 Исследования роста и развития детей Ce nter, Исфаханский университет медицинских наук, Исфахан, Иран
Адрес для корреспонденции: Prof.Роя Келишади, Исследовательский центр детского роста и развития Исфаханский университет медицинских наук, Исфахан, Иран. Электронная почта: ri.ca.ium.dem@idahsilekПоступила в редакцию 8 июня 2013 г .; Пересмотрено 3 ноября 2013 г .; Принято 27 ноября 2013 г.
Авторские права: © Journal of Research in Medical SciencesЭто статья в открытом доступе, распространяемая в соответствии с условиями Creative Commons Attribution-Noncommercial-Share Alike 3.0 Unported, что разрешает неограниченное использование, распространение и воспроизведение в на любом носителе при условии правильного цитирования оригинальной работы.
Эта статья цитируется в других статьях в PMC.Abstract
Хорошо известно, что недостаток или чрезмерное воздействие различных элементов оказывает заметное влияние на здоровье человека. Действие элемента определяется несколькими характеристиками, включая абсорбцию, метаболизм и степень взаимодействия с физиологическими процессами. Железо является важным элементом почти для всех живых организмов, поскольку оно участвует в широком спектре метаболических процессов, включая транспорт кислорода, синтез дезоксирибонуклеиновой кислоты (ДНК) и транспорт электронов.Однако, поскольку железо может образовывать свободные радикалы, его концентрацию в тканях организма необходимо строго регулировать, поскольку в чрезмерных количествах оно может привести к повреждению тканей. Нарушения метаболизма железа являются одними из наиболее распространенных заболеваний человека и охватывают широкий спектр заболеваний с различными клиническими проявлениями, от анемии до перегрузки железом и, возможно, до нейродегенеративных заболеваний. В этом обзоре мы обсуждаем последние достижения в исследованиях метаболизма и биодоступности железа, а также наше текущее понимание потребности человека в железе, а также последствий и причин дефицита железа.Наконец, мы обсуждаем стратегии предотвращения дефицита железа.
Ключевые слова: Анемия, потребность человека в железе, биодоступность железа, дефицит железа, метаболизм железа
ВВЕДЕНИЕ
С древних времен человек осознавал особую роль железа в здоровье и болезнях. [1] Железо вначале использовалось в медицине египтянами, индуистами, греками и римлянами. [2, 3] В 17 — веках железо использовалось для лечения хлороза (зеленой болезни), состояния, часто возникающего из-за дефицита железа.[4] Однако только в 1932 году важность железа была окончательно установлена убедительным доказательством того, что неорганическое железо необходимо для синтеза гемоглобина. [5] В течение многих лет пищевой интерес к железу был сосредоточен на его роли в образовании гемоглобина и транспорте кислорода. [6] В настоящее время, хотя низкое потребление железа и / или его биодоступность являются причиной большинства анемий в промышленно развитых странах, на них приходится лишь около половины анемии в развивающихся странах [7], где инфекционные и воспалительные заболевания (особенно малярия), кровопотеря от паразитарных инфекций. , и дефицит других питательных веществ (витамина А, рибофлавина, фолиевой кислоты и витамина B12) также являются важными причинами.[8]
Биохимия и физиология
В отличие от цинка, железо является распространенным элементом на Земле [2,9] и является биологически важным компонентом каждого живого организма. [10,11] Однако, несмотря на его геологическое изобилие, железо часто является фактором, ограничивающим рост в окружающей среде. [9] Этот кажущийся парадокс связан с тем фактом, что при контакте с кислородом железо образует оксиды, которые очень нерастворимы и, следовательно, не доступны для усвоения организмами [2]. В ответ возникли различные клеточные механизмы захвата железа из окружающей среды в биологически полезных формах.Примерами являются сидерофоры, секретируемые микробами для захвата железа в высокоспецифический комплекс [12], или механизмы восстановления железа из нерастворимого трехвалентного железа (Fe +3 ) до растворимой двухвалентной формы (Fe +2 ), как в дрожжах. [13] Многие механизмы, обнаруженные у низших организмов, имеют аналогичные аналоги у высших организмов, включая человека. В организме человека железо в основном существует в сложных формах, связанных с белком (гемопротеином), в виде гемовых соединений (гемоглобин или миоглобин), гемовых ферментов или негемовых соединений (ферменты флавин-железо, переносчики и ферритин).[3] Организму требуется железо для синтеза белков, переносящих кислород, в частности гемоглобина и миоглобина, а также для образования гемовых ферментов и других железосодержащих ферментов, участвующих в переносе электронов и окислении-восстановлении. [14,3] Почти Две трети железа в организме содержится в гемоглобине, присутствующем в циркулирующих эритроцитах, 25% содержится в легко мобилизуемых запасах железа, а оставшиеся 15% связаны с миоглобином в мышечной ткани и с различными ферментами, участвующими в окислительном процессе. метаболизм и многие другие функции клеток.[15]
Железо перерабатывается и, таким образом, сохраняется в организме. показана схематическая диаграмма цикла железа в организме. Железо доставляется в ткани с помощью циркулирующего трансферрина, переносчика, который захватывает железо, высвобождаемое в плазму, в основном из кишечных энтероцитов или ретикулоэндотелиальных макрофагов. Связывание нагруженного железом трансферрина с рецептором трансферрина на клеточной поверхности (TfR) 1 приводит к эндоцитозу и поглощению металлического груза. Интернализованное железо транспортируется в митохондрии для синтеза гема или кластеров железо-сера, которые являются неотъемлемой частью нескольких металлопротеинов, а избыток железа накапливается и детоксифицируется в цитозольном ферритине.
Железо связывается и транспортируется в организме через трансферрин и сохраняется в молекулах ферритина. После всасывания железа не существует физиологического механизма выведения избыточного железа из организма, кроме кровопотери, то есть беременности, менструации или другого кровотечения обычно низкий, но может колебаться от 5% до 35% в зависимости от обстоятельств и типа железа. [3]
Поглощение железа энтероцитами осуществляется переносчиком двухвалентного металла 1, входящим в группу переносчиков растворенных веществ мембранных транспортных белков.Это происходит преимущественно в двенадцатиперстной кишке и верхних отделах тощей кишки [16]. Затем он переносится через слизистую двенадцатиперстной кишки в кровь, где транспортируется трансферрином к клеткам или костному мозгу для эритропоэза [продуцирования красных кровяных телец (эритроцитов)]. [14,17,18] Существует механизм обратной связи, который усиливается. всасывание железа у людей с дефицитом железа. Напротив, люди с перегрузкой железом снижают абсорбцию железа через гепсидин. В настоящее время общепринято, что абсорбция железа контролируется ферропортином, который позволяет или не позволяет железу из клетки слизистой оболочки попадать в плазму.
Физическое состояние железа, поступающего в двенадцатиперстную кишку, сильно влияет на его всасывание. При физиологическом pH двухвалентное железо (Fe +2 ) быстро окисляется до нерастворимой трехвалентной формы (Fe +3 ). Желудочная кислота снижает pH в проксимальном отделе двенадцатиперстной кишки, снижая содержание Fe +3 в просвете кишечника за счет редуктазы железа, тем самым обеспечивая последующий транспорт Fe +2 через апикальную мембрану энтероцитов. Это увеличивает растворимость и поглощение трехвалентного железа.Когда продукция желудочного сока нарушена (например, ингибиторами кислотного насоса, такими как лекарство, прилосек), абсорбция железа существенно снижается.
Диетический гем также может транспортироваться через апикальную мембрану по еще неизвестному механизму и впоследствии метаболизироваться в энтероцитах гемоксигеназой 1 (HO-1) с высвобождением (Fe +2 ) [19]. Этот процесс более эффективен, чем абсорбция неорганического железа, и не зависит от рН двенадцатиперстной кишки. Таким образом, на него не влияют такие ингибиторы, как фитат и полифенолы.Следовательно, красное мясо с высоким содержанием гемоглобина является отличным источником железа. Непосредственно интернализованный Fe +2 обрабатывается энтероцитами и в конечном итоге (или нет) экспортируется через базолатеральную мембрану в кровоток через транспортер ферропортин Fe +2 . Ферропортин-опосредованный отток Fe +2 связан с его повторным окислением с Fe +2 , катализируемым мембраносвязанным ферроксидазой гефестином, который физически взаимодействует с ферропортином [20] и, возможно, также его плазменным гомологом церулоплазмином.Экспортируемое железо улавливается трансферрином, который поддерживает Fe +3 в окислительно-восстановительном инертном состоянии и доставляет его в ткани. Общее содержание железа в трансферрине (≈3 мг) соответствует менее 0,1% железа в организме, но оно очень динамично и подвергается более чем 10-кратному ежедневному обороту для поддержания эритропоэза. Пул трансферрина железа пополняется в основном за счет железа, рециркулируемого из неэффективных эритроцитов, и, в меньшей степени, за счет вновь абсорбированного пищевого железа. Стареющие эритроциты очищаются ретикулоэндотелиальными макрофагами, которые метаболизируют гемоглобин и гем и высвобождают железо в кровоток.По аналогии с кишечными энтероцитами, макрофаги экспортируют Fe +2 из своей плазматической мембраны через ферропортин в процессе, сопряженном с повторным окислением Fe +2 до Fe +3 церулоплазмином с последующей загрузкой Fe +3. на трансферрин. [21]
Theil et al ., [21] недавно сообщили, что существует также независимый механизм абсорбции растительных ферритинов, в основном присутствующих в бобовых. Однако актуальность переносчика ферритина неясна, поскольку большая часть ферритина, по-видимому, разлагается во время обработки и переваривания пищи, тем самым высвобождая неорганическое железо из оболочки ферритина для поглощения по нормальному механизму.[22] Поскольку одна молекула ферритина содержит 1000 или более атомов железа и на нее также не должны влиять ингибиторы абсорбции железа, такой механизм может стать важным источником железа в развивающихся странах, где обычно потребляются бобовые.
Регуляция гомеостаза железа
Поскольку железо требуется для ряда разнообразных клеточных функций, для поддержания гомеостаза железа требуется постоянный баланс между поглощением, транспортом, хранением и использованием железа. [11] Поскольку в организме отсутствует определенный механизм активного выведения железа, баланс железа в основном регулируется в точке абсорбции.[23,24]
Гепсидин — это циркулирующий пептидный гормон, секретируемый печенью, который играет центральную роль в регуляции гомеостаза железа. Это главный регулятор системного гомеостаза железа, координирующий использование и хранение железа с приобретением железа. [25] Этот гормон в основном вырабатывается гепатоцитами и является негативным регулятором поступления железа в плазму []. Гепсидин действует путем связывания с ферропортином, переносчиком железа, присутствующим на клетках двенадцатиперстной кишки, макрофагах и клетках плаценты.Связывание гепсидина вызывает интернализацию и деградацию ферропортина. [26] Потеря ферропортина с поверхности клетки предотвращает попадание железа в плазму []. Снижение поступления железа в плазму приводит к низкому насыщению трансферрина и меньшему количеству железа доставляется в развивающийся эритробласт. Напротив, снижение экспрессии гепсидина приводит к увеличению ферропортина на клеточной поверхности и увеличению абсорбции железа [27] []. У всех видов концентрация железа в биологических жидкостях строго регулируется, чтобы обеспечить необходимое количество железа и избежать токсичности, поскольку избыток железа может привести к образованию активных форм кислорода.[28] Гомеостаз железа у млекопитающих регулируется на уровне кишечной абсорбции, поскольку для железа не существует экскреторного пути.
Гепсидин-опосредованная регуляция гомеостаза железа. (а) Повышенная экспрессия гепсидина печенью является результатом воспалительных стимулов. Высокий уровень гепсидина в кровотоке приводит к интернализации и деградации ферропортина, экспортера железа. Потеря ферропортина на клеточной поверхности приводит к загрузке железа макрофагами, низким уровням железа в плазме и снижению эритропоэза из-за снижения количества железа, связанного с трансферрином.Снижение эритропоэза приводит к анемии хронического заболевания. (b) Нормальные уровни гепсидина в ответ на потребность в железе регулируют уровень импорта железа в плазму, нормальное насыщение трансферрина и нормальные уровни эритропоэза. (c) Гемохроматоз или перегрузка железом возникает из-за недостаточного уровня гепсидина, вызывая повышенный импорт железа в плазму, высокое насыщение трансферрина и избыточное отложение железа в печени. Источник: Де Доменико, и др. . [27]
Уровни гепсидина в плазме регулируются различными стимулами, включая цитокины, железо в плазме, анемию и гипоксию.Нарушение регуляции экспрессии гепсидина приводит к нарушениям железа. Избыточная экспрессия гепсидина приводит к анемии хронического заболевания, в то время как низкая выработка гепсидина приводит к наследственному гемохроматозу (HFE) с последующим накоплением железа в жизненно важных органах []. Большинство наследственных заболеваний, связанных с железом, возникает в результате недостаточного производства гепсидина по сравнению со степенью накопления железа в тканях. Было показано, что нарушение экспрессии гепсидина является результатом мутаций в любом из 4 различных генов: TfR2, HFE, гемохроматоз типа 2 (HFE2) и антимикробный пептид гепсидина (HAMP).Мутации в HAMP, гене, кодирующем гепсидин, приводят к болезни, связанной с перегрузкой железом, поскольку отсутствие гепсидина обеспечивает постоянное высокое всасывание железа. Роль других генов (TFR2, HFE и HFE2) в регуляции продукции гепсидина не ясна [27].
Хранение
Концентрация ферритина вместе с концентрацией гемосидерина отражает запасы железа в организме. Они хранят железо в нерастворимой форме и присутствуют в основном в печени, селезенке и костном мозге. [2] Большая часть железа связана с широко распространенным и высококонсервативным железосвязывающим белком ферритином.[18] Гемосидерин представляет собой комплекс хранения железа, который с меньшей готовностью выделяет железо для нужд организма. В условиях устойчивого состояния сывороточные концентрации ферритина хорошо коррелируют с общими запасами железа в организме. [29] Таким образом, сывороточный ферритин является наиболее удобным лабораторным тестом для оценки запасов железа.
Выделение
Помимо потерь железа из-за менструации, другого кровотечения или беременности, железо очень консервативно и нелегко выводится из организма. [30] Существует некоторая обязательная потеря железа из организма в результате физиологического отшелушивания клеток с эпителиальных поверхностей [30], включая кожу, мочеполовые и желудочно-кишечные тракты.[3] Однако, по оценкам, эти потери очень ограничены (≈1 мг / день). [31] Потери железа из-за кровотечения могут быть значительными, а чрезмерная менструальная кровопотеря является наиболее частой причиной дефицита железа у женщин.
БИОЛОГИЧЕСКАЯ ДОСТУПНОСТЬ
Пищевое железо встречается в двух формах: гемовая и негемовая. [23] Основными источниками гемового железа являются гемоглобин и миоглобин из мяса, птицы и рыбы, тогда как негемовое железо получают из злаков, бобовых, бобовых, фруктов и овощей.[32] Гемовое железо обладает высокой биодоступностью (15–35%), и диетические факторы мало влияют на его абсорбцию, тогда как абсорбция негемового железа намного ниже (2–20%) и сильно зависит от присутствия других пищевых компонентов. [23] Напротив, количество негемового железа в рационе во много раз превышает количество гемового железа в большинстве приемов пищи. Таким образом, несмотря на более низкую биодоступность, негемовое железо обычно вносит больший вклад в питание железом, чем гемовое железо. [33] Основными ингибиторами абсорбции железа являются фитиновая кислота, полифенолы, кальций и пептиды из частично переваренных белков.[23] Усилители — это аскорбиновая кислота и мышечная ткань, которые могут восстанавливать трехвалентное железо до двухвалентного железа и связывать его в растворимые комплексы, доступные для абсорбции. [23]
Факторы, повышающие абсорбцию железа
На абсорбцию железа влияет ряд диетических факторов. Аскорбат и цитрат частично увеличивают усвоение железа, действуя как слабые хелаторы, помогая растворить металл в двенадцатиперстной кишке []. [34] Железо легко переносится из этих соединений в клетки слизистой оболочки. Исследователи продемонстрировали дозозависимый усиливающий эффект нативной или добавленной аскорбиновой кислоты на абсорбцию железа.[34] Усиливающий эффект в значительной степени связан с его способностью восстанавливать трехвалентное железо до двухвалентного железа, но также из-за его способности хелатировать железо. [35] Аскорбиновая кислота преодолеет негативное влияние на абсорбцию железа всех ингибиторов, включая фитат, [36] полифенолы, [37], кальций и белки, содержащиеся в молочных продуктах [38], и увеличит абсорбцию как нативного, так и обогащенного железа. Во фруктах и овощах усиливающий эффект аскорбиновой кислоты часто нивелируется ингибирующим действием полифенолов.[39] Аскорбиновая кислота является единственным усилителем всасывания в вегетарианских диетах, а всасывание железа из вегетарианских и веганских блюд можно оптимизировать путем включения овощей, содержащих аскорбиновую кислоту. [40] Варка, промышленная обработка и хранение разлагают аскорбиновую кислоту и устраняют ее усиливающий эффект на усвоение железа. [41]
Таблица 1
Факторы, которые могут влиять на всасывание железа
Было показано усиливающее действие мяса, рыбы или птицы на всасывание железа из вегетарианских блюд [42], и 30 г мышечной ткани считается эквивалентом 25 мг аскорбиновой кислоты. .[33] Бьорн-Расмуссен и Халлберг [43] сообщили, что добавление курицы, говядины или рыбы к кукурузной муке увеличивало всасывание негемового железа в 2-3 раза без влияния того же количества белка, что и яичного альбумина. Как и в случае с аскорбиновой кислотой, было несколько сложнее продемонстрировать усиливающий эффект мяса при многократном приёме пищи и в полных исследованиях диеты. Reddy и др. ., [44] сообщили только о незначительном улучшении абсорбции железа (35%) в самостоятельно выбранных диетах в течение 5 дней, когда ежедневное потребление мышечной ткани было увеличено до 300 г / день, хотя в аналогичных 5-дневных рационах. В ходе дневного исследования 60 г свинины, добавленные к вегетарианской диете, увеличили всасывание железа на 50%.[45]
Факторы, ингибирующие абсорбцию железа
В растительной диете фитат (мио-инозитол гексакисфосфат) является основным ингибитором абсорбции железа. [23] Было показано, что отрицательное влияние фитата на абсорбцию железа зависит от дозы и начинается с очень низких концентраций 2-10 мг / прием пищи. [37,46] Молярное отношение фитата к железу может быть использовано для оценки влияния на абсорбцию. . Соотношение должно составлять 1: 1 или предпочтительно 0,4: 1 для значительного улучшения всасывания железа в простых злаковых или бобовых блюдах, не содержащих каких-либо усилителей усвоения железа, или 6: 1 в комбинированных блюдах с некоторыми овощами, содержащими аскорбин кислота и мясо как усилители.[47]
Полифенолы встречаются в различных количествах в растительной пище и напитках, таких как овощи, фрукты, некоторые злаки и бобовые, чай, кофе и вино. Ингибирующее действие полифенолов на абсорбцию железа было показано с черным чаем и, в меньшей степени, с травяными чаями. [48,49] В зерновых и бобовых культурах полифенолы усиливают ингибирующий эффект фитата, как было показано в исследовании, сравнивающем сорго с высоким и низким содержанием полифенолов. [23]
Было показано, что кальций отрицательно влияет на абсорбцию негемового и гемового железа, что отличает его от других ингибиторов, влияющих только на абсорбцию негемового железа.[50] Дозозависимые ингибирующие эффекты были показаны при дозах 75–300 мг, когда кальций добавлялся в булочки, и при дозах 165 мг кальция из молочных продуктов. [51] Предполагается, что исследования однократного приема пищи показывают отрицательное влияние кальция на абсорбцию железа, тогда как исследования многократного приема пищи с большим разнообразием продуктов и различными концентрациями других ингибиторов и усилителей показывают, что кальций лишь ограниченно влияет на абсорбцию железа. [52]
Было показано, что животные белки, такие как молочные белки, яичные белки и альбумин, ингибируют абсорбцию железа.[53] Было показано, что две основные белковые фракции коровьего молока, казеин и сыворотка, а также яичный белок ингибируют абсорбцию железа у человека. [54] Белки сои также снижают всасывание железа. [55]
Конкуренция с железом
Исследования конкуренции показывают, что некоторые другие тяжелые металлы могут участвовать в пути всасывания железа в кишечнике. К ним относятся свинец, марганец, кобальт и цинк. Поскольку дефицит железа часто сочетается с интоксикацией свинцом, это взаимодействие может вызвать особенно серьезные медицинские осложнения у детей.[56]
Свинец является особенно опасным элементом для метаболизма железа. [57] Свинец поглощается механизмом поглощения железа (DTM1) и вторично блокирует железо за счет конкурентного торможения. Кроме того, свинец препятствует ряду важных железозависимых метаболических этапов, таких как биосинтез гема. Это многогранное влияние имеет особенно тяжелые последствия для детей, поскольку свинец не только вызывает анемию, но и может ухудшить когнитивное развитие. Свинец естественным образом присутствует в больших количествах в грунтовых водах и почве в некоторых регионах и может тайно нанести вред здоровью детей.По этой причине большинство педиатров в США обычно проверяют содержание свинца в раннем возрасте с помощью простого анализа крови.
ТРЕБОВАНИЯ К ЧЕЛОВЕКУ
В раннем детстве потребности в железе удовлетворяются за счет небольшого количества железа, содержащегося в грудном молоке. [58] Потребность в железе заметно возрастает через 4-6 месяцев после рождения и составляет около 0,7-0,9 мг / день в течение оставшейся части первого года [58]. В возрасте от 1 до 6 лет содержание железа в организме снова увеличивается вдвое. [58] Потребность в железе также очень высока у подростков, особенно в период скачка роста.У девочек обычно происходит скачок роста до менархе, но к этому времени рост не заканчивается. У мальчиков наблюдается заметное увеличение массы и концентрации гемоглобина в период полового созревания. На этой стадии потребности в железе повышаются до уровня, превышающего средние потребности в железе у менструирующих женщин [58] [см.].
Таблица 2
Потребность в железе 97,5% людей с точки зрения абсорбированного железа a , в разбивке по возрастным группам и полу (Всемирная организация здравоохранения, 1989) ее тело.Точный баланс между потреблением и потерей пищи поддерживает этот баланс. Около 1 мг железа теряется каждый день из-за отшелушивания клеток кожи и слизистых оболочек, включая слизистую оболочку желудочно-кишечного тракта. [59] Менструация увеличивает среднесуточную потерю железа примерно до 2 мг в день у взрослых женщин в пременопаузе. [60] Увеличение массы тела во время скачков роста в неонатальном и детском возрасте временно увеличивает потребность в железе. [61]
Потребление железа с пищей необходимо для восполнения потери железа с калом и мочой, а также через кожу.Эти базальные потери составляют примерно 0,9 мг железа для взрослого мужчины и 0,8 мг для взрослой женщины. [62] У женщин репродуктивного возраста необходимо учитывать потерю железа с менструальной кровью [].
ГРУППЫ ПОВЫШЕННОГО РИСКА
Наибольшая вероятность дефицита железа обнаруживается в тех частях населения, которые не имеют надлежащего доступа к пище, богатой усвояемым железом, во время стадий высокой потребности в железе. Эти группы соответствуют детям, подросткам и женщинам репродуктивного возраста, особенно во время беременности.[63,58]
У младенцев и подростков повышенная потребность в железе является результатом быстрого роста. Для женщин репродуктивного возраста основная причина — чрезмерная кровопотеря во время менструации. Во время беременности потребность в железе значительно возрастает из-за быстрого роста плаценты и плода, а также увеличения глобулярной массы. [63] Напротив, взрослые мужчины и женщины в постменопаузе имеют низкий риск дефицита железа, и количество железа в нормальном рационе обычно достаточно для удовлетворения их физиологических потребностей.[63]
ПОСЛЕДСТВИЯ И ПРИЧИНЫ ДЕФИЦИТА ЖЕЛЕЗА
Последствия дефицита железа
Дефицит железа определяется как состояние, при котором отсутствуют мобилизуемые запасы железа и при котором появляются признаки нарушения поступления железа в ткани, включая эритрон. , отмечены. [64] Дефицит железа может сопровождаться анемией или без нее. Некоторые функциональные изменения могут произойти и в отсутствие анемии, но наиболее функциональные нарушения, по-видимому, возникают при развитии анемии. [2] Даже легкие и умеренные формы железодефицитной анемии могут быть связаны с функциональными нарушениями, влияющими на когнитивное развитие [65], механизмы иммунитета [66] и работоспособность.[67] Дефицит железа во время беременности связан с множеством неблагоприятных исходов как для матери, так и для ребенка, включая повышенный риск сепсиса, материнской смертности, перинатальной смертности и низкой массы тела при рождении. [68] Дефицит железа и анемия также снижают способность к обучению и связаны с повышенным уровнем заболеваемости. [68]
Причины дефицита железа
Дефицит железа возникает в результате истощения запасов железа и возникает, когда абсорбция железа не может идти в ногу с метаболическими потребностями в железе для поддержания роста и восполнения потери железа, что в первую очередь связано с кровопотерей .[2] Основные причины дефицита железа включают низкое потребление биодоступного железа, повышенную потребность в железе в результате быстрого роста, беременности, менструации и избыточную кровопотерю, вызванную патологическими инфекциями, такими как анкилостомы и власоглавы, вызывающие потерю крови из желудочно-кишечного тракта [2] 69,70,71,72] и нарушение всасывания железа. [73] Частота дефицита железа увеличивается у девочек-подростков, потому что менструальные потери железа накладываются на потребность в быстром росте [74]. Другими факторами риска дефицита железа у молодых женщин являются высокий паритет, использование внутриматочной спирали и вегетарианская диета.[75]
Дефицит железа в питании возникает, когда физиологические потребности не могут быть удовлетворены за счет абсорбции железа из рациона. [72] Биодоступность пищевого железа низка в группах населения, потребляющих однообразные растительные диеты с небольшим количеством мяса. [72] Во многих развивающихся странах растительные продукты для отлучения от груди редко обогащены железом, а частота анемии превышает 50% у детей младше 4 лет. [64]
Когда запасы железа истощаются и железа недостаточно для эритропоэза, синтез гемоглобина в предшественниках эритроцитов нарушается и появляются гематологические признаки железодефицитной анемии.
ОЦЕНКА СТАТУСА ЖЕЛЕЗА
Дефицит железа и, в конечном итоге, анемия развиваются поэтапно и могут быть оценены путем измерения различных биохимических показателей. Хотя некоторые ферменты железа чувствительны к дефициту железа [63], их активность не использовалась в качестве успешного рутинного измерения статуса железа [2].
Лабораторные измерения необходимы для правильной диагностики дефицита железа. Они наиболее информативны, когда несколько показателей уровня железа исследуются и оцениваются в контексте питания и истории болезни.
Пул железа в плазме или сыворотке — это фракция всего железа в организме, которая циркулирует в основном связанном с трансферрином. Три способа оценки уровня железа в плазме или сыворотке включают: 1) измерение общего содержания железа в единице объема в мкг / дл; 2) измерение общего количества сайтов связывания для атомов железа на трансферрине, известного как общая железосвязывающая способность в мкг / дл 2 ; и 3) оценка процента двух сайтов связывания на всех занятых молекулах трансферрина, называемого процентным насыщением трансферрина.[76] Однако заметные биологические вариации этих значений могут возникать в результате суточных колебаний, наличия инфекции или воспалительных состояний и недавнего приема железа с пищей. [76]
Протопорфирин цинка отражает нехватку железа на последних стадиях синтеза гемоглобина, так что цинк вставляется в молекулу протопорфирина вместо железа. Протопорфирин цинка может быть обнаружен в эритроцитах с помощью флуориметрии и является мерой тяжести дефицита железа. [76]
Сывороточный ферритин является хорошим индикатором запасов железа в организме в большинстве случаев.Когда концентрация сывороточного ферритина ≥15 мкг / л, присутствуют запасы железа; более высокие концентрации отражают размер хранилища железа; при низкой концентрации (<12 мкг / л для детей младше 5 лет и <15 мкг / л для детей старше 5 лет) запасы железа истощаются. [76] Однако ферритин является белком-реагентом острой фазы, и его сывороточные концентрации могут быть повышены независимо от изменения запасов железа, инфекции или воспаления. [76,2] Это означает, что может быть трудно интерпретировать концентрацию ферритина там, где инфекция болезни распространены.
Еще одним индикатором статуса железа является концентрация TfR в сыворотке крови. Поскольку TfR в основном происходит из развивающихся эритроцитов, он отражает интенсивность эритропоэза и потребность в железе. Когда запасы железа истощаются, концентрация повышается при железодефицитной анемии, что указывает на серьезную недостаточность железа. Это при условии, что нет других причин аномального эритропоэза. [76] Клинические исследования показывают, что сывороточный TfR менее подвержен воспалению, чем сывороточный ферритин. [77] Основным преимуществом TfR как индикатора является возможность оценки величины функционального дефицита железа после истощения запасов железа.[78]
Отношение TfR к ферритину (TfR / ферритин) было разработано для оценки изменений как в накопленном железе, так и в функциональном железе и считается более полезным, чем TfR или ферритин отдельно. [79] TfR / ферритин использовался для оценки запасов железа в организме как у детей, так и у взрослых. [80] Однако высокая стоимость и отсутствие стандартизации анализа TfR до сих пор ограничивали применимость метода [81].
Низкая концентрация гемоглобина является показателем анемии, конечной стадии дефицита железа.[76,2]
АНЕМИЯ И ЕЕ ПРИЧИНЫ
Анемия описывает состояние, при котором количество эритроцитов в крови низкое или в клетках крови содержится меньше нормального гемоглобина. Человека, страдающего анемией, называют анемичным. Цель эритроцитов — доставлять кислород из легких в другие части тела. Молекула гемоглобина является функциональной единицей эритроцитов и представляет собой сложную белковую структуру, которая находится внутри эритроцитов. Несмотря на то, что эритроциты производятся в костном мозге, в их производство вовлечены многие другие факторы.Например, железо — очень важный компонент молекулы гемоглобина; эритропоэтин, молекула, секретируемая почками, способствует образованию эритроцитов в костном мозге.
Наличие правильного количества эритроцитов и профилактика анемии требует взаимодействия между почками, костным мозгом и питательными веществами в организме. Если почки или костный мозг не функционируют, или организм плохо питается, то нормальное количество и функции эритроцитов может быть трудно поддерживать.
Анемия на самом деле является признаком болезненного процесса, а не самой болезни.Обычно его классифицируют как хронический или острый. Хроническая анемия возникает в течение длительного периода времени. Острая анемия возникает быстро. Определение того, присутствует ли анемия в течение длительного времени или это что-то новое, помогает врачам найти причину. Это также помогает предсказать, насколько серьезными могут быть симптомы анемии. При хронической анемии симптомы обычно начинаются медленно и постепенно прогрессируют; тогда как при острой анемии симптомы могут быть резкими и более тревожными.
Эритроциты живут около 100 дней, поэтому организм постоянно пытается их заменить.У взрослых производство эритроцитов происходит в костном мозге. Врачи пытаются определить, вызвано ли низкое количество эритроцитов повышенной кровопотерей эритроцитов или их снижением в костном мозге. Знание того, изменилось ли количество лейкоцитов и / или тромбоцитов, также помогает определить причину анемии.
По оценкам Всемирной организации здравоохранения (ВОЗ), два миллиарда человек во всем мире страдают анемией и примерно 50% всех анемий объясняются дефицитом железа. [64] Это происходит на всех этапах жизненного цикла, но чаще встречается у беременных женщин и маленьких детей.[82] Анемия является результатом множества причин, которые можно изолировать, но чаще всего они сосуществуют. Некоторые из этих причин включают следующие:
Железодефицитная анемия
Наиболее важной и частой причиной анемии является дефицит железа. [82] Если потребление железа ограничено или неадекватно из-за плохого питания, в результате может возникнуть анемия. Это называется железодефицитной анемией. Железодефицитная анемия также может возникать при наличии язвы желудка или других источников медленного хронического кровотечения (рак толстой кишки, рак матки, полипы кишечника, геморрой и т. Д.).[83]
Анемия хронического заболевания
Любое длительное заболевание может привести к анемии. Этот тип анемии является вторым по распространенности после анемии, вызванной дефицитом железа, и развивается у пациентов с острым или хроническим системным заболеванием или воспалением. [84] Это состояние было названо «анемией воспаления» из-за повышенного содержания гепсидина, который блокирует как рециркуляцию железа из макрофагов, так и абсорбцию железа. [85]
Анемия из-за активного кровотечения
Потеря крови из-за обильного менструального кровотечения или ран может вызвать анемию.[82] Язвы желудочно-кишечного тракта или раковые заболевания, такие как рак толстой кишки, могут медленно терять кровь и также могут вызывать анемию. [86,87]
Анемия, связанная с заболеванием почек
Почки выделяют гормон эритропоэтин, который помогает костному мозгу сделать эритроциты. У людей с хроническим (длительным) заболеванием почек выработка этого гормона снижена, а это, в свою очередь, снижает выработку эритроцитов, вызывая анемию. [88] Хотя дефицит эритропоэтина является основной причиной анемии при хронической почечной недостаточности, это не единственная причина.Следовательно, необходимо минимальное обследование, чтобы исключить дефицит железа и другие аномалии клеточной линии. [89]
Анемия, связанная с беременностью
Увеличение объема плазмы во время беременности приводит к разбавлению эритроцитов и может проявляться как анемия. [90] Железодефицитная анемия составляет 75% всех анемий во время беременности. [90]
Анемия, связанная с плохим питанием
Витамины и минералы необходимы для образования эритроцитов. Помимо железа, для правильного производства гемоглобина необходимы витамин B12, виамин А, фолиевая кислота, рибофлавин и медь.[82] Дефицит любого из этих питательных микроэлементов может вызвать анемию из-за недостаточного производства эритроцитов. Плохое питание — важная причина низкого уровня витаминов и, как следствие, анемии.
Ожирение и анемия
Ожирение характеризуется хроническим слабым системным воспалением, повышенным уровнем гепсидина, которое, в свою очередь, связано с анемией хронического заболевания. Ausk и Ioannou [91] предположили, что ожирение может быть связано с особенностями анемии хронического заболевания, включая низкую концентрацию гемоглобина, низкое содержание железа и трансферрина в сыворотке, а также повышенный уровень ферритина в сыворотке.Избыточный вес и ожирение были связаны с изменениями сывороточного железа, насыщения трансферрина и ферритина, которые, как ожидается, произойдут в условиях хронического системного воспаления. Воспаление, связанное с ожирением, может повышать концентрацию гепсидина и снижать доступность железа. Aeberli и др. ., [92] сравнили уровень железа, потребление железа с пищей и его биодоступность, а также циркулирующие уровни гепсидина, лептина и интерлейкина-6 (ИЛ-6) у детей с избыточной массой тела и детей с нормальным весом.Они указали, что существует пониженная доступность железа для эритропоэза у детей с избыточным весом, и что это, вероятно, связано с опосредованным гепсидином сниженным всасыванием железа и / или повышенным секвестрацией железа, а не с низким содержанием железа с пищей.
Алкоголизм
Алкоголь оказывает многочисленные неблагоприятные эффекты на различные типы клеток крови и их функции. [93] У алкоголиков часто есть дефектные эритроциты, которые преждевременно разрушаются. [93,94] Сам по себе алкоголь также может быть токсичным для костного мозга и может замедлять производство эритроцитов.[93,94] Кроме того, с алкоголизмом связаны плохое питание и дефицит витаминов и минералов. [95] Сочетание этих факторов может привести к анемии у алкоголиков.
Серповидно-клеточная анемия
Серповидно-клеточная анемия — одно из наиболее распространенных наследственных заболеваний. [96] Это заболевание, связанное с кровью, которое влияет на молекулу гемоглобина и приводит к изменению формы всей клетки крови в стрессовых условиях [97]. В таком состоянии проблема с гемоглобином бывает качественной или функциональной.Аномальные молекулы гемоглобина могут вызвать проблемы в целостности структуры эритроцитов, и они могут стать серповидными (серповидные клетки). [97] Существуют разные типы серповидно-клеточной анемии разной степени тяжести. Это особенно распространено у африканцев, ближневосточных и средиземноморских предков. [97]
Талассемия
Это еще одна группа причин анемии, связанных с гемоглобином, которая связана с отсутствием или ошибками в генах, ответственных за выработку гемоглобина. [97] Молекула гемоглобина имеет субъединицы, обычно называемые альфа- и бета-цепями глобина.Отсутствие определенной субъединицы определяет тип альфа- или бета-талассемии. [97,98] Существует много типов талассемии, которые различаются по степени тяжести от легкой (малая талассемия) до тяжелой (большая талассемия). [98] Они также являются наследственными, но вызывают количественные аномалии гемоглобина, то есть вырабатывается недостаточное количество молекул правильного типа. Альфа- и бета-талассемии являются наиболее распространенными наследственными моногенными заболеваниями в мире с наибольшей распространенностью в районах, где малярия была или все еще является эндемической.[97]
Апластическая анемия
Апластическая анемия — это заболевание, при котором разрушается костный мозг и снижается выработка клеток крови. [99] Это вызывает дефицит всех трех типов клеток крови (панцитопения), включая эритроциты (анемия), лейкоциты (лейкопения) и тромбоциты (тромбоцитопения). [100,101] Многие распространенные лекарства могут иногда вызывать этот тип анемии в качестве побочного эффекта. у некоторых людей. [99]
Гемолитическая анемия
Гемолитическая анемия — это тип анемии, при которой происходит разрыв эритроцитов, известный как гемолиз, который разрушается быстрее, чем костный мозг может их заменить.[102] Гемолитическая анемия может возникнуть по разным причинам и часто классифицируется как приобретенная или наследственная. Распространенными приобретенными причинами гемолитической анемии являются аутоиммунитет, микроангиопатия и инфекции. Нарушения ферментов эритроцитов, мембран и гемоглобина вызывают наследственную гемолитическую анемию. [102]
ПРЕДОТВРАЩЕНИЕ НЕДОСТАТОЧНОСТИ ЖЕЛЕЗА (СТРАТЕГИИ ВМЕШАТЕЛЬСТВА)
Четыре основных стратегии коррекции эффективности микронутриентов в популяциях могут использоваться для коррекции дефицита железа, как по отдельности, так и в комбинации.Это обучение в сочетании с модификацией диеты для улучшения потребления железа и его биодоступности; добавление железа (обеспечение железом, обычно в более высоких дозах, без еды), обогащение пищевых продуктов железом и новый подход к биофортификации. Однако есть некоторые трудности в применении некоторых из этих стратегий при рассмотрении железа.
Диверсификация продуктов питания
Модификации диеты для сокращения потребления Индийской стоматологической ассоциации включают увеличение потребления продуктов, богатых железом, особенно мясных продуктов, увеличение потребления фруктов и овощей, богатых аскорбиновой кислотой, для увеличения абсорбции негемового железа и снижение потребления чая и кофе, что подавляют всасывание негемового железа.[103,58] Другая стратегия — снизить содержание антинутриентов, чтобы сделать железо, поступающее из их пищевых источников, более доступным. Биодоступность железа может быть увеличена такими методами, как проращивание и ферментация, которые способствуют ферментативному гидролизу фитиновой кислоты в цельнозерновых зерновых и бобовых культурах за счет повышения активности эндогенных или экзогенных ферментов фитазы. [104] Даже использование неферментативных методов, таких как термическая обработка, замачивание и измельчение, для снижения содержания фитиновой кислоты в основных продуктах растительного происхождения было успешным в улучшении биодоступности железа (и цинка).[105,106]
Добавка
Для перорального приема добавок железа предпочтительны соли двухвалентного железа (сульфат двухвалентного железа и глюконат двухвалентного железа) из-за их низкой стоимости и высокой биодоступности. [72] Хотя абсорбция железа выше при приеме добавок железа натощак, тошнота и боль в эпигастрии могут развиться из-за введенных более высоких доз железа (обычно 60 мг Fe / день). Если возникают такие побочные эффекты, следует попытаться снизить дозу между приемами пищи или давать железо во время еды, хотя пища снижает всасывание лекарственного железа примерно на две трети.[107] Добавки железа во время беременности рекомендуется в развивающихся странах, где женщины часто вступают в беременность с низкими запасами железа. [108] Хотя обычно считалось, что польза от приема добавок железа перевешивает предполагаемый риск, есть некоторые свидетельства того, что добавление в дозах, рекомендованных для здоровых детей, несет в себе риск увеличения тяжести инфекционного заболевания на фоне малярии. [109,110]
Обогащение
Обогащение пищевых продуктов железом сложнее, чем обогащение такими питательными веществами, как цинк в муке, йод в соли и витамин А в кулинарном масле.[72] Наиболее биодоступные соединения железа растворимы в воде или разбавленной кислоте, но часто вступают в реакцию с другими пищевыми компонентами, вызывая неприятный запах, изменение цвета или окисление жиров. [103] Таким образом, менее растворимые формы железа, хотя и хуже усваиваются, часто выбираются для обогащения, чтобы избежать нежелательных сенсорных изменений. [72] Обогащение обычно производится с гораздо более низкими дозами железа, чем с добавками. Это ближе к физиологической среде и может быть самым безопасным вмешательством в малярийные районы. [111] Нет никаких опасений по поводу безопасности добавок железа или обогащения железа в немалярийных эндемичных районах.[112]
Соединения железа, рекомендованные [7] для обогащения пищевых продуктов, включают сульфат железа, фумарат железа, пирофосфат железа и порошок электролитического железа. Пшеничная мука является наиболее распространенным пищевым продуктом, обогащенным железом, и она обычно обогащается порошками элементарного железа, которые не рекомендуются ВОЗ. [7,113] Харрелл и Эгли [23] сообщили, что из 78 национальных программ по пшеничной муке только восемь улучшатся. статус железа. В этих программах использовались рекомендуемые соединения железа на рекомендованных уровнях.Другие страны использовали не рекомендуемые соединения или более низкие уровни железа по сравнению с потреблением муки. Коммерческое детское питание, такое как смеси и злаки, также обычно обогащено железом.
Биофортификация
Содержание железа варьируется от 25 до 56 мг / кг в различных сортах пшеницы и от 7 до 23 мг / кг в рисовых зернах. Однако большая часть этого железа удаляется в процессе измельчения. Поглощение железа зерновыми и бобовыми культурами, многие из которых имеют высокое содержание самородного железа, обычно низкое из-за высокого содержания в них фитата, а иногда и полифенолов.[48] Стратегии биофортификации включают селекцию растений и генную инженерию. Уровни железа в обычных бобах и просе были успешно увеличены путем селекции растений, но использование других основных продуктов питания является более трудным или невозможным (рис) из-за недостаточной естественной генетической изменчивости. Lucca и др. ., [114] увеличили содержание железа в эндосперме риса, чтобы улучшить его всасывание в кишечнике человека с помощью генной инженерии. Они ввели ген ферритина из Phaseolus vulgaris в рисовые зерна, увеличив содержание железа в них вдвое.Чтобы увеличить биодоступность железа, они ввели в эндосперм риса термотолерантную фитазу из Aspergillus fumigatus . Они указали, что этот рис с более высоким содержанием железа и богатой фитазой имеет большой потенциал для существенного улучшения питания железом в тех популяциях, где дефицит железа так широко распространен. [114] К сожалению, фитаза не устояла перед приготовлением. Важность различных минералов, таких как цинк [115] и железо, требует большего внимания на индивидуальном уровне и уровне общественного здравоохранения.
Сноски
Источник поддержки: Нет
Конфликт интересов: Не объявлен.
СПИСОК ЛИТЕРАТУРЫ
1. Борода Дж. Л., Доусон HD. Утюг. В: О’Делл Б.Л., Сунде Р.А., редакторы. Справочник по незаменимым в питании минеральным элементам. Нью-Йорк: CRC Press; 1997. С. 275–334. [Google Scholar] 2. Вуд Р.Дж., Ронненберг А. Железо. В: Shils ME, Shike M, Ross AC, Caballero B, Cousins RJ, редакторы. Современное питание в здоровье и болезнях. 10-е изд. Балтимор: Липпинкотт Уильямс и Уилкинс; 2005 г.С. 248–70. [Google Scholar] 3. Макдауэлл LR. 2-е изд. Амстердам: Elsevier Science; 2003. Минералы в питании животных и человека; п. 660. [Google Scholar] 4. Гуггенхайм KY. Хлороз: возникновение и исчезновение болезни, связанной с питанием. J Nutr. 1995; 125: 1822–5. [PubMed] [Google Scholar] 5. Ип Р., Даллман PR. Утюг. В: Ziegler EE, Filer LJ, редакторы. Присутствуют знания в области питания. 7-е изд. Вашингтон, округ Колумбия: ILSI Press; 1996. С. 278–92. [Google Scholar] 6. Андервуд Э.Дж., Саттл Н.Ф. 3-е изд. Уоллингфорд: международное издательство CABI; 1999 г.Минеральное питание скота; п. 614. [Google Scholar] 7. Аллен Л., де Бенуа Б., Дари О., Харрелл Р., редакторы. Женева: ВОЗ и ФАО; 2006. ВОЗ. Рекомендации по обогащению пищевых продуктов микронутриентами; п. 236. [Google Scholar] 8. Брабин Б.Дж., Премжи З., Верхое ff Ф. Анализ анемии и детской смертности. J Nutr. 2001; 131: 636–45С. [PubMed] [Google Scholar] 9. Quintero-Gutiérrez AG, González-Rosendo G, Sánchez-Muñoz J, Polo-Pozo J, Rodríguez-Jerez JJ. Биодоступность гемового железа в начинке для печенья с использованием поросят в качестве модели животных для человека.Int J Biol Sci. 2008; 4: 58–62. [Бесплатная статья PMC] [PubMed] [Google Scholar] 10. Айзен П., Эннс С., Весслинг-Резник М. Химия и биология метаболизма железа в эукариотах. Int J Biochem Cell Biol. 2001; 33: 940–59. [PubMed] [Google Scholar] 11. Лиу П. Т., Хейскала М., Петерсон П. А., Ян Ю. Роль железа в здоровье и болезнях. Мол Аспекты Мед. 2001; 2: 1–87. [PubMed] [Google Scholar] 12. Guerinot ML. Транспорт микробного железа. Annu Rev Microbiol. 1994; 48: 743–72. [PubMed] [Google Scholar] 13. Асквит К., Каплан Дж.Транспорт железа и меди в дрожжах и его значение для болезней человека. Trends Biochem Sci. 1998. 23: 135–8. [PubMed] [Google Scholar] 15. Вашингтон, округ Колумбия: Национальная академия прессы; 2001. МОМ. Институт медицины. утюг. В: Нормы потребления витамина A, витамина K, мышьяка, бора, хрома, меди, йода, железа, марганца, молибдена, никеля, кремния, ванадия и цинка; С. 290–393. [PubMed] [Google Scholar] 16. Muir A, Hopfer U. Региональная специфичность поглощения железа щеточно-граничными мембранами тонкого кишечника у нормальных мышей и мышей с дефицитом железа.Am J Physiol. 1985; 248: G376–9. [PubMed] [Google Scholar] 17. Фрейзер Д.М., Андерсон Г.Дж. Импорт железа. I. Абсорбция железа в кишечнике и ее регуляция. Am J Physiol Gastrointest Liver Physiol. 2005; 289: G631–5. [PubMed] [Google Scholar] 18. Наддур С.С., Шрирама К., Мудипалли А. Механизмы транспорта и гомеостаза железа: их роль в здоровье и болезнях. Индийский J Med Res. 2008; 128: 533–44. [PubMed] [Google Scholar] 20. Yeh KY, Yeh M, Mims L, Glass J. Кормление железом индуцирует миграцию и взаимодействие ферропортина 1 и гефестина в двенадцатиперстном эпителии крыс.Am J Physiol Gastrointest Liver Physiol. 2009. 296: 55–65. [Бесплатная статья PMC] [PubMed] [Google Scholar] 21. Тейл Э.С., Чен Х., Миранда С., Янсер Х., Эльзенханс Б., Нуньес М.Т. и др. Абсорбция железа из ферритина не зависит от гемового железа и солей двухвалентного железа у женщин и сегментов кишечника крыс. J Nutr. 2012; 142: 478–83. [Бесплатная статья PMC] [PubMed] [Google Scholar] 22. Hoppler M, Schoenbaechler A, Meile L, Hurrell RF, Walczyk T. Ферритин-железо высвобождается во время кипячения и in vitro при пищеварении в желудке .J Nutr. 2008. 138: 878–84. [PubMed] [Google Scholar] 23. Hurrell R, Egli I. Биодоступность железа и диетические контрольные значения. Am J Clin Nutr. 2010; 91: 1461–7S. [PubMed] [Google Scholar] 25. Немет Э., Ганц Т. Регулирование метаболизма железа гепсидином. Анну Рев Нутр. 2006; 26: 323–42. [PubMed] [Google Scholar] 26. Немет Э., Таттл М.С., Пауэлсон Дж., Вон М.Б., Донован А., Уорд Д.М. и др. Гепсидин регулирует отток клеточного железа, связываясь с ферропортином и индуцируя его интернализацию. Наука. 2004; 306: 2090–3.[PubMed] [Google Scholar] 28. Браун В., Киллманн Х. Бактериальные решения проблемы снабжения железом. Trends Biochem Sci. 1999; 24: 104–109. [PubMed] [Google Scholar] 29. Хант-младший. Насколько важна биодоступность железа с пищей? Am J Clin Nutr. 2001; 73: 3–4. [PubMed] [Google Scholar] 30. Хант-младший, Зито, Калифорния, Джонсон, Лос-Анджелес. Выведение железа из организма здоровыми мужчинами и женщинами. Am J Clin Nutr. 2009; 89: 1–7. [PubMed] [Google Scholar] 31. Фэрбенкс В.Ф. Железо в медицине и питании. В: Shils ME, Shike M, Ross AC, Caballero B, Cousins RJ, редакторы.Современное питание в здоровье и болезнях. 10-е изд. Балтимор: Липпинкотт Уильямс и Уилкинс; 1999. С. 193–221. [Google Scholar] 32. потребности человека в витаминах и минералах. Рим: ФАО; 2001. ФАО / ВОЗ. Пищевые подходы к удовлетворению потребностей в витаминах и минералах; С. 7–25. [Google Scholar] 33. Monsen ER, Hallberg L, Layrisse M, Hegsted DM, Cook JD, Mertz W. и др. Оценка доступного пищевого железа. Am J Clin Nutr. 1978; 31: 134–41. [PubMed] [Google Scholar] 34. Конрад ME, Umbreit JN. Краткий обзор: абсорбция железа — путь муцин-мобилферрин-интегрин.Конкурентоспособный путь поглощения металлов. Am J Hematol. 1993; 42: 67–73. [PubMed] [Google Scholar] 35. Конрад М.Э., Шаде С.Г. Хелаты аскорбиновой кислоты в абсорбции железа: роль соляной кислоты и желчи. Гастроэнтерология. 1968; 55: 35–45. [PubMed] [Google Scholar] 36. Холлберг Л., Брюн М., Россандер Л. Поглощение железа у человека: аскорбиновая кислота и дозозависимое ингибирование фитатом. Am J Clin Nutr. 1989; 49: 140–4. [PubMed] [Google Scholar] 37. Зигенберг Д., Бейнс Р.Д., Ботвелл Т.Х., Макфарлейн Б.Дж., Лампарелли Р.Д., Car NG и др.Аскорбиновая кислота предотвращает дозозависимое ингибирующее действие полифенолов и фитатов на абсорбцию негемового железа. Am J Clin Nutr. 1991; 53: 537–41. [PubMed] [Google Scholar] 38. Стекель А., Оливарес М., Писарро Ф., Чадуд П., Лопес И., Амар М. Поглощение обогащающего железа из молочных смесей у младенцев. Am J Clin Nutr. 1986; 43: 917–22. [PubMed] [Google Scholar] 39. Бюллетень D, Бейнс Р.Д., Ботвелл Т.Х., Гиллули М., Макфарлейн Б.Дж., Макфейл А.П. и др. Влияние фруктовых соков и фруктов на усвоение железа из рисовой муки.Br J Nutr. 1987; 57: 331–43. [PubMed] [Google Scholar] 40. Линч SR, Кук JD. Взаимодействие витамина С и железа. Ann N Y Acad Sci. 1980; 355: 32–44. [PubMed] [Google Scholar] 41. Teucher B, Olivares M, Cori H. Усилители поглощения железа: аскорбиновая кислота и другие органические кислоты. Int J Vitam Nutr Res. 2004; 74: 403–19. [PubMed] [Google Scholar] 42. Линч С.Р., Харрелл Р.Ф., Дассенко С.А., Кук Дж.Д. Влияние пищевых белков на биодоступность железа у человека. Adv Exp Med Biol. 1989; 249: 117–32. [PubMed] [Google Scholar] 43.Бьорн-Расмуссен Э., Халльберг Л. Влияние животных белков на усвоение пищевого железа человеком. Нутр Метаб. 1979; 23: 192–202. [PubMed] [Google Scholar] 44. Редди МБ, Харрелл Р.Ф., Кук JD. Разнообразное питание незначительно влияет на всасывание негемового железа у нормальных людей. J Nutr. 2006; 136: 576–81. [PubMed] [Google Scholar] 45. Бах Кристенсен М., Хелс О, Морберг С., Марвинг Дж., Бугель С., Тетенс I. Свинина увеличивает усвоение железа при 5-дневной полностью контролируемой диете по сравнению с вегетарианской диетой с аналогичным содержанием витамина С и фитиновой кислоты.Br J Nutr. 2005. 94: 78–83. [PubMed] [Google Scholar] 46. Харрелл Р.Ф., Джуллерат М.А., Редди М.Б., Линч С.Р., Дассенко С.А., Кук Дж.Д. Соевый белок, фитат и абсорбция железа у человека. Am J Clin Nutr. 1992; 56: 573–8. [PubMed] [Google Scholar] 47. Hurrell RF. Разложение фитиновой кислоты как средство улучшения усвоения железа. Int J Vitam Nutr Res. 2004. 74: 445–52. [PubMed] [Google Scholar] 48. Харрелл Р.Ф., Редди М., Кук Дж. Д.. Подавление абсорбции негемного железа у человека напитками, содержащими полифенолы. Br J Nutr.1999. 81: 289–95. [PubMed] [Google Scholar] 49. Холлберг Л., Россандер Л. Влияние различных напитков на усвоение негемового железа из сложных блюд. Hum Nutr Appl Nutr. 1982; 36: 116–23. [PubMed] [Google Scholar] 50. Hallberg L, Rossander-Hulthen L, Brune M, Gleerup A. Ингибирование усвоения гемового железа у человека кальцием. Br J Nutr. 1993; 69: 533–40. [PubMed] [Google Scholar] 51. Hallberg L, Rossander-Hulthen L. Потребность в железе у менструирующих женщин. Am J Clin Nutr. 1991; 54: 1047–58. [PubMed] [Google Scholar] 52.Линч SR. Влияние кальция на усвоение железа. Nutr Res Rev.2000; 13: 141–58. [PubMed] [Google Scholar] 53. Кук JD, Monsen ER. Поглощение пищевого железа у людей. III. Сравнение влияния животных белков на всасывание негемового железа. Am J Clin Nutr. 1976; 29: 859–67. [PubMed] [Google Scholar] 54. Харрелл РФ, Линч С.Р., Тринидад Т.П., Дассенко С.А., Кук Дж.Д. Абсорбция железа у людей: бычий сывороточный альбумин по сравнению с говяжьими мышцами и яичным белком. Am J Clin Nutr. 1988. 47: 102–7. [PubMed] [Google Scholar] 55.Линч С.Р., Дассенко С.А., Кук Дж.Д., Джульерат М.А., Харрелл РФ. Ингибирующий эффект фрагмента, связанного с соевым белком, на абсорбцию железа у людей. Am J Clin Nutr. 1994; 60: 567–72. [PubMed] [Google Scholar] 56. Piomelli S, Seaman C, Kapoor S. Вызванные свинцом аномалии метаболизма порфирина, связь с дефицитом железа. Ann N Y Acad Sci. 1987; 514: 278–88. [PubMed] [Google Scholar] 58. 2-е изд. Бангкок: 2004 г. ФАО / ВОЗ. Консультации экспертов по потребностям человека в витаминах и минералах, потребностях в витаминах и минералах в питании человека: отчет совместного экспертного заключения ФАО / ВОЗ; п.341. [Google Scholar] 59. Cook JD, Skikne BS, Lynch SR, Reusser ME. Оценки достаточности железа у населения США. Кровь. 1986; 68: 726–31. [PubMed] [Google Scholar] 60. Ботвелл TH, Чарльтон RW. Общий подход к проблемам железодефицита и перегрузки железом у населения в целом. Semin Hematol. 1982; 19: 54–67. [PubMed] [Google Scholar] 61. Гибсон Р.С., Макдональд А.С., Смит-Вандеркой П.Д. Параметры сывороточного ферритина и пищевого железа в выборке канадских детей дошкольного возраста. J Can Dietetic Assoc.1988; 49: 23–8. [Google Scholar] 62. ДеМайер Э.М., Даллман П., Герни Дж. М., Холлберг Л., Суд С. К., Срикантия С. Г., редакторы. Женева: Всемирная организация здравоохранения; 1989. ВОЗ. Профилактика и контроль железодефицитной анемии с помощью первичной медико-санитарной помощи: руководство для администраторов здравоохранения и руководителей программ; п. 58. [Google Scholar] 63. Даллман П. Айрон. В: Браун М.Л., редактор. Настоящие знания в области питания. 6-е изд. Вашингтон, округ Колумбия: Фонд питания; 1990. С. 241–50. [Google Scholar] 64. Женева: Швейцария: Всемирная организация здравоохранения; 2001 г.ВОЗ / ЮНИСЕФ / УООН. Оценка, профилактика и контроль железодефицитной анемии; п. 114. [Google Scholar] 65. Борода Дж. Л., Коннор-младший. Статус железа и нейронное функционирование. Анну Рев Нутр. 2003. 23: 41–58. [PubMed] [Google Scholar] 66. Failla ML. Микроэлементы и защита хозяина: последние достижения и сохраняющиеся проблемы. J Nutr. 2003; 133: S1443–7. [PubMed] [Google Scholar] 67. Витери Ф.Е., Торунь Б. Анемия и физическая работоспособность. В: Гарби Л., редактор. Клиники гематологии. Vol. 3. Лондон: У. Б. Сондерс; 1974. стр.609–26. [Google Scholar] 68. CDC. Табель успеваемости по грудному вскармливанию, США: показатели результатов (публикация из Центров по контролю и профилактике заболеваний, Национальное обследование иммунизации. 2010 г. [последний доступ 11 мая 2010 г.]. Http://www.cdc.gov/breastfeeding/data/index .htm .69. Купер Е.С., Банди Д.А. Трихоцефалопатия. Ballieres Clin Trop Med Commun Dis. 1987; 2: 629–43. [Google Scholar] 70. Всемирная организация здравоохранения, Женева; 1995. ВОЗ. Отчет неофициальной консультации ВОЗ. на анкилостомоз и анемию у девочек и женщин; с.46. [Google Scholar] 71. Crompton DW, Nesheim MC. Пищевая ценность кишечных гельминтозов в течение жизненного цикла человека. Анну Рев Нутр. 2002; 22: 35–99. [PubMed] [Google Scholar] 72. Ларок Р., Касапиа М., Готуццо Е., Дьеркос Т.В. Взаимосвязь между интенсивностью заражения гельминтами, передающимися через почву, и анемией во время беременности. Am J Trop Med Hyg. 2005; 73: 783–9. [PubMed] [Google Scholar] 73. Циммерманн МБ, Харрелл РФ. Недостаток пищевого железа. Ланцет. 2007; 370: 115–20. [Google Scholar] 74. Харви LJ, Armah CN, Dainty JR, Foxall RJ, John Lewis D, Langford NJ и др.Влияние менструальной кровопотери и диеты на дефицит железа у женщин в Великобритании. Br J Nutr. 2005. 94: 557–64. [PubMed] [Google Scholar] 75. Борода JL. Потребность в железе у девочек-подростков. Симпозиум: Повышение уровня железа у подростков до деторождения. J Nutr. 2000; 130: S440–2. [PubMed] [Google Scholar] 77. Бегин Ю. Растворимый рецептор трансферрина для оценки эритропоэза и статуса железа. Clinica Chimica Acta. 2003. 329: 9–22. [PubMed] [Google Scholar] 79. Повар JD, Flowers CH, Skikne BS. Количественная оценка bodyiron.Кровь. 2003. 101: 3359–64. [PubMed] [Google Scholar] 80. Кук JD, Boy E, Flowers C, Daroca Mdel C. Влияние высокогорной жизни на железо тела. Кровь. 2005; 106: 1441–6. [PubMed] [Google Scholar] 81. Ян З., Дьюи К.Г., Лоннердал Б., Хернелл О., Чапарро С., Аду-Афарвуа С. и др. Сравнение концентрации ферритина в плазме с соотношением рецептора трансферрина в плазме и ферритина для оценки запасов железа в организме: результаты 4 интервенционных испытаний. Am J Clin Nutr. 2008; 87: 1892–8. [PubMed] [Google Scholar] 82.Де Бенуа Б., Маклин Э., Эгли И., Когсуэлл М. — редакторы. Женева: Пресса ВОЗ, Всемирная организация здравоохранения; 2008. ВОЗ / CDC. Библиотечная каталогизация в публикации. Распространенность анемии в мире, 1993–2005 гг .: глобальная база данных ВОЗ по анемии; п. 40. [Google Scholar] 83. Джонсон-Уимбли Т.Д., Грэм Д.Ю. Диагностика и лечение железодефицитной анемии в 21 веке. Ther Adv Гастроэнтерол. 2011; 4: 177–84. [Бесплатная статья PMC] [PubMed] [Google Scholar] 84. Зарычанский Р., Хьюстон Д.С. Анемия хронического заболевания: вредное заболевание или адаптивная, полезная реакция? Can Med Assoc J.2008. 179: 333–7. [Бесплатная статья PMC] [PubMed] [Google Scholar] 85. Weiss G, Goodnough LT. Анемия хронического заболевания. N Engl J Med. 2005; 352: 1011–23. [PubMed] [Google Scholar] 86. 2-е изд. Женева: 2004 г. ВОЗ / CDC. Отчет о совместной технической консультации Всемирной организации здравоохранения / Центров по контролю и профилактике заболеваний по оценке статуса железа на уровне населения; п. 108. [Google Scholar] 87. Knight K, Wade S, Balducci L. Распространенность и исходы анемии при раке: систематический обзор литературы.Am J Med. 2004; 116: 11–26С. [PubMed] [Google Scholar] 88. О’Мара NB. Больные анемией с хроническими заболеваниями почек. Спектр диабета. 2008; 21: 12–9. [Google Scholar] 89. Нурко С. Анемия при хронической болезни почек: причины, диагностика, лечение. Cleve Clin J Med. 2006. 73: 289–97. [PubMed] [Google Scholar] 90. Горовиц К.М., Ингардия С.Дж., Боргида А.Ф. 2013, Анемия при беременности. Clin Lab Med. 2013; 33: 281–91. [PubMed] [Google Scholar] 91. Ауск К.Дж., Иоанну Г.Н. Связано ли ожирение с анемией хронического заболевания? Популяционное исследование.Ожирение. 2008. 16: 2356–61. [PubMed] [Google Scholar] 92. Aeberli I, Hurrell RF, Zimmermann MB. Дети с избыточным весом имеют более высокие концентрации циркулирующего гепсидина и более низкий статус железа, но их потребление железа с пищей и биодоступность сопоставимы с детьми с нормальным весом. Int J Obes. 2009; 33: 1111–7. [PubMed] [Google Scholar] 94. Lewis G, Wise MP, Poynton C, Godkin A. Случай стойкой анемии и злоупотребления алкоголем. Нат Клин Практ Гастроэнтерол Гепатол. 2007; 4: 521–6. [PubMed] [Google Scholar] 95. Lindenbaum J, Роман MJ.Пищевая анемия при алкоголизме. Am J Clin Nutr. 1980; 33: 2727–35. [PubMed] [Google Scholar] 96. Cox SE, L’Esperance V, Makani J, Soka D, Prentice AM, Hill CM и др. Серповидно-клеточная анемия: доступность железа и ночная оксиметрия. J Clin Sleep Med. 2012; 8: 541–5. [Бесплатная статья PMC] [PubMed] [Google Scholar] 98. Манси Х.Л., младший, Кэмпбелл Дж. Альфа- и бета-талассемия. Я семейный врач. 2009; 80: 339–44. [PubMed] [Google Scholar] 99. Сегель ГБ, Лихтман М.А. Апластическая анемия: приобретенная и наследственная. В: Каушанский К., Вильямс В.Дж., редакторы.Гематология Вильямса. 8-е изд. Нью-Йорк: McGraw-Hill Medical; 2010. С. 569–90. [Google Scholar] 100. Янг Н.С., Каладо Р.Т., Шейнберг П. Современные концепции патофизиологии и лечения апластической анемии. Кровь. 2006; 108: 2509–19. [Бесплатная статья PMC] [PubMed] [Google Scholar] 101. Шейнберг П., Чен Дж. Апластическая анемия: что мы узнали на моделях на животных и в клинике. Semin Hematol. 2013; 50: 156–64. [PubMed] [Google Scholar] 102. Dhaliwal G, Cornett PA, Tierney LM., Jr Гемолитическая анемия.Я семейный врач. 2004. 69: 2599–606. [PubMed] [Google Scholar] 103. Hurrell RF. Как обеспечить адекватное усвоение железа из продуктов, обогащенных железом. Nutr Rev. 2002; 60: S7–15. [PubMed] [Google Scholar] 104. Повар JD. Диагностика и лечение железодефицитной анемии. Лучшая практика Res Clin Haematol. 2005; 18: 319–32. [PubMed] [Google Scholar] 105. Schlemmer U, Frølich W, Prieto RM, Grases F. Фитат в пищевых продуктах и значение для человека: источники пищи, потребление, обработка, биодоступность, защитная роль и анализ.Mol Nutr Food Res. 2009; 53: S330–75. [PubMed] [Google Scholar] 106. Лян Дж., Хан Б.З., Ноут М.Дж., Хамер Р.Дж. Влияние замачивания, прорастания и ферментации на общую фитиновую кислоту и растворимый цинк in vitro в коричневом рисе. Food Chem. 2008; 110: 821–8. [PubMed] [Google Scholar] 107. Кавалли-Сфорца Т., Бергер Дж., Смитасири С., Витери Ф. Еженедельное употребление добавок железа и фолиевой кислоты для женщин репродуктивного возраста: обзор воздействия, извлеченные уроки, планы расширения и вклад в достижение целей развития тысячелетия.Nutr Rev.2005; 63: S152–8. [PubMed] [Google Scholar] 109. Oppenheimer SJ. Железо и его отношение к иммунитету и инфекционным заболеваниям. J Nutr. 2001; 131: S616–33. [PubMed] [Google Scholar] 110. Sazawal S, Black RE, Ramsan M, Chwaya HM, Stoltzfus RJ, Dutta A и др. Влияние обычных профилактических добавок с железом и фолиевой кислотой на госпитализацию и смертность детей дошкольного возраста в условиях высокой передачи малярии: рандомизированное плацебо-контролируемое исследование на уровне общины. Ланцет. 2006; 367: 133–43.[PubMed] [Google Scholar] 112. Hurrell RF. Обогащение железом: его эффективность и безопасность в отношении инфекций. Еда Nutr Bull. 2007. 28: 585–94. [PubMed] [Google Scholar] 114. Лукка П., Харрелл Р., Потрикус И. Борьба с железодефицитной анемией с помощью риса, богатого железом. J Am Coll Nutr. 2002; 21: 184С – 90. [PubMed] [Google Scholar] 115. Рухани Н., Харрелл Р., Келишади Р., Шулин Р. Цинк и его значение для здоровья человека: интегративный обзор. J Res Med Sci. 2013; 18: 144–57. [Бесплатная статья PMC] [PubMed] [Google Scholar]Обзор железа и его значения для здоровья человека
J Res Med Sci.2014 фев; 19 (2): 164–174.
Назанин Аббаспур
Департамент наук о системах окружающей среды, Институт наземных экосистем, Швейцарский федеральный технологический институт, Цюрих, Швейцария
Ричард Харрелл
1 Департамент здравоохранения и технологий, Лаборатория питания человека, Институт пищевых продуктов , Питание и здоровье, Швейцарский федеральный технологический институт, Цюрих, Швейцария
Роя Келишади
2 Исследовательский центр детского роста и развития, Исфаханский университет медицинских наук, Исфахан, Иран
Департамент науки о системах окружающей среды, Институт наземных исследований Экосистема, Швейцарский федеральный технологический институт, Цюрих, Швейцария
1 Департамент медицинских наук и технологий, Лаборатория питания человека, Институт питания, питания и здоровья Швейцарского федерального технологического института, Цюрих, Швейцария
2 Исследования роста и развития детей Ce nter, Исфаханский университет медицинских наук, Исфахан, Иран
Адрес для корреспонденции: Prof.Роя Келишади, Исследовательский центр детского роста и развития Исфаханский университет медицинских наук, Исфахан, Иран. Электронная почта: ri.ca.ium.dem@idahsilekПоступила в редакцию 8 июня 2013 г .; Пересмотрено 3 ноября 2013 г .; Принято 27 ноября 2013 г.
Авторские права: © Journal of Research in Medical SciencesЭто статья в открытом доступе, распространяемая в соответствии с условиями Creative Commons Attribution-Noncommercial-Share Alike 3.0 Unported, что разрешает неограниченное использование, распространение и воспроизведение в на любом носителе при условии правильного цитирования оригинальной работы.
Эта статья цитируется в других статьях в PMC.Abstract
Хорошо известно, что недостаток или чрезмерное воздействие различных элементов оказывает заметное влияние на здоровье человека. Действие элемента определяется несколькими характеристиками, включая абсорбцию, метаболизм и степень взаимодействия с физиологическими процессами. Железо является важным элементом почти для всех живых организмов, поскольку оно участвует в широком спектре метаболических процессов, включая транспорт кислорода, синтез дезоксирибонуклеиновой кислоты (ДНК) и транспорт электронов.Однако, поскольку железо может образовывать свободные радикалы, его концентрацию в тканях организма необходимо строго регулировать, поскольку в чрезмерных количествах оно может привести к повреждению тканей. Нарушения метаболизма железа являются одними из наиболее распространенных заболеваний человека и охватывают широкий спектр заболеваний с различными клиническими проявлениями, от анемии до перегрузки железом и, возможно, до нейродегенеративных заболеваний. В этом обзоре мы обсуждаем последние достижения в исследованиях метаболизма и биодоступности железа, а также наше текущее понимание потребности человека в железе, а также последствий и причин дефицита железа.Наконец, мы обсуждаем стратегии предотвращения дефицита железа.
Ключевые слова: Анемия, потребность человека в железе, биодоступность железа, дефицит железа, метаболизм железа
ВВЕДЕНИЕ
С древних времен человек осознавал особую роль железа в здоровье и болезнях. [1] Железо вначале использовалось в медицине египтянами, индуистами, греками и римлянами. [2, 3] В 17 — веках железо использовалось для лечения хлороза (зеленой болезни), состояния, часто возникающего из-за дефицита железа.[4] Однако только в 1932 году важность железа была окончательно установлена убедительным доказательством того, что неорганическое железо необходимо для синтеза гемоглобина. [5] В течение многих лет пищевой интерес к железу был сосредоточен на его роли в образовании гемоглобина и транспорте кислорода. [6] В настоящее время, хотя низкое потребление железа и / или его биодоступность являются причиной большинства анемий в промышленно развитых странах, на них приходится лишь около половины анемии в развивающихся странах [7], где инфекционные и воспалительные заболевания (особенно малярия), кровопотеря от паразитарных инфекций. , и дефицит других питательных веществ (витамина А, рибофлавина, фолиевой кислоты и витамина B12) также являются важными причинами.[8]
Биохимия и физиология
В отличие от цинка, железо является распространенным элементом на Земле [2,9] и является биологически важным компонентом каждого живого организма. [10,11] Однако, несмотря на его геологическое изобилие, железо часто является фактором, ограничивающим рост в окружающей среде. [9] Этот кажущийся парадокс связан с тем фактом, что при контакте с кислородом железо образует оксиды, которые очень нерастворимы и, следовательно, не доступны для усвоения организмами [2]. В ответ возникли различные клеточные механизмы захвата железа из окружающей среды в биологически полезных формах.Примерами являются сидерофоры, секретируемые микробами для захвата железа в высокоспецифический комплекс [12], или механизмы восстановления железа из нерастворимого трехвалентного железа (Fe +3 ) до растворимой двухвалентной формы (Fe +2 ), как в дрожжах. [13] Многие механизмы, обнаруженные у низших организмов, имеют аналогичные аналоги у высших организмов, включая человека. В организме человека железо в основном существует в сложных формах, связанных с белком (гемопротеином), в виде гемовых соединений (гемоглобин или миоглобин), гемовых ферментов или негемовых соединений (ферменты флавин-железо, переносчики и ферритин).[3] Организму требуется железо для синтеза белков, переносящих кислород, в частности гемоглобина и миоглобина, а также для образования гемовых ферментов и других железосодержащих ферментов, участвующих в переносе электронов и окислении-восстановлении. [14,3] Почти Две трети железа в организме содержится в гемоглобине, присутствующем в циркулирующих эритроцитах, 25% содержится в легко мобилизуемых запасах железа, а оставшиеся 15% связаны с миоглобином в мышечной ткани и с различными ферментами, участвующими в окислительном процессе. метаболизм и многие другие функции клеток.[15]
Железо перерабатывается и, таким образом, сохраняется в организме. показана схематическая диаграмма цикла железа в организме. Железо доставляется в ткани с помощью циркулирующего трансферрина, переносчика, который захватывает железо, высвобождаемое в плазму, в основном из кишечных энтероцитов или ретикулоэндотелиальных макрофагов. Связывание нагруженного железом трансферрина с рецептором трансферрина на клеточной поверхности (TfR) 1 приводит к эндоцитозу и поглощению металлического груза. Интернализованное железо транспортируется в митохондрии для синтеза гема или кластеров железо-сера, которые являются неотъемлемой частью нескольких металлопротеинов, а избыток железа накапливается и детоксифицируется в цитозольном ферритине.
Железо связывается и транспортируется в организме через трансферрин и сохраняется в молекулах ферритина. После всасывания железа не существует физиологического механизма выведения избыточного железа из организма, кроме кровопотери, то есть беременности, менструации или другого кровотечения обычно низкий, но может колебаться от 5% до 35% в зависимости от обстоятельств и типа железа. [3]
Поглощение железа энтероцитами осуществляется переносчиком двухвалентного металла 1, входящим в группу переносчиков растворенных веществ мембранных транспортных белков.Это происходит преимущественно в двенадцатиперстной кишке и верхних отделах тощей кишки [16]. Затем он переносится через слизистую двенадцатиперстной кишки в кровь, где транспортируется трансферрином к клеткам или костному мозгу для эритропоэза [продуцирования красных кровяных телец (эритроцитов)]. [14,17,18] Существует механизм обратной связи, который усиливается. всасывание железа у людей с дефицитом железа. Напротив, люди с перегрузкой железом снижают абсорбцию железа через гепсидин. В настоящее время общепринято, что абсорбция железа контролируется ферропортином, который позволяет или не позволяет железу из клетки слизистой оболочки попадать в плазму.
Физическое состояние железа, поступающего в двенадцатиперстную кишку, сильно влияет на его всасывание. При физиологическом pH двухвалентное железо (Fe +2 ) быстро окисляется до нерастворимой трехвалентной формы (Fe +3 ). Желудочная кислота снижает pH в проксимальном отделе двенадцатиперстной кишки, снижая содержание Fe +3 в просвете кишечника за счет редуктазы железа, тем самым обеспечивая последующий транспорт Fe +2 через апикальную мембрану энтероцитов. Это увеличивает растворимость и поглощение трехвалентного железа.Когда продукция желудочного сока нарушена (например, ингибиторами кислотного насоса, такими как лекарство, прилосек), абсорбция железа существенно снижается.
Диетический гем также может транспортироваться через апикальную мембрану по еще неизвестному механизму и впоследствии метаболизироваться в энтероцитах гемоксигеназой 1 (HO-1) с высвобождением (Fe +2 ) [19]. Этот процесс более эффективен, чем абсорбция неорганического железа, и не зависит от рН двенадцатиперстной кишки. Таким образом, на него не влияют такие ингибиторы, как фитат и полифенолы.Следовательно, красное мясо с высоким содержанием гемоглобина является отличным источником железа. Непосредственно интернализованный Fe +2 обрабатывается энтероцитами и в конечном итоге (или нет) экспортируется через базолатеральную мембрану в кровоток через транспортер ферропортин Fe +2 . Ферропортин-опосредованный отток Fe +2 связан с его повторным окислением с Fe +2 , катализируемым мембраносвязанным ферроксидазой гефестином, который физически взаимодействует с ферропортином [20] и, возможно, также его плазменным гомологом церулоплазмином.Экспортируемое железо улавливается трансферрином, который поддерживает Fe +3 в окислительно-восстановительном инертном состоянии и доставляет его в ткани. Общее содержание железа в трансферрине (≈3 мг) соответствует менее 0,1% железа в организме, но оно очень динамично и подвергается более чем 10-кратному ежедневному обороту для поддержания эритропоэза. Пул трансферрина железа пополняется в основном за счет железа, рециркулируемого из неэффективных эритроцитов, и, в меньшей степени, за счет вновь абсорбированного пищевого железа. Стареющие эритроциты очищаются ретикулоэндотелиальными макрофагами, которые метаболизируют гемоглобин и гем и высвобождают железо в кровоток.По аналогии с кишечными энтероцитами, макрофаги экспортируют Fe +2 из своей плазматической мембраны через ферропортин в процессе, сопряженном с повторным окислением Fe +2 до Fe +3 церулоплазмином с последующей загрузкой Fe +3. на трансферрин. [21]
Theil et al ., [21] недавно сообщили, что существует также независимый механизм абсорбции растительных ферритинов, в основном присутствующих в бобовых. Однако актуальность переносчика ферритина неясна, поскольку большая часть ферритина, по-видимому, разлагается во время обработки и переваривания пищи, тем самым высвобождая неорганическое железо из оболочки ферритина для поглощения по нормальному механизму.[22] Поскольку одна молекула ферритина содержит 1000 или более атомов железа и на нее также не должны влиять ингибиторы абсорбции железа, такой механизм может стать важным источником железа в развивающихся странах, где обычно потребляются бобовые.
Регуляция гомеостаза железа
Поскольку железо требуется для ряда разнообразных клеточных функций, для поддержания гомеостаза железа требуется постоянный баланс между поглощением, транспортом, хранением и использованием железа. [11] Поскольку в организме отсутствует определенный механизм активного выведения железа, баланс железа в основном регулируется в точке абсорбции.[23,24]
Гепсидин — это циркулирующий пептидный гормон, секретируемый печенью, который играет центральную роль в регуляции гомеостаза железа. Это главный регулятор системного гомеостаза железа, координирующий использование и хранение железа с приобретением железа. [25] Этот гормон в основном вырабатывается гепатоцитами и является негативным регулятором поступления железа в плазму []. Гепсидин действует путем связывания с ферропортином, переносчиком железа, присутствующим на клетках двенадцатиперстной кишки, макрофагах и клетках плаценты.Связывание гепсидина вызывает интернализацию и деградацию ферропортина. [26] Потеря ферропортина с поверхности клетки предотвращает попадание железа в плазму []. Снижение поступления железа в плазму приводит к низкому насыщению трансферрина и меньшему количеству железа доставляется в развивающийся эритробласт. Напротив, снижение экспрессии гепсидина приводит к увеличению ферропортина на клеточной поверхности и увеличению абсорбции железа [27] []. У всех видов концентрация железа в биологических жидкостях строго регулируется, чтобы обеспечить необходимое количество железа и избежать токсичности, поскольку избыток железа может привести к образованию активных форм кислорода.[28] Гомеостаз железа у млекопитающих регулируется на уровне кишечной абсорбции, поскольку для железа не существует экскреторного пути.
Гепсидин-опосредованная регуляция гомеостаза железа. (а) Повышенная экспрессия гепсидина печенью является результатом воспалительных стимулов. Высокий уровень гепсидина в кровотоке приводит к интернализации и деградации ферропортина, экспортера железа. Потеря ферропортина на клеточной поверхности приводит к загрузке железа макрофагами, низким уровням железа в плазме и снижению эритропоэза из-за снижения количества железа, связанного с трансферрином.Снижение эритропоэза приводит к анемии хронического заболевания. (b) Нормальные уровни гепсидина в ответ на потребность в железе регулируют уровень импорта железа в плазму, нормальное насыщение трансферрина и нормальные уровни эритропоэза. (c) Гемохроматоз или перегрузка железом возникает из-за недостаточного уровня гепсидина, вызывая повышенный импорт железа в плазму, высокое насыщение трансферрина и избыточное отложение железа в печени. Источник: Де Доменико, и др. . [27]
Уровни гепсидина в плазме регулируются различными стимулами, включая цитокины, железо в плазме, анемию и гипоксию.Нарушение регуляции экспрессии гепсидина приводит к нарушениям железа. Избыточная экспрессия гепсидина приводит к анемии хронического заболевания, в то время как низкая выработка гепсидина приводит к наследственному гемохроматозу (HFE) с последующим накоплением железа в жизненно важных органах []. Большинство наследственных заболеваний, связанных с железом, возникает в результате недостаточного производства гепсидина по сравнению со степенью накопления железа в тканях. Было показано, что нарушение экспрессии гепсидина является результатом мутаций в любом из 4 различных генов: TfR2, HFE, гемохроматоз типа 2 (HFE2) и антимикробный пептид гепсидина (HAMP).Мутации в HAMP, гене, кодирующем гепсидин, приводят к болезни, связанной с перегрузкой железом, поскольку отсутствие гепсидина обеспечивает постоянное высокое всасывание железа. Роль других генов (TFR2, HFE и HFE2) в регуляции продукции гепсидина не ясна [27].
Хранение
Концентрация ферритина вместе с концентрацией гемосидерина отражает запасы железа в организме. Они хранят железо в нерастворимой форме и присутствуют в основном в печени, селезенке и костном мозге. [2] Большая часть железа связана с широко распространенным и высококонсервативным железосвязывающим белком ферритином.[18] Гемосидерин представляет собой комплекс хранения железа, который с меньшей готовностью выделяет железо для нужд организма. В условиях устойчивого состояния сывороточные концентрации ферритина хорошо коррелируют с общими запасами железа в организме. [29] Таким образом, сывороточный ферритин является наиболее удобным лабораторным тестом для оценки запасов железа.
Выделение
Помимо потерь железа из-за менструации, другого кровотечения или беременности, железо очень консервативно и нелегко выводится из организма. [30] Существует некоторая обязательная потеря железа из организма в результате физиологического отшелушивания клеток с эпителиальных поверхностей [30], включая кожу, мочеполовые и желудочно-кишечные тракты.[3] Однако, по оценкам, эти потери очень ограничены (≈1 мг / день). [31] Потери железа из-за кровотечения могут быть значительными, а чрезмерная менструальная кровопотеря является наиболее частой причиной дефицита железа у женщин.
БИОЛОГИЧЕСКАЯ ДОСТУПНОСТЬ
Пищевое железо встречается в двух формах: гемовая и негемовая. [23] Основными источниками гемового железа являются гемоглобин и миоглобин из мяса, птицы и рыбы, тогда как негемовое железо получают из злаков, бобовых, бобовых, фруктов и овощей.[32] Гемовое железо обладает высокой биодоступностью (15–35%), и диетические факторы мало влияют на его абсорбцию, тогда как абсорбция негемового железа намного ниже (2–20%) и сильно зависит от присутствия других пищевых компонентов. [23] Напротив, количество негемового железа в рационе во много раз превышает количество гемового железа в большинстве приемов пищи. Таким образом, несмотря на более низкую биодоступность, негемовое железо обычно вносит больший вклад в питание железом, чем гемовое железо. [33] Основными ингибиторами абсорбции железа являются фитиновая кислота, полифенолы, кальций и пептиды из частично переваренных белков.[23] Усилители — это аскорбиновая кислота и мышечная ткань, которые могут восстанавливать трехвалентное железо до двухвалентного железа и связывать его в растворимые комплексы, доступные для абсорбции. [23]
Факторы, повышающие абсорбцию железа
На абсорбцию железа влияет ряд диетических факторов. Аскорбат и цитрат частично увеличивают усвоение железа, действуя как слабые хелаторы, помогая растворить металл в двенадцатиперстной кишке []. [34] Железо легко переносится из этих соединений в клетки слизистой оболочки. Исследователи продемонстрировали дозозависимый усиливающий эффект нативной или добавленной аскорбиновой кислоты на абсорбцию железа.[34] Усиливающий эффект в значительной степени связан с его способностью восстанавливать трехвалентное железо до двухвалентного железа, но также из-за его способности хелатировать железо. [35] Аскорбиновая кислота преодолеет негативное влияние на абсорбцию железа всех ингибиторов, включая фитат, [36] полифенолы, [37], кальций и белки, содержащиеся в молочных продуктах [38], и увеличит абсорбцию как нативного, так и обогащенного железа. Во фруктах и овощах усиливающий эффект аскорбиновой кислоты часто нивелируется ингибирующим действием полифенолов.[39] Аскорбиновая кислота является единственным усилителем всасывания в вегетарианских диетах, а всасывание железа из вегетарианских и веганских блюд можно оптимизировать путем включения овощей, содержащих аскорбиновую кислоту. [40] Варка, промышленная обработка и хранение разлагают аскорбиновую кислоту и устраняют ее усиливающий эффект на усвоение железа. [41]
Таблица 1
Факторы, которые могут влиять на всасывание железа
Было показано усиливающее действие мяса, рыбы или птицы на всасывание железа из вегетарианских блюд [42], и 30 г мышечной ткани считается эквивалентом 25 мг аскорбиновой кислоты. .[33] Бьорн-Расмуссен и Халлберг [43] сообщили, что добавление курицы, говядины или рыбы к кукурузной муке увеличивало всасывание негемового железа в 2-3 раза без влияния того же количества белка, что и яичного альбумина. Как и в случае с аскорбиновой кислотой, было несколько сложнее продемонстрировать усиливающий эффект мяса при многократном приёме пищи и в полных исследованиях диеты. Reddy и др. ., [44] сообщили только о незначительном улучшении абсорбции железа (35%) в самостоятельно выбранных диетах в течение 5 дней, когда ежедневное потребление мышечной ткани было увеличено до 300 г / день, хотя в аналогичных 5-дневных рационах. В ходе дневного исследования 60 г свинины, добавленные к вегетарианской диете, увеличили всасывание железа на 50%.[45]
Факторы, ингибирующие абсорбцию железа
В растительной диете фитат (мио-инозитол гексакисфосфат) является основным ингибитором абсорбции железа. [23] Было показано, что отрицательное влияние фитата на абсорбцию железа зависит от дозы и начинается с очень низких концентраций 2-10 мг / прием пищи. [37,46] Молярное отношение фитата к железу может быть использовано для оценки влияния на абсорбцию. . Соотношение должно составлять 1: 1 или предпочтительно 0,4: 1 для значительного улучшения всасывания железа в простых злаковых или бобовых блюдах, не содержащих каких-либо усилителей усвоения железа, или 6: 1 в комбинированных блюдах с некоторыми овощами, содержащими аскорбин кислота и мясо как усилители.[47]
Полифенолы встречаются в различных количествах в растительной пище и напитках, таких как овощи, фрукты, некоторые злаки и бобовые, чай, кофе и вино. Ингибирующее действие полифенолов на абсорбцию железа было показано с черным чаем и, в меньшей степени, с травяными чаями. [48,49] В зерновых и бобовых культурах полифенолы усиливают ингибирующий эффект фитата, как было показано в исследовании, сравнивающем сорго с высоким и низким содержанием полифенолов. [23]
Было показано, что кальций отрицательно влияет на абсорбцию негемового и гемового железа, что отличает его от других ингибиторов, влияющих только на абсорбцию негемового железа.[50] Дозозависимые ингибирующие эффекты были показаны при дозах 75–300 мг, когда кальций добавлялся в булочки, и при дозах 165 мг кальция из молочных продуктов. [51] Предполагается, что исследования однократного приема пищи показывают отрицательное влияние кальция на абсорбцию железа, тогда как исследования многократного приема пищи с большим разнообразием продуктов и различными концентрациями других ингибиторов и усилителей показывают, что кальций лишь ограниченно влияет на абсорбцию железа. [52]
Было показано, что животные белки, такие как молочные белки, яичные белки и альбумин, ингибируют абсорбцию железа.[53] Было показано, что две основные белковые фракции коровьего молока, казеин и сыворотка, а также яичный белок ингибируют абсорбцию железа у человека. [54] Белки сои также снижают всасывание железа. [55]
Конкуренция с железом
Исследования конкуренции показывают, что некоторые другие тяжелые металлы могут участвовать в пути всасывания железа в кишечнике. К ним относятся свинец, марганец, кобальт и цинк. Поскольку дефицит железа часто сочетается с интоксикацией свинцом, это взаимодействие может вызвать особенно серьезные медицинские осложнения у детей.[56]
Свинец является особенно опасным элементом для метаболизма железа. [57] Свинец поглощается механизмом поглощения железа (DTM1) и вторично блокирует железо за счет конкурентного торможения. Кроме того, свинец препятствует ряду важных железозависимых метаболических этапов, таких как биосинтез гема. Это многогранное влияние имеет особенно тяжелые последствия для детей, поскольку свинец не только вызывает анемию, но и может ухудшить когнитивное развитие. Свинец естественным образом присутствует в больших количествах в грунтовых водах и почве в некоторых регионах и может тайно нанести вред здоровью детей.По этой причине большинство педиатров в США обычно проверяют содержание свинца в раннем возрасте с помощью простого анализа крови.
ТРЕБОВАНИЯ К ЧЕЛОВЕКУ
В раннем детстве потребности в железе удовлетворяются за счет небольшого количества железа, содержащегося в грудном молоке. [58] Потребность в железе заметно возрастает через 4-6 месяцев после рождения и составляет около 0,7-0,9 мг / день в течение оставшейся части первого года [58]. В возрасте от 1 до 6 лет содержание железа в организме снова увеличивается вдвое. [58] Потребность в железе также очень высока у подростков, особенно в период скачка роста.У девочек обычно происходит скачок роста до менархе, но к этому времени рост не заканчивается. У мальчиков наблюдается заметное увеличение массы и концентрации гемоглобина в период полового созревания. На этой стадии потребности в железе повышаются до уровня, превышающего средние потребности в железе у менструирующих женщин [58] [см.].
Таблица 2
Потребность в железе 97,5% людей с точки зрения абсорбированного железа a , в разбивке по возрастным группам и полу (Всемирная организация здравоохранения, 1989) ее тело.Точный баланс между потреблением и потерей пищи поддерживает этот баланс. Около 1 мг железа теряется каждый день из-за отшелушивания клеток кожи и слизистых оболочек, включая слизистую оболочку желудочно-кишечного тракта. [59] Менструация увеличивает среднесуточную потерю железа примерно до 2 мг в день у взрослых женщин в пременопаузе. [60] Увеличение массы тела во время скачков роста в неонатальном и детском возрасте временно увеличивает потребность в железе. [61]
Потребление железа с пищей необходимо для восполнения потери железа с калом и мочой, а также через кожу.Эти базальные потери составляют примерно 0,9 мг железа для взрослого мужчины и 0,8 мг для взрослой женщины. [62] У женщин репродуктивного возраста необходимо учитывать потерю железа с менструальной кровью [].
ГРУППЫ ПОВЫШЕННОГО РИСКА
Наибольшая вероятность дефицита железа обнаруживается в тех частях населения, которые не имеют надлежащего доступа к пище, богатой усвояемым железом, во время стадий высокой потребности в железе. Эти группы соответствуют детям, подросткам и женщинам репродуктивного возраста, особенно во время беременности.[63,58]
У младенцев и подростков повышенная потребность в железе является результатом быстрого роста. Для женщин репродуктивного возраста основная причина — чрезмерная кровопотеря во время менструации. Во время беременности потребность в железе значительно возрастает из-за быстрого роста плаценты и плода, а также увеличения глобулярной массы. [63] Напротив, взрослые мужчины и женщины в постменопаузе имеют низкий риск дефицита железа, и количество железа в нормальном рационе обычно достаточно для удовлетворения их физиологических потребностей.[63]
ПОСЛЕДСТВИЯ И ПРИЧИНЫ ДЕФИЦИТА ЖЕЛЕЗА
Последствия дефицита железа
Дефицит железа определяется как состояние, при котором отсутствуют мобилизуемые запасы железа и при котором появляются признаки нарушения поступления железа в ткани, включая эритрон. , отмечены. [64] Дефицит железа может сопровождаться анемией или без нее. Некоторые функциональные изменения могут произойти и в отсутствие анемии, но наиболее функциональные нарушения, по-видимому, возникают при развитии анемии. [2] Даже легкие и умеренные формы железодефицитной анемии могут быть связаны с функциональными нарушениями, влияющими на когнитивное развитие [65], механизмы иммунитета [66] и работоспособность.[67] Дефицит железа во время беременности связан с множеством неблагоприятных исходов как для матери, так и для ребенка, включая повышенный риск сепсиса, материнской смертности, перинатальной смертности и низкой массы тела при рождении. [68] Дефицит железа и анемия также снижают способность к обучению и связаны с повышенным уровнем заболеваемости. [68]
Причины дефицита железа
Дефицит железа возникает в результате истощения запасов железа и возникает, когда абсорбция железа не может идти в ногу с метаболическими потребностями в железе для поддержания роста и восполнения потери железа, что в первую очередь связано с кровопотерей .[2] Основные причины дефицита железа включают низкое потребление биодоступного железа, повышенную потребность в железе в результате быстрого роста, беременности, менструации и избыточную кровопотерю, вызванную патологическими инфекциями, такими как анкилостомы и власоглавы, вызывающие потерю крови из желудочно-кишечного тракта [2] 69,70,71,72] и нарушение всасывания железа. [73] Частота дефицита железа увеличивается у девочек-подростков, потому что менструальные потери железа накладываются на потребность в быстром росте [74]. Другими факторами риска дефицита железа у молодых женщин являются высокий паритет, использование внутриматочной спирали и вегетарианская диета.[75]
Дефицит железа в питании возникает, когда физиологические потребности не могут быть удовлетворены за счет абсорбции железа из рациона. [72] Биодоступность пищевого железа низка в группах населения, потребляющих однообразные растительные диеты с небольшим количеством мяса. [72] Во многих развивающихся странах растительные продукты для отлучения от груди редко обогащены железом, а частота анемии превышает 50% у детей младше 4 лет. [64]
Когда запасы железа истощаются и железа недостаточно для эритропоэза, синтез гемоглобина в предшественниках эритроцитов нарушается и появляются гематологические признаки железодефицитной анемии.
ОЦЕНКА СТАТУСА ЖЕЛЕЗА
Дефицит железа и, в конечном итоге, анемия развиваются поэтапно и могут быть оценены путем измерения различных биохимических показателей. Хотя некоторые ферменты железа чувствительны к дефициту железа [63], их активность не использовалась в качестве успешного рутинного измерения статуса железа [2].
Лабораторные измерения необходимы для правильной диагностики дефицита железа. Они наиболее информативны, когда несколько показателей уровня железа исследуются и оцениваются в контексте питания и истории болезни.
Пул железа в плазме или сыворотке — это фракция всего железа в организме, которая циркулирует в основном связанном с трансферрином. Три способа оценки уровня железа в плазме или сыворотке включают: 1) измерение общего содержания железа в единице объема в мкг / дл; 2) измерение общего количества сайтов связывания для атомов железа на трансферрине, известного как общая железосвязывающая способность в мкг / дл 2 ; и 3) оценка процента двух сайтов связывания на всех занятых молекулах трансферрина, называемого процентным насыщением трансферрина.[76] Однако заметные биологические вариации этих значений могут возникать в результате суточных колебаний, наличия инфекции или воспалительных состояний и недавнего приема железа с пищей. [76]
Протопорфирин цинка отражает нехватку железа на последних стадиях синтеза гемоглобина, так что цинк вставляется в молекулу протопорфирина вместо железа. Протопорфирин цинка может быть обнаружен в эритроцитах с помощью флуориметрии и является мерой тяжести дефицита железа. [76]
Сывороточный ферритин является хорошим индикатором запасов железа в организме в большинстве случаев.Когда концентрация сывороточного ферритина ≥15 мкг / л, присутствуют запасы железа; более высокие концентрации отражают размер хранилища железа; при низкой концентрации (<12 мкг / л для детей младше 5 лет и <15 мкг / л для детей старше 5 лет) запасы железа истощаются. [76] Однако ферритин является белком-реагентом острой фазы, и его сывороточные концентрации могут быть повышены независимо от изменения запасов железа, инфекции или воспаления. [76,2] Это означает, что может быть трудно интерпретировать концентрацию ферритина там, где инфекция болезни распространены.
Еще одним индикатором статуса железа является концентрация TfR в сыворотке крови. Поскольку TfR в основном происходит из развивающихся эритроцитов, он отражает интенсивность эритропоэза и потребность в железе. Когда запасы железа истощаются, концентрация повышается при железодефицитной анемии, что указывает на серьезную недостаточность железа. Это при условии, что нет других причин аномального эритропоэза. [76] Клинические исследования показывают, что сывороточный TfR менее подвержен воспалению, чем сывороточный ферритин. [77] Основным преимуществом TfR как индикатора является возможность оценки величины функционального дефицита железа после истощения запасов железа.[78]
Отношение TfR к ферритину (TfR / ферритин) было разработано для оценки изменений как в накопленном железе, так и в функциональном железе и считается более полезным, чем TfR или ферритин отдельно. [79] TfR / ферритин использовался для оценки запасов железа в организме как у детей, так и у взрослых. [80] Однако высокая стоимость и отсутствие стандартизации анализа TfR до сих пор ограничивали применимость метода [81].
Низкая концентрация гемоглобина является показателем анемии, конечной стадии дефицита железа.[76,2]
АНЕМИЯ И ЕЕ ПРИЧИНЫ
Анемия описывает состояние, при котором количество эритроцитов в крови низкое или в клетках крови содержится меньше нормального гемоглобина. Человека, страдающего анемией, называют анемичным. Цель эритроцитов — доставлять кислород из легких в другие части тела. Молекула гемоглобина является функциональной единицей эритроцитов и представляет собой сложную белковую структуру, которая находится внутри эритроцитов. Несмотря на то, что эритроциты производятся в костном мозге, в их производство вовлечены многие другие факторы.Например, железо — очень важный компонент молекулы гемоглобина; эритропоэтин, молекула, секретируемая почками, способствует образованию эритроцитов в костном мозге.
Наличие правильного количества эритроцитов и профилактика анемии требует взаимодействия между почками, костным мозгом и питательными веществами в организме. Если почки или костный мозг не функционируют, или организм плохо питается, то нормальное количество и функции эритроцитов может быть трудно поддерживать.
Анемия на самом деле является признаком болезненного процесса, а не самой болезни.Обычно его классифицируют как хронический или острый. Хроническая анемия возникает в течение длительного периода времени. Острая анемия возникает быстро. Определение того, присутствует ли анемия в течение длительного времени или это что-то новое, помогает врачам найти причину. Это также помогает предсказать, насколько серьезными могут быть симптомы анемии. При хронической анемии симптомы обычно начинаются медленно и постепенно прогрессируют; тогда как при острой анемии симптомы могут быть резкими и более тревожными.
Эритроциты живут около 100 дней, поэтому организм постоянно пытается их заменить.У взрослых производство эритроцитов происходит в костном мозге. Врачи пытаются определить, вызвано ли низкое количество эритроцитов повышенной кровопотерей эритроцитов или их снижением в костном мозге. Знание того, изменилось ли количество лейкоцитов и / или тромбоцитов, также помогает определить причину анемии.
По оценкам Всемирной организации здравоохранения (ВОЗ), два миллиарда человек во всем мире страдают анемией и примерно 50% всех анемий объясняются дефицитом железа. [64] Это происходит на всех этапах жизненного цикла, но чаще встречается у беременных женщин и маленьких детей.[82] Анемия является результатом множества причин, которые можно изолировать, но чаще всего они сосуществуют. Некоторые из этих причин включают следующие:
Железодефицитная анемия
Наиболее важной и частой причиной анемии является дефицит железа. [82] Если потребление железа ограничено или неадекватно из-за плохого питания, в результате может возникнуть анемия. Это называется железодефицитной анемией. Железодефицитная анемия также может возникать при наличии язвы желудка или других источников медленного хронического кровотечения (рак толстой кишки, рак матки, полипы кишечника, геморрой и т. Д.).[83]
Анемия хронического заболевания
Любое длительное заболевание может привести к анемии. Этот тип анемии является вторым по распространенности после анемии, вызванной дефицитом железа, и развивается у пациентов с острым или хроническим системным заболеванием или воспалением. [84] Это состояние было названо «анемией воспаления» из-за повышенного содержания гепсидина, который блокирует как рециркуляцию железа из макрофагов, так и абсорбцию железа. [85]
Анемия из-за активного кровотечения
Потеря крови из-за обильного менструального кровотечения или ран может вызвать анемию.[82] Язвы желудочно-кишечного тракта или раковые заболевания, такие как рак толстой кишки, могут медленно терять кровь и также могут вызывать анемию. [86,87]
Анемия, связанная с заболеванием почек
Почки выделяют гормон эритропоэтин, который помогает костному мозгу сделать эритроциты. У людей с хроническим (длительным) заболеванием почек выработка этого гормона снижена, а это, в свою очередь, снижает выработку эритроцитов, вызывая анемию. [88] Хотя дефицит эритропоэтина является основной причиной анемии при хронической почечной недостаточности, это не единственная причина.Следовательно, необходимо минимальное обследование, чтобы исключить дефицит железа и другие аномалии клеточной линии. [89]
Анемия, связанная с беременностью
Увеличение объема плазмы во время беременности приводит к разбавлению эритроцитов и может проявляться как анемия. [90] Железодефицитная анемия составляет 75% всех анемий во время беременности. [90]
Анемия, связанная с плохим питанием
Витамины и минералы необходимы для образования эритроцитов. Помимо железа, для правильного производства гемоглобина необходимы витамин B12, виамин А, фолиевая кислота, рибофлавин и медь.[82] Дефицит любого из этих питательных микроэлементов может вызвать анемию из-за недостаточного производства эритроцитов. Плохое питание — важная причина низкого уровня витаминов и, как следствие, анемии.
Ожирение и анемия
Ожирение характеризуется хроническим слабым системным воспалением, повышенным уровнем гепсидина, которое, в свою очередь, связано с анемией хронического заболевания. Ausk и Ioannou [91] предположили, что ожирение может быть связано с особенностями анемии хронического заболевания, включая низкую концентрацию гемоглобина, низкое содержание железа и трансферрина в сыворотке, а также повышенный уровень ферритина в сыворотке.Избыточный вес и ожирение были связаны с изменениями сывороточного железа, насыщения трансферрина и ферритина, которые, как ожидается, произойдут в условиях хронического системного воспаления. Воспаление, связанное с ожирением, может повышать концентрацию гепсидина и снижать доступность железа. Aeberli и др. ., [92] сравнили уровень железа, потребление железа с пищей и его биодоступность, а также циркулирующие уровни гепсидина, лептина и интерлейкина-6 (ИЛ-6) у детей с избыточной массой тела и детей с нормальным весом.Они указали, что существует пониженная доступность железа для эритропоэза у детей с избыточным весом, и что это, вероятно, связано с опосредованным гепсидином сниженным всасыванием железа и / или повышенным секвестрацией железа, а не с низким содержанием железа с пищей.
Алкоголизм
Алкоголь оказывает многочисленные неблагоприятные эффекты на различные типы клеток крови и их функции. [93] У алкоголиков часто есть дефектные эритроциты, которые преждевременно разрушаются. [93,94] Сам по себе алкоголь также может быть токсичным для костного мозга и может замедлять производство эритроцитов.[93,94] Кроме того, с алкоголизмом связаны плохое питание и дефицит витаминов и минералов. [95] Сочетание этих факторов может привести к анемии у алкоголиков.
Серповидно-клеточная анемия
Серповидно-клеточная анемия — одно из наиболее распространенных наследственных заболеваний. [96] Это заболевание, связанное с кровью, которое влияет на молекулу гемоглобина и приводит к изменению формы всей клетки крови в стрессовых условиях [97]. В таком состоянии проблема с гемоглобином бывает качественной или функциональной.Аномальные молекулы гемоглобина могут вызвать проблемы в целостности структуры эритроцитов, и они могут стать серповидными (серповидные клетки). [97] Существуют разные типы серповидно-клеточной анемии разной степени тяжести. Это особенно распространено у африканцев, ближневосточных и средиземноморских предков. [97]
Талассемия
Это еще одна группа причин анемии, связанных с гемоглобином, которая связана с отсутствием или ошибками в генах, ответственных за выработку гемоглобина. [97] Молекула гемоглобина имеет субъединицы, обычно называемые альфа- и бета-цепями глобина.Отсутствие определенной субъединицы определяет тип альфа- или бета-талассемии. [97,98] Существует много типов талассемии, которые различаются по степени тяжести от легкой (малая талассемия) до тяжелой (большая талассемия). [98] Они также являются наследственными, но вызывают количественные аномалии гемоглобина, то есть вырабатывается недостаточное количество молекул правильного типа. Альфа- и бета-талассемии являются наиболее распространенными наследственными моногенными заболеваниями в мире с наибольшей распространенностью в районах, где малярия была или все еще является эндемической.[97]
Апластическая анемия
Апластическая анемия — это заболевание, при котором разрушается костный мозг и снижается выработка клеток крови. [99] Это вызывает дефицит всех трех типов клеток крови (панцитопения), включая эритроциты (анемия), лейкоциты (лейкопения) и тромбоциты (тромбоцитопения). [100,101] Многие распространенные лекарства могут иногда вызывать этот тип анемии в качестве побочного эффекта. у некоторых людей. [99]
Гемолитическая анемия
Гемолитическая анемия — это тип анемии, при которой происходит разрыв эритроцитов, известный как гемолиз, который разрушается быстрее, чем костный мозг может их заменить.[102] Гемолитическая анемия может возникнуть по разным причинам и часто классифицируется как приобретенная или наследственная. Распространенными приобретенными причинами гемолитической анемии являются аутоиммунитет, микроангиопатия и инфекции. Нарушения ферментов эритроцитов, мембран и гемоглобина вызывают наследственную гемолитическую анемию. [102]
ПРЕДОТВРАЩЕНИЕ НЕДОСТАТОЧНОСТИ ЖЕЛЕЗА (СТРАТЕГИИ ВМЕШАТЕЛЬСТВА)
Четыре основных стратегии коррекции эффективности микронутриентов в популяциях могут использоваться для коррекции дефицита железа, как по отдельности, так и в комбинации.Это обучение в сочетании с модификацией диеты для улучшения потребления железа и его биодоступности; добавление железа (обеспечение железом, обычно в более высоких дозах, без еды), обогащение пищевых продуктов железом и новый подход к биофортификации. Однако есть некоторые трудности в применении некоторых из этих стратегий при рассмотрении железа.
Диверсификация продуктов питания
Модификации диеты для сокращения потребления Индийской стоматологической ассоциации включают увеличение потребления продуктов, богатых железом, особенно мясных продуктов, увеличение потребления фруктов и овощей, богатых аскорбиновой кислотой, для увеличения абсорбции негемового железа и снижение потребления чая и кофе, что подавляют всасывание негемового железа.[103,58] Другая стратегия — снизить содержание антинутриентов, чтобы сделать железо, поступающее из их пищевых источников, более доступным. Биодоступность железа может быть увеличена такими методами, как проращивание и ферментация, которые способствуют ферментативному гидролизу фитиновой кислоты в цельнозерновых зерновых и бобовых культурах за счет повышения активности эндогенных или экзогенных ферментов фитазы. [104] Даже использование неферментативных методов, таких как термическая обработка, замачивание и измельчение, для снижения содержания фитиновой кислоты в основных продуктах растительного происхождения было успешным в улучшении биодоступности железа (и цинка).[105,106]
Добавка
Для перорального приема добавок железа предпочтительны соли двухвалентного железа (сульфат двухвалентного железа и глюконат двухвалентного железа) из-за их низкой стоимости и высокой биодоступности. [72] Хотя абсорбция железа выше при приеме добавок железа натощак, тошнота и боль в эпигастрии могут развиться из-за введенных более высоких доз железа (обычно 60 мг Fe / день). Если возникают такие побочные эффекты, следует попытаться снизить дозу между приемами пищи или давать железо во время еды, хотя пища снижает всасывание лекарственного железа примерно на две трети.[107] Добавки железа во время беременности рекомендуется в развивающихся странах, где женщины часто вступают в беременность с низкими запасами железа. [108] Хотя обычно считалось, что польза от приема добавок железа перевешивает предполагаемый риск, есть некоторые свидетельства того, что добавление в дозах, рекомендованных для здоровых детей, несет в себе риск увеличения тяжести инфекционного заболевания на фоне малярии. [109,110]
Обогащение
Обогащение пищевых продуктов железом сложнее, чем обогащение такими питательными веществами, как цинк в муке, йод в соли и витамин А в кулинарном масле.[72] Наиболее биодоступные соединения железа растворимы в воде или разбавленной кислоте, но часто вступают в реакцию с другими пищевыми компонентами, вызывая неприятный запах, изменение цвета или окисление жиров. [103] Таким образом, менее растворимые формы железа, хотя и хуже усваиваются, часто выбираются для обогащения, чтобы избежать нежелательных сенсорных изменений. [72] Обогащение обычно производится с гораздо более низкими дозами железа, чем с добавками. Это ближе к физиологической среде и может быть самым безопасным вмешательством в малярийные районы. [111] Нет никаких опасений по поводу безопасности добавок железа или обогащения железа в немалярийных эндемичных районах.[112]
Соединения железа, рекомендованные [7] для обогащения пищевых продуктов, включают сульфат железа, фумарат железа, пирофосфат железа и порошок электролитического железа. Пшеничная мука является наиболее распространенным пищевым продуктом, обогащенным железом, и она обычно обогащается порошками элементарного железа, которые не рекомендуются ВОЗ. [7,113] Харрелл и Эгли [23] сообщили, что из 78 национальных программ по пшеничной муке только восемь улучшатся. статус железа. В этих программах использовались рекомендуемые соединения железа на рекомендованных уровнях.Другие страны использовали не рекомендуемые соединения или более низкие уровни железа по сравнению с потреблением муки. Коммерческое детское питание, такое как смеси и злаки, также обычно обогащено железом.
Биофортификация
Содержание железа варьируется от 25 до 56 мг / кг в различных сортах пшеницы и от 7 до 23 мг / кг в рисовых зернах. Однако большая часть этого железа удаляется в процессе измельчения. Поглощение железа зерновыми и бобовыми культурами, многие из которых имеют высокое содержание самородного железа, обычно низкое из-за высокого содержания в них фитата, а иногда и полифенолов.[48] Стратегии биофортификации включают селекцию растений и генную инженерию. Уровни железа в обычных бобах и просе были успешно увеличены путем селекции растений, но использование других основных продуктов питания является более трудным или невозможным (рис) из-за недостаточной естественной генетической изменчивости. Lucca и др. ., [114] увеличили содержание железа в эндосперме риса, чтобы улучшить его всасывание в кишечнике человека с помощью генной инженерии. Они ввели ген ферритина из Phaseolus vulgaris в рисовые зерна, увеличив содержание железа в них вдвое.Чтобы увеличить биодоступность железа, они ввели в эндосперм риса термотолерантную фитазу из Aspergillus fumigatus . Они указали, что этот рис с более высоким содержанием железа и богатой фитазой имеет большой потенциал для существенного улучшения питания железом в тех популяциях, где дефицит железа так широко распространен. [114] К сожалению, фитаза не устояла перед приготовлением. Важность различных минералов, таких как цинк [115] и железо, требует большего внимания на индивидуальном уровне и уровне общественного здравоохранения.
Сноски
Источник поддержки: Нет
Конфликт интересов: Не объявлен.
СПИСОК ЛИТЕРАТУРЫ
1. Борода Дж. Л., Доусон HD. Утюг. В: О’Делл Б.Л., Сунде Р.А., редакторы. Справочник по незаменимым в питании минеральным элементам. Нью-Йорк: CRC Press; 1997. С. 275–334. [Google Scholar] 2. Вуд Р.Дж., Ронненберг А. Железо. В: Shils ME, Shike M, Ross AC, Caballero B, Cousins RJ, редакторы. Современное питание в здоровье и болезнях. 10-е изд. Балтимор: Липпинкотт Уильямс и Уилкинс; 2005 г.С. 248–70. [Google Scholar] 3. Макдауэлл LR. 2-е изд. Амстердам: Elsevier Science; 2003. Минералы в питании животных и человека; п. 660. [Google Scholar] 4. Гуггенхайм KY. Хлороз: возникновение и исчезновение болезни, связанной с питанием. J Nutr. 1995; 125: 1822–5. [PubMed] [Google Scholar] 5. Ип Р., Даллман PR. Утюг. В: Ziegler EE, Filer LJ, редакторы. Присутствуют знания в области питания. 7-е изд. Вашингтон, округ Колумбия: ILSI Press; 1996. С. 278–92. [Google Scholar] 6. Андервуд Э.Дж., Саттл Н.Ф. 3-е изд. Уоллингфорд: международное издательство CABI; 1999 г.Минеральное питание скота; п. 614. [Google Scholar] 7. Аллен Л., де Бенуа Б., Дари О., Харрелл Р., редакторы. Женева: ВОЗ и ФАО; 2006. ВОЗ. Рекомендации по обогащению пищевых продуктов микронутриентами; п. 236. [Google Scholar] 8. Брабин Б.Дж., Премжи З., Верхое ff Ф. Анализ анемии и детской смертности. J Nutr. 2001; 131: 636–45С. [PubMed] [Google Scholar] 9. Quintero-Gutiérrez AG, González-Rosendo G, Sánchez-Muñoz J, Polo-Pozo J, Rodríguez-Jerez JJ. Биодоступность гемового железа в начинке для печенья с использованием поросят в качестве модели животных для человека.Int J Biol Sci. 2008; 4: 58–62. [Бесплатная статья PMC] [PubMed] [Google Scholar] 10. Айзен П., Эннс С., Весслинг-Резник М. Химия и биология метаболизма железа в эукариотах. Int J Biochem Cell Biol. 2001; 33: 940–59. [PubMed] [Google Scholar] 11. Лиу П. Т., Хейскала М., Петерсон П. А., Ян Ю. Роль железа в здоровье и болезнях. Мол Аспекты Мед. 2001; 2: 1–87. [PubMed] [Google Scholar] 12. Guerinot ML. Транспорт микробного железа. Annu Rev Microbiol. 1994; 48: 743–72. [PubMed] [Google Scholar] 13. Асквит К., Каплан Дж.Транспорт железа и меди в дрожжах и его значение для болезней человека. Trends Biochem Sci. 1998. 23: 135–8. [PubMed] [Google Scholar] 15. Вашингтон, округ Колумбия: Национальная академия прессы; 2001. МОМ. Институт медицины. утюг. В: Нормы потребления витамина A, витамина K, мышьяка, бора, хрома, меди, йода, железа, марганца, молибдена, никеля, кремния, ванадия и цинка; С. 290–393. [PubMed] [Google Scholar] 16. Muir A, Hopfer U. Региональная специфичность поглощения железа щеточно-граничными мембранами тонкого кишечника у нормальных мышей и мышей с дефицитом железа.Am J Physiol. 1985; 248: G376–9. [PubMed] [Google Scholar] 17. Фрейзер Д.М., Андерсон Г.Дж. Импорт железа. I. Абсорбция железа в кишечнике и ее регуляция. Am J Physiol Gastrointest Liver Physiol. 2005; 289: G631–5. [PubMed] [Google Scholar] 18. Наддур С.С., Шрирама К., Мудипалли А. Механизмы транспорта и гомеостаза железа: их роль в здоровье и болезнях. Индийский J Med Res. 2008; 128: 533–44. [PubMed] [Google Scholar] 20. Yeh KY, Yeh M, Mims L, Glass J. Кормление железом индуцирует миграцию и взаимодействие ферропортина 1 и гефестина в двенадцатиперстном эпителии крыс.Am J Physiol Gastrointest Liver Physiol. 2009. 296: 55–65. [Бесплатная статья PMC] [PubMed] [Google Scholar] 21. Тейл Э.С., Чен Х., Миранда С., Янсер Х., Эльзенханс Б., Нуньес М.Т. и др. Абсорбция железа из ферритина не зависит от гемового железа и солей двухвалентного железа у женщин и сегментов кишечника крыс. J Nutr. 2012; 142: 478–83. [Бесплатная статья PMC] [PubMed] [Google Scholar] 22. Hoppler M, Schoenbaechler A, Meile L, Hurrell RF, Walczyk T. Ферритин-железо высвобождается во время кипячения и in vitro при пищеварении в желудке .J Nutr. 2008. 138: 878–84. [PubMed] [Google Scholar] 23. Hurrell R, Egli I. Биодоступность железа и диетические контрольные значения. Am J Clin Nutr. 2010; 91: 1461–7S. [PubMed] [Google Scholar] 25. Немет Э., Ганц Т. Регулирование метаболизма железа гепсидином. Анну Рев Нутр. 2006; 26: 323–42. [PubMed] [Google Scholar] 26. Немет Э., Таттл М.С., Пауэлсон Дж., Вон М.Б., Донован А., Уорд Д.М. и др. Гепсидин регулирует отток клеточного железа, связываясь с ферропортином и индуцируя его интернализацию. Наука. 2004; 306: 2090–3.[PubMed] [Google Scholar] 28. Браун В., Киллманн Х. Бактериальные решения проблемы снабжения железом. Trends Biochem Sci. 1999; 24: 104–109. [PubMed] [Google Scholar] 29. Хант-младший. Насколько важна биодоступность железа с пищей? Am J Clin Nutr. 2001; 73: 3–4. [PubMed] [Google Scholar] 30. Хант-младший, Зито, Калифорния, Джонсон, Лос-Анджелес. Выведение железа из организма здоровыми мужчинами и женщинами. Am J Clin Nutr. 2009; 89: 1–7. [PubMed] [Google Scholar] 31. Фэрбенкс В.Ф. Железо в медицине и питании. В: Shils ME, Shike M, Ross AC, Caballero B, Cousins RJ, редакторы.Современное питание в здоровье и болезнях. 10-е изд. Балтимор: Липпинкотт Уильямс и Уилкинс; 1999. С. 193–221. [Google Scholar] 32. потребности человека в витаминах и минералах. Рим: ФАО; 2001. ФАО / ВОЗ. Пищевые подходы к удовлетворению потребностей в витаминах и минералах; С. 7–25. [Google Scholar] 33. Monsen ER, Hallberg L, Layrisse M, Hegsted DM, Cook JD, Mertz W. и др. Оценка доступного пищевого железа. Am J Clin Nutr. 1978; 31: 134–41. [PubMed] [Google Scholar] 34. Конрад ME, Umbreit JN. Краткий обзор: абсорбция железа — путь муцин-мобилферрин-интегрин.Конкурентоспособный путь поглощения металлов. Am J Hematol. 1993; 42: 67–73. [PubMed] [Google Scholar] 35. Конрад М.Э., Шаде С.Г. Хелаты аскорбиновой кислоты в абсорбции железа: роль соляной кислоты и желчи. Гастроэнтерология. 1968; 55: 35–45. [PubMed] [Google Scholar] 36. Холлберг Л., Брюн М., Россандер Л. Поглощение железа у человека: аскорбиновая кислота и дозозависимое ингибирование фитатом. Am J Clin Nutr. 1989; 49: 140–4. [PubMed] [Google Scholar] 37. Зигенберг Д., Бейнс Р.Д., Ботвелл Т.Х., Макфарлейн Б.Дж., Лампарелли Р.Д., Car NG и др.Аскорбиновая кислота предотвращает дозозависимое ингибирующее действие полифенолов и фитатов на абсорбцию негемового железа. Am J Clin Nutr. 1991; 53: 537–41. [PubMed] [Google Scholar] 38. Стекель А., Оливарес М., Писарро Ф., Чадуд П., Лопес И., Амар М. Поглощение обогащающего железа из молочных смесей у младенцев. Am J Clin Nutr. 1986; 43: 917–22. [PubMed] [Google Scholar] 39. Бюллетень D, Бейнс Р.Д., Ботвелл Т.Х., Гиллули М., Макфарлейн Б.Дж., Макфейл А.П. и др. Влияние фруктовых соков и фруктов на усвоение железа из рисовой муки.Br J Nutr. 1987; 57: 331–43. [PubMed] [Google Scholar] 40. Линч SR, Кук JD. Взаимодействие витамина С и железа. Ann N Y Acad Sci. 1980; 355: 32–44. [PubMed] [Google Scholar] 41. Teucher B, Olivares M, Cori H. Усилители поглощения железа: аскорбиновая кислота и другие органические кислоты. Int J Vitam Nutr Res. 2004; 74: 403–19. [PubMed] [Google Scholar] 42. Линч С.Р., Харрелл Р.Ф., Дассенко С.А., Кук Дж.Д. Влияние пищевых белков на биодоступность железа у человека. Adv Exp Med Biol. 1989; 249: 117–32. [PubMed] [Google Scholar] 43.Бьорн-Расмуссен Э., Халльберг Л. Влияние животных белков на усвоение пищевого железа человеком. Нутр Метаб. 1979; 23: 192–202. [PubMed] [Google Scholar] 44. Редди МБ, Харрелл Р.Ф., Кук JD. Разнообразное питание незначительно влияет на всасывание негемового железа у нормальных людей. J Nutr. 2006; 136: 576–81. [PubMed] [Google Scholar] 45. Бах Кристенсен М., Хелс О, Морберг С., Марвинг Дж., Бугель С., Тетенс I. Свинина увеличивает усвоение железа при 5-дневной полностью контролируемой диете по сравнению с вегетарианской диетой с аналогичным содержанием витамина С и фитиновой кислоты.Br J Nutr. 2005. 94: 78–83. [PubMed] [Google Scholar] 46. Харрелл Р.Ф., Джуллерат М.А., Редди М.Б., Линч С.Р., Дассенко С.А., Кук Дж.Д. Соевый белок, фитат и абсорбция железа у человека. Am J Clin Nutr. 1992; 56: 573–8. [PubMed] [Google Scholar] 47. Hurrell RF. Разложение фитиновой кислоты как средство улучшения усвоения железа. Int J Vitam Nutr Res. 2004. 74: 445–52. [PubMed] [Google Scholar] 48. Харрелл Р.Ф., Редди М., Кук Дж. Д.. Подавление абсорбции негемного железа у человека напитками, содержащими полифенолы. Br J Nutr.1999. 81: 289–95. [PubMed] [Google Scholar] 49. Холлберг Л., Россандер Л. Влияние различных напитков на усвоение негемового железа из сложных блюд. Hum Nutr Appl Nutr. 1982; 36: 116–23. [PubMed] [Google Scholar] 50. Hallberg L, Rossander-Hulthen L, Brune M, Gleerup A. Ингибирование усвоения гемового железа у человека кальцием. Br J Nutr. 1993; 69: 533–40. [PubMed] [Google Scholar] 51. Hallberg L, Rossander-Hulthen L. Потребность в железе у менструирующих женщин. Am J Clin Nutr. 1991; 54: 1047–58. [PubMed] [Google Scholar] 52.Линч SR. Влияние кальция на усвоение железа. Nutr Res Rev.2000; 13: 141–58. [PubMed] [Google Scholar] 53. Кук JD, Monsen ER. Поглощение пищевого железа у людей. III. Сравнение влияния животных белков на всасывание негемового железа. Am J Clin Nutr. 1976; 29: 859–67. [PubMed] [Google Scholar] 54. Харрелл РФ, Линч С.Р., Тринидад Т.П., Дассенко С.А., Кук Дж.Д. Абсорбция железа у людей: бычий сывороточный альбумин по сравнению с говяжьими мышцами и яичным белком. Am J Clin Nutr. 1988. 47: 102–7. [PubMed] [Google Scholar] 55.Линч С.Р., Дассенко С.А., Кук Дж.Д., Джульерат М.А., Харрелл РФ. Ингибирующий эффект фрагмента, связанного с соевым белком, на абсорбцию железа у людей. Am J Clin Nutr. 1994; 60: 567–72. [PubMed] [Google Scholar] 56. Piomelli S, Seaman C, Kapoor S. Вызванные свинцом аномалии метаболизма порфирина, связь с дефицитом железа. Ann N Y Acad Sci. 1987; 514: 278–88. [PubMed] [Google Scholar] 58. 2-е изд. Бангкок: 2004 г. ФАО / ВОЗ. Консультации экспертов по потребностям человека в витаминах и минералах, потребностях в витаминах и минералах в питании человека: отчет совместного экспертного заключения ФАО / ВОЗ; п.341. [Google Scholar] 59. Cook JD, Skikne BS, Lynch SR, Reusser ME. Оценки достаточности железа у населения США. Кровь. 1986; 68: 726–31. [PubMed] [Google Scholar] 60. Ботвелл TH, Чарльтон RW. Общий подход к проблемам железодефицита и перегрузки железом у населения в целом. Semin Hematol. 1982; 19: 54–67. [PubMed] [Google Scholar] 61. Гибсон Р.С., Макдональд А.С., Смит-Вандеркой П.Д. Параметры сывороточного ферритина и пищевого железа в выборке канадских детей дошкольного возраста. J Can Dietetic Assoc.1988; 49: 23–8. [Google Scholar] 62. ДеМайер Э.М., Даллман П., Герни Дж. М., Холлберг Л., Суд С. К., Срикантия С. Г., редакторы. Женева: Всемирная организация здравоохранения; 1989. ВОЗ. Профилактика и контроль железодефицитной анемии с помощью первичной медико-санитарной помощи: руководство для администраторов здравоохранения и руководителей программ; п. 58. [Google Scholar] 63. Даллман П. Айрон. В: Браун М.Л., редактор. Настоящие знания в области питания. 6-е изд. Вашингтон, округ Колумбия: Фонд питания; 1990. С. 241–50. [Google Scholar] 64. Женева: Швейцария: Всемирная организация здравоохранения; 2001 г.ВОЗ / ЮНИСЕФ / УООН. Оценка, профилактика и контроль железодефицитной анемии; п. 114. [Google Scholar] 65. Борода Дж. Л., Коннор-младший. Статус железа и нейронное функционирование. Анну Рев Нутр. 2003. 23: 41–58. [PubMed] [Google Scholar] 66. Failla ML. Микроэлементы и защита хозяина: последние достижения и сохраняющиеся проблемы. J Nutr. 2003; 133: S1443–7. [PubMed] [Google Scholar] 67. Витери Ф.Е., Торунь Б. Анемия и физическая работоспособность. В: Гарби Л., редактор. Клиники гематологии. Vol. 3. Лондон: У. Б. Сондерс; 1974. стр.609–26. [Google Scholar] 68. CDC. Табель успеваемости по грудному вскармливанию, США: показатели результатов (публикация из Центров по контролю и профилактике заболеваний, Национальное обследование иммунизации. 2010 г. [последний доступ 11 мая 2010 г.]. Http://www.cdc.gov/breastfeeding/data/index .htm .69. Купер Е.С., Банди Д.А. Трихоцефалопатия. Ballieres Clin Trop Med Commun Dis. 1987; 2: 629–43. [Google Scholar] 70. Всемирная организация здравоохранения, Женева; 1995. ВОЗ. Отчет неофициальной консультации ВОЗ. на анкилостомоз и анемию у девочек и женщин; с.46. [Google Scholar] 71. Crompton DW, Nesheim MC. Пищевая ценность кишечных гельминтозов в течение жизненного цикла человека. Анну Рев Нутр. 2002; 22: 35–99. [PubMed] [Google Scholar] 72. Ларок Р., Касапиа М., Готуццо Е., Дьеркос Т.В. Взаимосвязь между интенсивностью заражения гельминтами, передающимися через почву, и анемией во время беременности. Am J Trop Med Hyg. 2005; 73: 783–9. [PubMed] [Google Scholar] 73. Циммерманн МБ, Харрелл РФ. Недостаток пищевого железа. Ланцет. 2007; 370: 115–20. [Google Scholar] 74. Харви LJ, Armah CN, Dainty JR, Foxall RJ, John Lewis D, Langford NJ и др.Влияние менструальной кровопотери и диеты на дефицит железа у женщин в Великобритании. Br J Nutr. 2005. 94: 557–64. [PubMed] [Google Scholar] 75. Борода JL. Потребность в железе у девочек-подростков. Симпозиум: Повышение уровня железа у подростков до деторождения. J Nutr. 2000; 130: S440–2. [PubMed] [Google Scholar] 77. Бегин Ю. Растворимый рецептор трансферрина для оценки эритропоэза и статуса железа. Clinica Chimica Acta. 2003. 329: 9–22. [PubMed] [Google Scholar] 79. Повар JD, Flowers CH, Skikne BS. Количественная оценка bodyiron.Кровь. 2003. 101: 3359–64. [PubMed] [Google Scholar] 80. Кук JD, Boy E, Flowers C, Daroca Mdel C. Влияние высокогорной жизни на железо тела. Кровь. 2005; 106: 1441–6. [PubMed] [Google Scholar] 81. Ян З., Дьюи К.Г., Лоннердал Б., Хернелл О., Чапарро С., Аду-Афарвуа С. и др. Сравнение концентрации ферритина в плазме с соотношением рецептора трансферрина в плазме и ферритина для оценки запасов железа в организме: результаты 4 интервенционных испытаний. Am J Clin Nutr. 2008; 87: 1892–8. [PubMed] [Google Scholar] 82.Де Бенуа Б., Маклин Э., Эгли И., Когсуэлл М. — редакторы. Женева: Пресса ВОЗ, Всемирная организация здравоохранения; 2008. ВОЗ / CDC. Библиотечная каталогизация в публикации. Распространенность анемии в мире, 1993–2005 гг .: глобальная база данных ВОЗ по анемии; п. 40. [Google Scholar] 83. Джонсон-Уимбли Т.Д., Грэм Д.Ю. Диагностика и лечение железодефицитной анемии в 21 веке. Ther Adv Гастроэнтерол. 2011; 4: 177–84. [Бесплатная статья PMC] [PubMed] [Google Scholar] 84. Зарычанский Р., Хьюстон Д.С. Анемия хронического заболевания: вредное заболевание или адаптивная, полезная реакция? Can Med Assoc J.2008. 179: 333–7. [Бесплатная статья PMC] [PubMed] [Google Scholar] 85. Weiss G, Goodnough LT. Анемия хронического заболевания. N Engl J Med. 2005; 352: 1011–23. [PubMed] [Google Scholar] 86. 2-е изд. Женева: 2004 г. ВОЗ / CDC. Отчет о совместной технической консультации Всемирной организации здравоохранения / Центров по контролю и профилактике заболеваний по оценке статуса железа на уровне населения; п. 108. [Google Scholar] 87. Knight K, Wade S, Balducci L. Распространенность и исходы анемии при раке: систематический обзор литературы.Am J Med. 2004; 116: 11–26С. [PubMed] [Google Scholar] 88. О’Мара NB. Больные анемией с хроническими заболеваниями почек. Спектр диабета. 2008; 21: 12–9. [Google Scholar] 89. Нурко С. Анемия при хронической болезни почек: причины, диагностика, лечение. Cleve Clin J Med. 2006. 73: 289–97. [PubMed] [Google Scholar] 90. Горовиц К.М., Ингардия С.Дж., Боргида А.Ф. 2013, Анемия при беременности. Clin Lab Med. 2013; 33: 281–91. [PubMed] [Google Scholar] 91. Ауск К.Дж., Иоанну Г.Н. Связано ли ожирение с анемией хронического заболевания? Популяционное исследование.Ожирение. 2008. 16: 2356–61. [PubMed] [Google Scholar] 92. Aeberli I, Hurrell RF, Zimmermann MB. Дети с избыточным весом имеют более высокие концентрации циркулирующего гепсидина и более низкий статус железа, но их потребление железа с пищей и биодоступность сопоставимы с детьми с нормальным весом. Int J Obes. 2009; 33: 1111–7. [PubMed] [Google Scholar] 94. Lewis G, Wise MP, Poynton C, Godkin A. Случай стойкой анемии и злоупотребления алкоголем. Нат Клин Практ Гастроэнтерол Гепатол. 2007; 4: 521–6. [PubMed] [Google Scholar] 95. Lindenbaum J, Роман MJ.Пищевая анемия при алкоголизме. Am J Clin Nutr. 1980; 33: 2727–35. [PubMed] [Google Scholar] 96. Cox SE, L’Esperance V, Makani J, Soka D, Prentice AM, Hill CM и др. Серповидно-клеточная анемия: доступность железа и ночная оксиметрия. J Clin Sleep Med. 2012; 8: 541–5. [Бесплатная статья PMC] [PubMed] [Google Scholar] 98. Манси Х.Л., младший, Кэмпбелл Дж. Альфа- и бета-талассемия. Я семейный врач. 2009; 80: 339–44. [PubMed] [Google Scholar] 99. Сегель ГБ, Лихтман М.А. Апластическая анемия: приобретенная и наследственная. В: Каушанский К., Вильямс В.Дж., редакторы.Гематология Вильямса. 8-е изд. Нью-Йорк: McGraw-Hill Medical; 2010. С. 569–90. [Google Scholar] 100. Янг Н.С., Каладо Р.Т., Шейнберг П. Современные концепции патофизиологии и лечения апластической анемии. Кровь. 2006; 108: 2509–19. [Бесплатная статья PMC] [PubMed] [Google Scholar] 101. Шейнберг П., Чен Дж. Апластическая анемия: что мы узнали на моделях на животных и в клинике. Semin Hematol. 2013; 50: 156–64. [PubMed] [Google Scholar] 102. Dhaliwal G, Cornett PA, Tierney LM., Jr Гемолитическая анемия.Я семейный врач. 2004. 69: 2599–606. [PubMed] [Google Scholar] 103. Hurrell RF. Как обеспечить адекватное усвоение железа из продуктов, обогащенных железом. Nutr Rev. 2002; 60: S7–15. [PubMed] [Google Scholar] 104. Повар JD. Диагностика и лечение железодефицитной анемии. Лучшая практика Res Clin Haematol. 2005; 18: 319–32. [PubMed] [Google Scholar] 105. Schlemmer U, Frølich W, Prieto RM, Grases F. Фитат в пищевых продуктах и значение для человека: источники пищи, потребление, обработка, биодоступность, защитная роль и анализ.Mol Nutr Food Res. 2009; 53: S330–75. [PubMed] [Google Scholar] 106. Лян Дж., Хан Б.З., Ноут М.Дж., Хамер Р.Дж. Влияние замачивания, прорастания и ферментации на общую фитиновую кислоту и растворимый цинк in vitro в коричневом рисе. Food Chem. 2008; 110: 821–8. [PubMed] [Google Scholar] 107. Кавалли-Сфорца Т., Бергер Дж., Смитасири С., Витери Ф. Еженедельное употребление добавок железа и фолиевой кислоты для женщин репродуктивного возраста: обзор воздействия, извлеченные уроки, планы расширения и вклад в достижение целей развития тысячелетия.Nutr Rev.2005; 63: S152–8. [PubMed] [Google Scholar] 109. Oppenheimer SJ. Железо и его отношение к иммунитету и инфекционным заболеваниям. J Nutr. 2001; 131: S616–33. [PubMed] [Google Scholar] 110. Sazawal S, Black RE, Ramsan M, Chwaya HM, Stoltzfus RJ, Dutta A и др. Влияние обычных профилактических добавок с железом и фолиевой кислотой на госпитализацию и смертность детей дошкольного возраста в условиях высокой передачи малярии: рандомизированное плацебо-контролируемое исследование на уровне общины. Ланцет. 2006; 367: 133–43.[PubMed] [Google Scholar] 112. Hurrell RF. Обогащение железом: его эффективность и безопасность в отношении инфекций. Еда Nutr Bull. 2007. 28: 585–94. [PubMed] [Google Scholar] 114. Лукка П., Харрелл Р., Потрикус И. Борьба с железодефицитной анемией с помощью риса, богатого железом. J Am Coll Nutr. 2002; 21: 184С – 90. [PubMed] [Google Scholar] 115. Рухани Н., Харрелл Р., Келишади Р., Шулин Р. Цинк и его значение для здоровья человека: интегративный обзор. J Res Med Sci. 2013; 18: 144–57. [Бесплатная статья PMC] [PubMed] [Google Scholar]Обзор железа и его значения для здоровья человека
J Res Med Sci.2014 фев; 19 (2): 164–174.
Назанин Аббаспур
Департамент наук о системах окружающей среды, Институт наземных экосистем, Швейцарский федеральный технологический институт, Цюрих, Швейцария
Ричард Харрелл
1 Департамент здравоохранения и технологий, Лаборатория питания человека, Институт пищевых продуктов , Питание и здоровье, Швейцарский федеральный технологический институт, Цюрих, Швейцария
Роя Келишади
2 Исследовательский центр детского роста и развития, Исфаханский университет медицинских наук, Исфахан, Иран
Департамент науки о системах окружающей среды, Институт наземных исследований Экосистема, Швейцарский федеральный технологический институт, Цюрих, Швейцария
1 Департамент медицинских наук и технологий, Лаборатория питания человека, Институт питания, питания и здоровья Швейцарского федерального технологического института, Цюрих, Швейцария
2 Исследования роста и развития детей Ce nter, Исфаханский университет медицинских наук, Исфахан, Иран
Адрес для корреспонденции: Prof.Роя Келишади, Исследовательский центр детского роста и развития Исфаханский университет медицинских наук, Исфахан, Иран. Электронная почта: ri.ca.ium.dem@idahsilekПоступила в редакцию 8 июня 2013 г .; Пересмотрено 3 ноября 2013 г .; Принято 27 ноября 2013 г.
Авторские права: © Journal of Research in Medical SciencesЭто статья в открытом доступе, распространяемая в соответствии с условиями Creative Commons Attribution-Noncommercial-Share Alike 3.0 Unported, что разрешает неограниченное использование, распространение и воспроизведение в на любом носителе при условии правильного цитирования оригинальной работы.
Эта статья цитируется в других статьях в PMC.Abstract
Хорошо известно, что недостаток или чрезмерное воздействие различных элементов оказывает заметное влияние на здоровье человека. Действие элемента определяется несколькими характеристиками, включая абсорбцию, метаболизм и степень взаимодействия с физиологическими процессами. Железо является важным элементом почти для всех живых организмов, поскольку оно участвует в широком спектре метаболических процессов, включая транспорт кислорода, синтез дезоксирибонуклеиновой кислоты (ДНК) и транспорт электронов.Однако, поскольку железо может образовывать свободные радикалы, его концентрацию в тканях организма необходимо строго регулировать, поскольку в чрезмерных количествах оно может привести к повреждению тканей. Нарушения метаболизма железа являются одними из наиболее распространенных заболеваний человека и охватывают широкий спектр заболеваний с различными клиническими проявлениями, от анемии до перегрузки железом и, возможно, до нейродегенеративных заболеваний. В этом обзоре мы обсуждаем последние достижения в исследованиях метаболизма и биодоступности железа, а также наше текущее понимание потребности человека в железе, а также последствий и причин дефицита железа.Наконец, мы обсуждаем стратегии предотвращения дефицита железа.
Ключевые слова: Анемия, потребность человека в железе, биодоступность железа, дефицит железа, метаболизм железа
ВВЕДЕНИЕ
С древних времен человек осознавал особую роль железа в здоровье и болезнях. [1] Железо вначале использовалось в медицине египтянами, индуистами, греками и римлянами. [2, 3] В 17 — веках железо использовалось для лечения хлороза (зеленой болезни), состояния, часто возникающего из-за дефицита железа.[4] Однако только в 1932 году важность железа была окончательно установлена убедительным доказательством того, что неорганическое железо необходимо для синтеза гемоглобина. [5] В течение многих лет пищевой интерес к железу был сосредоточен на его роли в образовании гемоглобина и транспорте кислорода. [6] В настоящее время, хотя низкое потребление железа и / или его биодоступность являются причиной большинства анемий в промышленно развитых странах, на них приходится лишь около половины анемии в развивающихся странах [7], где инфекционные и воспалительные заболевания (особенно малярия), кровопотеря от паразитарных инфекций. , и дефицит других питательных веществ (витамина А, рибофлавина, фолиевой кислоты и витамина B12) также являются важными причинами.[8]
Биохимия и физиология
В отличие от цинка, железо является распространенным элементом на Земле [2,9] и является биологически важным компонентом каждого живого организма. [10,11] Однако, несмотря на его геологическое изобилие, железо часто является фактором, ограничивающим рост в окружающей среде. [9] Этот кажущийся парадокс связан с тем фактом, что при контакте с кислородом железо образует оксиды, которые очень нерастворимы и, следовательно, не доступны для усвоения организмами [2]. В ответ возникли различные клеточные механизмы захвата железа из окружающей среды в биологически полезных формах.Примерами являются сидерофоры, секретируемые микробами для захвата железа в высокоспецифический комплекс [12], или механизмы восстановления железа из нерастворимого трехвалентного железа (Fe +3 ) до растворимой двухвалентной формы (Fe +2 ), как в дрожжах. [13] Многие механизмы, обнаруженные у низших организмов, имеют аналогичные аналоги у высших организмов, включая человека. В организме человека железо в основном существует в сложных формах, связанных с белком (гемопротеином), в виде гемовых соединений (гемоглобин или миоглобин), гемовых ферментов или негемовых соединений (ферменты флавин-железо, переносчики и ферритин).[3] Организму требуется железо для синтеза белков, переносящих кислород, в частности гемоглобина и миоглобина, а также для образования гемовых ферментов и других железосодержащих ферментов, участвующих в переносе электронов и окислении-восстановлении. [14,3] Почти Две трети железа в организме содержится в гемоглобине, присутствующем в циркулирующих эритроцитах, 25% содержится в легко мобилизуемых запасах железа, а оставшиеся 15% связаны с миоглобином в мышечной ткани и с различными ферментами, участвующими в окислительном процессе. метаболизм и многие другие функции клеток.[15]
Железо перерабатывается и, таким образом, сохраняется в организме. показана схематическая диаграмма цикла железа в организме. Железо доставляется в ткани с помощью циркулирующего трансферрина, переносчика, который захватывает железо, высвобождаемое в плазму, в основном из кишечных энтероцитов или ретикулоэндотелиальных макрофагов. Связывание нагруженного железом трансферрина с рецептором трансферрина на клеточной поверхности (TfR) 1 приводит к эндоцитозу и поглощению металлического груза. Интернализованное железо транспортируется в митохондрии для синтеза гема или кластеров железо-сера, которые являются неотъемлемой частью нескольких металлопротеинов, а избыток железа накапливается и детоксифицируется в цитозольном ферритине.
Железо связывается и транспортируется в организме через трансферрин и сохраняется в молекулах ферритина. После всасывания железа не существует физиологического механизма выведения избыточного железа из организма, кроме кровопотери, то есть беременности, менструации или другого кровотечения обычно низкий, но может колебаться от 5% до 35% в зависимости от обстоятельств и типа железа. [3]
Поглощение железа энтероцитами осуществляется переносчиком двухвалентного металла 1, входящим в группу переносчиков растворенных веществ мембранных транспортных белков.Это происходит преимущественно в двенадцатиперстной кишке и верхних отделах тощей кишки [16]. Затем он переносится через слизистую двенадцатиперстной кишки в кровь, где транспортируется трансферрином к клеткам или костному мозгу для эритропоэза [продуцирования красных кровяных телец (эритроцитов)]. [14,17,18] Существует механизм обратной связи, который усиливается. всасывание железа у людей с дефицитом железа. Напротив, люди с перегрузкой железом снижают абсорбцию железа через гепсидин. В настоящее время общепринято, что абсорбция железа контролируется ферропортином, который позволяет или не позволяет железу из клетки слизистой оболочки попадать в плазму.
Физическое состояние железа, поступающего в двенадцатиперстную кишку, сильно влияет на его всасывание. При физиологическом pH двухвалентное железо (Fe +2 ) быстро окисляется до нерастворимой трехвалентной формы (Fe +3 ). Желудочная кислота снижает pH в проксимальном отделе двенадцатиперстной кишки, снижая содержание Fe +3 в просвете кишечника за счет редуктазы железа, тем самым обеспечивая последующий транспорт Fe +2 через апикальную мембрану энтероцитов. Это увеличивает растворимость и поглощение трехвалентного железа.Когда продукция желудочного сока нарушена (например, ингибиторами кислотного насоса, такими как лекарство, прилосек), абсорбция железа существенно снижается.
Диетический гем также может транспортироваться через апикальную мембрану по еще неизвестному механизму и впоследствии метаболизироваться в энтероцитах гемоксигеназой 1 (HO-1) с высвобождением (Fe +2 ) [19]. Этот процесс более эффективен, чем абсорбция неорганического железа, и не зависит от рН двенадцатиперстной кишки. Таким образом, на него не влияют такие ингибиторы, как фитат и полифенолы.Следовательно, красное мясо с высоким содержанием гемоглобина является отличным источником железа. Непосредственно интернализованный Fe +2 обрабатывается энтероцитами и в конечном итоге (или нет) экспортируется через базолатеральную мембрану в кровоток через транспортер ферропортин Fe +2 . Ферропортин-опосредованный отток Fe +2 связан с его повторным окислением с Fe +2 , катализируемым мембраносвязанным ферроксидазой гефестином, который физически взаимодействует с ферропортином [20] и, возможно, также его плазменным гомологом церулоплазмином.Экспортируемое железо улавливается трансферрином, который поддерживает Fe +3 в окислительно-восстановительном инертном состоянии и доставляет его в ткани. Общее содержание железа в трансферрине (≈3 мг) соответствует менее 0,1% железа в организме, но оно очень динамично и подвергается более чем 10-кратному ежедневному обороту для поддержания эритропоэза. Пул трансферрина железа пополняется в основном за счет железа, рециркулируемого из неэффективных эритроцитов, и, в меньшей степени, за счет вновь абсорбированного пищевого железа. Стареющие эритроциты очищаются ретикулоэндотелиальными макрофагами, которые метаболизируют гемоглобин и гем и высвобождают железо в кровоток.По аналогии с кишечными энтероцитами, макрофаги экспортируют Fe +2 из своей плазматической мембраны через ферропортин в процессе, сопряженном с повторным окислением Fe +2 до Fe +3 церулоплазмином с последующей загрузкой Fe +3. на трансферрин. [21]
Theil et al ., [21] недавно сообщили, что существует также независимый механизм абсорбции растительных ферритинов, в основном присутствующих в бобовых. Однако актуальность переносчика ферритина неясна, поскольку большая часть ферритина, по-видимому, разлагается во время обработки и переваривания пищи, тем самым высвобождая неорганическое железо из оболочки ферритина для поглощения по нормальному механизму.[22] Поскольку одна молекула ферритина содержит 1000 или более атомов железа и на нее также не должны влиять ингибиторы абсорбции железа, такой механизм может стать важным источником железа в развивающихся странах, где обычно потребляются бобовые.
Регуляция гомеостаза железа
Поскольку железо требуется для ряда разнообразных клеточных функций, для поддержания гомеостаза железа требуется постоянный баланс между поглощением, транспортом, хранением и использованием железа. [11] Поскольку в организме отсутствует определенный механизм активного выведения железа, баланс железа в основном регулируется в точке абсорбции.[23,24]
Гепсидин — это циркулирующий пептидный гормон, секретируемый печенью, который играет центральную роль в регуляции гомеостаза железа. Это главный регулятор системного гомеостаза железа, координирующий использование и хранение железа с приобретением железа. [25] Этот гормон в основном вырабатывается гепатоцитами и является негативным регулятором поступления железа в плазму []. Гепсидин действует путем связывания с ферропортином, переносчиком железа, присутствующим на клетках двенадцатиперстной кишки, макрофагах и клетках плаценты.Связывание гепсидина вызывает интернализацию и деградацию ферропортина. [26] Потеря ферропортина с поверхности клетки предотвращает попадание железа в плазму []. Снижение поступления железа в плазму приводит к низкому насыщению трансферрина и меньшему количеству железа доставляется в развивающийся эритробласт. Напротив, снижение экспрессии гепсидина приводит к увеличению ферропортина на клеточной поверхности и увеличению абсорбции железа [27] []. У всех видов концентрация железа в биологических жидкостях строго регулируется, чтобы обеспечить необходимое количество железа и избежать токсичности, поскольку избыток железа может привести к образованию активных форм кислорода.[28] Гомеостаз железа у млекопитающих регулируется на уровне кишечной абсорбции, поскольку для железа не существует экскреторного пути.
Гепсидин-опосредованная регуляция гомеостаза железа. (а) Повышенная экспрессия гепсидина печенью является результатом воспалительных стимулов. Высокий уровень гепсидина в кровотоке приводит к интернализации и деградации ферропортина, экспортера железа. Потеря ферропортина на клеточной поверхности приводит к загрузке железа макрофагами, низким уровням железа в плазме и снижению эритропоэза из-за снижения количества железа, связанного с трансферрином.Снижение эритропоэза приводит к анемии хронического заболевания. (b) Нормальные уровни гепсидина в ответ на потребность в железе регулируют уровень импорта железа в плазму, нормальное насыщение трансферрина и нормальные уровни эритропоэза. (c) Гемохроматоз или перегрузка железом возникает из-за недостаточного уровня гепсидина, вызывая повышенный импорт железа в плазму, высокое насыщение трансферрина и избыточное отложение железа в печени. Источник: Де Доменико, и др. . [27]
Уровни гепсидина в плазме регулируются различными стимулами, включая цитокины, железо в плазме, анемию и гипоксию.Нарушение регуляции экспрессии гепсидина приводит к нарушениям железа. Избыточная экспрессия гепсидина приводит к анемии хронического заболевания, в то время как низкая выработка гепсидина приводит к наследственному гемохроматозу (HFE) с последующим накоплением железа в жизненно важных органах []. Большинство наследственных заболеваний, связанных с железом, возникает в результате недостаточного производства гепсидина по сравнению со степенью накопления железа в тканях. Было показано, что нарушение экспрессии гепсидина является результатом мутаций в любом из 4 различных генов: TfR2, HFE, гемохроматоз типа 2 (HFE2) и антимикробный пептид гепсидина (HAMP).Мутации в HAMP, гене, кодирующем гепсидин, приводят к болезни, связанной с перегрузкой железом, поскольку отсутствие гепсидина обеспечивает постоянное высокое всасывание железа. Роль других генов (TFR2, HFE и HFE2) в регуляции продукции гепсидина не ясна [27].
Хранение
Концентрация ферритина вместе с концентрацией гемосидерина отражает запасы железа в организме. Они хранят железо в нерастворимой форме и присутствуют в основном в печени, селезенке и костном мозге. [2] Большая часть железа связана с широко распространенным и высококонсервативным железосвязывающим белком ферритином.[18] Гемосидерин представляет собой комплекс хранения железа, который с меньшей готовностью выделяет железо для нужд организма. В условиях устойчивого состояния сывороточные концентрации ферритина хорошо коррелируют с общими запасами железа в организме. [29] Таким образом, сывороточный ферритин является наиболее удобным лабораторным тестом для оценки запасов железа.
Выделение
Помимо потерь железа из-за менструации, другого кровотечения или беременности, железо очень консервативно и нелегко выводится из организма. [30] Существует некоторая обязательная потеря железа из организма в результате физиологического отшелушивания клеток с эпителиальных поверхностей [30], включая кожу, мочеполовые и желудочно-кишечные тракты.[3] Однако, по оценкам, эти потери очень ограничены (≈1 мг / день). [31] Потери железа из-за кровотечения могут быть значительными, а чрезмерная менструальная кровопотеря является наиболее частой причиной дефицита железа у женщин.
БИОЛОГИЧЕСКАЯ ДОСТУПНОСТЬ
Пищевое железо встречается в двух формах: гемовая и негемовая. [23] Основными источниками гемового железа являются гемоглобин и миоглобин из мяса, птицы и рыбы, тогда как негемовое железо получают из злаков, бобовых, бобовых, фруктов и овощей.[32] Гемовое железо обладает высокой биодоступностью (15–35%), и диетические факторы мало влияют на его абсорбцию, тогда как абсорбция негемового железа намного ниже (2–20%) и сильно зависит от присутствия других пищевых компонентов. [23] Напротив, количество негемового железа в рационе во много раз превышает количество гемового железа в большинстве приемов пищи. Таким образом, несмотря на более низкую биодоступность, негемовое железо обычно вносит больший вклад в питание железом, чем гемовое железо. [33] Основными ингибиторами абсорбции железа являются фитиновая кислота, полифенолы, кальций и пептиды из частично переваренных белков.[23] Усилители — это аскорбиновая кислота и мышечная ткань, которые могут восстанавливать трехвалентное железо до двухвалентного железа и связывать его в растворимые комплексы, доступные для абсорбции. [23]
Факторы, повышающие абсорбцию железа
На абсорбцию железа влияет ряд диетических факторов. Аскорбат и цитрат частично увеличивают усвоение железа, действуя как слабые хелаторы, помогая растворить металл в двенадцатиперстной кишке []. [34] Железо легко переносится из этих соединений в клетки слизистой оболочки. Исследователи продемонстрировали дозозависимый усиливающий эффект нативной или добавленной аскорбиновой кислоты на абсорбцию железа.[34] Усиливающий эффект в значительной степени связан с его способностью восстанавливать трехвалентное железо до двухвалентного железа, но также из-за его способности хелатировать железо. [35] Аскорбиновая кислота преодолеет негативное влияние на абсорбцию железа всех ингибиторов, включая фитат, [36] полифенолы, [37], кальций и белки, содержащиеся в молочных продуктах [38], и увеличит абсорбцию как нативного, так и обогащенного железа. Во фруктах и овощах усиливающий эффект аскорбиновой кислоты часто нивелируется ингибирующим действием полифенолов.[39] Аскорбиновая кислота является единственным усилителем всасывания в вегетарианских диетах, а всасывание железа из вегетарианских и веганских блюд можно оптимизировать путем включения овощей, содержащих аскорбиновую кислоту. [40] Варка, промышленная обработка и хранение разлагают аскорбиновую кислоту и устраняют ее усиливающий эффект на усвоение железа. [41]
Таблица 1
Факторы, которые могут влиять на всасывание железа
Было показано усиливающее действие мяса, рыбы или птицы на всасывание железа из вегетарианских блюд [42], и 30 г мышечной ткани считается эквивалентом 25 мг аскорбиновой кислоты. .[33] Бьорн-Расмуссен и Халлберг [43] сообщили, что добавление курицы, говядины или рыбы к кукурузной муке увеличивало всасывание негемового железа в 2-3 раза без влияния того же количества белка, что и яичного альбумина. Как и в случае с аскорбиновой кислотой, было несколько сложнее продемонстрировать усиливающий эффект мяса при многократном приёме пищи и в полных исследованиях диеты. Reddy и др. ., [44] сообщили только о незначительном улучшении абсорбции железа (35%) в самостоятельно выбранных диетах в течение 5 дней, когда ежедневное потребление мышечной ткани было увеличено до 300 г / день, хотя в аналогичных 5-дневных рационах. В ходе дневного исследования 60 г свинины, добавленные к вегетарианской диете, увеличили всасывание железа на 50%.[45]
Факторы, ингибирующие абсорбцию железа
В растительной диете фитат (мио-инозитол гексакисфосфат) является основным ингибитором абсорбции железа. [23] Было показано, что отрицательное влияние фитата на абсорбцию железа зависит от дозы и начинается с очень низких концентраций 2-10 мг / прием пищи. [37,46] Молярное отношение фитата к железу может быть использовано для оценки влияния на абсорбцию. . Соотношение должно составлять 1: 1 или предпочтительно 0,4: 1 для значительного улучшения всасывания железа в простых злаковых или бобовых блюдах, не содержащих каких-либо усилителей усвоения железа, или 6: 1 в комбинированных блюдах с некоторыми овощами, содержащими аскорбин кислота и мясо как усилители.[47]
Полифенолы встречаются в различных количествах в растительной пище и напитках, таких как овощи, фрукты, некоторые злаки и бобовые, чай, кофе и вино. Ингибирующее действие полифенолов на абсорбцию железа было показано с черным чаем и, в меньшей степени, с травяными чаями. [48,49] В зерновых и бобовых культурах полифенолы усиливают ингибирующий эффект фитата, как было показано в исследовании, сравнивающем сорго с высоким и низким содержанием полифенолов. [23]
Было показано, что кальций отрицательно влияет на абсорбцию негемового и гемового железа, что отличает его от других ингибиторов, влияющих только на абсорбцию негемового железа.[50] Дозозависимые ингибирующие эффекты были показаны при дозах 75–300 мг, когда кальций добавлялся в булочки, и при дозах 165 мг кальция из молочных продуктов. [51] Предполагается, что исследования однократного приема пищи показывают отрицательное влияние кальция на абсорбцию железа, тогда как исследования многократного приема пищи с большим разнообразием продуктов и различными концентрациями других ингибиторов и усилителей показывают, что кальций лишь ограниченно влияет на абсорбцию железа. [52]
Было показано, что животные белки, такие как молочные белки, яичные белки и альбумин, ингибируют абсорбцию железа.[53] Было показано, что две основные белковые фракции коровьего молока, казеин и сыворотка, а также яичный белок ингибируют абсорбцию железа у человека. [54] Белки сои также снижают всасывание железа. [55]
Конкуренция с железом
Исследования конкуренции показывают, что некоторые другие тяжелые металлы могут участвовать в пути всасывания железа в кишечнике. К ним относятся свинец, марганец, кобальт и цинк. Поскольку дефицит железа часто сочетается с интоксикацией свинцом, это взаимодействие может вызвать особенно серьезные медицинские осложнения у детей.[56]
Свинец является особенно опасным элементом для метаболизма железа. [57] Свинец поглощается механизмом поглощения железа (DTM1) и вторично блокирует железо за счет конкурентного торможения. Кроме того, свинец препятствует ряду важных железозависимых метаболических этапов, таких как биосинтез гема. Это многогранное влияние имеет особенно тяжелые последствия для детей, поскольку свинец не только вызывает анемию, но и может ухудшить когнитивное развитие. Свинец естественным образом присутствует в больших количествах в грунтовых водах и почве в некоторых регионах и может тайно нанести вред здоровью детей.По этой причине большинство педиатров в США обычно проверяют содержание свинца в раннем возрасте с помощью простого анализа крови.
ТРЕБОВАНИЯ К ЧЕЛОВЕКУ
В раннем детстве потребности в железе удовлетворяются за счет небольшого количества железа, содержащегося в грудном молоке. [58] Потребность в железе заметно возрастает через 4-6 месяцев после рождения и составляет около 0,7-0,9 мг / день в течение оставшейся части первого года [58]. В возрасте от 1 до 6 лет содержание железа в организме снова увеличивается вдвое. [58] Потребность в железе также очень высока у подростков, особенно в период скачка роста.У девочек обычно происходит скачок роста до менархе, но к этому времени рост не заканчивается. У мальчиков наблюдается заметное увеличение массы и концентрации гемоглобина в период полового созревания. На этой стадии потребности в железе повышаются до уровня, превышающего средние потребности в железе у менструирующих женщин [58] [см.].
Таблица 2
Потребность в железе 97,5% людей с точки зрения абсорбированного железа a , в разбивке по возрастным группам и полу (Всемирная организация здравоохранения, 1989) ее тело.Точный баланс между потреблением и потерей пищи поддерживает этот баланс. Около 1 мг железа теряется каждый день из-за отшелушивания клеток кожи и слизистых оболочек, включая слизистую оболочку желудочно-кишечного тракта. [59] Менструация увеличивает среднесуточную потерю железа примерно до 2 мг в день у взрослых женщин в пременопаузе. [60] Увеличение массы тела во время скачков роста в неонатальном и детском возрасте временно увеличивает потребность в железе. [61]
Потребление железа с пищей необходимо для восполнения потери железа с калом и мочой, а также через кожу.Эти базальные потери составляют примерно 0,9 мг железа для взрослого мужчины и 0,8 мг для взрослой женщины. [62] У женщин репродуктивного возраста необходимо учитывать потерю железа с менструальной кровью [].
ГРУППЫ ПОВЫШЕННОГО РИСКА
Наибольшая вероятность дефицита железа обнаруживается в тех частях населения, которые не имеют надлежащего доступа к пище, богатой усвояемым железом, во время стадий высокой потребности в железе. Эти группы соответствуют детям, подросткам и женщинам репродуктивного возраста, особенно во время беременности.[63,58]
У младенцев и подростков повышенная потребность в железе является результатом быстрого роста. Для женщин репродуктивного возраста основная причина — чрезмерная кровопотеря во время менструации. Во время беременности потребность в железе значительно возрастает из-за быстрого роста плаценты и плода, а также увеличения глобулярной массы. [63] Напротив, взрослые мужчины и женщины в постменопаузе имеют низкий риск дефицита железа, и количество железа в нормальном рационе обычно достаточно для удовлетворения их физиологических потребностей.[63]
ПОСЛЕДСТВИЯ И ПРИЧИНЫ ДЕФИЦИТА ЖЕЛЕЗА
Последствия дефицита железа
Дефицит железа определяется как состояние, при котором отсутствуют мобилизуемые запасы железа и при котором появляются признаки нарушения поступления железа в ткани, включая эритрон. , отмечены. [64] Дефицит железа может сопровождаться анемией или без нее. Некоторые функциональные изменения могут произойти и в отсутствие анемии, но наиболее функциональные нарушения, по-видимому, возникают при развитии анемии. [2] Даже легкие и умеренные формы железодефицитной анемии могут быть связаны с функциональными нарушениями, влияющими на когнитивное развитие [65], механизмы иммунитета [66] и работоспособность.[67] Дефицит железа во время беременности связан с множеством неблагоприятных исходов как для матери, так и для ребенка, включая повышенный риск сепсиса, материнской смертности, перинатальной смертности и низкой массы тела при рождении. [68] Дефицит железа и анемия также снижают способность к обучению и связаны с повышенным уровнем заболеваемости. [68]
Причины дефицита железа
Дефицит железа возникает в результате истощения запасов железа и возникает, когда абсорбция железа не может идти в ногу с метаболическими потребностями в железе для поддержания роста и восполнения потери железа, что в первую очередь связано с кровопотерей .[2] Основные причины дефицита железа включают низкое потребление биодоступного железа, повышенную потребность в железе в результате быстрого роста, беременности, менструации и избыточную кровопотерю, вызванную патологическими инфекциями, такими как анкилостомы и власоглавы, вызывающие потерю крови из желудочно-кишечного тракта [2] 69,70,71,72] и нарушение всасывания железа. [73] Частота дефицита железа увеличивается у девочек-подростков, потому что менструальные потери железа накладываются на потребность в быстром росте [74]. Другими факторами риска дефицита железа у молодых женщин являются высокий паритет, использование внутриматочной спирали и вегетарианская диета.[75]
Дефицит железа в питании возникает, когда физиологические потребности не могут быть удовлетворены за счет абсорбции железа из рациона. [72] Биодоступность пищевого железа низка в группах населения, потребляющих однообразные растительные диеты с небольшим количеством мяса. [72] Во многих развивающихся странах растительные продукты для отлучения от груди редко обогащены железом, а частота анемии превышает 50% у детей младше 4 лет. [64]
Когда запасы железа истощаются и железа недостаточно для эритропоэза, синтез гемоглобина в предшественниках эритроцитов нарушается и появляются гематологические признаки железодефицитной анемии.
ОЦЕНКА СТАТУСА ЖЕЛЕЗА
Дефицит железа и, в конечном итоге, анемия развиваются поэтапно и могут быть оценены путем измерения различных биохимических показателей. Хотя некоторые ферменты железа чувствительны к дефициту железа [63], их активность не использовалась в качестве успешного рутинного измерения статуса железа [2].
Лабораторные измерения необходимы для правильной диагностики дефицита железа. Они наиболее информативны, когда несколько показателей уровня железа исследуются и оцениваются в контексте питания и истории болезни.
Пул железа в плазме или сыворотке — это фракция всего железа в организме, которая циркулирует в основном связанном с трансферрином. Три способа оценки уровня железа в плазме или сыворотке включают: 1) измерение общего содержания железа в единице объема в мкг / дл; 2) измерение общего количества сайтов связывания для атомов железа на трансферрине, известного как общая железосвязывающая способность в мкг / дл 2 ; и 3) оценка процента двух сайтов связывания на всех занятых молекулах трансферрина, называемого процентным насыщением трансферрина.[76] Однако заметные биологические вариации этих значений могут возникать в результате суточных колебаний, наличия инфекции или воспалительных состояний и недавнего приема железа с пищей. [76]
Протопорфирин цинка отражает нехватку железа на последних стадиях синтеза гемоглобина, так что цинк вставляется в молекулу протопорфирина вместо железа. Протопорфирин цинка может быть обнаружен в эритроцитах с помощью флуориметрии и является мерой тяжести дефицита железа. [76]
Сывороточный ферритин является хорошим индикатором запасов железа в организме в большинстве случаев.Когда концентрация сывороточного ферритина ≥15 мкг / л, присутствуют запасы железа; более высокие концентрации отражают размер хранилища железа; при низкой концентрации (<12 мкг / л для детей младше 5 лет и <15 мкг / л для детей старше 5 лет) запасы железа истощаются. [76] Однако ферритин является белком-реагентом острой фазы, и его сывороточные концентрации могут быть повышены независимо от изменения запасов железа, инфекции или воспаления. [76,2] Это означает, что может быть трудно интерпретировать концентрацию ферритина там, где инфекция болезни распространены.
Еще одним индикатором статуса железа является концентрация TfR в сыворотке крови. Поскольку TfR в основном происходит из развивающихся эритроцитов, он отражает интенсивность эритропоэза и потребность в железе. Когда запасы железа истощаются, концентрация повышается при железодефицитной анемии, что указывает на серьезную недостаточность железа. Это при условии, что нет других причин аномального эритропоэза. [76] Клинические исследования показывают, что сывороточный TfR менее подвержен воспалению, чем сывороточный ферритин. [77] Основным преимуществом TfR как индикатора является возможность оценки величины функционального дефицита железа после истощения запасов железа.[78]
Отношение TfR к ферритину (TfR / ферритин) было разработано для оценки изменений как в накопленном железе, так и в функциональном железе и считается более полезным, чем TfR или ферритин отдельно. [79] TfR / ферритин использовался для оценки запасов железа в организме как у детей, так и у взрослых. [80] Однако высокая стоимость и отсутствие стандартизации анализа TfR до сих пор ограничивали применимость метода [81].
Низкая концентрация гемоглобина является показателем анемии, конечной стадии дефицита железа.[76,2]
АНЕМИЯ И ЕЕ ПРИЧИНЫ
Анемия описывает состояние, при котором количество эритроцитов в крови низкое или в клетках крови содержится меньше нормального гемоглобина. Человека, страдающего анемией, называют анемичным. Цель эритроцитов — доставлять кислород из легких в другие части тела. Молекула гемоглобина является функциональной единицей эритроцитов и представляет собой сложную белковую структуру, которая находится внутри эритроцитов. Несмотря на то, что эритроциты производятся в костном мозге, в их производство вовлечены многие другие факторы.Например, железо — очень важный компонент молекулы гемоглобина; эритропоэтин, молекула, секретируемая почками, способствует образованию эритроцитов в костном мозге.
Наличие правильного количества эритроцитов и профилактика анемии требует взаимодействия между почками, костным мозгом и питательными веществами в организме. Если почки или костный мозг не функционируют, или организм плохо питается, то нормальное количество и функции эритроцитов может быть трудно поддерживать.
Анемия на самом деле является признаком болезненного процесса, а не самой болезни.Обычно его классифицируют как хронический или острый. Хроническая анемия возникает в течение длительного периода времени. Острая анемия возникает быстро. Определение того, присутствует ли анемия в течение длительного времени или это что-то новое, помогает врачам найти причину. Это также помогает предсказать, насколько серьезными могут быть симптомы анемии. При хронической анемии симптомы обычно начинаются медленно и постепенно прогрессируют; тогда как при острой анемии симптомы могут быть резкими и более тревожными.
Эритроциты живут около 100 дней, поэтому организм постоянно пытается их заменить.У взрослых производство эритроцитов происходит в костном мозге. Врачи пытаются определить, вызвано ли низкое количество эритроцитов повышенной кровопотерей эритроцитов или их снижением в костном мозге. Знание того, изменилось ли количество лейкоцитов и / или тромбоцитов, также помогает определить причину анемии.
По оценкам Всемирной организации здравоохранения (ВОЗ), два миллиарда человек во всем мире страдают анемией и примерно 50% всех анемий объясняются дефицитом железа. [64] Это происходит на всех этапах жизненного цикла, но чаще встречается у беременных женщин и маленьких детей.[82] Анемия является результатом множества причин, которые можно изолировать, но чаще всего они сосуществуют. Некоторые из этих причин включают следующие:
Железодефицитная анемия
Наиболее важной и частой причиной анемии является дефицит железа. [82] Если потребление железа ограничено или неадекватно из-за плохого питания, в результате может возникнуть анемия. Это называется железодефицитной анемией. Железодефицитная анемия также может возникать при наличии язвы желудка или других источников медленного хронического кровотечения (рак толстой кишки, рак матки, полипы кишечника, геморрой и т. Д.).[83]
Анемия хронического заболевания
Любое длительное заболевание может привести к анемии. Этот тип анемии является вторым по распространенности после анемии, вызванной дефицитом железа, и развивается у пациентов с острым или хроническим системным заболеванием или воспалением. [84] Это состояние было названо «анемией воспаления» из-за повышенного содержания гепсидина, который блокирует как рециркуляцию железа из макрофагов, так и абсорбцию железа. [85]
Анемия из-за активного кровотечения
Потеря крови из-за обильного менструального кровотечения или ран может вызвать анемию.[82] Язвы желудочно-кишечного тракта или раковые заболевания, такие как рак толстой кишки, могут медленно терять кровь и также могут вызывать анемию. [86,87]
Анемия, связанная с заболеванием почек
Почки выделяют гормон эритропоэтин, который помогает костному мозгу сделать эритроциты. У людей с хроническим (длительным) заболеванием почек выработка этого гормона снижена, а это, в свою очередь, снижает выработку эритроцитов, вызывая анемию. [88] Хотя дефицит эритропоэтина является основной причиной анемии при хронической почечной недостаточности, это не единственная причина.Следовательно, необходимо минимальное обследование, чтобы исключить дефицит железа и другие аномалии клеточной линии. [89]
Анемия, связанная с беременностью
Увеличение объема плазмы во время беременности приводит к разбавлению эритроцитов и может проявляться как анемия. [90] Железодефицитная анемия составляет 75% всех анемий во время беременности. [90]
Анемия, связанная с плохим питанием
Витамины и минералы необходимы для образования эритроцитов. Помимо железа, для правильного производства гемоглобина необходимы витамин B12, виамин А, фолиевая кислота, рибофлавин и медь.[82] Дефицит любого из этих питательных микроэлементов может вызвать анемию из-за недостаточного производства эритроцитов. Плохое питание — важная причина низкого уровня витаминов и, как следствие, анемии.
Ожирение и анемия
Ожирение характеризуется хроническим слабым системным воспалением, повышенным уровнем гепсидина, которое, в свою очередь, связано с анемией хронического заболевания. Ausk и Ioannou [91] предположили, что ожирение может быть связано с особенностями анемии хронического заболевания, включая низкую концентрацию гемоглобина, низкое содержание железа и трансферрина в сыворотке, а также повышенный уровень ферритина в сыворотке.Избыточный вес и ожирение были связаны с изменениями сывороточного железа, насыщения трансферрина и ферритина, которые, как ожидается, произойдут в условиях хронического системного воспаления. Воспаление, связанное с ожирением, может повышать концентрацию гепсидина и снижать доступность железа. Aeberli и др. ., [92] сравнили уровень железа, потребление железа с пищей и его биодоступность, а также циркулирующие уровни гепсидина, лептина и интерлейкина-6 (ИЛ-6) у детей с избыточной массой тела и детей с нормальным весом.Они указали, что существует пониженная доступность железа для эритропоэза у детей с избыточным весом, и что это, вероятно, связано с опосредованным гепсидином сниженным всасыванием железа и / или повышенным секвестрацией железа, а не с низким содержанием железа с пищей.
Алкоголизм
Алкоголь оказывает многочисленные неблагоприятные эффекты на различные типы клеток крови и их функции. [93] У алкоголиков часто есть дефектные эритроциты, которые преждевременно разрушаются. [93,94] Сам по себе алкоголь также может быть токсичным для костного мозга и может замедлять производство эритроцитов.[93,94] Кроме того, с алкоголизмом связаны плохое питание и дефицит витаминов и минералов. [95] Сочетание этих факторов может привести к анемии у алкоголиков.
Серповидно-клеточная анемия
Серповидно-клеточная анемия — одно из наиболее распространенных наследственных заболеваний. [96] Это заболевание, связанное с кровью, которое влияет на молекулу гемоглобина и приводит к изменению формы всей клетки крови в стрессовых условиях [97]. В таком состоянии проблема с гемоглобином бывает качественной или функциональной.Аномальные молекулы гемоглобина могут вызвать проблемы в целостности структуры эритроцитов, и они могут стать серповидными (серповидные клетки). [97] Существуют разные типы серповидно-клеточной анемии разной степени тяжести. Это особенно распространено у африканцев, ближневосточных и средиземноморских предков. [97]
Талассемия
Это еще одна группа причин анемии, связанных с гемоглобином, которая связана с отсутствием или ошибками в генах, ответственных за выработку гемоглобина. [97] Молекула гемоглобина имеет субъединицы, обычно называемые альфа- и бета-цепями глобина.Отсутствие определенной субъединицы определяет тип альфа- или бета-талассемии. [97,98] Существует много типов талассемии, которые различаются по степени тяжести от легкой (малая талассемия) до тяжелой (большая талассемия). [98] Они также являются наследственными, но вызывают количественные аномалии гемоглобина, то есть вырабатывается недостаточное количество молекул правильного типа. Альфа- и бета-талассемии являются наиболее распространенными наследственными моногенными заболеваниями в мире с наибольшей распространенностью в районах, где малярия была или все еще является эндемической.[97]
Апластическая анемия
Апластическая анемия — это заболевание, при котором разрушается костный мозг и снижается выработка клеток крови. [99] Это вызывает дефицит всех трех типов клеток крови (панцитопения), включая эритроциты (анемия), лейкоциты (лейкопения) и тромбоциты (тромбоцитопения). [100,101] Многие распространенные лекарства могут иногда вызывать этот тип анемии в качестве побочного эффекта. у некоторых людей. [99]
Гемолитическая анемия
Гемолитическая анемия — это тип анемии, при которой происходит разрыв эритроцитов, известный как гемолиз, который разрушается быстрее, чем костный мозг может их заменить.[102] Гемолитическая анемия может возникнуть по разным причинам и часто классифицируется как приобретенная или наследственная. Распространенными приобретенными причинами гемолитической анемии являются аутоиммунитет, микроангиопатия и инфекции. Нарушения ферментов эритроцитов, мембран и гемоглобина вызывают наследственную гемолитическую анемию. [102]
ПРЕДОТВРАЩЕНИЕ НЕДОСТАТОЧНОСТИ ЖЕЛЕЗА (СТРАТЕГИИ ВМЕШАТЕЛЬСТВА)
Четыре основных стратегии коррекции эффективности микронутриентов в популяциях могут использоваться для коррекции дефицита железа, как по отдельности, так и в комбинации.Это обучение в сочетании с модификацией диеты для улучшения потребления железа и его биодоступности; добавление железа (обеспечение железом, обычно в более высоких дозах, без еды), обогащение пищевых продуктов железом и новый подход к биофортификации. Однако есть некоторые трудности в применении некоторых из этих стратегий при рассмотрении железа.
Диверсификация продуктов питания
Модификации диеты для сокращения потребления Индийской стоматологической ассоциации включают увеличение потребления продуктов, богатых железом, особенно мясных продуктов, увеличение потребления фруктов и овощей, богатых аскорбиновой кислотой, для увеличения абсорбции негемового железа и снижение потребления чая и кофе, что подавляют всасывание негемового железа.[103,58] Другая стратегия — снизить содержание антинутриентов, чтобы сделать железо, поступающее из их пищевых источников, более доступным. Биодоступность железа может быть увеличена такими методами, как проращивание и ферментация, которые способствуют ферментативному гидролизу фитиновой кислоты в цельнозерновых зерновых и бобовых культурах за счет повышения активности эндогенных или экзогенных ферментов фитазы. [104] Даже использование неферментативных методов, таких как термическая обработка, замачивание и измельчение, для снижения содержания фитиновой кислоты в основных продуктах растительного происхождения было успешным в улучшении биодоступности железа (и цинка).[105,106]
Добавка
Для перорального приема добавок железа предпочтительны соли двухвалентного железа (сульфат двухвалентного железа и глюконат двухвалентного железа) из-за их низкой стоимости и высокой биодоступности. [72] Хотя абсорбция железа выше при приеме добавок железа натощак, тошнота и боль в эпигастрии могут развиться из-за введенных более высоких доз железа (обычно 60 мг Fe / день). Если возникают такие побочные эффекты, следует попытаться снизить дозу между приемами пищи или давать железо во время еды, хотя пища снижает всасывание лекарственного железа примерно на две трети.[107] Добавки железа во время беременности рекомендуется в развивающихся странах, где женщины часто вступают в беременность с низкими запасами железа. [108] Хотя обычно считалось, что польза от приема добавок железа перевешивает предполагаемый риск, есть некоторые свидетельства того, что добавление в дозах, рекомендованных для здоровых детей, несет в себе риск увеличения тяжести инфекционного заболевания на фоне малярии. [109,110]
Обогащение
Обогащение пищевых продуктов железом сложнее, чем обогащение такими питательными веществами, как цинк в муке, йод в соли и витамин А в кулинарном масле.[72] Наиболее биодоступные соединения железа растворимы в воде или разбавленной кислоте, но часто вступают в реакцию с другими пищевыми компонентами, вызывая неприятный запах, изменение цвета или окисление жиров. [103] Таким образом, менее растворимые формы железа, хотя и хуже усваиваются, часто выбираются для обогащения, чтобы избежать нежелательных сенсорных изменений. [72] Обогащение обычно производится с гораздо более низкими дозами железа, чем с добавками. Это ближе к физиологической среде и может быть самым безопасным вмешательством в малярийные районы. [111] Нет никаких опасений по поводу безопасности добавок железа или обогащения железа в немалярийных эндемичных районах.[112]
Соединения железа, рекомендованные [7] для обогащения пищевых продуктов, включают сульфат железа, фумарат железа, пирофосфат железа и порошок электролитического железа. Пшеничная мука является наиболее распространенным пищевым продуктом, обогащенным железом, и она обычно обогащается порошками элементарного железа, которые не рекомендуются ВОЗ. [7,113] Харрелл и Эгли [23] сообщили, что из 78 национальных программ по пшеничной муке только восемь улучшатся. статус железа. В этих программах использовались рекомендуемые соединения железа на рекомендованных уровнях.Другие страны использовали не рекомендуемые соединения или более низкие уровни железа по сравнению с потреблением муки. Коммерческое детское питание, такое как смеси и злаки, также обычно обогащено железом.
Биофортификация
Содержание железа варьируется от 25 до 56 мг / кг в различных сортах пшеницы и от 7 до 23 мг / кг в рисовых зернах. Однако большая часть этого железа удаляется в процессе измельчения. Поглощение железа зерновыми и бобовыми культурами, многие из которых имеют высокое содержание самородного железа, обычно низкое из-за высокого содержания в них фитата, а иногда и полифенолов.[48] Стратегии биофортификации включают селекцию растений и генную инженерию. Уровни железа в обычных бобах и просе были успешно увеличены путем селекции растений, но использование других основных продуктов питания является более трудным или невозможным (рис) из-за недостаточной естественной генетической изменчивости. Lucca и др. ., [114] увеличили содержание железа в эндосперме риса, чтобы улучшить его всасывание в кишечнике человека с помощью генной инженерии. Они ввели ген ферритина из Phaseolus vulgaris в рисовые зерна, увеличив содержание железа в них вдвое.Чтобы увеличить биодоступность железа, они ввели в эндосперм риса термотолерантную фитазу из Aspergillus fumigatus . Они указали, что этот рис с более высоким содержанием железа и богатой фитазой имеет большой потенциал для существенного улучшения питания железом в тех популяциях, где дефицит железа так широко распространен. [114] К сожалению, фитаза не устояла перед приготовлением. Важность различных минералов, таких как цинк [115] и железо, требует большего внимания на индивидуальном уровне и уровне общественного здравоохранения.
Сноски
Источник поддержки: Нет
Конфликт интересов: Не объявлен.
СПИСОК ЛИТЕРАТУРЫ
1. Борода Дж. Л., Доусон HD. Утюг. В: О’Делл Б.Л., Сунде Р.А., редакторы. Справочник по незаменимым в питании минеральным элементам. Нью-Йорк: CRC Press; 1997. С. 275–334. [Google Scholar] 2. Вуд Р.Дж., Ронненберг А. Железо. В: Shils ME, Shike M, Ross AC, Caballero B, Cousins RJ, редакторы. Современное питание в здоровье и болезнях. 10-е изд. Балтимор: Липпинкотт Уильямс и Уилкинс; 2005 г.С. 248–70. [Google Scholar] 3. Макдауэлл LR. 2-е изд. Амстердам: Elsevier Science; 2003. Минералы в питании животных и человека; п. 660. [Google Scholar] 4. Гуггенхайм KY. Хлороз: возникновение и исчезновение болезни, связанной с питанием. J Nutr. 1995; 125: 1822–5. [PubMed] [Google Scholar] 5. Ип Р., Даллман PR. Утюг. В: Ziegler EE, Filer LJ, редакторы. Присутствуют знания в области питания. 7-е изд. Вашингтон, округ Колумбия: ILSI Press; 1996. С. 278–92. [Google Scholar] 6. Андервуд Э.Дж., Саттл Н.Ф. 3-е изд. Уоллингфорд: международное издательство CABI; 1999 г.Минеральное питание скота; п. 614. [Google Scholar] 7. Аллен Л., де Бенуа Б., Дари О., Харрелл Р., редакторы. Женева: ВОЗ и ФАО; 2006. ВОЗ. Рекомендации по обогащению пищевых продуктов микронутриентами; п. 236. [Google Scholar] 8. Брабин Б.Дж., Премжи З., Верхое ff Ф. Анализ анемии и детской смертности. J Nutr. 2001; 131: 636–45С. [PubMed] [Google Scholar] 9. Quintero-Gutiérrez AG, González-Rosendo G, Sánchez-Muñoz J, Polo-Pozo J, Rodríguez-Jerez JJ. Биодоступность гемового железа в начинке для печенья с использованием поросят в качестве модели животных для человека.Int J Biol Sci. 2008; 4: 58–62. [Бесплатная статья PMC] [PubMed] [Google Scholar] 10. Айзен П., Эннс С., Весслинг-Резник М. Химия и биология метаболизма железа в эукариотах. Int J Biochem Cell Biol. 2001; 33: 940–59. [PubMed] [Google Scholar] 11. Лиу П. Т., Хейскала М., Петерсон П. А., Ян Ю. Роль железа в здоровье и болезнях. Мол Аспекты Мед. 2001; 2: 1–87. [PubMed] [Google Scholar] 12. Guerinot ML. Транспорт микробного железа. Annu Rev Microbiol. 1994; 48: 743–72. [PubMed] [Google Scholar] 13. Асквит К., Каплан Дж.Транспорт железа и меди в дрожжах и его значение для болезней человека. Trends Biochem Sci. 1998. 23: 135–8. [PubMed] [Google Scholar] 15. Вашингтон, округ Колумбия: Национальная академия прессы; 2001. МОМ. Институт медицины. утюг. В: Нормы потребления витамина A, витамина K, мышьяка, бора, хрома, меди, йода, железа, марганца, молибдена, никеля, кремния, ванадия и цинка; С. 290–393. [PubMed] [Google Scholar] 16. Muir A, Hopfer U. Региональная специфичность поглощения железа щеточно-граничными мембранами тонкого кишечника у нормальных мышей и мышей с дефицитом железа.Am J Physiol. 1985; 248: G376–9. [PubMed] [Google Scholar] 17. Фрейзер Д.М., Андерсон Г.Дж. Импорт железа. I. Абсорбция железа в кишечнике и ее регуляция. Am J Physiol Gastrointest Liver Physiol. 2005; 289: G631–5. [PubMed] [Google Scholar] 18. Наддур С.С., Шрирама К., Мудипалли А. Механизмы транспорта и гомеостаза железа: их роль в здоровье и болезнях. Индийский J Med Res. 2008; 128: 533–44. [PubMed] [Google Scholar] 20. Yeh KY, Yeh M, Mims L, Glass J. Кормление железом индуцирует миграцию и взаимодействие ферропортина 1 и гефестина в двенадцатиперстном эпителии крыс.Am J Physiol Gastrointest Liver Physiol. 2009. 296: 55–65. [Бесплатная статья PMC] [PubMed] [Google Scholar] 21. Тейл Э.С., Чен Х., Миранда С., Янсер Х., Эльзенханс Б., Нуньес М.Т. и др. Абсорбция железа из ферритина не зависит от гемового железа и солей двухвалентного железа у женщин и сегментов кишечника крыс. J Nutr. 2012; 142: 478–83. [Бесплатная статья PMC] [PubMed] [Google Scholar] 22. Hoppler M, Schoenbaechler A, Meile L, Hurrell RF, Walczyk T. Ферритин-железо высвобождается во время кипячения и in vitro при пищеварении в желудке .J Nutr. 2008. 138: 878–84. [PubMed] [Google Scholar] 23. Hurrell R, Egli I. Биодоступность железа и диетические контрольные значения. Am J Clin Nutr. 2010; 91: 1461–7S. [PubMed] [Google Scholar] 25. Немет Э., Ганц Т. Регулирование метаболизма железа гепсидином. Анну Рев Нутр. 2006; 26: 323–42. [PubMed] [Google Scholar] 26. Немет Э., Таттл М.С., Пауэлсон Дж., Вон М.Б., Донован А., Уорд Д.М. и др. Гепсидин регулирует отток клеточного железа, связываясь с ферропортином и индуцируя его интернализацию. Наука. 2004; 306: 2090–3.[PubMed] [Google Scholar] 28. Браун В., Киллманн Х. Бактериальные решения проблемы снабжения железом. Trends Biochem Sci. 1999; 24: 104–109. [PubMed] [Google Scholar] 29. Хант-младший. Насколько важна биодоступность железа с пищей? Am J Clin Nutr. 2001; 73: 3–4. [PubMed] [Google Scholar] 30. Хант-младший, Зито, Калифорния, Джонсон, Лос-Анджелес. Выведение железа из организма здоровыми мужчинами и женщинами. Am J Clin Nutr. 2009; 89: 1–7. [PubMed] [Google Scholar] 31. Фэрбенкс В.Ф. Железо в медицине и питании. В: Shils ME, Shike M, Ross AC, Caballero B, Cousins RJ, редакторы.Современное питание в здоровье и болезнях. 10-е изд. Балтимор: Липпинкотт Уильямс и Уилкинс; 1999. С. 193–221. [Google Scholar] 32. потребности человека в витаминах и минералах. Рим: ФАО; 2001. ФАО / ВОЗ. Пищевые подходы к удовлетворению потребностей в витаминах и минералах; С. 7–25. [Google Scholar] 33. Monsen ER, Hallberg L, Layrisse M, Hegsted DM, Cook JD, Mertz W. и др. Оценка доступного пищевого железа. Am J Clin Nutr. 1978; 31: 134–41. [PubMed] [Google Scholar] 34. Конрад ME, Umbreit JN. Краткий обзор: абсорбция железа — путь муцин-мобилферрин-интегрин.Конкурентоспособный путь поглощения металлов. Am J Hematol. 1993; 42: 67–73. [PubMed] [Google Scholar] 35. Конрад М.Э., Шаде С.Г. Хелаты аскорбиновой кислоты в абсорбции железа: роль соляной кислоты и желчи. Гастроэнтерология. 1968; 55: 35–45. [PubMed] [Google Scholar] 36. Холлберг Л., Брюн М., Россандер Л. Поглощение железа у человека: аскорбиновая кислота и дозозависимое ингибирование фитатом. Am J Clin Nutr. 1989; 49: 140–4. [PubMed] [Google Scholar] 37. Зигенберг Д., Бейнс Р.Д., Ботвелл Т.Х., Макфарлейн Б.Дж., Лампарелли Р.Д., Car NG и др.Аскорбиновая кислота предотвращает дозозависимое ингибирующее действие полифенолов и фитатов на абсорбцию негемового железа. Am J Clin Nutr. 1991; 53: 537–41. [PubMed] [Google Scholar] 38. Стекель А., Оливарес М., Писарро Ф., Чадуд П., Лопес И., Амар М. Поглощение обогащающего железа из молочных смесей у младенцев. Am J Clin Nutr. 1986; 43: 917–22. [PubMed] [Google Scholar] 39. Бюллетень D, Бейнс Р.Д., Ботвелл Т.Х., Гиллули М., Макфарлейн Б.Дж., Макфейл А.П. и др. Влияние фруктовых соков и фруктов на усвоение железа из рисовой муки.Br J Nutr. 1987; 57: 331–43. [PubMed] [Google Scholar] 40. Линч SR, Кук JD. Взаимодействие витамина С и железа. Ann N Y Acad Sci. 1980; 355: 32–44. [PubMed] [Google Scholar] 41. Teucher B, Olivares M, Cori H. Усилители поглощения железа: аскорбиновая кислота и другие органические кислоты. Int J Vitam Nutr Res. 2004; 74: 403–19. [PubMed] [Google Scholar] 42. Линч С.Р., Харрелл Р.Ф., Дассенко С.А., Кук Дж.Д. Влияние пищевых белков на биодоступность железа у человека. Adv Exp Med Biol. 1989; 249: 117–32. [PubMed] [Google Scholar] 43.Бьорн-Расмуссен Э., Халльберг Л. Влияние животных белков на усвоение пищевого железа человеком. Нутр Метаб. 1979; 23: 192–202. [PubMed] [Google Scholar] 44. Редди МБ, Харрелл Р.Ф., Кук JD. Разнообразное питание незначительно влияет на всасывание негемового железа у нормальных людей. J Nutr. 2006; 136: 576–81. [PubMed] [Google Scholar] 45. Бах Кристенсен М., Хелс О, Морберг С., Марвинг Дж., Бугель С., Тетенс I. Свинина увеличивает усвоение железа при 5-дневной полностью контролируемой диете по сравнению с вегетарианской диетой с аналогичным содержанием витамина С и фитиновой кислоты.Br J Nutr. 2005. 94: 78–83. [PubMed] [Google Scholar] 46. Харрелл Р.Ф., Джуллерат М.А., Редди М.Б., Линч С.Р., Дассенко С.А., Кук Дж.Д. Соевый белок, фитат и абсорбция железа у человека. Am J Clin Nutr. 1992; 56: 573–8. [PubMed] [Google Scholar] 47. Hurrell RF. Разложение фитиновой кислоты как средство улучшения усвоения железа. Int J Vitam Nutr Res. 2004. 74: 445–52. [PubMed] [Google Scholar] 48. Харрелл Р.Ф., Редди М., Кук Дж. Д.. Подавление абсорбции негемного железа у человека напитками, содержащими полифенолы. Br J Nutr.1999. 81: 289–95. [PubMed] [Google Scholar] 49. Холлберг Л., Россандер Л. Влияние различных напитков на усвоение негемового железа из сложных блюд. Hum Nutr Appl Nutr. 1982; 36: 116–23. [PubMed] [Google Scholar] 50. Hallberg L, Rossander-Hulthen L, Brune M, Gleerup A. Ингибирование усвоения гемового железа у человека кальцием. Br J Nutr. 1993; 69: 533–40. [PubMed] [Google Scholar] 51. Hallberg L, Rossander-Hulthen L. Потребность в железе у менструирующих женщин. Am J Clin Nutr. 1991; 54: 1047–58. [PubMed] [Google Scholar] 52.Линч SR. Влияние кальция на усвоение железа. Nutr Res Rev.2000; 13: 141–58. [PubMed] [Google Scholar] 53. Кук JD, Monsen ER. Поглощение пищевого железа у людей. III. Сравнение влияния животных белков на всасывание негемового железа. Am J Clin Nutr. 1976; 29: 859–67. [PubMed] [Google Scholar] 54. Харрелл РФ, Линч С.Р., Тринидад Т.П., Дассенко С.А., Кук Дж.Д. Абсорбция железа у людей: бычий сывороточный альбумин по сравнению с говяжьими мышцами и яичным белком. Am J Clin Nutr. 1988. 47: 102–7. [PubMed] [Google Scholar] 55.Линч С.Р., Дассенко С.А., Кук Дж.Д., Джульерат М.А., Харрелл РФ. Ингибирующий эффект фрагмента, связанного с соевым белком, на абсорбцию железа у людей. Am J Clin Nutr. 1994; 60: 567–72. [PubMed] [Google Scholar] 56. Piomelli S, Seaman C, Kapoor S. Вызванные свинцом аномалии метаболизма порфирина, связь с дефицитом железа. Ann N Y Acad Sci. 1987; 514: 278–88. [PubMed] [Google Scholar] 58. 2-е изд. Бангкок: 2004 г. ФАО / ВОЗ. Консультации экспертов по потребностям человека в витаминах и минералах, потребностях в витаминах и минералах в питании человека: отчет совместного экспертного заключения ФАО / ВОЗ; п.341. [Google Scholar] 59. Cook JD, Skikne BS, Lynch SR, Reusser ME. Оценки достаточности железа у населения США. Кровь. 1986; 68: 726–31. [PubMed] [Google Scholar] 60. Ботвелл TH, Чарльтон RW. Общий подход к проблемам железодефицита и перегрузки железом у населения в целом. Semin Hematol. 1982; 19: 54–67. [PubMed] [Google Scholar] 61. Гибсон Р.С., Макдональд А.С., Смит-Вандеркой П.Д. Параметры сывороточного ферритина и пищевого железа в выборке канадских детей дошкольного возраста. J Can Dietetic Assoc.1988; 49: 23–8. [Google Scholar] 62. ДеМайер Э.М., Даллман П., Герни Дж. М., Холлберг Л., Суд С. К., Срикантия С. Г., редакторы. Женева: Всемирная организация здравоохранения; 1989. ВОЗ. Профилактика и контроль железодефицитной анемии с помощью первичной медико-санитарной помощи: руководство для администраторов здравоохранения и руководителей программ; п. 58. [Google Scholar] 63. Даллман П. Айрон. В: Браун М.Л., редактор. Настоящие знания в области питания. 6-е изд. Вашингтон, округ Колумбия: Фонд питания; 1990. С. 241–50. [Google Scholar] 64. Женева: Швейцария: Всемирная организация здравоохранения; 2001 г.ВОЗ / ЮНИСЕФ / УООН. Оценка, профилактика и контроль железодефицитной анемии; п. 114. [Google Scholar] 65. Борода Дж. Л., Коннор-младший. Статус железа и нейронное функционирование. Анну Рев Нутр. 2003. 23: 41–58. [PubMed] [Google Scholar] 66. Failla ML. Микроэлементы и защита хозяина: последние достижения и сохраняющиеся проблемы. J Nutr. 2003; 133: S1443–7. [PubMed] [Google Scholar] 67. Витери Ф.Е., Торунь Б. Анемия и физическая работоспособность. В: Гарби Л., редактор. Клиники гематологии. Vol. 3. Лондон: У. Б. Сондерс; 1974. стр.609–26. [Google Scholar] 68. CDC. Табель успеваемости по грудному вскармливанию, США: показатели результатов (публикация из Центров по контролю и профилактике заболеваний, Национальное обследование иммунизации. 2010 г. [последний доступ 11 мая 2010 г.]. Http://www.cdc.gov/breastfeeding/data/index .htm .69. Купер Е.С., Банди Д.А. Трихоцефалопатия. Ballieres Clin Trop Med Commun Dis. 1987; 2: 629–43. [Google Scholar] 70. Всемирная организация здравоохранения, Женева; 1995. ВОЗ. Отчет неофициальной консультации ВОЗ. на анкилостомоз и анемию у девочек и женщин; с.46. [Google Scholar] 71. Crompton DW, Nesheim MC. Пищевая ценность кишечных гельминтозов в течение жизненного цикла человека. Анну Рев Нутр. 2002; 22: 35–99. [PubMed] [Google Scholar] 72. Ларок Р., Касапиа М., Готуццо Е., Дьеркос Т.В. Взаимосвязь между интенсивностью заражения гельминтами, передающимися через почву, и анемией во время беременности. Am J Trop Med Hyg. 2005; 73: 783–9. [PubMed] [Google Scholar] 73. Циммерманн МБ, Харрелл РФ. Недостаток пищевого железа. Ланцет. 2007; 370: 115–20. [Google Scholar] 74. Харви LJ, Armah CN, Dainty JR, Foxall RJ, John Lewis D, Langford NJ и др.Влияние менструальной кровопотери и диеты на дефицит железа у женщин в Великобритании. Br J Nutr. 2005. 94: 557–64. [PubMed] [Google Scholar] 75. Борода JL. Потребность в железе у девочек-подростков. Симпозиум: Повышение уровня железа у подростков до деторождения. J Nutr. 2000; 130: S440–2. [PubMed] [Google Scholar] 77. Бегин Ю. Растворимый рецептор трансферрина для оценки эритропоэза и статуса железа. Clinica Chimica Acta. 2003. 329: 9–22. [PubMed] [Google Scholar] 79. Повар JD, Flowers CH, Skikne BS. Количественная оценка bodyiron.Кровь. 2003. 101: 3359–64. [PubMed] [Google Scholar] 80. Кук JD, Boy E, Flowers C, Daroca Mdel C. Влияние высокогорной жизни на железо тела. Кровь. 2005; 106: 1441–6. [PubMed] [Google Scholar] 81. Ян З., Дьюи К.Г., Лоннердал Б., Хернелл О., Чапарро С., Аду-Афарвуа С. и др. Сравнение концентрации ферритина в плазме с соотношением рецептора трансферрина в плазме и ферритина для оценки запасов железа в организме: результаты 4 интервенционных испытаний. Am J Clin Nutr. 2008; 87: 1892–8. [PubMed] [Google Scholar] 82.Де Бенуа Б., Маклин Э., Эгли И., Когсуэлл М. — редакторы. Женева: Пресса ВОЗ, Всемирная организация здравоохранения; 2008. ВОЗ / CDC. Библиотечная каталогизация в публикации. Распространенность анемии в мире, 1993–2005 гг .: глобальная база данных ВОЗ по анемии; п. 40. [Google Scholar] 83. Джонсон-Уимбли Т.Д., Грэм Д.Ю. Диагностика и лечение железодефицитной анемии в 21 веке. Ther Adv Гастроэнтерол. 2011; 4: 177–84. [Бесплатная статья PMC] [PubMed] [Google Scholar] 84. Зарычанский Р., Хьюстон Д.С. Анемия хронического заболевания: вредное заболевание или адаптивная, полезная реакция? Can Med Assoc J.2008. 179: 333–7. [Бесплатная статья PMC] [PubMed] [Google Scholar] 85. Weiss G, Goodnough LT. Анемия хронического заболевания. N Engl J Med. 2005; 352: 1011–23. [PubMed] [Google Scholar] 86. 2-е изд. Женева: 2004 г. ВОЗ / CDC. Отчет о совместной технической консультации Всемирной организации здравоохранения / Центров по контролю и профилактике заболеваний по оценке статуса железа на уровне населения; п. 108. [Google Scholar] 87. Knight K, Wade S, Balducci L. Распространенность и исходы анемии при раке: систематический обзор литературы.Am J Med. 2004; 116: 11–26С. [PubMed] [Google Scholar] 88. О’Мара NB. Больные анемией с хроническими заболеваниями почек. Спектр диабета. 2008; 21: 12–9. [Google Scholar] 89. Нурко С. Анемия при хронической болезни почек: причины, диагностика, лечение. Cleve Clin J Med. 2006. 73: 289–97. [PubMed] [Google Scholar] 90. Горовиц К.М., Ингардия С.Дж., Боргида А.Ф. 2013, Анемия при беременности. Clin Lab Med. 2013; 33: 281–91. [PubMed] [Google Scholar] 91. Ауск К.Дж., Иоанну Г.Н. Связано ли ожирение с анемией хронического заболевания? Популяционное исследование.Ожирение. 2008. 16: 2356–61. [PubMed] [Google Scholar] 92. Aeberli I, Hurrell RF, Zimmermann MB. Дети с избыточным весом имеют более высокие концентрации циркулирующего гепсидина и более низкий статус железа, но их потребление железа с пищей и биодоступность сопоставимы с детьми с нормальным весом. Int J Obes. 2009; 33: 1111–7. [PubMed] [Google Scholar] 94. Lewis G, Wise MP, Poynton C, Godkin A. Случай стойкой анемии и злоупотребления алкоголем. Нат Клин Практ Гастроэнтерол Гепатол. 2007; 4: 521–6. [PubMed] [Google Scholar] 95. Lindenbaum J, Роман MJ.Пищевая анемия при алкоголизме. Am J Clin Nutr. 1980; 33: 2727–35. [PubMed] [Google Scholar] 96. Cox SE, L’Esperance V, Makani J, Soka D, Prentice AM, Hill CM и др. Серповидно-клеточная анемия: доступность железа и ночная оксиметрия. J Clin Sleep Med. 2012; 8: 541–5. [Бесплатная статья PMC] [PubMed] [Google Scholar] 98. Манси Х.Л., младший, Кэмпбелл Дж. Альфа- и бета-талассемия. Я семейный врач. 2009; 80: 339–44. [PubMed] [Google Scholar] 99. Сегель ГБ, Лихтман М.А. Апластическая анемия: приобретенная и наследственная. В: Каушанский К., Вильямс В.Дж., редакторы.Гематология Вильямса. 8-е изд. Нью-Йорк: McGraw-Hill Medical; 2010. С. 569–90. [Google Scholar] 100. Янг Н.С., Каладо Р.Т., Шейнберг П. Современные концепции патофизиологии и лечения апластической анемии. Кровь. 2006; 108: 2509–19. [Бесплатная статья PMC] [PubMed] [Google Scholar] 101. Шейнберг П., Чен Дж. Апластическая анемия: что мы узнали на моделях на животных и в клинике. Semin Hematol. 2013; 50: 156–64. [PubMed] [Google Scholar] 102. Dhaliwal G, Cornett PA, Tierney LM., Jr Гемолитическая анемия.Я семейный врач. 2004. 69: 2599–606. [PubMed] [Google Scholar] 103. Hurrell RF. Как обеспечить адекватное усвоение железа из продуктов, обогащенных железом. Nutr Rev. 2002; 60: S7–15. [PubMed] [Google Scholar] 104. Повар JD. Диагностика и лечение железодефицитной анемии. Лучшая практика Res Clin Haematol. 2005; 18: 319–32. [PubMed] [Google Scholar] 105. Schlemmer U, Frølich W, Prieto RM, Grases F. Фитат в пищевых продуктах и значение для человека: источники пищи, потребление, обработка, биодоступность, защитная роль и анализ.Mol Nutr Food Res. 2009; 53: S330–75. [PubMed] [Google Scholar] 106. Лян Дж., Хан Б.З., Ноут М.Дж., Хамер Р.Дж. Влияние замачивания, прорастания и ферментации на общую фитиновую кислоту и растворимый цинк in vitro в коричневом рисе. Food Chem. 2008; 110: 821–8. [PubMed] [Google Scholar] 107. Кавалли-Сфорца Т., Бергер Дж., Смитасири С., Витери Ф. Еженедельное употребление добавок железа и фолиевой кислоты для женщин репродуктивного возраста: обзор воздействия, извлеченные уроки, планы расширения и вклад в достижение целей развития тысячелетия.Nutr Rev.2005; 63: S152–8. [PubMed] [Google Scholar] 109. Oppenheimer SJ. Железо и его отношение к иммунитету и инфекционным заболеваниям. J Nutr. 2001; 131: S616–33. [PubMed] [Google Scholar] 110. Sazawal S, Black RE, Ramsan M, Chwaya HM, Stoltzfus RJ, Dutta A и др. Влияние обычных профилактических добавок с железом и фолиевой кислотой на госпитализацию и смертность детей дошкольного возраста в условиях высокой передачи малярии: рандомизированное плацебо-контролируемое исследование на уровне общины. Ланцет. 2006; 367: 133–43.[PubMed] [Google Scholar] 112. Hurrell RF. Обогащение железом: его эффективность и безопасность в отношении инфекций. Еда Nutr Bull. 2007. 28: 585–94. [PubMed] [Google Scholar] 114. Лукка П., Харрелл Р., Потрикус И. Борьба с железодефицитной анемией с помощью риса, богатого железом. J Am Coll Nutr. 2002; 21: 184С – 90. [PubMed] [Google Scholar] 115. Рухани Н., Харрелл Р., Келишади Р., Шулин Р. Цинк и его значение для здоровья человека: интегративный обзор. J Res Med Sci. 2013; 18: 144–57. [Бесплатная статья PMC] [PubMed] [Google Scholar]функций железа в организме
Утюг выполняет в организме множество важных функций.Он в первую очередь участвует в передаче кислорода от легких к тканям. Однако железо также играет роль в метаболизме как компонент некоторых белков и ферментов.
Железо в свободном состоянии токсично для организма. Он связан с белками либо за счет связывания лиганда, либо за счет включения в группу порфирина — кольцевую молекулу. Комплекс двухвалентной формы железа и протопорфирина IX известен как гем. Гемовое железо содержится в белках, связанных с транспортом кислорода, включая гемоглобин и миоглобин.Негемовое железо можно найти в белках, связанных с окислительным фосфорилированием, и в белках-хранилищах железа, таких как трансферрин и ферритин.
Продукты, содержащие железо. Здоровое питание. Авторское право на изображение: bitt24 / Shutterstock
Гемоглобин и миоглобин
Около 70 процентов железа в организме содержится в гемоглобине и миоглобине. Гемоглобин — это белок красных кровяных телец, ответственный за перенос кислорода к тканям из легких. Миоглобин — это белок, содержащийся в мышцах, который используется для хранения кислорода.
Гемоглобин — это система транспортировки кислорода, обнаруженная в красных кровяных тельцах всех позвоночных и некоторых беспозвоночных. У человека гемоглобин состоит из четырех глобулярных белковых субъединиц. Четыре субъединицы образуют карман, который связывает гемовую группу.
Кислород связывается с атомом железа в молекуле гемоглобина в легких с образованием оксигемоглобина. Это происходит в капиллярах альвеол легких. Он выпускается по месту назначения в камерах. Гемоглобин переносит CO2 обратно в легкие для выдоха в виде отходов, но CO2 связывается с белковой частью молекулы гемоглобина, а не со связанным железом в гемовой группе.
Подобно гемоглобину, миоглобин связывает железо внутри гемовой группы. Однако структурно он намного проще, состоящий из одной полипептидной цепи из 154 аминокислот. Он обнаружен только в сердечных миоцитах и окислительных скелетных мышцах. Миоглобин — это белок, запасающий кислород. У морских млекопитающих он обеспечивает снабжение кислородом в течение продолжительных периодов времени, когда животное ныряет под воду. В это время миоглобин выделяет кислород для поддержания аэробного метаболизма в мышцах. Было показано, что у людей уровень миоглобина повышается на больших высотах.
Железозависимые ферменты
Большое количество ферментов требует железа в качестве кофактора для своих функций. Среди наиболее значимых из них — ферменты, участвующие в окислительном фосфорилировании — метаболическом пути, преобразующем питательные вещества в энергию. Ферменты цитохрома связывают гемовое железо, а некоторые белковые комплексы в процессе окислительного фосфорилирования имеют центры железо-сера, которые имеют решающее значение для их функции.
Ферритин и трансферрин
Пищевое железо хранится в составе белкового комплекса, называемого ферритином.Ферритин состоит из 24 субъединиц, которые образуют капсулу вокруг связанных атомов железа. Каждый комплекс связывает от 2000 до 45000 атомов железа. Другой белок, трансферрин, вырабатываемый в печени, переносит железо из крови в другие места для хранения. Основными местами хранения железа в организме являются печень, скелетные мышцы и ретикулоэндотелиальные клетки. Если емкость этих клеток превышена, железо откладывается рядом с комплексами ферритин-железо в клетках. Эти отложения называются гемосидерином.Железо в гемосидерине недоступно для клетки. Отложения гемосидерина могут быть обнаружены в организме после кровотечения.
Общее использование железа в организме регулируется мРНК ферритина и трансферрина, которые содержат элементы, чувствительные к железу (IRE). Для гомеостаза железа необходима аскорбиновая кислота (витамин С), которая стимулирует абсорбцию пищевого железа и способствует поглощению железа, связанного с трансферрином, в плазме. Аскорбиновая кислота также стимулирует синтез ферритина, ингибируя деградацию ферритина и выход железа из клетки.
Дополнительная информация
Что нужно знать
Чувствовали ли вы в последнее время усталость? Сможете ли вы подняться по лестнице, не задыхаясь, даже если вы в хорошей физической форме? Если это так, возможно, вам не хватает железа, особенно если вы женщина.
Хотя многие люди не думают о железе как о питательном веществе, вы можете быть удивлены, узнав, что низкий уровень железа является наиболее распространенным дефицитом питания в США. Согласно данным Центров США, почти 10% женщин испытывают дефицит железа. Контроль и профилактика заболеваний.
Давайте посмотрим, почему железо так важно для вашего тела, что может случиться, если вы не получаете его в достаточном количестве, и когда вам нужно принимать добавки железа.
Зачем вам железо?
Железо — важный минерал. «Основная причина, по которой мы нуждаемся в нем, заключается в том, что он помогает транспортировать кислород по всему телу», — говорит Пол Томас, доктор медицинских наук, научный консультант Управления диетических добавок Национального института здоровья.
Железо является важным компонентом гемоглобина, вещества красных кровяных телец, которое переносит кислород из легких и переносит его по всему телу.Гемоглобин составляет около двух третей железа в организме. Если у вас недостаточно железа, ваше тело не сможет вырабатывать достаточно здоровых красных кровяных телец, переносящих кислород. Недостаток эритроцитов называется железодефицитной анемией.
Продолжение
Без здоровых эритроцитов ваше тело не может получать достаточно кислорода. «Если вы не получаете достаточного количества кислорода в организме, вы чувствуете усталость», — говорит Томас. Это истощение может повлиять на все, от функции вашего мозга до способности вашей иммунной системы бороться с инфекциями.Если вы беременны, серьезный дефицит железа может увеличить риск рождения вашего ребенка слишком рано или меньше, чем обычно.
Утюг имеет и другие важные функции. «Железо также необходимо для поддержания здоровья клеток, кожи, волос и ногтей», — заявила в интервью по электронной почте Элейн Чоттинер, доктор медицинских наук, доцент и директор клиник общей гематологии Медицинского центра Мичиганского университета.
Сколько железа вам нужно?
Сколько железа вам нужно каждый день, зависит от вашего возраста, пола и общего состояния здоровья.
Младенцам и детям ясельного возраста в целом нужно больше железа, чем взрослым, потому что их тела растут очень быстро. В детстве мальчики и девочки нуждаются в одинаковом количестве железа — 10 миллиграммов в день с 4 до 8 лет и 8 мг в день с 9 до 13 лет.
Продолжение
Начиная с подросткового возраста суточная потребность женщины в железе увеличивается. Женщинам нужно больше железа, потому что они теряют кровь каждый месяц во время менструации. Вот почему женщинам в возрасте от 19 до 50 необходимо получать 18 мг железа каждый день, в то время как мужчинам того же возраста достаточно 8 мг.
После менопаузы железо у женщины должно снизиться по мере завершения менструального цикла. После наступления менопаузы и мужчинам, и женщинам требуется одинаковое количество железа — 8 мг в день.
Вам может потребоваться больше железа из пищевых источников или из добавок железа, если вы:
- Беременны или кормите грудью
- У вас почечная недостаточность (особенно если вы проходите диализ, который может вывести железо из организма)
- Есть язва, которая может вызвать потерю крови
- Есть желудочно-кишечное расстройство, которое мешает вашему организму нормально усваивать железо (например, целиакия, болезнь Крона или язвенный колит)
- Принимайте слишком много антацидов, которые могут помешать вашему организму абсорбирует железо
- Перенесли операцию по снижению веса (бариатрическую)
- Много тренируйтесь (интенсивные упражнения могут разрушить эритроциты)
Если вы вегетарианец или веган, вам также может понадобиться принимать добавки железа, потому что Организм не поглощает железо, содержащееся в растениях, так же как и железо из мяса.
Как узнать, что у вас дефицит железа?
«Люди часто не знают, что у них анемия, пока у них не появятся признаки или симптомы — они кажутся бледными или« желтоватыми », утомлены или им трудно заниматься», — говорит Шоттинер.
Если у вас мало железа, вы также можете:
- Чувствовать одышку
- Учащенное сердцебиение
- Холодные руки и ноги
- Жаждать странных веществ, таких как грязь или глина
- Хрупкость и ложка форма ногтей или выпадение волос
- Язвы в углу рта
- Болезненный язык
- Тяжелый дефицит железа может вызвать затруднения при глотании
Если вы устали и тянетесь, обратитесь к врачу.«Достаточно легко обнаружить и диагностировать различные стадии дефицита железа с помощью простого анализа крови», — говорит Томас. Беременным женщинам и людям с желудочно-кишечными расстройствами, такими как болезнь Крона, язвенный колит или глютеновая болезнь, следует регулярно проверять содержание железа в крови.
Вам нужно принимать добавки с железом?
Если у вас низкий уровень железа, употребления в пищу продуктов с высоким содержанием железа, таких как обогащенные злаки, красное мясо, сушеные фрукты и бобы, может быть недостаточно, чтобы дать вам то, что вам нужно.Ваш врач может порекомендовать вам принимать добавки железа.
Продолжение
Витамины для беременных обычно содержат железо, но не все витамины для беременных содержат рекомендуемое количество. Проконсультируйтесь с врачом, прежде чем принимать какие-либо добавки.
Пока вы принимаете добавки с железом, ваш врач должен проверить вашу кровь, чтобы увидеть, улучшился ли ваш уровень железа.
Могут ли добавки с железом вызывать побочные эффекты?
Добавки железа могут вызывать побочные эффекты, обычно расстройство желудка, такое как тошнота, рвота, диарея, темный стул или запор.Беременные женщины особенно подвержены запорам. Чтобы облегчить этот симптом, добавьте в свой рацион дополнительную клетчатку. Смягчитель стула также может улучшить ваше самочувствие.
Начиная с низкой дозы железа, а затем постепенно увеличивая дозу до рекомендуемой суточной дозы, можно свести к минимуму побочные эффекты. Если добавки с железом беспокоят ваш желудок, врач может скорректировать дозу или форму применяемого железа. Вы также можете попробовать принимать добавки во время еды.
Можно ли взять слишком много железа?
В отличии от некоторых дополнений, когда сабж железо, больше точно не лучше.Взрослые не должны принимать более 45 мг железа в день, если они не проходят лечение железом под тщательным медицинским наблюдением.
Продолжение
Для детей передозировка железа может быть особенно токсичной. «Добавки железа убивают маленьких детей, потому что их потребности в железе по сравнению с потребностями взрослых относительно низки», — говорит Томас. Если вы принимаете добавки с железом, очень важно хранить их в высоком закрытом шкафу, вдали от досягаемости ваших детей. Симптомы отравления железом включают сильную рвоту, диарею, боль в животе, обезвоживание и кровавый стул у детей.
Взрослым трудно передозировать железо только из пищи и добавок, потому что в организме взрослого человека есть системы, регулирующие количество усваиваемого железа. Однако людям с наследственным гемохроматозом трудно регулировать абсорбцию железа.
Хотя большинство людей усваивают только около 10% потребляемого железа, люди с гемохроматозом поглощают до 30%. В результате содержание железа в их организме может достигать опасного уровня. Этот избыток железа может откладываться в таких органах, как печень, сердце и поджелудочная железа, что может привести к таким состояниям, как цирроз, сердечная недостаточность и диабет.По этой причине людям с гемохроматозом не следует принимать добавки железа.
Рекомендуемое потребление, преимущества и источники питания
Железо — это минерал, жизненно важный для правильного функционирования гемоглобина, белка, необходимого для транспортировки кислорода в крови. Железо также играет роль во множестве других важных процессов в организме.
Нехватка железа в крови может привести к ряду серьезных проблем со здоровьем, включая железодефицитную анемию. Около 10 миллионов человек в Соединенных Штатах имеют низкий уровень железа, и примерно у 5 миллионов из них диагностирована железодефицитная анемия.
Этот раздел Центра знаний MNT является частью коллекции статей о пользе для здоровья популярных витаминов и минералов. В нем подробно рассматривается рекомендуемое потребление железа, его возможная польза для здоровья, продукты с высоким содержанием железа и любые потенциальные риски для здоровья, связанные с потреблением слишком большого количества железа.
Поделиться на Pinterest Возраст и пол человека могут повлиять на количество железа, необходимое ему в рационе.Рекомендуемая суточная норма элементарного железа зависит от возраста и пола человека.У вегетарианцев также разные потребности в железе.
Младенцы:
- От 0 до 6 месяцев: 0,27 миллиграмма (мг)
- От 7 до 12 месяцев: 11 мг
Дети:
- От 1 до 3 лет: 7 мг
- от 4 до 8 лет: 10 мг
Мужчины:
- От 9 до 13 лет: 8 мг
- От 14 до 18 лет: 11 мг
- 19 лет и старше: 8 мг
Женщины:
- 9 до 13 лет: 8 мг
- От 14 до 18 лет: 15 мг
- От 19 до 50 лет: 18 мг
- От 51 года и старше: 8 мг
- Во время беременности: 27 мг
- При кормлении грудью от 14 до 18 лет возраст: 10 мг
- При лактации в возрасте старше 19 лет: 9 мг
Добавки железа могут быть полезны, когда людям трудно получить достаточное количество железа только с помощью диетических мер, например, с помощью растительной диеты.Лучше попытаться потреблять достаточно пищи в одиночку, удалив или уменьшив факторы, которые могут препятствовать усвоению железа, и потребляя продукты, богатые железом.
Это связано с тем, что многие продукты, богатые железом, также содержат ряд других полезных питательных веществ, которые вместе поддерживают общее состояние здоровья.
Железо помогает сохранить многие жизненно важные функции организма, включая общую энергию и концентрацию внимания, желудочно-кишечные процессы, иммунную систему и регулирование температуры тела.
Преимущества железа часто остаются незамеченными до тех пор, пока человек не получает его в достаточном количестве.Железодефицитная анемия может вызывать усталость, учащенное сердцебиение, бледность кожи и одышку.
Здоровая беременность
Объем крови и производство красных кровяных телец резко увеличиваются во время беременности, чтобы обеспечить растущий плод кислородом и питательными веществами. В результате возрастает спрос на железо. Хотя организм обычно максимизирует усвоение железа во время беременности, недостаточное потребление железа или другие факторы, влияющие на его усвоение, могут привести к дефициту железа.
Низкое потребление железа во время беременности увеличивает риск преждевременных родов и низкой массы тела при рождении, а также низких запасов железа и нарушений когнитивного или поведенческого развития у младенцев.Беременные женщины с низким содержанием железа могут быть более подвержены инфекциям, потому что железо также поддерживает иммунную систему.
Очевидно, что препараты железа необходимы беременным женщинам и женщинам с дефицитом железа. Тем не менее, исследования продолжаются в отношении возможности рекомендовать дополнительное количество железа всем беременным женщинам, даже тем, у кого уровень железа нормальный. Утверждается, что все беременные женщины должны принимать от 30 до 60 миллиграммов (мг) добавок железа каждый день беременности, независимо от уровня железа.
Энергия
Недостаток железа в рационе может повлиять на эффективность использования энергии организмом. Железо переносит кислород к мышцам и мозгу и имеет решающее значение как для умственной, так и для физической работоспособности. Низкий уровень железа может привести к потере внимания, повышенной раздражительности и снижению выносливости.
Улучшение спортивных результатов
Дефицит железа чаще встречается у спортсменов, особенно у молодых спортсменок, чем у людей, не ведущих активный образ жизни.
Это, по-видимому, особенно верно для спортсменок, занимающихся выносливостью, например, бегунов на длинные дистанции. Некоторые эксперты предполагают, что спортсменкам-женщинам, работающим на выносливость, следует добавлять дополнительно 10 мг элементарного железа в день к текущей суточной суточной норме потребления железа.
Дефицит железа у спортсменов снижает спортивные результаты и ослабляет активность иммунной системы. Недостаток гемоглобина может значительно снизить работоспособность при физических нагрузках, поскольку снижает способность организма переносить кислород к мышцам.
Железо имеет низкую биодоступность, что означает, что тонкий кишечник с трудом усваивает большие количества. Это снижает его доступность для использования и увеличивает вероятность дефицита.
Эффективность всасывания зависит от ряда факторов, включая:
- источник железа
- другие компоненты диеты
- здоровье желудочно-кишечного тракта
- использование лекарств или добавок
- общее состояние человека
- наличие промоторов железа, таких как витамин C
Во многих странах продукты из пшеницы и детские смеси обогащены железом.
Существует два типа диетического железа, известных как гем и негем. Пищевые продукты животного происхождения, включая мясо и морепродукты, содержат гемовое железо. Гемовое железо легче усваивается организмом.
Негемовое железо, которое содержится в растениях, требует, чтобы организм предпринял несколько шагов для его усвоения. Источники железа на растительной основе включают бобы, орехи, сою, овощи и обогащенные злаки.
Биодоступность гемового железа животного происхождения может достигать 40 процентов. Однако негемовое железо из растительных источников имеет биодоступность от 2 до 20 процентов.По этой причине рекомендуемая суточная норма для вегетарианцев в 1,8 раза выше, чем для тех, кто ест мясо, чтобы компенсировать более низкий уровень усвоения растительной пищи.
Употребление продуктов, богатых витамином С, наряду с негемовыми источниками железа может значительно увеличить усвоение железа.
При соблюдении вегетарианской диеты также важно учитывать компоненты пищи и лекарства, которые блокируют или снижают абсорбцию железа, такие как:
- ингибиторы протонной помпы и омепразол, используемые для снижения кислотности содержимого желудка
- полифенолы в злаки и бобовые, а также шпинат
- танины в кофе, чае, в вине и некоторых ягодах
- фосфаты в газированных напитках, таких как газированные напитки
- фитаты в бобах и зернах
Некоторые из лучших источников железа включают:
- Консервы из моллюсков: 3 унции (унции) содержат 26 миллиграммов (мг) железа.
- Обогащенный, простой, сухой овес: В 100 г содержится 24,72 мг.
- Белая фасоль: Одна чашка дает 21.09.
- Темный шоколад (от 45 до 69 процентов какао): Один батончик содержит 12,99 мг.
- Приготовленные тихоокеанские устрицы: 3 унции содержат 7,82 мг.
- Вареный шпинат: В одной чашке содержится 6,43 мг.
- Говяжья печень: 3 унции обеспечивает 4,17 мг.
- Вареная и высушенная чечевица: Полстакана дает 3 штуки.3 мг.
- Фирменный тофу: В половине чашки содержится 2,03 мг.
- Вареный и высушенный нут: Полстакана содержит 2,37 мг.
- Консервированные, тушеные помидоры: В половине чашки содержится 1,7 мг.
- Постный, говяжий фарш: 3 унции содержат 2,07 мг.
- Средний запеченный картофель: Это дает 1,87 мг.
- Жареные орехи кешью: В 3 унциях содержится 2 мг.
Кальций может замедлять абсорбцию как гемового, так и негемового железа.В большинстве случаев типичная разнообразная диета в западном стиле считается сбалансированной с точки зрения усилителей и ингибиторов всасывания железа.
Для взрослых дозы перорального приема железа могут составлять от 60 до 120 мг элементарного железа в день. Эти дозы обычно применяются для беременных женщин с тяжелым дефицитом железа. Расстройство желудка — частый побочный эффект приема добавок железа, поэтому может помочь разделение доз в течение дня.
Взрослые со здоровой пищеварительной системой имеют очень низкий риск перегрузки железом из пищевых источников.
Люди с генетическим заболеванием, называемым гемохроматозом, подвергаются высокому риску перегрузки железом, поскольку они поглощают гораздо больше железа из пищи по сравнению с людьми без этого заболевания.
Это может привести к накоплению железа в печени и других органах. Он также может вызывать образование свободных радикалов, которые повреждают клетки и ткани, включая печень, сердце и поджелудочную железу, а также повышают риск некоторых видов рака.
Частый прием добавок железа, содержащих более 20 мг элементарного железа за один раз, может вызвать тошноту, рвоту и боль в желудке, особенно если добавка не принимается во время еды.В тяжелых случаях передозировка железа может привести к органной недостаточности, внутреннему кровотечению, коме, судорогам и даже смерти.
Важно хранить добавки железа в недоступном для детей месте, чтобы снизить риск передозировки со смертельным исходом.
По данным Poison Control, случайное употребление добавок железа было наиболее частой причиной смерти от передозировки лекарств у детей в возрасте до 6 лет до 1990-х годов.
Изменения в производстве и распространении добавок железа помогли уменьшить случайные передозировки железа у детей, такие как замена сахарного покрытия на железных таблетках пленочным покрытием, использование защитных крышек для бутылочек и индивидуальная упаковка высоких доз железа.В период с 1998 по 2002 год был зарегистрирован только один случай смерти от передозировки железом.
Некоторые исследования показали, что чрезмерное потребление железа может увеличить риск рака печени. Другие исследования показывают, что высокий уровень железа может увеличить риск диабета 2 типа.
Совсем недавно ученые начали исследовать возможную роль избытка железа в развитии и прогрессировании неврологических заболеваний, таких как болезнь Альцгеймера и болезнь Паркинсона. Железо также может играть прямую повреждающую роль в травмах головного мозга в результате кровотечения в головном мозге.Исследования на мышах показали, что высокое содержание железа увеличивает риск остеоартрита.
Добавки железа могут снизить доступность некоторых лекарств, включая леводопу, которая используется для лечения синдрома беспокойных ног и болезни Паркинсона, и левотироксина, который используется для лечения слабо функционирующей щитовидной железы.
Ингибиторы протонной помпы (ИПП), используемые для лечения рефлюксной болезни, могут снизить количество железа, которое может усваиваться организмом как из пищи, так и из пищевых добавок.

